אנגיופויאטין ועיכוב ליפאזות של ליפופרוטאינים ואנדותליאלים - Angiopoietins inhibit lipoprotein and endothelial lipases
| מדריך בדיקות מעבדה | |
| Angiopoietin-like 3 | |
|---|---|
| שמות אחרים | ANGPTL3 |
| |
| מעבדה | כימיה בדם |
| טווח ערכים תקין | בפלזמה: 119.57 ± 20.11 ng/mL. |
| יוצר הערך | פרופ' בן-עמי סלע |
ראו גם – Angiopoietin-like protein 3
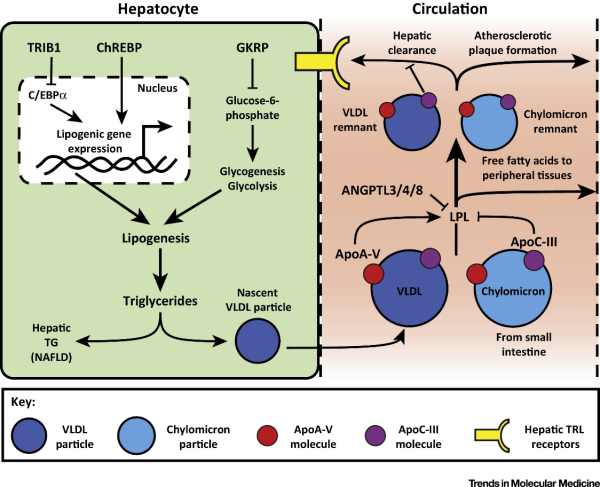
angiopoietin-like 3 הוא חלבון שמקודד באדם על ידי הגן ANGPTL3 (Conklin וחב' ב-Genomics משנת 1999). חלבון זה מבוטא בעיקר בכבד ומאופיין על ידי המבנה של אנגיו-פויאטינים המכיל פפטיד signal, מקטע N-טרמינלי סלילני, ומקטע C-טרמינלי דמוי-פיברינוגן (להלן FBN). מקטע ה-FBN נמצא קושר אינטגרינים מסוג α-5/β-3 וקישור זה משרה ספיחה של תאי אנדותל ונדידת תאים. החלבון ANGPLT3 משחק תפקיד ברגולציה של אנגיוגניות, ופועל גם כמעכב של האנזים lipoprotein lipase (להלן LPL) ושל endothelial lipase (להלן EL) (Tikka ו-Jauhiainen ב-Endocrine משנת 2016, ו-Wang וחב' -Proc Natl Acad Sci USA משנת 2015), ועל ידי כך מגביר את ריכוז הטריגליצרידים, LDL ו-HDL בפלזמה של עכברים ובני-אדם. ANGPLT3 מעכב את ההידרוליזה של HDL-phospholipid ולפיכך מגביר ריכוזי HDL בפלזמה. חלבון זה משחק תפקיד חשוב בסיוע לקליטה של טריגליצרידים מהצירקולציה לתוך רקמת השומן "הלבנה" דרך שפעול של Angptl8 (Zhang וחב' ב-Open Biol משנת 2016, ו-Ren וחב' ב־J Physiol Endocrinol Metab משנת 2012), ובכך הוא מעכב לאחר הארוחה את פעילות האנזים LPL בלב ובשרירי השלד (Fu וחב' ב-Sci Rep משנת 2012, ו-Zhang וחב' ב-Open Biol משנת 2016). באדם, וריאנטים עם loss-of-function גנטי בעותק אחד, רמות LDL בנסיוב פוחתות, ואילו באלה עם וריאנטים של loss-of-function בשני עותקים, מוצאים רמות נמוכות של LDL, HDL ושל טריגליצרידים (Musunuru וחב' ב-N Eng J Med משנת 2010).
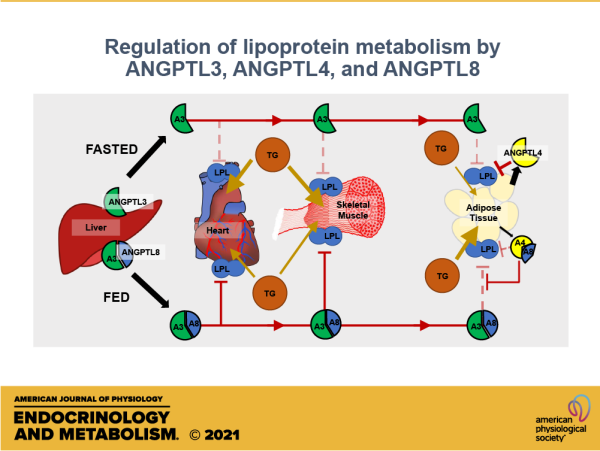
משפחת ANGPLT ובעיקר ANGPTL4, ANGPLT3 ו-ANGPLT8 הם מווסתים חשובים של ליפופרוטאינים בפלזמה. באנשים עם חסר של ANGPTL3 הנגרם על ידי איבוד הומוזיגוטי של הוריאנטים של הגן Angplt3, רמות כל הליפופרוטאינים בפלזמה פוחתות בהרבה. מפגע פלזמטי זה הקרוי familial combined hypolipidemia 0 להלן FHBL2) אינו כרוך בביטויים פתולוגיים מוגדרים. באלה הנושאים של וריאנטים הטרוזיגוטיים של loss-of-function מוצאים בפלזמה רמות נמוכות של סך-כולסטרול ושל טריגליצרידים, והם מצויים בסיכון נמוך יותר לפתח טרשת עורקים או מחלה קרדיו-וסקולרית, בהשוואה לאלה ללא וריאנטים אלה. תצפיות אלה סללו את הדרך לפיתוח של אסטרטגיות להפחתת ליפופרוטאינים אתרוגניים באדם, על ידי אינאקטיבציה של ANGPTL3 או על ידי נוגדנים חד-שבטיים ספציפיים, או על ידי אוליגו-נוקלאוטידים anti-sense. משפחת ה-ANGPTLs מייצגת שמונה גליקופרוטאינים המופרשים, ומתפקדים ב-remodeling של הרקמות, במטבוליזם של ליפידים, בהתרחבות של תאי גזע, בדלקת ובאנגיוגניות (Hato וחב' ב-Trends Cardiovasc Med משנת 2009, ו-Santulli ב-Front Endocrinol משנת 2014). שלושה ANGPTLs, שהם: ANGPTL4 ,ANGPLT3 ו-ANGPLT8, נמצאו קריטיים במטבוליזם של ליפידים ובוויסות של ליפידים בפלזמה (Mattijssen ו-Kersten ב-Biochim Biophys Acta משנת 2012, ו-Zhang ב-Open Biol משנת 2016).
היפוליפידמיה משפחתית משולבת באדם
בבני אדם, פנוטיפ של ליפופרוטאין הדומה לזה שבעכברי u KK/San תואר לראשונה על ידי Musunuru וחב' במשפחה גדולה שהייתה חשודה במקור כמושפעת מ-familial hypobetalipoproteinemia (או FHBL1) לאור העובדה שהיו בה רמות נמוכות של LDL (Musunuru וחב' ב-N Eng J Med משנת 2010). שני בני משפחה זו היו בעלי רמות נמוכות במיוחד של כולסטרול ושל LDL, ורמות נמוכות של טריגליצרידים ושל HDL. ריצוף של ה-exome גילה ששני בני משפחה אלה היו compound heterozygous של וריאנטים loss-of-function של ANGPLT3 הצפוי לגרום לחסר מוחלט של ANGPLT3. פנוטיפ ליפופרוטאיני חדש זה מוגדר כ-Familial Combined Hypolipidemia (או FHBL2). סריקה גנטית של המשפחה הזו זיהו 13 הטרוזיגוטים. וריאנט nonsense p.(S17*) של ANGPLT3 נמצא גם במדגם של נבדקים היפו-ליפידמיים המתגוררים במרכז איטליה, בו ריצוף מחודש של הגן של Angplt3 בתשע משפחות ובמדגם גדול של 352 פרטים באוכלוסייה המקומית הביא לזיהוי של 62 נשאים של וריאנט זה (8 הומוזיגוטיים ו-54 הטרוזיגוטיים) (Minicocci וחב' ב-J Clin Endocrinol Metab משנת 2012). במדגם זה להומוזיגוטיים היו רמות נמוכות שלא היו ניתנות לזיהוי של ANGPLT3, רמות נמוכות של טריגליצרידים ושל כולסטרול, ורמות של ירידה ניכרת בכל סוגי הליפופרוטאינים (VLDL, LDL ו-HDL). להטרוזיגוטים יש ירידה של 50% ברמת ANGPLT3 בצירקולציה, ורמות מופחתות של סך-כולסטרול ושל HDL, בהשוואה לאלה שאינם נשאים, ורמות של LDL וטריגליצרידים מופחתות בהשוואה לנבדקי ביקורת.
יתרה מכך, להומוזיגוטים של p.(S17*) הייתה פעילות גבוהה יותר משמעותית של LPL בהשוואה לנבדקי ביקורת, ורמות נמוכות יותר של חומצות שומן חופשיות, מה שמצביע על ליפוליזה מופחתת של רקמת שומן (Robciuc וחב' ב-Arterioscler Thromb Vasc Biol משנת 2013). אנשים נוספים עם familial combined hypolipidemia כתוצאה מווריאנטים שונים של loss-of-function של Angplt3 זוהו במשפחות איטלקיות וספרדיות, כמו גם במדגם של בני אדם עם היפו-כולסטרולמיה ראשונית (Pisciotta וחב' ב-Circ Cardiovasc Genet משנת 2012, Martín-Campos וחב' ב-Clin Chim Acta משנת 2012, ו-Noto וחב' ב-Arterioscler Thromb Vasc Biol משנת 2012). מנקודת מבט קלינית, נשאים של שני אללים של loss-of-function של Angplt3 שזוהו בלימודי משפחות, לא הראו פנוטיפ פתולוגי מובהק. באופן יותר ספציפי, הם לא הראו ביטויים קליניים של טרשת עורקים בגיל צעיר או סיכון מוגבר של מחלה לבבית איסכמית, שהייתה יכולה להיות צפויה לאור העובדה של חשיפה רבת שנים לרמות נמוכות של HDL (Perk וחב' ב-Eur Heart J משנת 2012). הערכה של הסטאטוס הווסקולרי בקבוצה של מטופלים מהקטגוריה של FHBL2 (שבעה הומוזיגוטים ו-59 הטרוזיגוטים), נשאי המוטציה loss-of-function של Angplt3, מצאה שאלה עם FHBL2 לא הראו שינויים משמעותיים בעובי של ה-intima-media בעורק הקרוטידי בהשוואה לנבדקי ביקורת. ממצאים אלה מצביעים על כך שלמרות הנוכחות של רמות נמוכות של HDL, אלה עם FHBL2 מוגנים מהתפתחות של טרשת עורקים טרם-עת על ידי הפחתה בו-זמנית של ליפופרוטאינים אתרוגניים כמו VLDL ו-LDL.
נקודת מפתח אחרת בהקשר של פנוטיפים קליניים ב-FHBL2' קשורה למחלת כבד שומני, תרחיש המופיע לעיתים קרובות באנשים עם FHBL1 (Tarugi ו-Averna ב-Adv Clin Chem משנת 2011). מחקרים קליניים הראו שב- FHBL2 לא הייתה עלייה במצבי כבד שומני בהשוואה לביקורת (Di Costanzo וחב' ב-J Clin Lipidol משנת 2017). וריאנטים של loss-of-function בגן Angptl3, זוהו במחקרי אוכלוסיות, כאשר מחקרי GWAS מוקדמים הראו שווריאנטים אלה היו כרוכים בשינויים ברמות של טריגליצרידים, סך-כולסטרול, LDL ו-HDL (Kathiresam וחב' ב-Nature Genet משנת 2008, ו-Teslovich וחב' ב-Nature משנת 2010). בנוסף, ריצוף מחודש של Angptl3 באוכלוסיות מסוימות הראה שווריאנטים loss-of-function היו כרוכים עם רמות נמוכות של טריגליצרידים בפלזמה. במחקר נוסף, נתוני ריצוף של Angptl3 הביאו לזיהוי של 23 וריאנטים של loss-of-function. וריאנטים אלה נמצאו ב-130 מתוך 40,112 נבדקים. יתרה מכך, בנשאים הטרוגניים של וריאנט loss-of-function של Angptl3 שנבחרו מתוך מדגם של למעלה מ-20,000 נבדקים שנכללו במחקר Myocardial Infarction Genetics Consortium' הרמות בפלזמה של סך-כולסטרול, של LDL ושל טריגליצרידים פחתו ב-11%, ב-12% וב-17%, בהתאמה, ללא הבדל משמעותי ברמת HDL, בהשוואה ללא נשאים. בנוסף, בעלי המחקר מצאו שבנשאים ההטרוגניים של וריאנטים loss-of-function ב־Angptl3 הייתה ירידה של 34% בסיכון למחלת עורקים כליליים (להלן CAD).
ANGPTL3 והמטבוליזם של ליפופרוטאינים
ANGPTL3 מסונתז בכבד כחלבון קודמן (precursor), המותמר לחלבון הבשל על ידי ביקוע פרוטאוליטי על ידי מספר convertases בכבד כגון eurin, ו-PCSK2, PCSK4, PACE4, PCSK5 ו-PCSK7. תהליך הביקוע מייצר מקטע N-טרמינלי פעיל, בעל פעילות LPL מעכבת, מה שמוכח בתצפית לפיה השמט של האזור ה-N-טרמינלי של ANGPTL3 מבטל לחלוטין את פעילותו המעכבת (Ono ANGPTL3 ב-J Biol Chem משנת 2003). תהליך ביקוע נתמך על ידי ANGPTL8. המקטע החופשי ה-N-טרמינלי של ANGPTL3, מעכב את LPL (Quagliarini וחב' ב-Proc Natl Acad Sci USA משנת 2012). הקשר בין ANGPLT3 לבין המטבוליזם של ליפופרוטאינים בפלזמה התברר מהזיהוי של זן העכברים KK המאופיין על ידי סוכרת, obesity והיפר-טריגליצרידמיה. לעומתם, עכברי KK/San למרות הפנוטיפ של סוכרת ו-obesity המאפיין אותם, הם בעלי רמה נמוכה של טריגליצרידים, בהשוואה לעכברי KK. ההיפו-טריגליצרידמיה שלהם היא כתוצאה מרמה נמוכה מאוד של VLDL. עכברים אלה נמצאו הומוזיגוטיים לווריאנט loss-of-function של הגן המקודד ל-ANGPLT3 ולחסר מוחלט של ANGPLT3 (Koishi וחב' ב-Nature Genet משנת 2002). ההיפו-ליפידמיה הנצפית בזן העכבר המוטנט הזה נמצאה כרוכה בפעילות מוגברת של LPL (Shimizugawa וחב' ב-J Biol Chem משנת 2002). מאז התצפית הזו, מחקרים נוספים שבוצעו בעכברי -/-,Angptl3 לא רק אישרו ש-Angptl3 הוא מעכב של LPL, אלא גם הראו שחסר מוחלט של Angptl3 כרוך בהפחתה של ליפופרוטאינים המכילים טריגליצרידים (VLDL) אלא גם הראו הפחתה בליפופרוטאינים המכילים כולסטרול כגון LDL ו-HDL (Fujimoto וחב' ב-Ex Amin משנת 2006). מאידך גיסא, ביטוי-יתר של Angplt3 בעכברים הגדיל את רמת טריגליצרידים בפלזמה על ידי עיכוב הפעילות של LPL (Köster וחב' ב-Endocrinology משנת 2005).
ANGPTL3 וסוכרת
מחקרים in vivo ו-in vitro מצאו שאינסולין פועל כמווסת שלילי של יצירת ANGPTL3 בתאי הפטומה בחולדות ובאדם. כמות ה-mRNA של ANGPTL3 וכמות ANGPTL3 המופרש, פוחתות בתלות ברמת אינסולין. אך בניגוד בולט, הביטוי של הגן Angptl3 ורמת חלבון זה בפלזמה גדלו בעכברים חסרי אינסולין כתוצאה מטיפול עם streptozotocin (Shimamura וחב' ב-Biochim Biophys Res Commun משנת 2004). בנוסף, רמת ANGPTL3 mRNA ורמת החלבון עצמו גדלו פי-3 בעכברים obese עם סוכרת מסוג 2 (עכברים מסוג (db/db) (Inukai וחב' באותו כתב עת מאותה שנה). מחקר דומה בוצע באדם בו נבחנה השפעת אינסולין in vivo על ANGPTL3 בצירקולציה (Haridas וחב' ב-J Clin Endocrinol Metab משנת 2015). במחקר זה נמצא שהיפר-אינסולינמיה גרמה לירידה ברמות ANGPTL3 בפלזמה, וכן שבשורת תאים הפטוציטים של אדם, אינסולין הפחית את הביטוי של הגן Angptl3 ואת הפרשת החלבון האמור לתוך המדיום. תוצאות אלו מצביעות על כך שהביטוי של ANGPTL3 גדל במצבים של חוסר אינסולין או במצבים של אנשים סוכרתיים העמידים לאינסולין, מה שמצביע על כך שרמות ANGPTL3 מוגברות בפלזמה תורמות להיפר-טריגליצרידמיה סוכרתית.
מעכבים של ANGPTL3
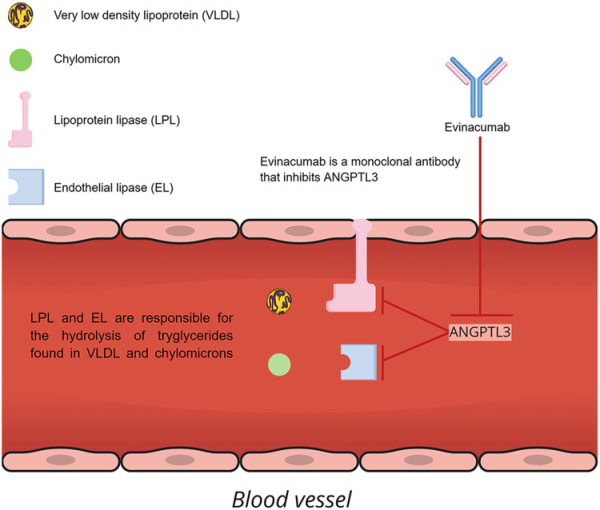
Evinacumab: מעכב זה (שם מותג Evkeeza) הוא נוגדן חד-שבטי הומני לחלוטין שיוצר על ידי Regeneron Pharmaceutical Inc, תוך שימוש בטכנולוגיה של VelocImmunne. טכנולוגיה זו מבוססת על עכברים שהונדסו גנטית עם מערכת חיסון מאונשת לייצור של נוגדנים מאונשים באופן טוטלי. (Raal וחב' ב-N Eng J Med משנת 2020). Evinacumab הוא נוגדן IgG4-κ המורכב משני שרשרות כבדות מסוג γ שאורכו 463 חומצות אמינו וזוג שרשרות קלות מסוג κ שכל אחת מהן באורך של 214 חומצות אמינו. השרשרות הכבדות קשורות ביניהן על ידי קשרים די-סולפידים באזור הציר (hinge) שלהם (Poiron וחב' ב-JOBIM משנת 2010). כאשר מזריקים מתחת לעור או בעירוי לוריד את evinacumab, הוא נקשר ל-ANGPTL3 ומונע מ-LPL וכן מ-EL (endothelial lipase) את ההידרוליזה של ליפידים. הבטיחות, הסבילות והפרמקו-קינטיקה של evinacumab נקבעו בניסוי קליני אקראי, כפול-סמיות ומבוקר כנגד פלצבו, ב-96 לבנים ויפנים בריאים, עם רמות LDL שבין 100–160 מיליגרם/דציליטר.
משתתפי הניסוי חולקו באקראי ל-4 קבוצות: אלה שטופלו עם evinacumab שהוזרקו תת-עורית עם 300 מיליגרם באופן חד-פעמי; אלה שהוזרקו תת-עורית עם 300 מיליגרם אחת לשבוע 8 פעמים; ואלה שקיבלו את החומר לתוך הווריד במינון של 5 מיליגרם או של 15 מיליגרם/ק"ג משקל גוף אחת ל-4 שבועות. כל קבוצה הייתה בת 24 משתתפים, מתוכם 12 לבנים ו-12 יפנים. שהוזרקו עם evinacumab או עם פלצבו, וכולם היו המעקב למשך 24 שבועות. Einacumab נסבל היטב על ידי המטופלים בכל המינונים, והבטיחות של החומר נמצאה זהה לזאת של פלצבו, ללא תופעות לוואי שהביאו לפרישה מהניסוי. מבחינה פרמקו-דינמית, הזרקת evinacumab גרמה להפחתה ברמות LDL, טריגליצרידים ו-ApoB בשתי הקבוצות האתניות בניסוי זה (Harada-Shiba וחב' ב-Atherosclerosis משנת 2020). מספר ניסויים ניסוח לקבוע את היעילות של evinacumab בהפחתת רמות LDL בפלזמה במטופלים עם היפר-כולסטרולמיה עיקשת. ניסוי אחד ב-phase 2, כלל 9 משתתפים עם HoFH (או compound heterozygous familial cholesterolemia) שלא הגיבו לטיפולים אגרסיביים להפחתת רמת ליפידים.
הוראות לביצוע הבדיקה
את הדם שלא על ידי מטופלים בהפארין, יש ליטול לאחר 12 שעות צום לילי, למבחנת ספירת-דם (EDTA, פקק סגלגל) או למבחנה כימית רגילה (פקק צהוב או אדום). לאחר 30 דקות בטמפרטורת החדר. דגימת הדם מסורכזת במהירות של 3,000 סיבובים לדקה, למשך 20 דקות והנוזל העליון נשמר בקירור בטמפרטורה של-80°C עד לבדיקה. הליפידים בנסיוב נמדדים באנלייזר כימי Hitachi 747. ריכוז ANGPTL3 בפלזמה נקבע בשיטת ELISA. דגימות הפלזמה נמהלות 1:4 ב-sample diluent. דגימות הנסיוב או הפלזמה ואנטיגן ביוטין (50 מיקרוליטר) מוספות לבארות של פלטת 96 בארות, והפלטה עוברת הדגרה למשך 30 דקות בטמפרטורה של 37 מעלות צלזיוס. לאחר שטיפה של 5 פעמים עם 300 מיקרוליטר של תמיסת PBST (50 מיקרומולר אשלגן פוספט, ו-0.15% דטרגנט Tween, pH7.4), יש להוסיף לכל באר 50 מיקרוליטר של avidin (תמיסת 100 μL avidin-HRP), ולהדגיר למשך 30 דקות בטמפרטורה של 37 מעלות צלזיוס. לאחר 5 שטיפות נוספות יש להוסיף לכל באר 50 מיקרוליטר של תמיסות צבע A ו-B, והפלטה מודגרת בחושך למשך 10 דקות בטמפרטורת 37 מעלות צלזיוס. הפלטות עוברות אנליזה תוך 10 דקות, תוך שימוש ב־ultraviolet spectrophotometer באורך גל של 450 ננומטר.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק