החתימה הגנטית של גידולי הילדות - The genetic signature of childhood tumors
הופניתם מהדף החתימה הגנטית של גידולי הילדות לדף הנוכחי.
| החתימה הגנטית של גידולי הילדות | ||
|---|---|---|
| The genetic signature of childhood tumors | ||
| יוצר הערך | ד"ר איריס קוונצל | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן
מבוא
גידולים ממאירים של רקמה רכה (soft tissue sarcoma) הם קבוצה הטרוגנית של גידולים ממקור מזנכימלי - רקמת שומן, שריר, סחוס, וכלי דם ("sarc" פירושו בשר). קבוצה זו מהווה 1 אחוז מכלל הגידולים הממאירים במבוגרים, ו-7 אחוזים מכלל הגידולים הממאירים בילדים. מאחר שעל פי הסיווג האחרון של ארגון הבריאות העולמי (WHO - World Health Organization) נכללות בתוכו מעל 50 אבחנות היסטולוגיות, אנו דנים בגידולים ששכיחותם כקבוצה אינה גדולה, והקבוצה עצמה כוללת מגוון רחב של אבחנות היסטולוגיות.
בשל השכיחות הנמוכה, הרבגוניות בתוך הקבוצה והקושי להבחין בין תת-קבוצות, הגישה למחקר קליני בגידולי רקמה רכה במשך מעל 30 שנים הייתה גישת "מיטת סדום": מיזוג כל המחלות לסל אחד של טיפול אחיד. גישה זאת אמנם אפשרה מחקרים מרובי משתתפים, אולם מנעה את האפשרות לזהות תת-קבוצות היסטולוגיות שעבורן הטיפול האחיד יעיל יותר או פחות, כשתגובה של תת-קבוצה היסטולוגית נדירה נמהלה בכלל אוכלוסיית המחקר. מחקר בסיסי הוגבל גם הוא (בדומה למחקר קליני) על ידי הקושי לחלק את גידולי הרקמה הרכה לתת-קבוצות.
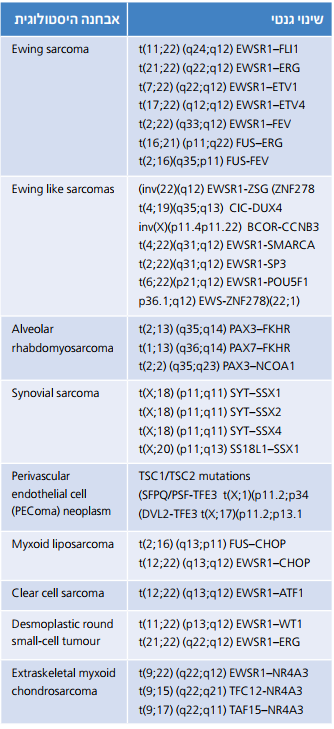
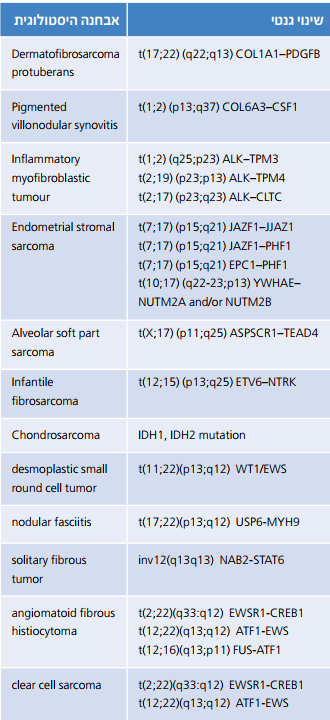
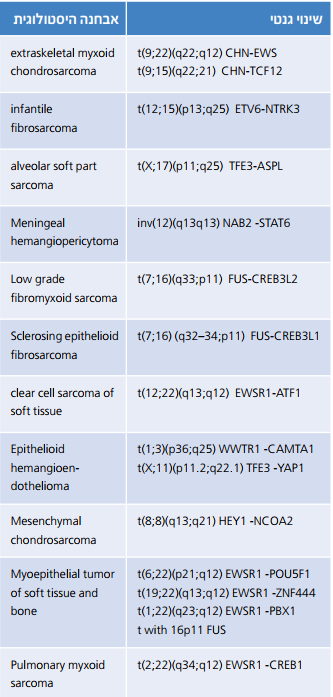
ניתן לאפיין גידולי רקמה רכה רבים באמצעות שינויים גנומיים סומטיים הנשנים באותו סוג גידול, ואופיינים לו[1]. שינויים אלו (טבלה מספר 1) יכולים לשמש אותנו לצרכים אבחנתיים ולהוות בסיס למחקר בסיסי ומטרות טיפוליות. איתורם בגידול נעשה באופן שגרתי על ידי בדיקות FISH (Fluorescence In Situ Hybridization) ו-PCR (Polymerase Chain Reaction). אלו משמשות לזיהוי הפרעות סומטיות בדנ"א או ביטוי שלהן ברנ"א, אולם יש להן מגבלה ברורה. שתי השיטות נבנו לצורך איתור פגם סומטי מוגדר מראש, ולכן המידע שיספקו תלוי בהשערה האבחנתית אותה (ורק אותה) יוכלו לאשש או להפריך.
הופעתן של טכנולוגיות בשיטת ריצוף מקבילי (או בשם אחר - next generation sequencing) פתחה בפנינו אפשרות להתגבר על מגבלה זו. בדיקת ריצוף מקבילי בוחנת בו זמנית טווח מטרות גדול (החל בגנים ספורים וכלה ב-whole genome/transcriptome, בהתאם לבדיקה שנבחרה), והיא יכולה לכלול טרנסלוקציות (SNV) - Single Nucleotide Variants ו-(CNV) Copy Number Variations.
הקושי להבחין באמצעות היסטולוגיה ואפילו היסטולוגיה מלווה בבדיקות מולקולריות המבוצעות על פי שיקול דעתו של הפתולוג בין תת-סוגים של גידולי רקמה רכה (FISH, PCR), בא לידי ביטוי בשיעור הגבוה של חוסר הסכמה (discordance) בין פתולוגים. שיעורי אי ההסכמה המרכזיים (major discordance) המדווחים בין פתולוג מאבחן ובין פתולוג יועץ מומחה בסרקומות (referral center/central reviewer) לגבי האבחנה נעים בין 10 אחוזים ל-14 אחוזים, ושיעורי חוסר התאמה כלשהי נעים בין 26 אחוזים ובין 45 אחוזים בעבודות שונות[2][3][4].
אבחנה מבוססת מולקולרית של גידולי רקמה רכה
מספר עבודות הראו את החשיבות של ריצוף מקבילי לצרכים אבחנתיים בגידולי רקמה רכה. בעבודה של Avenarius וחבריו, נערכה בחינה מחדש של גידולי רקמה רכה בילדים, מן השנים 2002–2017. באמצעות ריצוף מקבילי נבחנו כל הדגימות בהן נעשו על פי שיקול דעת הפתולוג בדיקות PCR ראשוניות (אחת או יותר) אך לא סייעו לאבחנה. מתוך 90 דגימות, נמצאו שינויים סומטיים ב-41 (45 אחוזים), וב-25 מהם (27.8 אחוזים) השינוי שנמצא עשוי היה להשפיע על אבחנה וטיפול אילו היה ידוע בזמן אמיתי[5]. בעבודה שמקורה ב-ACC Italian Sarcoma Working Group, נבחנו מחדש 150 גידולי רקמה רכה באמצעות ריצוף מקבילי, לאחר אבחנה של פתולוג ובדיקות מולקולריות ראשוניות (FISH/PCR). בכ-9 אחוזים מהמקרים נמצאה אבחנה מולקולרית שלא אותרה קודם[6]. בעבודה דומה של Ng וחבריו, מתוך 96 גידולי רקמה רכה, ב-15 מקרים (כ-15 אחוזים) נמצאה אבחנה מולקולרית שלא אותרה קודם באמצעות בדיקות PCR/FISH על ידי פאנל של ריצוף מקבילי[7].
ניתן לומר אפוא שאבחנה מולקולרית של גידולי רקמה רכה באמצעים של ריצוף מקבילי, כאשר היא מתווספת על אבחנה מורפולוגית ואימונוהיסטוכימיה, נותנת מענה טוב לאתגר האבחנתי של מגוון רחב של גידולים נדירים. אין ספק שיש משמעות לאבחנה מדויקת לצורכי מחקר, בסיסי או קליני.
את הצורך באבחנה מדויקת לצורכי טיפול כבר בימים אלו נברר כעת.
טיפול מבוסס עיבוד מולקולרי בגידולי רקמה רכה
טיפול מכוון שינויים סומטיים נשנים (recurrent somatic changes) בתת-סוגים היסטולוגיים
טיפול כימי, טיפול במעכבי טירוזין קינאז (tyrosine kinase) וגורמי גדילה, טיפול מכוון לגורמי שעתוק ומנגנונים אפיגנטיים ואימונותרפיה יכולים להינתן באופן מותאם לתת-סוג הגידול. בחלק זה נביא דוגמה לכל אפשרות טיפולית כזאת, ונסביר את התאמתה לתת-הסוג הספציפי.
טיפול כימי בליפוסרקומה מיקסואידית של תאים עגולים - MLPS myxoid round cell liposarcoma
עבודות בגידולי רקמה רכה שבחנו יעילות טיפול כימי קו ראשון מותאם לתת-הסוג ההיסטולוגי מול היעילות של טיפול אחיד בדוקסורוביצין, הידרוכלוריד, איפוספמיד - Doxorubicin, Hydrochloride, Ifosfamide (שהוגדר כטיפול קו ראשון סטנדרטי) הראו ככלל יתרון דווקא לטיפול האחיד על פני אלו שנבחרו על פי תת-הסוג ההיסטולוגי[8][9]. היוצא מכלל זה הוא גידול ממקור שומני ליפוסרקומה מיקסואידית של תאים עגולים (MLPS - Myxoid liposarcoma), אשר טביעת האצבע המולקולרית שלו היא הטרנסלוקציה (q13;p11)(12;16t), הגורמת לאיחוי הגנים FUS ו-DDIT3 (ולעיתים רחוקות יותר טרנסלוקציה הגורמת לאיחוי EWSR1 ו-DDIT3).
התגובה של MLPS ל-Trabectedin (yondelis[10]) (תרופה כימית שהופקה לראשונה ממלפפוני ים) ייחודית לתת-סוג זה מבין גידולי הרקמה הרכה.
באותן עבודות בהן הושווה טיפול מותאם לתת-סוג לטיפול אחיד (בקו ראשון) טיפול ב-Trabectedin ב-MLPS היה היחיד שהראה יעילות זהה לזו של הטיפול האחיד[8].
לפעולה האנטי-נאופלסטית של Trabectedin פנים רבות: הוא מעודד פירוק בפרוטאזום של RNA polymerase II, ועל ידי כך משרה גם שינויים בסביבה האימונולוגית והווסקולרית הקרובה של הגידול, וגם בהפרשת גורמי גדילה וציטוקינים סיסטמית, הוא מעכב תיקון דנ״א במנגנון ה-NER, ועל ידי כך חושף את התאים ללטאליות סינתטית (synthetic lethality) אולם באופן ייחודי ל-MLPS, הקישור של Trabectedin ל-minor groove בדנ"א מונע קשירה של תוצר הטרנסלוקציה האונקוגני FUS-CHOP לאזור ה-major groove של הדנ"א, ובהתאם מונע את הפעולה שלו על המקדמים (promoters) דוגמת pentraxin3 ו-fibronectin1 [11].
עיכוב הפעולה של גורם שעתוק (transcription factor) הוא מנגנון פעולה ייחודי בנוף הטיפולים האנטינאופלסטיים, והיעילות של Trabectedin ב-MLPS קשורה ישירות (לפחות בחלקה) למבנה המולקולרי של הגידול.
מספר עבודות הדגימו את היעילות של Trabectedin ב-MLPS. באחת מהן נבחן Trabectedin מול טיפול אחיד מבוסס Doxorubicin בקבוצת סרקומות הקשורות בהתקה. הניסוי הופסק מבלי שהראה יתרון לאחת הזרועות בשל פרישה גבוהה של חולים, אשר למעשה העידה על יתרון של ה-Trabectedin: הסיבה לפרישה בקבוצת ה-Trabectedin הייתה הזדמנות לכריתת גידול שארי (23.5 אחוזים בקבוצת ה-Trabectedin לעומת 16.2 אחוזים בקבוצת הביקורת), ואילו החלפת טיפול לפני התקדמות הייתה גבוהה יותר בקבוצת הביקורת לעומת קבוצת ה-Trabectedin (24.3 אחוזים לעומת 17.6 אחוזים). כשליש מן החולים במחקר זה היו חולים עם MLPS, והשתייכות לתת-הסוג הזה היוותה גורם פרוגנוסטי טוב בעבודה זו[9].
טיפול מכוון לפעילות יתר של גורמי גדילה וטירוזין קינאז בפיברוסרקומה אינפנטילית (Infantile Fibrosarcoma - IFS)
פיברוסרקומה אינפנטילית (IFS) היא גידול רקמה רכה אופייני לילדות מוקדמת. זהו גידול הרקמה הרכה השכיח ביותר מתחת לגיל שנה, ו-90 אחוזים מן החולים מאובחנים לפני גיל שנתיים. הטיפול ב-IFS הוא כירורגי בעיקר, ופיזור גרורתי אינו שכיח (כ-10 אחוזים המקרים). אולם בעת האבחנה למעלה ממחצית המקרים אינם ניתנים להסרה כירורגית, וזקוקים לטיפול מולטידיסציפלינרי: טיפול תרופתי, ואחריו ניתוח שמרני[12]. מאחר שמעל 80 אחוזים מהחולים צפויים להחלים ממחלתם, חשוב מאוד לצמצם את עומס הטיפול ותופעות הלוואי ארוכות הטווח (כולל נזקי כימותרפיה ונזקים אנטומיים ופונקציונליים של ניתוח).
IFS קשורה ברוב גדול (מעל 85 אחוזים) של המקרים בהתקה ETV6-NTRK3 או EML4-NTRK3, ובמיעוט המקרים בפגמים סומטיים (התקה/מוטציה/חסר חלקי) המערבים BRAF ,NTRK1 ו-MET.
NTRK1, NTRK2, NTRK3 הם חלבונים מקבוצת טירוזין קינאז רצפטור, בעלי זיקה גבוהה לגורמי גדילה ספציפיים. בתגובה להפעלה על ידי גורמי גדילה הם עוברים הומו-דימריזציה, מועברים מן הממברנה אל תוך התא, ושם פועלים על ידי פוספורילציה של שיירי טירוזין להפעלת מסלולי גדילה, הישרדות ופרוליפרציה (RAS/MEK/ERK PI3k/Akt). איחוי החלק התוך תאי של NTRK לגורמי שעתוק דוגמת ETV6, גורמת להפעלה קבועה של ה-NTRK, ולתהליכים התוך תאיים האונקוגניים הנובעים ממנה.
נוספה לאפשרויות הטיפול קבוצת תרופות המעכבות את פעולת ה-NTRK. הן כוללות Larotrectinib (vitrakvi[10]), Entrectinib (rozlytrek[10]) - המאושרות לשימוש על ידי ה-FDA, ו-Repotrectinib, Lestaurtinib, Selitrectinib ואחרות הנמצאות בשלבי אישור מתקדמים.
Larotrectinib היא התרופה הראשונה שאושרה לשימוש בכל גיל לטיפול בגידולים הקשורים בהתקה של NTRK1, NTK2, NTRK3. ב-IFS שיעור התגובה לטיפול זה הוא 96 אחוזים, ושיעור תופעות הלוואי המשמעותיות (דרגה 3–4) קטן מ-5 אחוזים[13].
במקרי IFS בהם נדרש טיפול סיסטמי בנוסף על טיפול כירורגי, קיימת הסכמה על טיפול במעכבי NTRK כקו ראשון במחלה גרורתית או מסכנת חיים באופן מיידי. השאלה אם תרופות דוגמת Larotrectinib ו-Entrectinib יכולות להחליף כבר בימים אלו טיפול כימותרפי בכל המקרים עדיין פתוחה, והבחירה בהם או בכימותרפיה סיסטמית נתונה בידי הרופא המטפל והמשפחה[14].
טיפול מכוון לגורמי שעתוק ומנגנונים אפי-גנטיים בסרקומה סינוביאלית (synovial sarcoma)
גורמי גדילה וטירוזין קינאזות הם אמנם מערכת מורכבת, אך הם מוכרים לנו זמן רב, מסלולי פעולתם מתוארים היטב, מתרחשים על פני ממברנת התא או בציטופלזמה, ומהווים מטרה נוחה לטיפול. אלא שהם מאפיינים מיעוט קטן של גידולי הרקמה הרכה.
גורמי שעתוק וחלבוני בקרה אפי-גנטית הם מערכת מורכבת עוד יותר. המבנה התלת- ממדי של גורמי שעתוק לא תמיד יציב, פעולתם ממוקמת בגרעין התא, מתוארת פחות, ולפיכך קשה יותר לכוון אליהם טיפול. דוגמה לטיפול המכוון לגורמי שעתוק ובקרה אפי-גנטית היא סרקומה סינוביאלית.
זהו גידול רקמה רכה שממוקם לרוב ברקמות העמוקות של הגפיים, במתבגרים ובמבוגרים צעירים. טביעת האצבע המולקולרית שלו היא הטרנסלוקציה (t(X;18) (p11.2;q11.2, המערבת את הגן SS18, ואחד מהגנים SSX1 או SSX2. זהו גידול רגיש יחסית לכימותרפיה קונבנציונלית דוגמת אנטרציקלינים, Ifosfamide, וגם למעכבי טירוזין קינאז דוגמת pazopanib (votrient)[10].
ההבנה של מנגנון הפעולה של SS18 והשינוי בפעולתו שגורמת ההתקה ל-SSX אפשרו פיתוח תרופות מכוונות למטרה זו.
SS18 הוא מרכיב אחד של קומפלקס חלבוני - SWI/SNF. קומפלקס זה מורכב מ-15 מרכיבים חלבוניים, שחלקם משותפים לכל הרקמות, וחלקם ייחודיים לרקמה. לקומפלקס SWI/SNF יש תפקיד חשוב בתיאום ותזמון ביטוי של גנים על ידי חשיפה של מעצמים (enhancers) ומקדמים (promoters) לפעולת גורמי שעתוק באמצעות מודיפיקציה של היסטונים, מתילציה של דנ"א ועיצוב מחדש של כרומטין.
כאשר חלבון הכימרה SSX-SS18 לוקח את מקומו של ה-SS18 המקורי הוא מונע את הקישור של מרכיב נוסף -SMARCB1/ INI1 למקומו בקומפלקס, ומשנה את תפקודו של הקומפלקס השלם ואתרי הקישור שלו לדנ"א. באותם אתרים אליהם נקשר עתה קומפלקס SWI/SNF ה"פגום" הוא מונע קישור של קומפלקס אחר - PRC (Polycomb Repression Complex), וכך נוצרת תמונה חריגה של ביטוי גנים ויצירת חלבונים של סרקומה סינוביאלית, על המאפיינים הממאירים והאינונומודולטוריים שלה[15][16].
ההבנה של המערכת האפיגנטית המורכבת הזאת מאפשרת טיפול מכוון מטרה מולקולרית - כך נמצאים כבר היום בשימוש מעכבי HDAC (Histone deacetylase inhibitors), ותרופה המכוונת לחלבון BRD9 (מרכיב של התצורה הלא-קלאסית של הקומפלקס SWI/SNF, FHD-609) נמצאת לקראת ניסוי פאזה ראשונה בבני אדם.
אימונותרפיה בסרקומה סינוביאלית (synovial sarcoma)
תת-סוגים של גידולי רקמה רכה שונים זה מזה באימונוגניות שלהם: עומס המוטציות וביטוי גנים ספציפיים המייצרים תגובה אימונית, כמו גם במאפיינים האימונולוגיים של סביבת הגידול: כמות תאי ה-T המסנינים את הגידול, הקלונאליות של תאי T (אולי כביטוי של ספציפיות לחלבוני גידול), היחס בין תאי T אפקטוריים (+CD8) לבין תאי T רגולטוריים (+FOXP3) בגידול, ביטוי חלבוני checkpoint דוגמת PD1 ו-PDL1, התמיינות המאקרופאגים בסביבת הגידול לפנוטיפ M1 המעודד פעילות תאי T לפנוטיפ M2 המעכב אותה.
לאור המורכבות הטכנולוגית באפיון סביבת הגידול (המצריכה למשל, שימוש ב-single cell PCR) עבודות על אפיון אימונולוגי של תת-סוגי גידולים של רקמה רכה הופיעו במאה ה-21, והשימוש הקליני בהן ראשוני מאוד. ניתן לומר, שתת-סוגים מסוימים של גידולים (למשל כאלו הכרוכים בהתקה), הם גידולים "קרים" אימונולוגית, ואילו תת-סוגים מסוימים "חמים" אימונולוגית. לא מפתיע אם כן, שהיעילות של אימונותרפיה בגידולי רקמה רכה אינה אחידה, ותלויה בתת-הסוג של הגידול. למשל: גידולים הנוטים לבטא PD-L1, וכאלו המוסננים יותר על ידי לימפוציטים עם ביטוי של CD8, הם אלו המראים תגובה לטיפול במעכבי נקודות בקרה (checkpoint inhibitors), ובמיוחד לשילוב של שתי תרופות מקבוצה זו.
דוגמה לגישה זו היא טיפול מכוון NY-ESO בסרקומה סינוביאלית.
חלבונים מקבוצת ה-cancer testis antigen הם קבוצה של כ-70 חלבונים, המבוטאים באופן תקין על תאי זרע ותאי שליה, אינם מתבטאים כלל על תאים סומטיים תקינים, ומתבטאים באופן אברנטי על תאי גידול במגוון ממאירויות.
אחד החלבונים האלה, NY-ESO (1- New York Esophageal Squamous Cell Carcinoma), מתבטא באופן הומוגני (ב-50 עד 70 אחוזים מהתאים) בכ-80 אחוזים ממקרי סרקומה סינוביאלית, ובכ-90 אחוזים מהמקרים של ליפוסרקומה מיקסואידית/של תאים עגולים - myxoid/round cell liposarcoma.
NY-ESO יוצר תגובה אימונית מדידה, הומורלית ותאית, גם ללא התערבות אולם ניתן להעצים אותה על ידי תמרון מערכת החיסון.
טכניקה אחת היא מודיפיקציה של תאי T של החולה: בתאי T אוטולוגיים, מושתל באמצעות רטרו-וירוס קולטן (קולטן תא T) לאחד האפיטופים של NY-ESO (האפיטופ אשר בו נעשה שימוש במרבית העבודות מוצג על גבי 0201 MHC class 1 HLA-A, ולכן הקולטן ספציפי ל-MHC זה). התאים מוחזרים לחולה אחרי טיפול כימי סיסטמי (שמטרתו לגרום לדיכוי חיסוני תאי - lymphodepletion).
בשתי קבוצות חולים קטנות עם סרקומה סינוביאלית מפושטת, 50 עד 61 אחוזים מהחולים הראו תגובה אובייקטיבית לטיפול, שנמשכה בין שלושה חודשים לשלוש שנים, ומשך תגובה חציוני של 30 שבועות[17][18].
מחקרים קליניים נוספים בטיפול תאי בסרקומה סינוביאלית מנסים לשלב בין תאי T שעברו מודיפיקציה למעכבי נקודות בקרה, לייצר תאי T הנושאים קולטנים ליותר מחלבון או אפיטופ אחד או לבחור מתוך רפרטואר תאי ה-T המסנינים את הגידול את אלו הספציפיים לחלבונים או אפיטופים מסוימים ולהחזירם לחולה לאחר הדגרה מחוץ לגוף.
טכניקה אחרת היא "חיסון" על ידי חלבון NY-ESO: "הדבקה" של החולה בלנטיוירוס (lentivirus) ספציפי לתאים דנדריטיים הנושא איתו את ה-NY-ESO, כך שהתאים הדנדריטיים יציגו את החלבון לתאי מערכת החיסון (ובעיקר תאי T) של המטופל. לתהליך הזה ניתן להוסיף אגוניסטים נוספים של מערכת החיסון. בעבודה אחת שבדקה תגובה ל"חיסון" NY-ESO, בשילוב עם boost של NY-ESO ואגוניסט ל-toll like receptor 4 שניתן מקומית, ב-61.9 אחוזים מחולי סרקומה סינוביאלית הושגה שליטה במחלה למשך זמן חציוני של 4.6 חודשים[19]. ניסויים קליניים בוחנים כעת יעילות ורעילות "חיסונים" מכווני NY-ESO בשילוב עם אימונותרפיה נוספת.
טיפול מכוון שינויים סומטיים וסביבת גידול (Somatic changes) אימונולוגית - אגנוסטי לגידול
גישה הפוכה כביכול למגמה לטפל בסרקומות בהתאם לתת-הסוג אך מבוססת גם היא על עיבוד מולקולרי של הגידול, היא הניסיון להפוך את המאפיינים המולקולריים הגורמים להפרעה בפרוליפרציה, מיגרציה, וסקולריזציה, מטבוליזם, מוות והישרדות תקינים של תאים למטרה בטיפול, ללא תלות בסוג הממאירות בה נמצאו.
מספר קבוצות מחקר (Peds-MiOncoSeq, BASIC3, INFORM, MOSCATO-01, MSK-IMPACT, iCat, MAPPYACT) ואחרות הראו שניתן לבצע ריצוף מקבילי של גידולים מוצקים בילדים על פלטפורמות הנמצאות בשימוש קליני. קבוצות אלו הראו שיעורים גבוהים של הצלחה טכנית בביצוע הבדיקה ובנו מנגנוני דיווח והעברת מידע למטופלים. מטרות טיפוליות נמצאו בעבודות אלו ב-35–60 אחוזים מהגידולים, אך רק למיעוט המטופלים (3 עד 18 אחוזים) ניתן טיפול על פי תוצאות העיבוד המולקולרי.
על פי מידע זה תוכננו מחקרי המשך. מחקרים אלו מכוונים למטרות טיפוליות נדירות, כאלו הקיימות במיעוט מהגידולים בכל תת-סוג, ולכן מתכונתם שונה מזו שהייתה מקובלת בעבר.
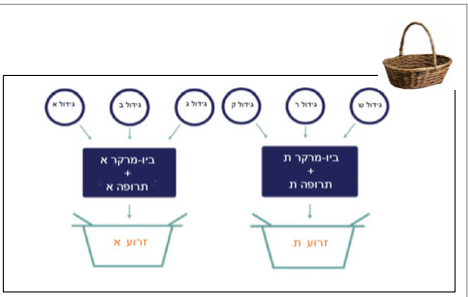
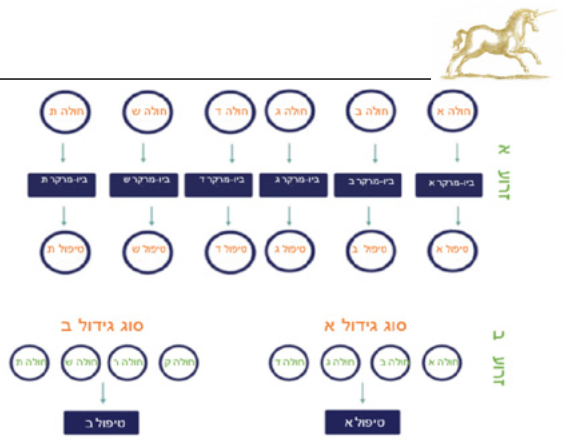
מחקר סל (Basket study) - מחקר העשוי לרוב ממספר זרועות, בכל אחת ניתן טיפול שונה. הטיפול נקבע על פי ביו-מרקר מולקולרי, ללא תלות בסוג הגידול.
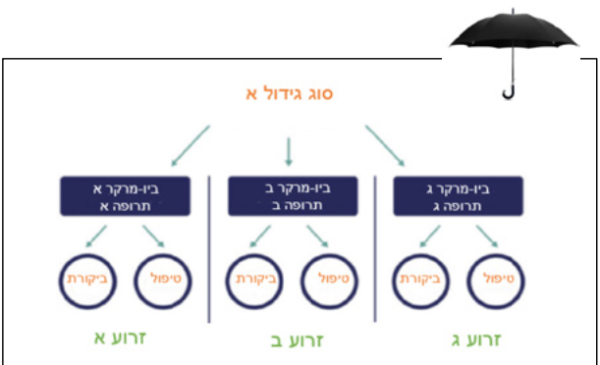
מחקר מטרייה (Umbrella study) - מחקר שבו למחלה יחידה ניתן טיפול שונה בזרועות מחקר שונות, על פי ביו-מרקר המאפיין חלק זה מן החולים.
מחקר בן נבדק אחד (N of one study) - קבוצת מומחים בוחרת טיפול מותאם אישית למחלה והמאפיינים המולקולריים שלה לכל חולה בנפרד. נתוני תוצאות הטיפול נאספים עבור כל החולים.
גם המדדים בהם נבחנות תוצאות המחקרים שונים לעיתים מאלו שהיו מקובלים בעבר. למשל, במחקרים בהם נבדקות קבוצות חולים קטנות ללא קבוצת ביקורת, לאחר מספר קווי טיפול קודמים, מושווה משך התגובה לטיפול הנוכחי למשך התגובה לטיפול הקודם שקיבל אותו חולה, וה"תוצאה" היא היחס ביניהם.
המבנה המאפשר מחקר בקבוצות הגדולות ביותר הוא מבנה מחקר סל.
שני מחקרי סל גדולים, שונים זה מזה מתודולוגית, מנוהלים בילדים: ה-NCI pediatric MATCH (Molecular Analysis for Therapy Choice) מנוהל על ידי קבוצה אמריקאית - COG (Children's Oncology Group) - מוכללים בו ילדים ומתבגרים עם ממאירות סולידית, היסטיוציטרית ולימפומה שאינה הודג'קין עמידה לטיפול או נשנית. חומר גנטי מדגימה של הגידול עובר ריצוף מקבילי לזיהוי מוטציות (דנ"א) והתקות (רנ"א) על פלטפורמה שנבנתה במיוחד עבור מחקר ה-MATCH. על פי תנאי המחקר, כאשר מזוהים שינויים סומטיים שנקבעו מראש, המטופל מופנה לטיפול בתרופה יחידה מכוונת לפגם הסומטי הספציפי. פתוחות שבע זרועות במחקר זה, במסגרתן ניתנות התרופות LY3023414, Olaparib (Lynparza)[10], Larotrectinib, Tazemetostat, Selumetinib, Ensartinib, ו-Vemurafenib (Zelboraf)[10] לחולים שבגידולים שלהם נמצאו פגמים במסלול mTor, הפרעות תיקון דנ"א, התקה המערבת NTRK, פגמים בקומפלקסים הפעילים אפיגנטית /SWI SNF ו-PRC, פגמים ב- ALK/ROS1 והמוטציה BRAF V600 בהתאמה. זרועות נוספות צפויות להתווסף ככל שיצטבר מידע על יעילות קלינית/פרה-קלינית של תרופות נוספות. מחקר זה יכלול לפחות 20 מטופלים בכל זרוע, כשהתוצאה הנבחנת היא תגובה מדידה אובייקטיבית לטיפול.
ה-AcSe-ESMART מנוהל על ידי קבוצה אירופית, כחלק ממחקרי ה-Innovative Therapies for Children with Cancer (ITCC) העיבוד הגנטי של הגידול יכול להיעשות על אחת ממספר פלטפורמות (INFORM ,MAPPYACT ואחרות) נכללים בו ילדים ומתבגרים עם גידול מוצק או המטולוגי עמיד לטיפול או נשנה. קבוצת מומחים (Molecular Tumor Board) עורכת דיון בתוצאות העיבוד הגנטי, ומכוונת את המטופל לאחת מזרועות המחקר במסגרת ה-ESMART או למחקר אחר בתוך קבוצת ה-ITCC (בין אם מוגבל על ידי אבחנה או מחקר בתרופה יחידה אגנוסטי לאבחנה). שבע זרועות פתוחות במחקר זה, בחלקן משולבות תרופות מכוונות מטרה גנומית עם כימותרפיה קונבנציונלית או קרינה.
הן מכוונות לפגמים בתיקון דנ"א: AZD1775 בשילוב עם Carboplatin או אולפאריב עם Temozolomide (Temodal)[10], מסלול ה-mTor: Vistusertib או Vistusertib בשילוב עם Toptecan (Hycamtin [10]) - טמוזולומיד cyclin dependent kinase 4/6 Ribociclib (Kisqali[10]), וטופוטקאן או ריבוציקליב ו-Everolimus (Afinitor[10]), ו-1-PD (Nivolumab - Opdivo[10]) עם cyclophosphamide וקרינה.
מספר גדול של מחקרים בילדים בנויים כמחקרי סל בעלי זרוע אחת: Larotrectinib לגידולים עם התקה המערבת NTRK (NCT02637687), Tazemetostat לגידולים בהם חסר 1-INI (NCT02601937), Crizotinib (Xalkori[10]) לגידולים עם הפרעה ב-1-ALK ROS או MEK (NCT02034981), Ceritinib (zykadia[10]) לגידולים עם הפרעה ב-ALK (NCT01742286), Dabrafenib (tafinlar[10]) ו-Trametinib (mekinist[10]) לגידולים עם הפרעה ב-BRAF, (NCT02684058) ו-Afatinib (Giotrif [10]) לגידולים עם הפרעה במסלול ה-ErbB (NCT02372006). שתי דוגמאות למחקר סל, שבעקבותיהן אישר ה-FDA (Food and Drug Administration) וגם משרד הבריאות הישראלי טיפול מכוון מטרה ביולוגית ואגנוסטי לאבחנה הם טיפול בLarotrectinib לגידול מכל סוג שבו יש התקה של NTRK1/NTRK2/NTRK3, וטיפול במעכבי נקודות בקרה לכל גידול שיש בו הפרעה בתיקון דנ"א הגורמת לאי יציבות גנומית (microsatellite instability).
התקה הכוללת NTRK1/NTRK2/NTRK3 קיימת בשכיחות גבוהה במספר קטן של גידולים, אך בשכיחות של מתחת ל-1 אחוז מופיעה במגוון רחב של גידולים. בתוצאות שנאספו במספר ניסויים קליניים, נרשמה תגובה אובייקטיבית ב-79 אחוזים מהמטופלים וב-20 אחוזים מן המגיבים - תגובה מלאה, משך זמן תגובה חציוני של כשלוש שנים (35.2 חודשים) ותופעות לואי משמעותיות (SAE) בפחות מ-5 אחוזים מהחולים.
התרופה נמצאת בניסויים קליניים כטיפול קו ראשון בחולים עם התקה הכוללת NTRK, ללא התחשבות באבחנה ההיסטולוגית[13].
בגידולים בהם קיים פגם במנגנון הפועל להחלפת בסיסים שהוכנסו באופן לא תואם בעת שעתוק דנ"א (mismatch repair) מצטברים שינויים גנומיים סומטיים: שינויים באזורי מיקרוסטליטים (High Microsatellite Instability - MSI-H) וריבוי נאו-אנטיגנים. מצב זה הופך את הגידול לרגיש יותר לאימונותרפיה, ובפרט לטיפול במעכבי נקודות בקרה. מידע מצטבר מחמש עבודות שכללו ביחד 149 חולים עם MSI-H/ MMRd (KN-012, KN-028, KN-016, KN-158, KN-164), הראה שיעור תגובה של 39.7 אחוזים ושיעור תגובה מלאה של 7 אחוזים. כ-80 אחוזים מהתגובות נמשכו מעל שישה חודשים. על בסיס מידע זה אושר Pembrolizumab (Keytruda[10]) לשימוש במחלה עמידה או מתקדמת, בכל מחלה עם MSI-H/dMMR [20].
סיכום
זיהוי פגמים גנומיים סומטיים בגידול ואפיון אימונולוגי של גידולים באמצעים של ריצוף מקבילי, מאפשרים לנו סיווג הגידולים לתת-קבוצות אבחנתיות נכונות, ואולי אף חשוב מכך - לתת-קבוצות בעלות פגמים מולקולריים משותפים. מאמצי מחקר רבים מושקעים בפיתוח טכנולוגיות ותרופות מכוונות למטרות מולקולריות ספציפיות, וגם במחקר קליני מכוון מידע מולקולרי.
תוצאות ראשוניות של מחקרים קליניים מבוססי מידע מולקולרי הן לא רבות.
במונחים של תוצאות טיפול בסרטן בילדים - ההצלחות הן משמעותיות אך חלקיות במרבית הקבוצות, ומצוינות בתת-קבוצות קטנות ספציפיות.
יש להניח שבעתיד הקרוב נלמד לבחור טוב יותר את המטרות המולקולריות של הטיפול, לשלב כמה מטרות בטיפול בו זמנית על מנת למנוע עמידות, נגדיל את מבחר התרופות מכוונות המטרה ואת מבחר ההתערבויות במערכת החיסון, ונלמד לעשות שימוש באמצעים טכנולוגיים נוספים (כמו ריצוף מקבילי של דנ"א גידולי ישירות מן הדם).
ביבליוגרפיה
- ↑ Mertens F, Antonescu CR, Mitelman F. Gene fusions in soft tissue tumors: recurrent and overlapping pathogenetic themes. Genes Chromosomes Cancer. 2016 Apr;55(4):291-310. Epub 2015 Dec 18.
- ↑ Arbiser ZK, Folpe AL, Weiss SW. Consultative (expert) second opinions in soft tissue pathology: analysis of problem-prone diagnostic situations. Am J Clin Pathol. 2001 Oct;116(4): 473-6.
- ↑ Randall RL, Bruckner JD, Papenhausen MD, et al. Errors in diagnosis and margin determination of soft-tissue sarcomas initially treated at non-tertiary centers. Orthopedics. 2004 Feb;27(2):209-12.
- ↑ Thway K, Fisher C. Histopathological diagnostic discrepancies in soft tissue tumours referred to a specialist centre. Sarcoma. 2009; 2009:741975. Epub 2009 May 27.
- ↑ Avenarius MR, Miller CR, Arnold MA, et al. Genetic characterization of pediatric sarcomas by targeted RNA sequencing. J Mol Diagn. 2020 Oct;22(10):1238-45. Epub 2020 Aug 1.
- ↑ Racanelli D, Brenca M, Baldazzi D, et al. Next¬generation sequencing approaches for the identification of pathognomonic fusion transcripts in sarcomas: the experience of the Italian ACC Sarcoma Working Group. Front Oncol. 2020 Apr 15;10:489.
- ↑ Chang KTE, Goytain A, Tucker T, et al. Development and evaluation of a pan-sarcoma fusion gene detection assay using the NanoString nCounter Platform. J Mol Diagn. 2018 Jan;20(1):63-77. Epub 2017 Nov 20.
- ↑ 8.0 8.1 Gronchi A, Ferrari S, Quagliuolo V, et al. Histotype- tailored neoadjuvant chemotherapy versus standard chemotherapy in patients with high-risk soft-tissue sarcomas (ISG-STS 1001): an international, open¬label, randomised, controlled, phase 3, multicentre trial. Lancet Oncol. 2017 Jun;18(6):812-22. Epub 2017 May 9.
- ↑ 9.0 9.1 Blay JY, Leahy MG, Nguyen BB, et al. Randomised phase III trial of trabectedin versus doxorubicin-based chemotherapy as first-line therapy in translocation- related sarcomas. Eur J Cancer. 2014 Apr;50(6):1137- 47. Epub 2014 Feb 7.
- ↑ 10.00 10.01 10.02 10.03 10.04 10.05 10.06 10.07 10.08 10.09 10.10 10.11 10.12 10.13 10.14 10.15 10.16 או תרופות המכילות חומר פעיל זהה או דומה, בעלות שמות מסחריים אחרים
- ↑ Assi T, Kattan J, Rassy EE, et al. A comprehensive review of the current evidence for trabectedin in advanced myxoid liposarcoma. Cancer Treat Rev. 2019 Jan;72:37-44. Epub 2018 Nov 15.
- ↑ Orbach D, Rey A, Cecchetto G, et al. Infantile fibrosarcoma: management based on the European experience. J Clin Oncol. 2010 Jan;28(2):318-23. Epub 2009 Nov 16.
- ↑ 13.0 13.1 Hong DS, DuBois SG, Kummar S, et al. Larotrectinib in patients with TRK fusion-positive solid tumours: a pooled analysis of three phase 1/2 clinical trials. Lancet Oncol. 2020 Apr;21(4):531-40. Epub 2020 Feb 24.
- ↑ Orbach D, Sparber-Sauer M, Laetsch TW, et al. Spotlight on the treatment of infantile fibrosarcoma in the era of neurotrophic tropomyosin receptor kinase inhibitors: international consensus and remaining controversies. E J Cancer. 2020 Sep;137:183-92. Epub 2020 Aug 9.
- ↑ Kadoch C, Crabtree GR. Reversible disruption of mSWI/SNF (BAF) complexes by the SS18-SSX oncogenic fusion in synovial sarcoma. Cell. 2013 March 28;153(1):71-85.
- ↑ Jerby-Arnon L, Neftel C, Shore ME, et al. Opposing immune and genetic mechanisms shape oncogenic programs in synovial sarcoma. Nat Med. 2021 Feb;27(2)289-300. Epub 2021 Jan 25.
- ↑ Robbins PF, Kassim SH, Tran TLN, et al. A pilot trial using lymphocytes genetically engineered with an NY- ESO-1-reactive T cell receptor: long term follow up and correlates with response. Clin Cancer Res. 2015 Mar 1;21(5):1019-27. Epub 2014Dec 23.
- ↑ D'Angelo P, Melchiori L, Merchant MS, et al. Antitumor activity associated with prolonged persistence of adoptively transferred NY-ESO-1c259 T cells in synovial sarcoma. Cancer Discov. 2018 Aug;8(8):944-57. Epub2018Jun 11.
- ↑ Somaiah N, Chawla ST, Block MS, et al. A phase 1b study evaluating the safety, tolerability, and immunogenicity of CMB305, a lentiviral-based prime-boost vaccine regimen, in patients with locally advanced, relapsed, or metastatic cancer expressing NY-ESO-1. Oncoimmunology. 2020 Nov;19(1):1847846.
- ↑ Marcus L, Lemery SJ, Keegan P, et al. FDA approval summary: pembrolizumab for the treatment of microsatellite instability-high solid tumors. Clin Cancer Res. 2019 Jul 1;25(13):3753-58. Epub 2019 Feb 20.
המידע שבדף זה נכתב על ידי ד"ר איריס קוונצל - מערך המטואונקולוגיה והשתלות מח עצם ילדים, המרכז הרפואי שיבא, תל השומר


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק