אבחון וטיפול בזיהום בדרכי השתן בילדים - הנחיה קלינית
הופניתם מהדף הנחיה קלינית בנושא אבחון וטיפול בזיהום בדרכי השתן בילדים לדף הנוכחי.
|
| ||
|---|---|---|
| אבחון וטיפול בזיהום בדרכי השתן בילדים | ||
| ||
| הוועדה המקצועית | איגוד רופאי הילדים, איגוד רופאי המשפחה, האיגוד הישראלי לנפרולוגיית ילדים, החברה הישראלית לרפואה ילדים בקהילה (חיפ"א), החברה הישראליח לפדיאטרייה קלינית (חיפ"ק), החוג למחלות זיהומיות בילדים | |
| עריכה | חברי הוועדה | |
| תחום | אורולוגיה, ילדים | |
| קישור | באתר doctorsonly | |
| תאריך פרסום | דצמבר 2022 | |
| הנחיות קליניות מתפרסמות ככלי עזר לרופא/ה ואינן באות במקום שיקול דעתו/ה בכל מצב נתון | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – זיהום בדרכי השתן
הקדמה
זיהום בדרכי השתן (זד"ש) מהווה את אחת הסיבות השכיחות לביקור אצל רופאים ולטיפול אנטיביוטי בקהילה. במסגרת מדיניות של הנחלת השימוש המושכל באנטיביוטיקה בקרב רופאי הילדים בקהילה, חובר בשנת 2014 מסמך קווים מנחים לאבחון וטיפול בזיהום ראשון בדרכי השתן בילדים. בשנת 2021 בוצע עדכון נוסף של ההנחיות על ידי ועדה מקצועית שכללה: נציגים מהחוג למחלות זיהומיות בילדים, החוג לאורולוגיה ילדים, החוג לנפרולוגיה ילדים ורופאי ילדים בקהילה. ההנחיות מיועדות לכל הרופאים המטפלים בילדים. להנחיות אלו נוספו פרקים חדשים הדנים בהתוויות לטיפול אנטיביוטי מונע, המלצות לבירור הדמייתי, הצורך בייעוץ נפרולוגי ואורולוגי, והגישה להפרעה בתפקוד השלפוחית והמעי בילדים עם זד"ש.
תמצית המלצות הוועדה לאבחון, טיפול ובירור של זד"ש
המלצות לאבחנה של זד"ש
- יש לחשוד בזד"ש במקרים הבאים
- חום ביילוד (עד גיל חודש)
- חום בגילאי 1–3 חודשים (בהיעדר מקור ברור אחר לחום)
- בנות עד גיל 2 שנים, בנים שאינם נימולים עד גיל שנה, ובנים נימולים עד גיל 6 חודשים עם חום (מעל 39 מעלות צלזיוס) הנמשך 2 יממות או יותר (בהיעדר מקור ברור אחר לחום)
- בכל גיל בנוכחות אחד מהבאים:
- תסמינים המחשידים לזד"ש
- חום ללא מקור ברור בנוכחות היסטוריה של זיהום קודם בדרכי השתן, או מום במערכת השתן
- חום ממושך ללא מקור
בדיקת שתן כללית משקית יכולה לשמש כבדיקת סקר בעלת ערך מנבא גבוה שלילי לקיום זד"ש. באם בדיקת שתן כללית תקינה, אין חובה לשלוח גם שתן לתרבית, למעט במצבים הבאים:
- עד גיל 2 חודשים (או עד גיל 8 ימים על פי ההנחיות האמריקאיות העדכניות)
- בחשד קליני גבוה לזד"ש
- בנוכחות תמונה קלינית של אלח דם
אין להתחיל טיפול אנטיביוטי בחשד לזד"ש מבלי לשלוח תרבית שתן. תרבית שתן משקית אינה מומלצת כאמצעי לאבחנת זד"ש בשל הסיכוי הגבוה לתוצאה כוזבת חיובית בתרבית שתן. תרבית שתן הנלקחת בצורה זו היא אינפורמטיבית רק אם תוצאתה שלילית.
המלצות לטיפול אנטיביוטי
ישנה חשיבות לאבחון מוקדם והתחלת טיפול מהר ככל האפשר, רצוי תוך 48 שעות מתחילת החום, במתן פומי או תוך-ורידי/שרירי.
- הטיפול המומלץ במסגרת הקהילה
יש להבחין בין ציסטיטיס (דלקת בכיס השתן) ובין פיילונפריטיס (זיהום ברקמת הכליה).
בדלקת בשלפוחית (Cystitis) מומלץ טיפול אמפירי בתכשיר אנטיביוטי פומי, כגון: (Trimethoprim-sulphametoxazole (TMP-SMX, Nitrofurantoin או Cephalexin. משך הטיפול המקובל הוא 3 עד 5 ימים.
בדלקת בכליה (Pyelonephritis) יש לשקול טיפול אמפירי תוך-ורידי/שרירי בשל שיעור עמידות גבוה לתכשירים פומיים. האופציה העדיפה היא Gentamicin כאשר החלופה יכולה להיות Ceftriaxone.
ניתן להתחיל טיפול אנטיביוטי פומי במסגרת הקהילה בתינוקות מעל גיל 3 חודשים כאשר התמונה הקלינית אינה חמורה, בהיעדר מחלות רקע משמעותיות או סימני ציחיון, וכשניתן להבטיח היענות מלאה לטיפול פומי.
חלופות עדיפות לטיפול פומי אמפירי הן: Amoxicillin-Clavulanate או Cefuroxime. בילדים עם מומים ידועים בדרכי השתן, או בילדים עם זיהומים חוזרים שנמצאים תחת טיפול מניעתי יש צורך לשקול גם כיסוי אמפירי לחיידקים כגון: Pseudomonas aeruginosa ו-Enterococcus עד לקבלת תשובת תרבית.
לאחר קבלת תשובת תרבית השתן יש להתאים את הטיפול האנטיביוטי לסוג החיידק ורגישותו.
בדלקת בכליה משך הטיפול הוא לרוב 7 עד 10 ימים כאשר ישנה תגובה טובה לטיפול ובהיעדר סיבוכים. תגובה קלינית הולמת לטיפול נצפית כמעט תמיד תוך 72 שעות מתחילתו. חום המתמיד מעבר ל-72 שעות, בעיקר אם מלווה גם בחוסר שיפור קליני ומעבדתי, מצריך בחינה מחדש של האבחנה ואפשרות של סיבוכים כגון: מורסה כלייתית או נפרוניה באמצעות סונר דרכי שתן. אם קיימת תגובה קלינית לטיפול, אין צורך בתרבית שתן חוזרת לאחר סיום הטיפול או במהלכו.
המלצות לבירור בעקבות זד"ש
- סונר כליות ודרכי שתן מומלץ במקרים הבאים
- לאחר אירוע ראשון של זיהום בכליה
- לאחר 2 אירועים של זיהום בשלפוחית
(בילדים גמולים מומלץ שבדיקת הסונר תכלול גם בדיקת התרוקנות שלפוחית ומדידת שארית שתן)
- הפנייה לנפרולוג/אורולוג ילדים מומלצת במקרים הבאים
- לאחר 2 אירועים של זיהום בכליה
- במקרה של סונר כליות לא תקין
- זיהומים בדרכי השתן המלווים בתסמינים המתאימים לליקוי בתפקוד השלפוחית והמעי במקרים עמידים לטיפול התנהגותי (ראו סעיף 10)
- במקרים של תפקוד כלייתי לא תקין חובה להפנות לנפרולוג ילדים
בדיקות הדמיה נוספות תתבצענה בהתאם לשיקול דעתו של נפרולוג/אורולוג מטפל ובהן:
- מיפוי כליות (DMSA) Dimercapto succinic acid להערכת קיומן של צלקות בכליה או אזורי דיספלזיה (כעבור 4 עד 6 חודשים מחלוף הזיהום) יש לשקול במצבים הבאים:
- בעקבות אירועים חוזרים של זד"ש המלווה בחום - Febrile UTI (FUTI)
- כאשר עולה חשד לצלקות כלייתיות בסונר
- VCUG (Voiding cystourethrogram) לאור חוסר אחידות בהמלצות בספרות ומחלוקות בין מומחים בתחום, ההחלטה על ביצוע VCUG נתונה לשיקול דעתו של נפרולוג/אורולוג מטפל ותיבחן בכל מקרה לגופו
המלצות לטיפול אנטיביוטי מונע
מחקרים שונים הראו תוצאות סותרות לגבי יעילותו של טיפול אנטיביוטי מניעתי במניעת זיהומים חוזרים בדרכי השתן וצלקות.
- מומלץ לשקול טיפול אנטיביוטי מניעתי בייעוץ נפרולוג/אורולוג במקרים הבאים
- לאחר שני אירועי זיהום בכליה. יש הדוגלים במתן טיפול אנטיביוטי מונע לאחר שני אירועי זיהום בכליה (ללא ביצוע VCUG) עד להשלמת מיפוי DMSA כעבור 4 עד 6 חודשים מהזיהום האחרון. ההחלטה על המשך טיפול אנטיביוטי מונע וביצוע VCUG מתקבלת בהתאם לנוכחות צלקות במיפוי DMSA. גישה אחרת היא לבצע VCUG לאחר שני אירועי זיהום בכליה, בעיקר כאשר יש סבירות גבוהה לקיומו של רפלוקס עם צורך בתיקון ניתוחי
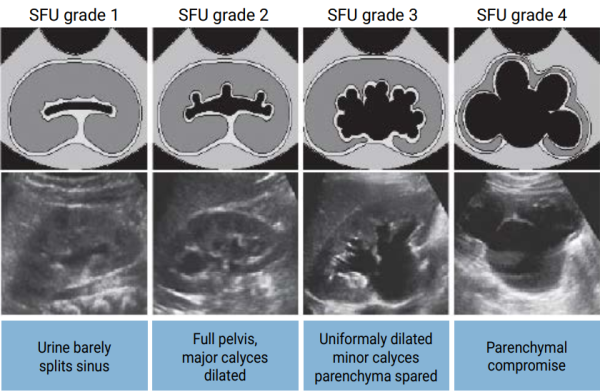
- בילודים עם הידרואורטרונפרוזיס או הידרונפרוזיס משמעותי על פי סונר (SFU דרגה 3–4) או בחשד לחסימה בדרכי השתן
- זיהומים חוזרים בדרכי השתן בנוכחות ליקוי בתפקוד השלפוחית והמעי Bladder and Bowel Dysfunction (BBD) (שאינם על רקע פגיעה עצבית) עד לטיפול בליקוי
התכשירים האנטיביוטיים המועדפים למניעה הם TMP-SMX או Nitrofurantoin. טיפול בתכשיר Cephalexin הוא טיפול טוב, אך עלול להשרות עמידויות בחיידקי המעיים ולכן, יינתן בהיעדר חלופה אחרת לפי שיקול דעתו של הרופא המטפל. אין חובה להתאים את הטיפול המניעתי לרגישות החיידק בזד"ש.
המלצות לליקוי בתפקוד השלפוחית, המעי והסוגרים
לרופא הילדים תפקיד משמעותי באבחון וטיפול ראשוני בהפרעות אלו אצל ילדים עם זיהומים חוזרים בדרכי השתן. חשוב לברר אם הילד נוטה להתאפק בהטלת שתן, והאם יש תמרוני התאפקות. יש לבצע הערכת חומרת תסמיני תפקוד השלפוחית בנוסף, להערכת עצירות ותפקוד מערכת העיכול. בנוסף, יש לברר סוגיות התנהגותיות או פסיכוסוציאליות חריגות, אשר עשויות להיות קשורות להפרעות בהטלת השתן והצואה. במהלך הבדיקה הגופנית חשוב להתמקד בבדיקת הבטן, אברי המין ופי הטבעת. המשך תהליך האבחון של חומרת הבעיה יכלול שאלון הפרעה בהטלת השתן, הערכת תצורת צואה, יומן השתנה וסונר של דרכי השתן (כולל לאחר התרוקנות השלפוחית). הטיפול הראשוני בהפרעה בתפקוד השלפוחית והמעי הוא טיפול התנהגותי הכולל השתנה יזומה כל 2 או 3 שעות לילדים הנוטים להתאפק, שיפור ההיגיינה בגניטליה, שתיית מים מרובה לילדים הממעטים בשתייה וטיפול בעצירות. במקרים עמידים לטיפול התנהגותי יש להפנות לאורולוג ילדים ובמידת הצורך, גם לגסטרואנטרולוג ילדים, להעמקת הבירור ובמידת הצורך, התחלת טיפול תרופתי או ניתוחי.
הגדרות
זיהום בדרכי השתן (Urinary tract infection) יכול לערב את דרכי השתן העליונות ורקמת הכליה, או את דרכי השתן התחתונות בלבד.
דלקת בשלפוחית (Cystitis) - זיהום בשלפוחית ודרכי השתן התחתונות. הזיהום בדרך כלל מופיע ללא חום, ואינו גורם לצלקות בכליות, כיוון שאינו מערב את רקמת הכליה. לזיהום בדרכי השתן המסתמן ללא חום סיסטמי ניתן להתייחס כאל אירוע שמערב את דרכי השתן התחתונות בלבד.
דלקת בכליה (Pyelonephiritis) - זיהום בדרכי השתן העליונות (מרמת השופכנים ועד לכליות) המהווה גורם סיכון להתפתחות של צלקות בכליות.
Febrile UTI (fUTI) - זיהום בדרכי השתן המלווה בחום. במקרים של fUTI האבחנה על בסיס התסמינים והסימנים בין זיהום של שלפוחית השתן לבין זיהום של הכליות אינה תמיד אפשרית ובפרט, בילדים צעירים. מאחר שעיקר הזיהומים שכיחים בקבוצת גיל זו, מקובל להתייחס לחום כמדד לקיום זיהום בכליה.
צלקת כלייתית - פגיעה בלתי הפיכה בחלק מרקמת הכליה הנוטה להופיע לאחר אירוע של דלקת כלייתית או דיספלזיה מולדת. צלקות כלייתיות מרובות עלולות להוביל בהמשך ליתר לחץ דם, פרוטאינוריה והפרעה קבועה בתפקוד הכליה המעורבת. המטרה העיקרית של אבחון וטיפול מוקדם בזיהום כלייתי היא מניעת הצטלקות כלייתית חדשה.
בקטראוריה אסימפטומטית - מוגדרת כצמיחה משמעותית של חיידק בשתן (ייתכן גם של חיידק עמיד) בהיעדר תלונות או סימנים המחשידים לזד"ש. בקטראוריה אסימפטומטית תיתכן בכל גיל, כולל: בילדים ופעוטות, ותוארה באופן שכיח יותר בבנות. שכיחותה בילדים היא כ-1 עד 3 אחוזים. מצב זה נוטה לחלוף מעצמו כעבור חודשים אחדים, אך לעיתים, נעלם רק כעבור שנים. במצב זה, לא נדרש טיפול אנטיביוטי, אלא אם הילד מועמד להתערבות אורולוגית פולשנית (כגון: צנתור במערכת השתן שכרוכה בו פגיעה ברירית). טיפול אנטיביוטי מעלה את הסיכון להתפתחות עמידויות, כרוך בתופעות לוואי, ואף עלול להגביר את הסיכון לזיהום בשתן[1][2].
אפידמיולוגיה
זד"ש מהווה את אחד הזיהומים החיידקיים השכיחים ביותר בילדים, עם שכיחות גבוהה יותר בבנים לא נימולים מתחת לגיל 3 חודשים, ובבנות מתחת לגיל שנה. זיהום בדרכי השתן העליונות (pyelonephiritis) אופייני יותר לקבוצת הגיל הצעירה, בעוד שזיהום בדרכי השתן התחתונות והשלפוחית (Cystitis) אופייני יותר לבנות בגיל בית הספר[2][3][4]. מעבר לתקופת הינקות הזיהום שכיח יותר בבנות. שיעור ההיארעות בתינוקות ובילדי בית ספר יסודי הוא בין 1 ל-3 אחוזים[5] הסיכון להישנות כעבור 6 עד 12 חודשים לאחר הזיהום הראשון הוא בין 12 ל-30 אחוזים. מרבית ההישנויות נגרמות מהדבקה חדשה על ידי חיידק מחיידקי אוכלוסיית המעי[6][7].
גורמי סיכון לזד"ש
מין נקבי, גיל צעיר, גזע לבן, ליקוי בתפקוד השלפוחית והמעי (bladder-bowel dysfunction), מומים מולדים של דרכי השתן והכליות (Congenital Anomalies of Kidneys and the Urinary Tract - CAKUT), נוכחות גופים זרים כגון צנתר שתן והיעדר ברית מילה, מהווים גורמי סיכון לזד"ש[2][8][9]. גורמי סיכון נוספים בילדים גדולים יותר כוללים: עצירות, vulvitis, ובמתבגרים כוללים: אבני כליה, פעילות מינית וסוכרת. גורמים גנטיים משפיעים אף הם על הסיכון לזד"ש[9].
מתן טיפול אנטיביוטי מכל סיבה, עלול להעלות את הסיכון לזיהום על ידי שינוי הפלורה סביב השופכה (periurethral). אמבטיות קצף יכולות, לעיתים נדירות, לגרום לגירוי מקומי בגניטליה וברקמה הפריאורטרלית, שיכול להתפרש באופן מוטעה כזד"ש[10]. יש מידע דל התומך בכך שאמבטיית קצף גורמת לזיהום[11][12]. כפי שצוין לעיל, ברית מילה היא בעלת השפעה מגינה על היארעות זד"ש: בבנים נימולים שכיחות זד"ש נמוכה יותר. כך למשל, בשנה הראשונה לחיים שכיחות הזיהום גבוהה פי 10 בבנים לא נימולים מאשר בבנים נימולים או בבנות[2].
גורמי סיכון להצטלקות כלייתית
הסיבוך ארוך הטווח המשמעותי ביותר של זיהום בכליה (pyelonephiritis) הוא הופעת הצטלקות כלייתית. השכיחות של הופעת צלקות כלייתיות לאחר זד"ש (fUTI) היא כ-15 אחוזים[13]. הגורמים שנמצאו קשורים להופעת צלקות נרכשות לאחר זיהום בכליה כוללים: משך חום מעל 72 שעות לפני התחלת טיפול[14], זיהומים חוזרים בדרכי השתן, מזהמים שונים מ-E coli[15] ודרגה גבוהה של VUR (בייחוד דרגות 5-4)[16]. פעמים רבות, דרגה גבוהה של VUR תופיע עם דיספלזיה כלייתית ראשונית. לעיתים, קיים קושי להבדיל במיפוי בין דיספלזיה ראשונית לבין צלקות עקב זד"ש. גיל צעיר נחשב בעבר כגורם סיכון, אך מחקרים אחרונים גילו שילדים גדולים הם כנראה בסיכון גבוה יותר להופעת הצטלקות כלייתית[17]. נטייה גנטית להצטלקות תוארה בפולימורפיזם בגן HSPA1B ובחלבון HSP72[18] וכן, בווריאנטים בגן toll-like receptor 4[19]. בנוסף, פולימורפיזם בגנים angiotensin-converting enzyme ו-transforming growth factor b1 תוארו כבעלי תפקיד בהצטלקות כלייתית[20].
חשיבות האבחון המוקדם
אבחון מהיר וטיפול מוקדם חשובים לשם מניעת סיבוכים חריפים והופעת הצטלקויות בכליה. התהליך הדלקתי המלווה את הזיהום הנחוץ לצורך חיסול הפתוגן גורם גם נזק לרקמת הכליה באמצעות גרימת איסכמיה רקמתית, מוות של תאים טובולריים ו-reperfusion injury. תהליכים אלו מובילים בסופו של דבר לפיברוזיס והצטלקות[21][22]. ברוב הילדים ההצטלקות הכלייתית לא תהיה בעלת משמעות קלינית, אך ביכולתה לגרום ליתר-לחץ דם, לפרוטאינוריה, ולירידה הדרגתית בתפקוד הכלייתי במקרים שבהם מתרחשת הצטלקות משמעותית דו-צדדית[23][24][25]. עיכוב בטיפול האנטיביוטי קשור לעלייה בסיכון להצטלקות. בילדים שהחלו טיפול מוקדם, תוך יממה מתחילת החום, שיעור ההצטלקות הכלייתית היה נמוך ב-74 אחוזים מאשר בילדים שהחלו טיפול לאחר 72 שעות מתחילת החום[23].
אטיולוגיה
חיידקי מעיים אירוביים גורמים ליותר מ-90 אחוזים ממקרי הזד"ש, בהם מתגים גרם-שליליים הם השכיחים ביותר, במנגנון של זיהום עולה (ascending infection). החיידק השכיח ביותר הוא אי קולי (E.coli) הגורם לבין 70 עד 90 אחוזים מהזיהומים. חיידקי מעיים נוספים הם זנים של Proteus, Klebsiella, Enterobacter ועוד[26]. מבין המתגים הגרם-שליליים שלא ממקור המעיים, Pseudomonas aeruginosa הוא השכיח ביותר, במיוחד בילדים הסובלים מזיהומים חוזרים, מומים במערכת השתן, או שנושאים גופים זרים בדרכי השתן כגון צנתרים קבועים וכדומה[27]. זיהומים בחיידקים גרם-חיוביים שכיחים פחות וכוללים את החיידקים: Staphylococcus saprophyticus, Enterococcus ואת Staphylococcus aureus הנדיר יותר[26].
ביטויים קליניים שכיחים
התסמינים והסימנים של זד"ש בילדים משתנים עם הגיל. חום ללא סיבה ידועה במיוחד, אם נמשך מעבר ל-48 שעות, הוא הסימן השכיח ביותר של זד"ש בכל קבוצות הגיל. סימנים ותסמינים אפשריים של זד"ש בגיל הילוד כוללים גם תת-חום, תמונה קלינית של אלח דם, חוסר תיאבון, אי שקט, כישלון בשגשוג, צהבת ממושכת, והקאה חוזרת. בגילאים מאוחרים יותר ייתכנו ביטויים כגון: הקאה חוזרת, כאב בטן, אי שקט או תלונות מכוונות כגון: צריבה במתן שתן, תכיפות ודחיפות במתן שתן, כאב במותניים, צמרמורת, והרטבת יום או לילה שניונית[28]. בעת קבלת אנמנזה יש לשים לב לפרטים מחשידים ובהם: מחלות חום חוזרות ללא סיבה, מומים בדרכי השתן בסונר טרום לידתי, זיהום או מום בדרכי השתן באחאים, עצירות ממושכת, הפרעות בהטלת השתן כגון: זרם שתן חלש, התאפקות מהטלת השתן, הרגלי היגיינה לא מספקים וכדומה.
אבחנה
מומלץ לשלול זד"ש (באמצעות בדיקת שתן כללית ואם התוצאות חשודות לזד"ש באמצעות תרבית שתן) במקרים הבאים[29][30]:
- חום בילוד (עד גיל חודש)
- חום בגילאי 1 עד 3 חודשים (בהיעדר מקור ברור אחר לחום בבדיקה גופנית)
- בנות עד גיל 2 שנים, בנים שאינם נימולים עד גיל שנה, ובנים נימולים עד גיל 6 חודשים עם חום (מעל 39 מעלות), הנמשך 2 יממות או יותר (בהיעדר מקור ברור אחר לחום)[31]
- בכל גיל בנוכחות אחד מהבאים:
- תסמינים המחשידים לזיהום בדרכי השתן (גם במקרים שמטופלים באנטיביוטיקה מניעתית)
- חום ללא מקור ברור בנוכחות היסטוריה של זד"ש, או מום בדרכי השתן
- חום ממושך ללא מקור
ככלל, בילדים עם מקור ברור לחום אין צורך לשלול זד"ש. המקרים היוצאים מן הכלל הם: מצב קליני המעלה חשד לאלח דם, מומים ידועים בדרכי השתן, זיהומים קודמים בשתן או מהלך מחלה לא שגרתי.
במרפאה שאין בה אפשרות לבצע את הבירור הנדרש תישקל הפניה למוקד/מוקד רפואה דחופה/חדר מיון.
- מצבים שבהם מומלץ לשלוח תרבית שתן למרות בדיקת שתן כללית תקינה
- תינוקות עד גיל 2 חודשים (או עד גיל 8 ימים על פי ההנחיות האמריקאיות העדכניות)[32]
- חשד קליני גבוה לזד"ש
- תמונה קלינית של אלח דם
האבחנה של זד"ש מתבססת על שילוב של תסמינים קליניים, ממצאים חשודים בבדיקת שתן כללית וצמיחה בתרבית השתן. נהוג להשתמש בבדיקת השתן לכללית ובמיקרוסקופיה כמדדים מיידיים בעלי ערך מנבא חיובי או שלילי לקיום הזיהום. בדיקות עזר נוספות כמו: ספירת דם, שקיעת דם ו-(CRP) C-Reactive protein אינן תורמות לאבחון זד"ש, אך יכולות לסייע בהערכת חומרת המחלה.
בדיקת השתן לכללית - Urinalysis (טבלה מספר 1)
השתן הנבדק בבדיקה זו חייב להיות טרי. הרכיבים העיקריים הנבדקים בשתן לכללית הם:
נוכחות כדוריות לבנות בשתן באמצעות זיהוי תגובת Leukocyte esterase (תוצר פירוק של כדוריות לבנות בשתן) וניטריט, המיוצר על ידי מתגים גרם-שליליים כתוצר חיזור של ניטרטים שמקורם בתזונה[33]. קיום כדוריות דם או גם חלבון בשתן אינם מנבאים זד"ש באופן מהימן, אף כי בדיקת השתן לכללית יכולה להיעשות בצורה אוטומטית במעבדה, השיטה הנפוצה והמהירה ביותר, בעיקר במרפאת הקהילה ובחדרי המיון, היא באמצעות מקלון לבדיקת השתן (Dipstick)[34][35].
- חשוב לדעת את המגבלות הבאות של בדיקת שתן לכללית
כדוריות לבנות: נמצא, כי במחלות רבות מחוץ למערכת השתן ניתן לזהות נוכחות כדוריות לבנות בדגימת השתן, עובדה המפחיתה מהייחודיות והערך המנבא החיובי של הבדיקה. מאידך, ישנם דיווחים כי בזד"ש הנגרם מחיידקים ספציפיים כגון: Enterococcus, Klebsiella ו-Pseudomonas, תיתכן היעדרות של כדוריות לבנות בשתן[36].
ניטריטים: ייצורם דורש שהות של השתן בשלפוחית לתקופה ממושכת, ואילו אצל תינוקות, ובעיקר ביילודים קיימת, מדרך הטבע, השתנה תכופה. בנוסף, הבדיקה צפויה להיות שלילית במקרה של זיהום בחיידקים גרם-חיוביים שמטבעם אינם מחזרים ניטרט.
שתי מגבלות אלה מביאות לכך שהרגישות של הבדיקות, כל אחת בפני עצמה, ושילובן, בעיקר בילדים צעירים מגיל 2 חודשים תוארה כבלתי מספקת, וכך, גם הערכים המנבאים החיוביים והשליליים לזד"ש[37][38][39]. לעומת זאת, מעל גיל 2 חודשים, הערך המנבא השלילי של בדיקת שתן לכללית תקינה הוא גבוה מאוד (מעל 99 אחוזים) וניתן להשתמש בה כמבחן סקירה לזד"ש, ולבצע תרבית שתן רק לאלה מהילדים בהם היא חיובית. עם זאת, התפרסמו מחקרים שקראו תיגר על קביעה זו והמבקשים לאמץ את בדיקת השתן הכללית כבדיקת סקר גם ביילודים צעירים[40][41][42]. על בסיס עבודות אלו חושב הסיכוי "לפספוס" של תרבית שתן חיובית בנוכחות בדיקת שתן כללית תקינה כעומד על בין 0.6 ל-2 אחוזים[38][41]. מכאן, שבנוכחות בדיקת שתן תקינה בילודים תידרשנה בין 200 ל-500 (NNT - Number Needed to Treat) בדיקות פולשניות (קטטר או SPA) לצורך זיהוי של תרבית שתן חיובית אחת (שבסבירות גבוהה מבטאת קונטמינציה או בקטראוריה אסימפטומטית ולא זיהום אמיתי). בהתבסס על הממצאים הללו אומצו ההנחיות האמריקאיות העדכניות לבירור חום ביילוד, גישה שאינה מחייבת בירור הכולל תרבית שתן בנוכחות בדיקת שתן תקינה בילודים מעבר לגיל 8 ימים[32].
עם זאת, כשקיים חשד קליני גבוה לקיום זד"ש, גם אם בדיקת השתן לכללית היא שלילית, ובעיקר בתינוקות צעירים, מומלץ לקחת תרבית שתן.
בדיקת שתן מיקרוסקופית של דגימת שתן טרייה ללא סירכוז, בהגדלה של 1000, נועדה לזהות חיידקים וכדוריות לבנות. הגדרת מספר הכדוריות הלבנות המרמז לזד"ש שנויה במחלוקת (מעל 5 עד 10 כדוריות לבנות לשדה מיקרוסקופ (per high power field) בשתן לא מסורכז). לבדיקת שתן מיקרוסקופית ישנה תוספת רגישות שולית על פני בדיקת שתן כללית ו/או בסטיק (נספח טבלה 1)[43][44].
תרבית שתן
- אופן לקיחת השתן
בילדים, השולטים על מתן השתן ניתן לקבל דגימת שתן מאמצע הזרם לאחר ניקוי קפדני של אזור השופכה בסבון או נוזל אנטיספטי (clean voided midstream urine).
בתינוקות וילדים שעדיין לא נגמלו מחיתולים קיימות מספר שיטות לקבלת דגימת שתן:
- בתינוקות זכרים נימולים בחודשי החיים הראשונים, ניתן לקבל דגימת אמצע זרם בשיטה הבאה: השכבת הילד על גבו, חשיפת הפין, ניקויו בתמיסה אנטיספטית, ואיסוף שתן אמצע זרם באמצעות כוסית סטרילית. מרבית התינוקות יטילו שתן בתוך מספר דקות. גירוי מקביל של האזור הסופרה-פובי באמצעות גזה לחה וקרה, עשוי להחיש את ההשתנה (Quick-Wee-method)[3][45]. ניתן גם להחזיק את הילד בבתי השחי ולגרום לו להשתין על ידי גירוי הקשת הספינלית בגב[37]
- דגימת שתן הנלקחת ישירות משלפוחית השתן. גישה זו מומלצת בילדים צעירים (ובעיקר בבנות) שאינם שולטים על מתן השתן. יתרונה העיקרי הוא במהימנותה הגבוהה מבחינת תוצאת תרבית השתן. חסרונה הוא בכך שהיא פולשנית ומחייבת מיומנות ביצוע[46]
- בשיטה זו קיימות שתי דרכים
- צנתור שלפוחית השתן. מומלץ לא להשתמש בתרבית במיליליטר הראשון של השתן (אפשר להשתמש בשתן הנזכר למעלה לבדיקה הכללית) עקב האפשרות לזיהום בחיידקים המאכלסים את השופכה
- ניקור על חיקי - Supra pubic aspiration
איסוף שתן באמצעות שקית - השיטה אינה פולשנית וניתנת לביצוע במסגרת מרפאה או בבית הילד אך בדיקת שתן משקית מומלצת רק לצורך בדיקת שתן כללית. לא מומלץ להשתמש בדגימת שתן משקית לצורך תרבית שתן. החיסרון העיקרי של בדיקה משקית הוא הסיכוי הגבוה לזיהום חיצוני והסבירות הגבוהה ביותר, עד כדי 85 אחוזים, לקבלת תוצאה כוזבת חיובית (False positive) בתרבית השתן. תוצאה כזו עלולה לגרום לאבחנה שגויה ולמתן טיפול אנטיביוטי מיותר. תרבית שתן הנלקחת בצורה זו היא אינפורמטיבית רק אם היא שלילית[47].
השתן המתקבל חייב לעבור עיבוד מהיר ולהגיע תוך 4 שעות למעבדה המיקרוביולוגית (או להישמר בקור של 4 מעלות למשך לא יותר מ-24 שעות ממועד לקיחתו). המדדים לאבחון סופי של זד"ש על ידי תרבית לפי צורת לקיחת השתן מופיעים בטבלה מספר 1[30].
| מספר החיידקים בדגימה הנחשב למשמעותי (למיליליטר) | אופן לקיחת התרבית |
| 1,000< | ניקור על חיקי (SPA) |
| 50,000-10,000< | צנתור של שלפוחית השתן (קטטר) |
| 100,000< | אמצע הזרם |
ככלל, צמיחה של שני פתוגנים בתרבית שתן מרמזת לקונטמינציה. בילדים הסובלים מזיהומים חוזרים בדרכי השתן יש להתחשב בצמיחה משמעותית גם של שני פתוגנים. כאשר צומחים שני פתוגנים, המעבדה תדווח על זיהוי ורגישות של שניהם. בנוכחות סימנים ותסמינים מתאימים לזיהום בשתן תיחשב גם צמיחה של פתוגן מתחת לסף המצוין כהוכחה לזד"ש[2].
טיפול אנטיביוטי בזיהום בדרכי השתן
רצוי שהקלינאי יכיר את שיעורי העמידות לאנטיביוטיקות שגרתיות המשמשות לטיפול בזד"ש במסגרת שבה הוא עובד, על פי פרסומים מדעיים או פנימיים של המוסד (אנטיביוגרם). זאת כדי לבחור בצורה אופטימלית את הטיפול האנטיביוטי. רצוי להתחיל טיפול אנטיביוטי בזד"ש תוך 48 שעות מתחילת החום, כאשר יש חשד קליני ומעבדתי לאבחנה זו, וקודם לכן נשלחה לטיפול תרבית שתן. ככלל, ניתן לטפל בזד"ש המלווה בחום באנטיביוטיקה פומית או דרך הווריד. במצב הנוכחי בישראל, בו אין זמינות של צפלוספורינים מדור 3 הניטלים דרך הפה, קיימת עמידות משמעותית של חיידקים הגורמים לזד"ש בפני אנטיביוטיקות הניתנות דרך הפה. מסקירת ספרות ילדים בישראל אודות זד"ש שפורסמה בתחילת שנות האלפיים, עולה כי שיעור העמידות של הפתוגנים הגרם-שליליים הגורמים לזד"ש באנטיביוטיקות השונות הוא לפי האחוזים הבאים[48][49][50][51][52]:
- בין 10 ל-38 אחוזים ב-Amoxicillin-clavulanate
- בין 10 ל-60 אחוזים ב-Cephalexin
- בין 6 ל-18 אחוזים ב-Cefuroxime
- בין 17 ל-40 אחוזים ב-Trimethoprim-sulphamethoxazole (TMP-SMX)
- בין 1 ל-17 אחוזים ב-Nitrofurantoin
- בין 2 ל-15 אחוזים ב-Ceftriaxone
- בין 3 ל-9 אחוזים ב-Gentamicin
- בין 0 ל-8 אחוזים ב-Amikacin
מצבים שבהם יש לשקול בחיוב טיפול דרך הווריד
- מראה טוקסי
- גיל עד 3 חודשים
- מחלות רקע משמעותיות העשויות להחמיר כתוצאה מזד"ש
- דיכוי חיסוני משמעותי
- הקאה חוזרת או חוסר יכולת לבלוע תרופה דרך הפה
- התייבשות
- לא ניתן להבטיח היענות מלאה למתן טיפול מתאים
- חסר או קושי בהשגת אנטיביוטיקה ספציפית הניטלת דרך הפה
- חיידקים עמידים לאנטיביוטיקה הניטלת דרך הפה שבודדו בתרביות שתן בעבר
- בעת כישלון טיפולי של אנטיביוטיקה הניטלת דרך הפה
במקרים גבוליים לאשפוז, בהם הנטייה של הקלינאי היא לטיפול בקהילה, ניתן לשקול טיפול באנטיביוטיקה בהזרקה דרך השריר או הווריד ל-24–48 שעות, תוך מעקב הדוק (טיפול זה יכול להינתן ב-Gentamicin או Ceftriaxone במתן של פעם ביום).
אם הוחל בטיפול בזד"ש דרך הווריד, ניתן לשקול מעבר לטיפול פומי ושחרור עם אנטיביוטיקה מתאימה וצרת טווח ככל האפשר, לאחר שיפור קליני במצב הילד כאשר רצוי שיתקיימו הבאים: ללא חום לפחות 24 שעות, תרבית דם ללא צמיחת פתוגן, זיהוי ורגישות הפתוגן בשתן התקבלו מהמעבדה טרם השחרור, קיים טיפול מתאים פומי וניתן להבטיח מעקב רפואי. ילדים עם זד"ש הנגרם מ-Pseudomonas aeruginosa יכולים לקבל טיפול פומי ב-Ciprofloxacin, באם החיידק רגיש, תוך מתן הסבר להורים על תרופה זו.
בזד"ש ללא חום בתינוק מעבר לגיל חודש, מדובר בדלקת בשלפוחית ועל כן הטיפול המומלץ הוא טיפול פומי.
תכשירים אנטיביוטיים מומלצים לזד"ש
בדלקת בשלפוחית ניתן לטפל אמפירית במגוון תכשירים אנטיביוטיים כגון: Trimethoprim-sulphamethoxazole (TMP-SMX), Nitrofurantoin או Cephalexin. רצוי להשתמש ב-Fosfomycin כקו טיפול שני לחיידקים עמידים לאנטיביוטיקות קו ראשון. משך הטיפול המקובל הוא בין 3 ל-5 ימים כאשר ב-Fosfomycin מדובר על מנה אחת[43].
בזד"ש עם חום קיימת עמידות לא מבוטלת של חיידקים לתרופות הפומיות הקיימות בישראל. האופציות העדיפות לטיפול פומי הן: Amoxicillin-clavulanate ו-Cefuroxime, אם כי גם לתרופות הללו קיימת עמידות לא מבוטלת. בטיפול באשפוז עם אנטיביוטיקה דרך הווריד, האפשרות העדיפה היא Gentamicin, כאשר חלופה יכולה להיות Ceftriaxone או Cefotaxime. ניתן לטפל ב-Cefuroxime במוסדות שבהם ידוע כי שיעור העמידות לתכשיר זה הוא נמוך. אם נבחר טיפול בצפלוספורינים דור 3, כדאי לנטר את שיעור העמידות במוסד לתכשיר זה כמו גם את שיעור חיידקי המעיים מייצרי Extended-spectrum β-lactamase (ESBL), העמידים לאנטיביוטיקות אלו בקרב ילדים עם זד"ש[53][54].
אם בעברו של החולה התגלו חיידקים עמידים לאנטיביוטיקה (בזיהומים קודמים או נשאות ידועה), מומלץ להתייעץ עם מומחה למחלות זיהומיות לגבי הטיפול האמפירי. המלצה זו מתייחסת גם למקרים של חשד לזיהום ב-Pseudomonas aeruginosa - חיידק הבולט בעיקר בזד"ש חוזרים, בילדים עם מומים בדרכי השתן, בנוכחות גוף זר רפואי בדרכי השתן ולאחר ניתוחים בדרכי השתן[55].
משך הטיפול הוא לרוב 7 עד 10 ימים בזיהום לא מסובך המגיב היטב לטיפול. תגובה קלינית הולמת לטיפול נצפית כמעט תמיד תוך 72 שעות מתחילתו. חום המתמיד מעבר ל-72 שעות, בעיקר אם מלווה גם בחוסר שיפור קליני ומעבדתי, מצריך בחינה מחדש של האבחנה, ואפשרות של סיבוכים כגון: מורסה כלייתית או נפרוניה באמצעות סונר כליות. אי יציבות המודינמית, אי ספיקת כליות, תפוקת שתן נמוכה או מסה בטנית מחשידים אף הם לסיבוך[43].
אם קיימת תגובה קלינית לטיפול אין צורך בתרבית שתן חוזרת לאחר סיום הטיפול או במהלכו.
סטרואידים, יחד עם אנטיביוטיקה, לטיפול בדלקת בכליה, לא הוערכו במחקרים רבי משתתפים מבוקרים ועל כן אינם מומלצים בשלב זה.
- טבלה מספר 2 - מינוני תכשירים אנטיביוטיים לטיפול בזד"ש
| הערות | מינון מקסימלי (מ"ג/יממה) | מנות ביום | מינון יומי מקובל בתפקוד כלייתי תקין (מ"ג/ק"ג/יממה) | שם מסחרי לדוגמה | שם האנטיביוטיקה (גנרי) |
|---|---|---|---|---|---|
| תכשירים במתן פומי | |||||
| מומלץ רק כטיפול דפיניטיבי לחיידק רגיש לאנטיביוטיקה זו | 1500 | 3 | 50 | Moxypen | Amoxicillin |
| 1750 | 2 | 40 | Augmentin | Amoxicillin-clavulanate (formulation 7:1) | |
| רצוי לא להשתמש לפני גיל 2 חודשים. לא מומלץ לתת ב-/eGFR<15ml min/1.73m2 | 320 | 2 | 8 של טרימטופרים) (=1 מיליליטר/קילוגרם/יממה בתרחיף המכיל Trimethoprim 40 מיליגרם/5 מיליליטר) | Resprim | Trimethoprim-sulphamethoxazole |
| 4000 | 3 | 100-50 | Ceforal | Cephalexin | |
| 1000 | 2 | 30 | Zinnat | Cefuroxime | |
לשימוש בזיהום בשלפוחית בלבד. קיים בסירופ או כהכנה רוקחית של כדורים שניתן לפתוח ולשפוך את האבקה. התוויות נגד:
|
400 | 4 | 7-5 | Uvamin | Nitrofurantoin |
| מומלץ רק כקו טיפול שני בזיהום בשלפוחית לחיידקים עמידים | מנה חד-פעמית | מעל גיל 12, מינון חד-פעמי 3 גרם. מתחת לגיל 12, קיימים נתונים מוגבלים בהיקפם על מינון חד-פעמי של 2 גרם. | Monurol | Fosfomycin | |
| רק בעת שאין תכשיר אנטיביוטי מתאים אחר, ולאחר הסבר להורים. אין צורך באישור 29ג'. | 1000 | 2 | 30 | Ciprodex | Ciprofloxacin |
| תכשירים במתן תוך ורידי | |||||
| 2000 | 1 | 50 | Rocephin | Ceftriaxone | |
| מעקב רמות ב-eGFR<50ml/min/1.73m2 | 1 | 5 | Garamycin | Gentamicin | |
בירור בעקבות זד"ש
ישנן בספרות אסכולות שונות[29][30][56] (AAP, ESPU, NICE), שמתייחסות לבירור הדרוש לאחר אירוע ראשון של זד"ש מעבר לגיל היילוד. להלן הבירור ההדמייתי שמומלץ לשקול לאחר זד"ש:
סונר כליות ודרכי שתן
סונר חשוב להערכת גודל הכליות, ומראה את הרקמה הכלייתית. קיום ומידת הרחבה של גביעים, אגן או גם שופכן. בנוסף, חשוב להעריך את גודל ועובי הדופן של שלפוחית השתן. ככלל, מומלץ שבדיקת הסונר תכלול גם בדיקת התרוקנות שלפוחית ומדידת שארית שתן.
- התוויות לביצוע סונר כליות
- לאחר אירוע ראשון של זיהום בכליה
- לאחר שני אירועים של זיהום בשלפוחית
אם הסונר בוצע במהלך הזיהום ונצפו בו עיבוי של דופן כיס השתן, או הפרעת התרוקנות, מומלץ לחזור על הבדיקה לאחר חלוף הזיהום. אם הפתולוגיה נותרה בעינה, יש להפנות להמשך בירור.
הפניה לנפרולוג/אורולוג ילדים מומלצת במקרים הבאים
- לאחר שני אירועים של זיהום בכליה
- במקרה של סונר כליות לא תקין
- זד"ש המלווה בתסמינים המתאימים לליקוי בתפקוד השלפוחית והמעי במקרים עמידים לטיפול התנהגותי (ראו סעיף 10)
- במקרים של תפקוד כלייתי לא תקין חובה להפנות לנפרולוג ילדים
בדיקות הדמיה נוספות תבוצענה בהתאם לשיקול דעתו של נפרולוג/אורולוג המטפל
מיפוי כליות Dimercapto Succinic Acid) DMSA)
במיפוי כליות DMSA (סטטי) מזריקים חומר מסומן עם טכנציום העובר סינון גלומרולרי ונספג חזרה בטובולי הפרוקסימלי, כך שאינו מופרש למערכת השתן, אלא נקלט ונשאר בקורטקס הכליה. כאשר רקמת הכליה אינה תקינה (בשל דיספלזיה, צלקת או זיהום אקוטי ברקמה), המיפוי ידגים פגם מילוי (אזור פוטופוני) או קליטה בלתי הומוגנית בקורטקס הכלייתי. מיפוי DMSA נותן מידע על נוכחות של צלקות, נוכחות רקמת כליות לא תקינה (דיספלסטית), וגם על התרומה היחסית של כל כליה לסך התפקוד הכלייתי. להדגמת צלקות כלייתיות, מומלץ לבצע מיפוי זה כעבור 4–6 חודשים מחלוף הזיהום.
- יש לשקול ביצוע מיפוי DMSA בהתוויות הבאות
- בעקבות אירועים חוזרים של fUTI לצורך הערכת קיומן של צלקות בכליות או דיספלזיה מולדת
- בחשד לצלקות או דיספלזיה כלייתיות בסונר
Voiding cystourethrogram) VCUG)
מטרת בדיקת ה-VCUG (ציסטוגרפיה) היא לאבחן רפלוקס ולהדגים את מבנה ותפקוד השלפוחית, צוואר השלפוחית, והשופכה בזמן מילוי והתרוקנות. ציסטוגרפיה תתבצע לפחות בין 2 ל-3 שבועות לאחר חלוף ה-fUTI. לאור חוסר אחידות בהמלצות בספרות ומחלוקות בין מומחים בתחום, ההחלטה על ביצוע VCUG נתונה לשיקול דעתו של נפרולוג/אורולוג מטפל ותיבחן בכל מקרה לגופו[57][58]. הנחיות למתן אנטיביוטיקה מניעתית טרם הבדיקה משתנות בין בתי חולים שונים. על הרופא המטפל לתת אנטיביוטיקה על פי הנחיות אלה. ברוב המקומות מבוצעת בדיקת הציסטוגרפיה תחת סדציה, לאור היותה פולשנית ולא נעימה. בתחילת שנות האלפיים נכנסה בחלק מבתי החולים בדיקת ציסטוגרפיה בעזרת סונר - voiding Contrastenhanced sonography - ce-VUS), אשר במהלכה מוחדר צנתר לשלפוחית כיס השתן, ודרכו מוזלף תכשיר ניגודי אולטרסוני המכיל מולקולות של Sulphur hexafluoride. למרות יתרון הבדיקה שאינה כוללת קרינה, בדיקה זו אינה מהווה את בדיקת הבחירה. ce-VUS היא בדיקה שתלויה בבודק, ובשל אופייה קיימת בעייתיות בהבנת האנטומיה של דרכי השתן, ובפרט בהבנת התנהגות השלפוחית במהלך ההתרוקנות. VCUG "רשמי" נותרת בדיקת הבחירה בהחלטה על ניתוח לתיקון רפלוקס.
טיפול אנטיביוטי מונע
מטרת הטיפול האנטיביוטי המונע היא למנוע זיהומים חוזרים בכליות והיווצרות צלקות. מחקרים שונים הראו תוצאות סותרות לגבי יעילותו של טיפול אנטיביוטי מניעתי במניעת זיהומים חוזרים בדרכי השתן. אין בספרות הוכחות ברורות לכך, שטיפול מניעתי אכן מונע היווצרות צלקות בכליות. זאת בהתבסס על שני מחקרים קליניים כפולי סמיות גדולים שבדקו טיפול מניעתי לעומת פלצבו, ועל מטה-אנליזה של מספר מחקרים. עם זאת, בחלק מהמאמרים נצפתה ירידה בשכיחות זיהומים חוזרים בדרכי השתן בילדים שטופלו מניעתית לעומת פלצבו[59]. לפי מחקר RIVUR יש לטפל ב-14 ילדים לצורך מניעת זיהום אחד ( NNT -number needed to treat)[60], בעוד שעל פי מחקר PRIVENT יש לטפל במשך שנתיים ב-8 ילדים למניעת זיהום אחד[61].
- מומלץ לשקול טיפול אנטיביוטי מניעתי בייעוץ נפרולוג/אורולוג במקרים הבאים
- בילדים עם לפחות שני אירועים מוכחים של זיהום בכליה. יש הדוגלים במתן טיפול אנטיביוטי מונע לאחר שני אירועי זיהום בכליה (ללא ביצוע VCUG) עד להשלמת מיפוי DMSA כעבור 4 עד 6 חודשים מהזיהום האחרון. ההחלטה על המשך טיפול אנטיביוטי מונע וביצוע VCUG, מתקבלת בהתאם לנוכחות צלקות במיפוי DMSA[38]. גישה אחרת היא לבצע VCUG לאחר שני אירועי זיהום בכליה, בעיקר כאשר יש סבירות גבוהה לקיומו של רפלוקס עם צורך בתיקון ניתוחי
- ביילודים עם סיכון מוגבר לזד"ש כגון הידרואורטרונפרוזיס או הידרונפרוזיס משמעותי על פי סונר (SFU דרגה 3–4 ראו תרשים 1), או בחשד לחסימה בדרכי השתן בהתאם לשיקול דעתו של נפרולוג/אורולוג מטפל[62][63]. ה-NNT למניעת זד"ש אחד בילדים עם הידרונפרוזיס משמעותי הוא 7[62]
- בילדים עם ליקוי בתפקוד השלפוחית והמעי BBD (Bladder and Bowel Dysfunction) וזיהומים חוזרים, עד לטיפול ב-BBD[64] (ראו סעיף 10)
אין חובה להתאים את סוג הטיפול המניעתי לרגישות החיידק בזד"ש. המינון המומלץ הוא בדרך כלל שליש מהמינון הטיפולי המקובל. הטיפול יינתן בדרך כלל פעם ביום בערב. בחירת הטיפול המניעתי תעשה על פי שיקול דעתו של הרופא המטפל, תוך התחשבות בשיקולים נוספים הקשורים בילד (כגון גיל, סבילות לתרופה, רגישויות) וזמינות התרופה.
- סוגי טיפול אנטיביוטי מונע
- Nitrofurantoin - נמצא יעיל יותר במניעת זד"ש וכמשרה פחות עמידויות של חיידקים. מינון מומלץ 1 מיליגרם/קילוגרם פעם ביום בערב (ראו התוויות נגד למתן מקרודנטין בטבלה 2)
- TMP-SMX - מינון מומלץ 2 מיליגרם/קילוגרם של טרימטופרים (0.3 מיליגרם/קילוגרם TMP-SMX) פעם ביום בערב. ניטרופורנטואין ו-TMP-SMX נספגים בחלקים העליונים של מערכת העיכול ולכן משרים פחות עמידויות של חיידקים
- Cephalexin - מהווה טיפול מניעתי טוב, בעיקר בתינוקות קטנים או בילדים בהם יש קונטרה אינדיקציה לטיפול תרופתי אחר. התרופה נספגת בקולון ולכן עלולה להשרות עמידויות בחיידקי המעיים מסוג ESBL, ויכולה להוות גורם סיכון לזיהום עם Pseudomonas[65]. עקב כך מומלץ להשתמש בה לפרק זמן קצר של מספר חודשים. מינון מומלץ 15 מיליגרם/קילוגרם פעם ביום בערב
ליקוי בתפקוד השלפוחית והמעי בילדים עם דלקות בדרכי השתן (Bladder-Bowel Dysfunction)
נייר עמדה זה מתמקד בליקויים בתפקוד השלפוחית, המעי והסוגרים שאינם על רקע פגיעה עצבית בילדים עם זד"ש. ליקויים בתפקוד השלפוחית והמעי מתבטאים בצריבה בהטלת השתן, תכיפות, דחיפות, התאפקות בהטלת השתן, היסוס, אי-נקיטת שתן במהלך היום והלילה ואצירת שתן. תופעות אלה יכולות להיות מלוות גם בעצירות ודליפת צואה. הליקויים בתפקוד השלפוחית והמעי מהווים גורם סיכון לזד"ש[5][64][66][67], לצלקות כלייתיות ולפגיעה בתפקוד הכלייתי. בנוסף, הם עלולים לגרום להשפעות רגשיות וחברתיות שליליות, הפוגעות במערכות יחסים משפחתיות וחברתיות, ובאיכות החיים של הילד[68].
ליקויים בתפקוד השלפוחית והמעי שכיחים בכמחצית מהילדים הסובלים מרפלוקס שלפוחיתי-שופכני המלווה בזיהומים חוזרים בדרכי השתן[64][65][69]. ליקויים אלו מהווים גורם מנבא שלילי לרזולוציה ספונטנית של הרפלוקס[70][71] ומקטינים את סיכויי ההצלחה של ניתוח אנדוסקופי לתיקון הרפלוקס[72].
לרופאי הילדים בקהילה ולרופאי המשפחה יש תפקיד משמעותי באבחון וטיפול ראשוני בהפרעות אלה. ידע נכון בזיהוי וניהול הבעיה עשוי לצמצם את מספר הזיהומים בדרכי השתן ולשפר את הדימוי העצמי ואיכות החיים של הילדים.
אבחון ליקוי בתפקוד השלפוחית והמעי
מרבית האבחנה של הפרעות בתפקוד השלפוחית והמעי מתקבלת משיחה עם הילד וההורים[73]. יש להבין האם הילד נוטה להתאפק בהטלת השתן בזמן שהוא מוסח במשחק, משתמש בצעצועים אלקטרוניים או צופה בטלוויזיה, כיוון שהתנהגות זו יכולה להוביל לתדירות ריקון נמוכה ולהגביר את הסיכון לזד"ש. יש לבצע הערכת חומרת תסמיני תפקוד השלפוחית, הכוללים: תכיפות ודחיפות בהטלת השתן, דליפת שתן במשך היום והלילה, ותמרוני התאפקות כמו שיכול רגליים, לחיצה על העטרה בבנים ולחיצה על פיית השופכה בבנות. כמו כן, חשובה הערכת תפקוד מערכת העיכול שכולל את תדירות פעולת המעיים, מידת מוצקות הצואה, כאב ומאמץ בזמן הצאייה (דפקציה) והצטאות (דליפת צואה). על הרופא המטפל, אשר מכיר את הילד ומשפחתו, לברר בנוסף לגבי סוגיות התנהגותיות או פסיכוסוציאליות חריגות, אשר עלולות להיות קשורות להפרעות בהטלת השתן והצאייה. יש לבחון את סביבת הגן או בית הספר ותנאי השירותים מאחר שאלה עלולים לגרום להתאפקות או להימנעות בהטלת שתן או גם צואה במסגרות שמחוץ לבית.
במהלך הבדיקה הפיזיקלית, חשוב להתמקד בבדיקת הבטן לשלילת גושי צואה ובדיקת איברי המין (בבנים יש לוודא שאין היצרות בפיית השופכה ובבנות יש לוודא שאין הידבקות שפתיים). בדיקת פי הטבעת חשובה לאבחון דליפת צואה, פיסורה או טחורים, היכולים לרמז על צואה נוקשה בקוטר גדול, או להעלות את החשד לתקיפה מינית. המשך תהליך האבחון של חומרת הבעיה כולל: שאלון הפרעה בהטלת השתן (נספח 3), הערכת תצורת צואה על פי סולם בריסטול (נספח 4), יומן השתנה, וסונר של דרכי השתן (כולל: לאחר התרוקנות השלפוחית) על מנת לשלול פתולוגיות של דרכי השתן. במידת הצורך, יש להפנות להמשך בירור וטיפול על ידי אורולוג ילדים.
טיפול
הטיפול הראשוני בליקוי בתפקוד השלפוחית והמעי הוא טיפול התנהגותי הכולל השתנה יזומה בכל 2 עד 3 שעות בילדים הנוטים להתאפק (גם בהיעדר תחושת הצורך להתרוקן), שיפור ההיגיינה בגניטליה בדגש על ניגוב נכון אצל ילדות צעירות, ושתיית מים מרובה בילדים הממעטים בשתייה (מומלצת כוס מים אחת לכל שנת גיל עד גיל 8 ובהמשך 8 כוסות מים ביום, לא כולל השתייה בארוחות). שתייה מרובה חייבת להיות מלווה בהתרוקנות תכופה על מנת למנוע מצבים של התאפקות. הטיפול בעצירות יכול לגרום לרזולוציה של הזיהומים החוזרים בדרכי השתן ולשפר את תפקוד שלפוחית השתן והסוגרים. בעצירות יש להתחיל בטיפול משמעותי הכולל שינוי תזונתי לכלכלה מרובת סיבים וטיפול במרככי צואה כגון polyethylene glycol (למשל נורמלקס) ובמידת הצורך, בחוקנים. יש לעקוב לאורך זמן ולוודא שיש יציאה רכה פעם ביום. במקרים עמידים לטיפול התנהגותי יש להפנות לאורולוג ילדים ובמידת הצורך גם לגסטרואנטרולוג ילדים, להעמקת הבירור, ואז במידת הצורך, התחלת טיפול תרופתי או ניתוחי.
נספחים
טבלה 1: הרגישות והסגוליות של מרכיבי בדיקת השתן לכללית לנוכחות זד"ש
המספרים המוצגים בעמודות "רגישות" ו"סגוליות" מתייחסים לאחוזים
| בדיקה | רגישות | סגוליות |
| כדוריות לבנות | 83 (בין 67 ל-94) | 78 (בין 64 ל-94) |
| ניטריט | 53 (בין 15 ל-82) | 98 (בין 94 ל-100) |
| כדוריות לבנות או ניטריט | 93 (בין 90 ל-100) | 72 (בין 58 ל-91) |
| מיקרוסקופיה (ללא סירכוז) - כדוריות לבנות | 73 (בין 32 ל-100) | 81 (בין 45 ל-98) |
| מיקרוסקופיה (ללא סירכוז) - חיידקים | 81 (בין 16 ל-91) | 83 (בין 11 ל-100) |
| כדוריות לבנות או ניטריט או מיקרוסקופיה חיובית | 99.8 (בין 99 ל-100) | 70 (בין 60 ל-92) |
תרשים 1: דירוג הידרונפרוזיס בסונר
שאלון הפרעה בהטלת השתן (ונקובר)
ניקוד מעל 13 נחשב כלא תקין.
תאריך לידה: :____/ ____/ ____
מין: זכר / נקבה
בכל שאלה סמן ב-✔ את התשובה המתאימה
1. בורח לי שתן בתחתונים במשך שעות היום
- __אף פעם
- __פעם אחת בשבוע
- __3-2 פעמים בשבוע
- __5-4 פעמים בשבוע
- __כל יום
2. כאשר בורח לי שתן בתחתונים הם
- __לא בורח לי
- __כמעט יבשים
- __לחים
- __רטובים
- __ספוגים
3. ביום רגיל אני הולך לשירותים כדי להשתין
- __2-1 פעמים
- __4-3 פעמים
- __6-5 פעמים
- __8-7 פעמים
- __יותר מ-8 פעמים
4. אני מרגיש שאני חייב למהר לשירותים כדי להשתין
- __אף פעם
- __פחות מחצי מהזמן
- __חצי מהזמן
- __יותר מחצי מהזמן
- __כל יום
5.אני עוצר את השתן על ידי שיכול רגליים או ישיבה
- __אף פעם
- __פחות מחצי מהזמן
- __חצי מהזמן
- __יותר מחצי מהזמן
- __כל יום
6. כואב לי בזמן שאני משתין
- __אף פעם
- __פחות מחצי מהזמן
- __חצי מהזמן
- __יותר מחצי מהזמן
- __כל יום
7. אני מרטיב את המיטה שלי בלילה
- __אף פעם
- __2-1 לילות בחודש
- __4-3 לילות בחודש
- __5-4 לילות בחודש
- __כל לילה
8. אני קם בלילה כדי להשתין
- __אף פעם
- __4-3 לילות בחודש
- __2-1 לילות בשבוע
- __5-4 לילות בשבוע
- __כל לילה
9. כאשר אני משתין הזרם עוצר ומתחדש
- __אף פעם
- __פחות מחצי מהזמן
- __חצי מהזמן
- __יותר מחצי מהזמן
- __כל יום
10. אני צריך ללחוץ או להמתין לפני שהשתן שלי מתחיל
- __אף פעם
- __פחות מחצי מהזמן
- __חצי מהזמן
- __יותר מחצי מהזמן
- __כל יום
11. יש לי יציאה (קקי)
- __יותר מפעם אחת
- __פעם ביום
- __פעם ביומיים
- __פעם ב-3 ימים
- __יותר מאשר פעם ב-3 ימים
12. היציאה שלי (קקי) קשה
- __אף פעם
- __פחות מחצי מהזמן
- __חצי מהזמן
- __יותר מחצי מהזמן
- __כל יום
13. יש לי תאונות של יציאה (קקי) בתחתונים
- __אף פעם
- __2-1 לילות בשבוע
- __3 פעמים בשבוע
- __5-4 פעמים בשבוע
- __כל יום
חברי הוועדה
חברי הוועדה לעדכון הקווים המנחים הנוכחיים (לפי סדר א"ב)
- ד"ר דיאנה טשר, מומחית ברפואת ילדים, מומחית במחלות זיהומיות. יו"ר הוועדה
- ד"ר ליאת אשכנזי-הופנונג, מומחית ברפואת ילדים, מומחית במחלות זיהומיות
- ד"ר דויד בן מאיר, מומחה באורולוגיה
- ד"ר יוסי גלושטיין, מומחה ברפואת ילדים
- פרופסור דני גליקמן, מומחה ברפואת ילדים, מומחה במחלות זיהומיות
- ד"ר גיא הידש, מומחה באורולוגיה
- פרופסור מרים דוידוביץ, מומחית ברפואת ילדים, מומחית בנפרולגית ילדים
- ד"ר אירית וייסמן, מומחית ברפואת ילדים, מומחית בנפרולוגית ילדים
- ד"ר אורלי חסקין, מומחית ברפואת ילדים, מומחית בנפרולוגית ילדים
- ד"ר דני לוטן, מומחה ברפואת ילדים, מומחה בנפרולוגית ילדים
שמות עורכי המהדורה הקודמת (לפי סדר א"ב)
- ד"ר יעקב אורקין, מומחה ברפואת ילדים
- ד"ר רקפת בכרך, מומחית ברפואת משפחה
- ד"ר מיכאל גולדמן, מומחה ברפואת ילדים, מומחה בנפרולוגיית ילדים
- ד"ר שמואל גור, מומחה ברפואת ילדים ד"ר צחי גרוסמן, מומחה ברפואת ילדים
- ד"ר מרים דוידוביץ, מומחית ברפואת ילדים, מומחית בנפרולוגיית ילדים
- ד"ר זאב חורב, מומחה ברפואת ילדים
- ד"ר הדר ידני, מומחה ברפואת ילדים
- פרופסור פרנסיס מימוני, מומחה ברפואת ילדים, מומחה בנאונטולוגייה
- פרופסור דן מירון, מומחה ברפואת ילדים, מומחה למחלות זיהומיות בילדים
- פרופסור אלי סומך, מומחה ברפואת ילדים, מומחה למחלות זיהומיות בילדים
- ד"ר שרון צחורי, מומחית ברפואת ילדים
- ד"ר נתי קלר, מומחה במיקרוביולוגיה קלינית
ביבליוגרפיה
- ↑ Linshaw M. Asymptomatic bacteriuria and vesicoureteral reflux in children. Kidney Int. 1996;50(1):312-329
- ↑ 2.0 2.1 2.2 2.3 2.4 Swerkersson S, Jodal U, Åhrén C, Sixt R, Stokland E, Hansson S. Urinary tract infection in infants: the significance of low bacterial count. doi:10.1007/s00467-015-3199-y
- ↑ 3.0 3.1 Shaikh N, Morone NE, Bost JE, Farrell MH. Prevalence of urinary tract infection in childhood: A meta-analysis. Pediatr Infect Dis J. 2008;27(4):302-308. doi:10.1097/INF.0b013e31815e4122
- ↑ Kanellopoulos TA, Salakos C, Spiliopoulou I, Ellina A, Nikolakopoulou NM, Papanastasiou DA. First urinary tract infection in neonates, infants and young children: a comparative study. Pediatr Nephrol 2006;21(8):1131-1137
- ↑ 5.0 5.1 Conway PH, Cnaan A, Zaoutis T, Henry B V, Grundmeier RW, Keren R. Recurrent. Urinary Tract Infections in Children Risk Factors and Association With Prophylactic Antimicrobials. https://jamanetwork.com/.
- ↑ Dai B, Liu Y, Jia J, Mei C. Long-term antibiotics for the prevention of recurrent urinary tract infection in children: a systematic review and meta-analysis. Arch Dis Child. 2010;95(7):499-508.
- ↑ Hellerstein S. Urinary tract infections in children: why they occur and how to prevent them. Am Fam Physician. 1998;57(10):2440.
- ↑ Wiswell TE, Miller GM, Gelston Jr HM, Jones SK, Clemmings AF. Effect of circumcision status on periurethral bacterial flora during the first year of life. J Pediatr. 1988;113(3):442-446.
- ↑ 9.0 9.1 Godaly G, Ambite I, Svanborg C. Innate immunity and genetic determinants of urinary tract infection susceptibility. Curr Opin Infect Dis. 2015;28(1):88.
- ↑ Lidefelt K-J, Bollgren I, Nord CE. Changes in periurethral microflora after antimicrobial drugs. Arch of Disease Child. 1991;66:683-685. doi:10.1136/adc.66.6.683.
- ↑ Modgil G, Baverstock A. Should bubble baths be avoided in children with urinary tract infections? Arch Dis Child. 2006;91(10):863-865.
- ↑ Bass NH. "Bubble Bath" as an Irritant to the: Urinary Tract of Children. Clin Pediatr (Phila). 1968;7(3):174.
- ↑ Snodgrass WT, Shah A, Yang M, et al. Prevalence and risk factors for renal scars in children with febrile UTI and/or VUR: A cross-sectional observational study of 565 consecutive patients. doi:10.1016/j.jpurol.2012.11.019 .
- ↑ Karavanaki KA, Soldatou A, Koufadaki AM, Tsentidis C, Haliotis FA, Stefanidis CJ. Delayed treatment of the first febrile urinary tract infection in early childhood increased the risk of renal scarring. Acta Paediatr. 2017;106(1):149-154.
- ↑ Mattoo TK, Chesney RW, Greenfield SP, et al. Article Renal Scarring in the Randomized Intervention for Children with Vesicoureteral Reflux (RIVUR) Trial. Clin J Am Soc Nephrol. 2016;11:54-61. doi:10.2215/CJN.05210515.
- ↑ Shaikh N, Ewing AL, Bhatnagar S, Hoberman A. Risk of renal scarring in children with a first urinary tract infection: a systematic review. Pediatrics. 2010;126(6):1084-1091.
- ↑ Shaikh N, Craig JC, Rovers MM, et al. Identification of Children and Adolescents at Risk for Renal Scarring After a First Urinary Tract Infection A Meta-analysis With Individual Patient Data. JAMA Pediatr. 2014;168(10):893-900. doi:10.1001/jamapediatrics.2014.637.
- ↑ Karoly E, Fekete A, Banki NF, et al. RAPID COMMUNICATION Heat Shock Protein 72 (HSPA1B) Gene Polymorphism and Toll-Like Receptor (TLR) 4 Mutation Are Associated with Increased Risk of Urinary Tract Infection in Children. 2007. doi:10.1203/pdr.0b013e318030d1f4.
- ↑ Akil I, Ozkinay F, Onay H, Canda E, Gumuser G, Kavukcu S. Assessment of Toll-like receptor-4 gene polymorphism on pyelonephritis and renal scar. Int J Immunogenet. 2012;39(4):303-307.
- ↑ Zaffanello M, Tardivo S, Cataldi L, et al. Genetic susceptibility to renal scar formation after urinary tract infection: a systematic review and meta-analysis of candidate gene polymorphisms. Pediatr Nephrol. 2011;26:1017-1029. doi:10.1007/s00467-010-1695-7.
- ↑ Glauser MP, Meylan P, Bille J. Pediatric Nephrology The Inflammatory Response and Tissue Damage The Example of Renal Scars Following Acute Renal Infection*. Vol 1.; 1987.
- ↑ Murugapoopathy V, Mccusker C, Gupta IR. The pathogenesis and management of renal scarring in children with vesicoureteric reflux and pyelonephritis. doi:10.1007/s00467-018-4187-9.
- ↑ 23.0 23.1 Shaikh N, Mattoo TK, Keren R, et al. Early Antibiotic Treatment for Pediatric Febrile Urinary Tract Infection and Renal Scarring. JAMA Pediatr. 2016;170(9):848-854. doi:10.1001/jamapediatrics.2016.1181.
- ↑ Wennerström M, Hansson S, Hedner T, Himmelmann A, Jodal U. Ambulatory blood pressure 16-26 years after the first urinary tract infection in childhood. J Hypertens. 2000;18(4):485-491.
- ↑ Mattoo TK. Vesicoureteral Reflux and Reflux Nephropathy. 2011. doi:10.1053/j.ackd.2011.07.006.
- ↑ 26.0 26.1 Edlin RS, Shapiro DJ, Hersh AL, Copp HL. Antibiotic resistance patterns of outpatient pediatric urinary tract infections. J Urol. 2013;190(1):222-227.
- ↑ Bitsori M, Maraki S, Koukouraki S, Galanakis E. Pseudomonas aeruginosa urinary tract infection in children: risk factors and outcomes. J Urol. 2012;187(1):260-264.
- ↑ Tullus K, Shaikh N. Urinary tract infections in children. Lancet. 2020;395(10237):1659-1668.
- ↑ 29.0 29.1 Robinson JL, Finlay JC, Lang ME, Bortolussi R. Urinary Tract Infections in Infants and Children: Diagnosis and Management. Vol 19;2011.www.cps.ca.
- ↑ 30.0 30.1 30.2 NI for H and CE (Great Britain). Urinary Tract Infection in under 16s: Diagnosis and Management. National Institute for Health and Care Excellence (NICE); 2018.
- ↑ Shaikh N, Morone NE, Bost JE, Farrell MH. Prevalence of Urinary Tract Infection in Childhood A Meta-Analysis. 2008. doi:10.1097/INF.0b013e31815e4122.
- ↑ 32.0 32.1 Pantell RH, Roberts KB, Adams WG, et al. Evaluation and management of well-appearing febrile infants 8 to 60 days old. Pediatrics. 2021;148(2).
- ↑ Robinson JL, Finlay JC, Lang ME, et al. Urinary tract infection in infants and children: Diagnosis and management. Paediatr Child Health. 2014;19(6):315-319.
- ↑ Bodeus M, Hubinont C, Bernard P, Bouckaert A, Thomas K, Goubau P. Prenatal diagnosis of human cytomegalovirus by culture and polymerase chain reaction: 98 pregnancies leading to congenital infection. Prenat Diagn. 1999. doi:10.1002/(SICI)1097-0223(199904)19:4<314::AID-PD542>3.0.CO;2-H.
- ↑ Glissmeyer EW, Kent Korgenski E, Wilkes J, et al. Dipstick Screening for Urinary Tract Infection in Febrile Infants ABBREVIATIONS CFU-colony-forming unit CI-confidence interval CLIA-Clinical Laboratory Improvement Amendment EB-CPM-evidence-based care process model EDW-Enterprise Data Warehouse HPF-high-power microscopic field NPV-negative predictive value PCH-Primary Children’s Hospital PPV- positive predictive value SBI-serious bacterial infection UTI-urinary tract infection WBC-white blood cell. Pediatrics. 2014;133(5):1121-1127. doi:10.1542/peds.2013-3291.
- ↑ Shaikh N, Shope TR, Hoberman A, Vigliotti A, Kurs-Lasky M, Martin JM. Association between uropathogen and pyuria. Pediatrics. 2016;138(1).
- ↑ 37.0 37.1 Bonadio W, Maida G. Urinary tract infection in outpatient febrile infants younger than 30 days of age: a 10- year evaluation. Pediatr Infect Dis J. 2014;33(4):342-344.
- ↑ 38.0 38.1 38.2 Tzimenatos L, Mahajan P, Dayan PS, et al. Accuracy of the urinalysis for urinary tract infections in febrile infants 60 days and younger. Pediatrics. 2018;141(2).
- ↑ Crain EF, Gershel JC. Urinary tract infections in febrile infants younger than 8 weeks of age. Pediatrics. 1990;86(3):363-367.
- ↑ Herreros ML, Tagarro A, Garcia-Pose A, Sánchez A, Cañete A, Gili P. Performing a urine dipstick test with a clean-catch urine sample is an accurate screening method for urinary tract infections in young infants. Acta Paediatr. 2018;107(1):145-150.
- ↑ 41.0 41.1 Schroeder AR, Chang PW, Shen MW, Biondi EA, Greenhow TL. Diagnostic accuracy of the urinalysis for urinary tract infection in infants<3 months of age. Pediatrics. 2015;135(6):965-971.
- ↑ Lavelle JM, Blackstone MM, Funari MK, et al. Two-step process for ED UTI screening in febrile young children: reducing catheterization rates. Pediatrics. 2016;138(1).
- ↑ 43.0 43.1 43.2 Subcommittee on Urinary Tract Infection SC on QI and M. Urinary tract infection: clinical practice guideline for the diagnosis and management of the initial UTI in febrile infants and children 2 to 24 months. 2011.
- ↑ Bachur R, Harper MB. Reliability of the Urinalysis for Predicting Urinary Tract Infections in Young Febrile Children.
- ↑ Kaufman J, Tosif S, Fitzpatrick P. Quick-Wee: a novel non-invasive urine collection method. Emerg Med J. 2017;34:63-64. doi:10.1136/emermed-2016-206000.
- ↑ Mattoo TK, Shaikh N, Nelson CP. Contemporary Management of Urinary Tract Infection in Children. Pediatrics. 2021;147(2).
- ↑ Al-Orifi F, McGillivray D, Tange S, Kramer MS. Urine culture from bag specimens in young children: are the risks too high? J Pediatr. 2000;137(2):221-226.
- ↑ Eremenko R, Barmatz S, Lumelsky N, Colodner R, Strauss M, Alkan Y. Urinary Tract Infection in Outpatient Children and Adolescents: Risk Analysis of Antimicrobial Resistance. Isr Med Assoc J IMAJ. 2020;22(4):236-240.
- ↑ Shaki D, Hodik G, Elamour S, et al. Urinary tract infections in children < 2 years of age hospitalized in a tertiary medical center in Southern Israel: epidemiologic, imaging, and microbiologic characteristics of first episode in life. Eur J Clin Microbiol Infect Dis. 2020:1-9.
- ↑ Sakran W, Smolkin V, Odetalla A, Halevy R, Koren A. Community-acquired urinary tract infection in hospitalized children: etiology and antimicrobial resistance. A comparison between first episode and recurrent infection. Clin Pediatr (Phila). 2015;54(5):479-483.
- ↑ Graif N, Abozaid S, Peretz A. Trends in Distribution and Antibiotic Resistance of Bacteria Isolated from Urine Cultures of Children in Northern Israel Between 2010 and 2017. doi:10.1089/mdr.2020.0111.
- ↑ Yakubov R, van den Akker M, Machamad K, Hochberg A, Nadir E, Klein A. Antimicrobial resistance among uropathogens that cause childhood community-acquired urinary tract infections in central Israel. Pediatr Infect Dis J. 2017;36(1):113-115.
- ↑ 54. Megged O. Extended-spectrum p-lactamase-producing bacteria causing community-acquired urinary tract infections in children. Pediatr Nephrol. 2014;29(9):1583-1587.
- ↑ Dayan N, Dabbah H, Weissman I, Aga I, Even L, Glikman D. Urinary tract infections caused by community- acquired extended-spectrum p-lactamase-producing and nonproducing bacteria: A comparative study. J Pediatr. 2013;163(5). doi:10.1016/j.jpeds.2013.06.078.
- ↑ Goldman M, Rosenfeld-Yehoshua N, Lerner-Geva L, Lazarovitch T, Schwartz D, Grisaru-Soen G. Clinical features of community-acquired Pseudomonas aeruginosa urinary tract infections in children. Pediatr Nephrol. 2008;23(5):765-768.
- ↑ A’t Hoen L, Bogaert G, Radmayr C, et al. Update of the EAU/ESPU guidelines on urinary tract infections in children. J Pediatr Urol. 2021.
- ↑ Marcus N, Ashkenazi S, Samra Z, Cohen A, Livni G. Community-acquired Pseudomonas aeruginosa urinary tract infections in children hospitalized in a tertiary center: relative frequency, risk factors, antimicrobial resistance and treatment. Infection. 2008;36(5):421-426.
- ↑ Lee LC, Lorenzo AJ, Koyle MA. The role of voiding cystourethrography in the investigation of children with urinary tract infections. Can Urol Assoc J. 2016;10(5-6):210.
- ↑ WilliamsG CJ. Cochrane Library Cochrane Database of Systematic Reviews Long-term antibiotics for preventing recurrent urinary tract infection in children (Review). 2019. doi:10.1002/14651858.CD001534. pub4
- ↑ Investigators RT. Antimicrobial prophylaxis for children with vesicoureteral reflux. N Engl J Med. 2014;370(25):2367-2376.
- ↑ 62. Craig JC, Simpson JM, Williams GJ, et al. Antibiotic prophylaxis and recurrent urinary tract infection in children. N Engl J Med. 2009;361(18):1748-1759.
- ↑ 62.0 62.1 Herz D, Merguerian P, McQuiston L. Continuous antibiotic prophylaxis reduces the risk of febrile UTI in children with asymptomatic antenatal hydronephrosis with either ureteral dilation, high-grade vesicoureteral reflux, or ureterovesical junction obstruction. J Pediatr Urol. 2014;10(4):650-654.
- ↑ Braga LH, Mijovic H, Farrokhyar F, Pemberton J, DeMaria J, Lorenzo AJ. Antibiotic prophylaxis for urinary tract infections in antenatal hydronephrosis. Pediatrics. 2013;131(1):e251-e261.
- ↑ 64.0 64.1 64.2 Shaikh N, Hoberman A, Keren R, et al. Recurrent urinary tract infections in children with bladder and bowel dysfunction. Pediatrics. 2016;137(1).
- ↑ 65.0 65.1 Koff SA, Wagner TT, Jayanthi VR. The relationship among dysfunctional elimination syndromes, primary vesicoureteral reflux and urinary tract infections in children. J Urol. 1998;160(3 Part 2):1019-1022.
- ↑ Chang S-J, Tsai L-P, Hsu C-K, Yang SS. Elevated postvoid residual urine volume predicting recurrence of urinary tract infections in toilet-trained children. doi:10.1007/s00467-014-3009-y.
- ↑ Chung KLY, Chao NSY, Liu CSW, Tang PMY, Liu KKW, Leung MWY. Abnormal voiding parameters in children with severe idiopathic constipation. doi:10.1007/s00383-014-3511-0.
- ↑ Julia Goncalves de Mello M, Pacheco Martins Ribeiro Neto J, Nelson Fernandes Barbosa L, Just da Costa Silva E, Andrade Veloso L. Quality of life, cognitive level and school performance in children with functional lower urinary tract dysfunction. doi:10.5935/0101-2800.20160033.
- ↑ Jodal Jean Smellie Hildegard Lax Peter F Hoyer UM, Bachmann H, Rascher W, et al. Ten-year results of randomized treatment of children with severe vesicoureteral reflux. Final report of the International Reflux Study in Children. Pediatr Nephrol. 2006;21:785-792. doi:10.1007/s00467-006-0063-0.
- ↑ Alexander SE, Arlen AM, Storm DW, Kieran K, Cooper CS. Bladder Volume at Onset of Vesicoureteral Reflux is an Independent Risk Factor for Breakthrough Febrile Urinary Tract Infection. J Urol. 2015;193(4):1342- 1346. doi:10.1016/J.JURO.2014.10.002.
- ↑ Arlen AM, Alexander SE, Wald M, Cooper CS. Computer model predicting breakthrough febrile urinary tract infection in children with primary vesicoureteral reflux. J Pediatr Urol. 2016;12(5):288-e1.
- ↑ Giurici N, Pennesi M. Importance of bladder bowel dysfunction in patients with urinary tract infection. J Pediatr. 2012;161(2):370.
- ↑ Yang S, Chua ME, Bauer S, et al. Diagnosis and management of bladder bowel dysfunction in children with urinary tract infections: a position statement from the International Children’s Continence Society. Pediatr Nephrol. 2018;33:2207-2219. doi:10.1007/s00467-017-3799-9.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק