קרצינומה של הקיבה - היבטים כירורגיים - Gastric carcinoma - surgical aspects
הופניתם מהדף כריתת קיבה לדף הנוכחי.
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הקיבה והתריסריון | |
בשנים האחרונות, ניכרת ירידה של ממש בשכיחותן של השאתות הממאירות בקיבה באוכלוסיה הכללית. השכיחות המדווחת בארה"ב היא 4 לכל 100,000 תושבים. השאת שכיחה יותר בגברים מאשר בנשים, ובגיל המבוגר (50-70). בישראל הייתה נטייה דומה לירידה בשיעור שאתות הקיבה, אולם מאז העלייה מחבר העמים ניכרת עלייה בשכיחות האבחון בישראל, שכן בחבר העמים שכיחות המחלה גבוהה יחסית.
גורמים אטיולוגיים
האטיולוגיה לא-ברורה. שכיחות גבוהה של ממאירויות בקיבה מצויה באוכלוסיות הבאות:
- הניזונים מדיאטה המורכבת מאורז רותח, מיין אורז, מסלומון מעושן וכדומה
- השחורים בארה"ב ויפאנים (5-40/100,000)
- משפחות
- מעשנים
- בעלי קבוצת דם A
- בעלי פוליפים אדנומתיים, שקוטרם גדול מ-2 ס"מ. פוליפים אלה נפוצים במיוחד בחולים בעשורים החמישי עד השביעי לחייהם. ב-20% מחולים אלה הפוליפ הוא קרצינומה
- בעלי פוליפים הלוקים גם באכלוראידריה (Achlorhydria). ב-80% מהחולים שבהם נמצאו שאתות ממאירות נמצאה גם אכלוראידריה
- חולים הלוקים באנמיה ממארת (Pernicious anemia). בחולים אלה נמצאו פי 3 שאתות ממאירות בקיבה מאשר באוכלוסייה רגילה
- הלוקים בדלקת קיבה ניוונית (Atrophic gastritis). נמצא כי מחלה זו שכיחה באותן קבוצות שבהן שכיחה גם הקרצינומה של הקיבה, וייתכן מכנה משותף ביניהן
- הסובלים ממטפלזיות של רירית הקיבה וכן הלוקים באינטסטינליזציה, אם כי קשה להוכיח כי אכן מדובר בגורמי סיכון יתר להופעת שאתות ממאירות
- הלוקים ב-Giant hypertrophic gastritis. דלקת קיבה זו מתנהגת כמו פוליפים מרובים בקיבה ויש בה פוטנציאל להתפתחות שאתות ממאירות. לכן, במצבים אלה יש לטפל במיוחד כששכיחות ההיפוכלוראידריה בהם גבוהה. בחולים אלה אין צורך בכירורגיה נרחבת, אלא די באנטרקטומיה, מכיוון שברוב החולים המחלה מוגבלת לאזור זה
פתולוגיה
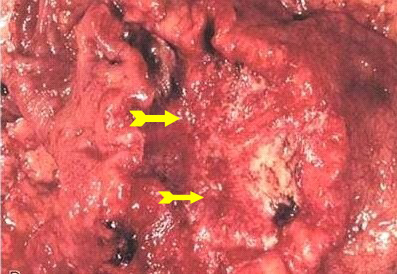
המחלה נדירה מאוד לפני גיל 50, שיאה בעשור השמיני לחיים, והיא נוטה לשכיחות יתר בגברים. 95% מהשאתות בקיבה הן אדנוקרצינומה. שאתות אחרות כגון הלימפומה או ליומיוסרקומה, הן נדירות. מקור הגידולים הוא בתאי בלוטות הרירית באזור האנטרום, השוער והעקומה הקטנה. כיבים שפירים נוטים אף הם להתפתח באותו אזור, על העקומה הקטנה. כיבים בעקומה הגדולה הם בדרך כלל ממאירים. בורמן מנה 4 צורות פתולוגיות של השאת, שיש להן קשר לפרוגנוזה:
- קבוצה ראשונה
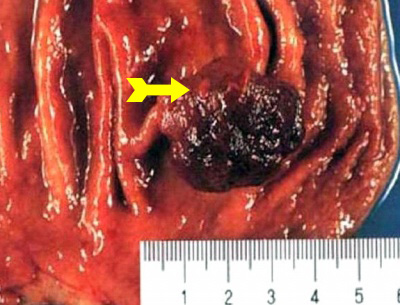
- (25%) Polypoid lesion or Fungating
- מבנה פוליפואידי מוגבל, יחיד בלא התכייבות. (תמונה 10.3)
- קבוצה שנייה
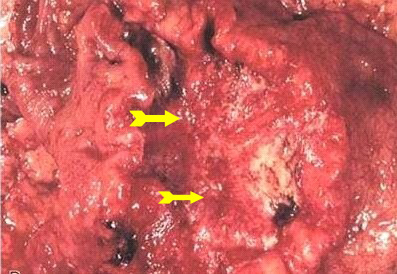
- (25%) Ulcerative lesion
- שאת מכויבת בעלת שוליים מורמים וגבול חד. (תמונה 11.3)
- קבוצה שלישית
- (35%) Infiltrating lesion
- שאת מכויבת בעלת שוליים מורמים, אבל בלי גבול חד (פולשנית) (תמונה 12.3).
- קבוצה רביעית
- (15%) Diffused lesion — שאת מפושטת.
התמונה ההיסטולוגית יכולה לנוע מתאים בעלי התמיינות טובה ועד כאלה בלא התמיינות. לרוב באותו גידול תימצא תמונה מעורבת.
חוקרים יפאנים טבעו את המושג Early carcinoma בסרטן הקיבה, בהתייחסם לקרצינומות המוגבלות רק לרירית ולתת-רירית של הקיבה, בלא חדירה לשריר, ובלי להתחשב בקיומן של גרורות בבלוטות הלימפה. הם מתארים 3 קבוצות של שאתות כאלה:
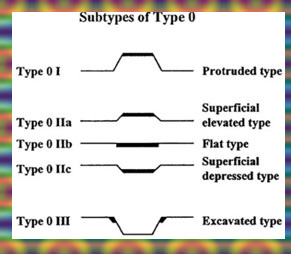
- שאתות הבולטות אל נהור הקיבה (Protuberant) (תמונה 10.3).
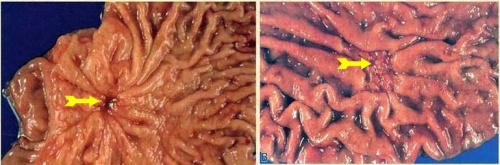
- שאתות שטוחות (Superficial), שייתכן למוצאן ב-3 צורות:
- בולטות במקצת;
- שטחיות ממש;
- שקועות במקצת (תמונה 13.3).
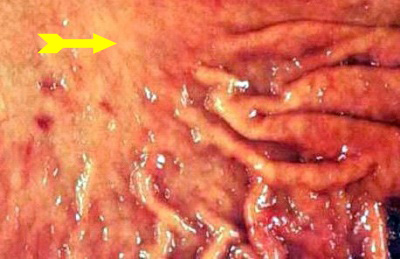
- שאתות מכויבות (Excaveted) (תמונה 14.3).
את הצורות השונות ניתן גם לתאר באופן סכמתי כמתואר באיור 20.3 .
לטענת חוקרים אלה, גילוי השאתות בשלב זה וטיפול כירורגי מתאים משנים את הפרוגנוזה באורח ניכר. הפרוגנוזה טובה יותר בצורה הבולטת מאשר בצורה המכויבת, וקיימים שילובים בין הצורות השונות.
ההיבט החשוב ביותר בשאת של הקיבה בשלב מוקדם הוא, ששיעור ההיוותרות בחיים ל-5 שנים לאחר כריתת הקיבה מגיע לכדי 90%, אפילו בחולים הלוקים בתסנין בתת-רירית. מספרים אלה בולטים בהשוואה לשיעור ההיוותרות בחיים הירוד (10% בלבד לאחר 5 שנים) בחולים בעלי שאת קיבה בשלב מאוחר.
שיעור השאתות בשלב מוקדם המאובחנות באנדוסקופיה מכלל שאתות הקיבה המאובחנות בשיטה זו הוא: 20%-5.5%. לעומת שיעור זה, מדווחים החוקרים היפאנים על 20%, ואלו מאירופה מדווחים על 5.5%. בישראל כ-12% משאתות הקיבה הן שאתות בשלב מוקדם, 40% מהן היו בקבוצת השאתות המכויבות, 15% היו פוליפואידיות, ו-45% היו מקבוצת השאתות השטחיות. השאתות פזורות במידה שווה באנטרום ובגוף הקיבה. 48% ממוקמות בעקומה הקטנה של הקיבה.
ההתפשטות לבלוטות הלימפה מתחלקת ל-4 אזורים:
- אזור 1 - בלוטות בליגמנט הגסטרוקולי סביב העורק הגסטרואפיפלואי הימני (DJ) ומשם לבלוטות באזור הצליאק (D2).
- אזור 2 - בלוטות בליגמנט הגטטרוקולי ובליגמנט הגטטרוטפלני, טביב העורק הגטטרואפיפלואי השמאלי (Dx) ומשם לבלוטות בשער הטחול, באזור הלבלב (D2) וטביב אבי העורקים (D3).
- אזור 3 - בלוטות טביב העורק הגסטרי השמאלי (Dx) ומשם לבלוטות באזור הצליאק (D2).
- אזור 4 - בלוטות לאורך העקומה הקטנה והשוער ומשם לבלוטות בשער הכבד, טביב הצליאק (D2) ואבי העורקים (D3).
ב-75%-60% מהחולים לאחר כריתה מרפאת (קורטיבית) או פליאטיבית ניתן למצוא בלוטות נגועות. נגיעות של בלוטות הלימפה מקטינה את הסיכויים להיוותרות בחיים ל-5 שנים מ-48% ל-21%.
שכיחות נגיעותן של בלוטות הלימפה משתנה לפי עומק חדירת השאת. אם רק הרירית נגועה, הרי שגרורות בבלוטות הלימפה הן נדירות. במקרים שבהם התסנין השאתי חודר גם לתת-רירית, דווח על פגיעה בבלוטות הלימפה בשיעור של כ-12%. אם השאת חודרת את הדופן, שיעור המעורבות של בלוטות הלימפה הוא 90%-75%.
דרכים נוספות להתפשטות השאת, שלא דרך הלימפה, הן:
- התפשטות ישירה לאיברים סמוכים.
- התפשטות דרך מחזור הדם למערכת השערית ולכבד, ומשם מערכתית לריאות, לעצמות ועוד.
- דרך חלל הצפק, דרך הפדר (Omentum) והפריטונאום הפריאטלי אל השחלות (Krukenberg's tumor), ואל האגן הקטן, ובתוך כך יצירת Blumer's shelf ב- Cul de sac, שהוא למעשה ביטוי לקרצינומה מפושטת.
כיום מקובל לדרג את השאת לפי TNM.
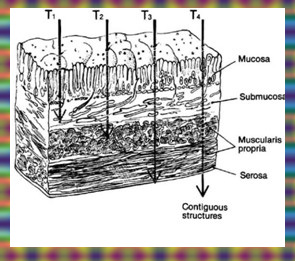
ה-T מסמלת:
- T1 - שאת המוגבלת לרירית.
- T2 - שאת החודרת לכל עובי הדופן, אך אינה עוברת אותה.
- T3 - שאת החודרת את הסרוזה עם או בלי חדירה לאיברים סמוכים.
- 4T - שאת חודרת לאיברים סמוכים.
- Tx - אין סיכום לגבי מידת החדירות.
ה-N מסמלת:
- N0 - בלוטות לא-נגועות.
- N1 - בלוטות פריגסטריות נגועות בסמוך לקיבה (3 ס"מ – D1)
- N2 - בלוטות רחיקניות נגועות סביב הצליאק (D2)
- N3 - בלוטות רחיקניות נגועות סביב האורטה (D3).
ה-M מסמלת:
- M0 - בלא גרורות מרוחקות.
- M1 - עדות לגרורות, לא כולל התפשטות ישירה.
לפי ה-TNM השאת הממאירה בקיבה מדורגת כדלקמן:
- stage 1 - T2N0M0 ו-T1N0-1M0.
- stage 2 - T1N2M0, T2N1M0,T3N0M0
- stage 3 - T2N2M0,T3N1M0T4N0-1M0
- 4 stage - כל TN עם M1.
עומק החדירה מוצג באיור 21.3.
התסמינים הקליניים
רוב הקרצינומות בשלבים המוקדמים הן א-תסמיניות. הופעת תסמינים נובעת מהפרעות בתנועתיות הקיבה, או מחסימות בה. החולה יחוש מלאות, חולשה, ירידה במשקל וחוסר תיאבון.
ירידה במשקל - התסמין הבולט ביותר בחולים אלה. תסמין זה מעיד בדרך כלל על נוכחות שאת מפושטת, אם כי ידוע שגם שאתות קטנות שאינן מפושטות עלולות לגרום לירידה במשקל, וזאת על-ידי שחרור מטבוליטים הגורמים להאצת תהליך הגליקונאוגנזיס בכבד.
הקאות - מופיעות בשלב מאוחר של החסימה, וזאת מכיוון שהחסימה מתפתחת בקצב איטי וגורמת להרחבת הקיבה ולהתעבות הדופן. אם השאת ממוקמת בשוער, התמונה החסימתית תופיעה מוקדם יותר.
דימום חד - אחד מתסמיני הקרצינומה. גם אנמיה עקב דימום כרוני מהכיב שכיחה, וייתכן שתתבטא בחולשה.
85% מהחולים מתלוננים על כאבים בעת האבחנה. ייתכן שהכאבים יהיו דומים לכאבי כיב, המגיבים לטיפול בסותרי חומצה, או כאבים סוב-סטרנליים ופאראקורדאליים, הדומים לתעוקת חזה.
התנקבות חופשית - התנקבות השאת לחלל הצפק המלווה בדלקת הצפק ובהקאות דמיות, ייתכן שתהיה התסמין הראשון למחלה, אם כי הופעתו נדירה.
דיספפסיה, ירידה במשקל ואנמיה - בחולים לאחר גיל 40 - מחייבות בירור בכיוון של שאת בקיבה.
בבדיקה נימוש לעתים גוש קשה, לא-רגיש ונייד באפיגסטריום, מופרד מהכבד. בדיקה חלחולתית תדגים לעתים תסנין שאתי בדוגלס. בבדיקת בלוטות הלימפה הסופרה-קלויקולריות לעתים נדירות נימושות הבלוטות על-שם וירכאוף, המעידות על שאת מפושטת מאוד. כבד מוגדל, מגורגר וקשה מעיד על גרורות בו.
אבחנה
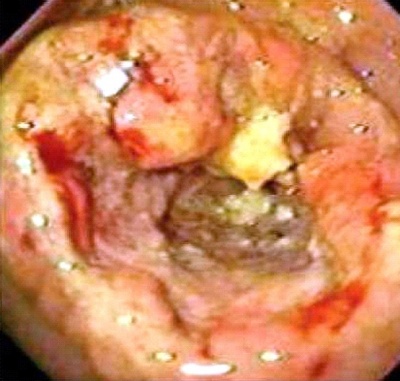
גסטרוסקופיה - אבחנתית ב-97% מהמקרים. בעזרת הגסטרוסקופיה ניתן ליטול ביופסיות להיסטולוגיה, ו- Brush ציטולוגיה (תמונה 16.3).
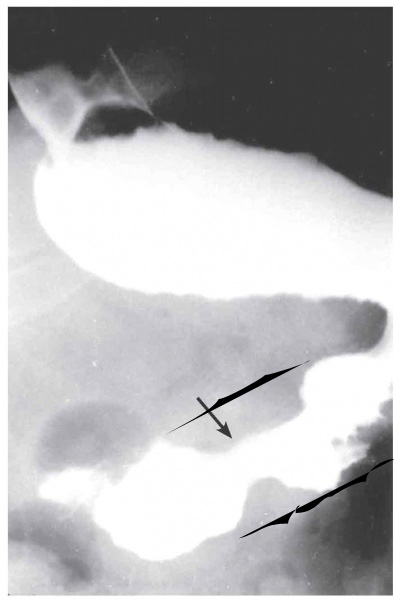
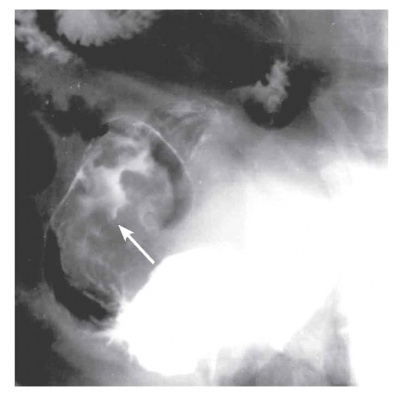
בליעת בריום - מראה גוש או פוליפ ולפעמים כיב אשר אינו עובר בתחתיתו את גבול הקיבה. בשאת ממארת של הקיבה אין התכנסות של קפלי הרירית לעבר הכיב — ממצא המאפיין כיב שפיר. כיבים אלה גדולים מ-1 ס"מ. בעזרת טכניקת Double contrast ניתן כיום להדגים את הרירית ולגלות קרצינומות מוקדמות ופוליפים קטנים (תצלומים 16.3 ו-17.3). דיוק הבדיקה הוא 75% עם שיעור בדיקות שליליות כזובות (False negative) של 15%.
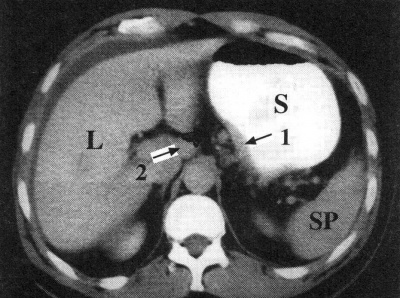
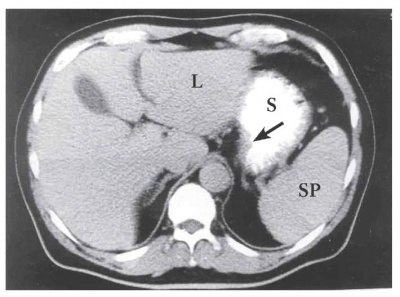
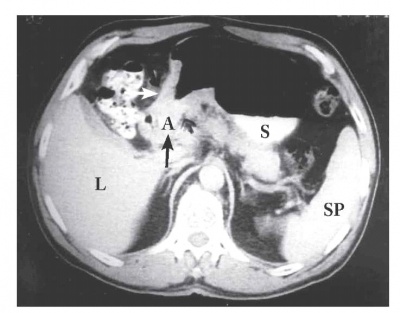
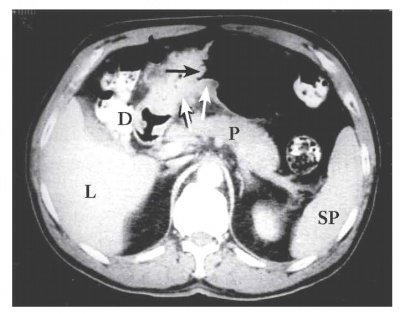
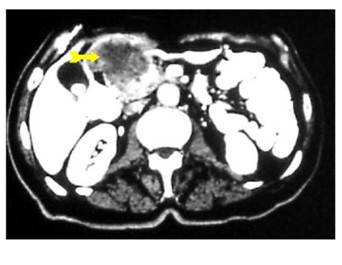
טומוגרפיה ממוחשבת - מאפשרת להדגים את גודל השאת, התפשטותה לאיברים סמוכים, בלוטות לימפה מוגדלות או גרורות לאיברים אחרים (תצלומים 21.3-18.3). ב-CT הדיוק באבחנת T4 הוא 90% וב-T1 הוא 23%.
במעבדה ייתכן שיימצאו אנמיה עקב חוסר ברזל, דם סמוי בצואה ואכלוראידריה.
Endoscopic ultrasound) EUS) - בעזרת ה-US המוחדר לקיבה דרך אנדוסקופ אפשר להעריך את גודל השאת, עומק החדירה שלה, נוכחות בלוטות מוגדלות או חשודות וכן לדגום את הבלוטות על-ידי מחט עדינה (FNA). דיוק הערכה של דרגת ה-T הוא 85% ושל ה-N הוא 75% (תצלומים 22.3 ו-23.3).
PET-CT – בדיקה זו משמשת בהערכה מידת התפשטות המחלה בעיקר בהערכת בלוטות נגועות ובתגובה לטיפול כימותרפי.
טיפול
עקרונית, הטיפול בשאת ממארת בקיבה הוא כריתה כירורגית. קרצינומה של הקיבה היא שאת אגרסיבית ועמידותו של המאכסן בפני התפשטותה נמוכה. 28% מהחולים לא מגיעים לניתוח (מחלה מתקדמת - Non-operable). 25% מהמנותחים לא יעברו כל כריתה עקב מחלה מפושטת (Non-resectable). 50% מהמנותחים עוברים כריתת קיבה פליאטיבית (Paliative - R1-R2). 25% מהמנותחים עוברים כריתת קיבה מרפאת (Cure - R0). משקל רב יש לנוכחות של גרורות בבלוטות הלימפה. בכריתה מרפאת החתך חייב לעבור בשוליים בריאים. המרחק מהשאת לקו החתך חייב לכסות גם את ההתפשטות הלימפתית התוך-דופנית. מרחק זה אינו חד-משמעי. לפי זינגר די ב-6 ס"מ בכיוון הוושט, שהוא המרחק המקובל להתפשטות סובמוקוזאלית של השאת, ו-3 ס"מ מעל התריסריון, שהוא המרחק הגדול ביותר שבו נמצאה נגיעות בחולים שבהם השאת ניתנה לכריתה.
כריתה רדיקלית היא מרפאת אם:
- נכרתת כל השאת בתוספת שוליים של 4 ס"מ לפחות.
- שולי החתך נקיים בבדיקה של חתכים קפואים עם אישור היסטולוגי בחתכים בפאראפין.
- נכרתו כל קשריות הלימפה האזוריות העלולות להיות נגועות.
- אין עדות לגרורות בשאר חלקי הבטן.
הסייגים לקריטריונים אלה הם:
- ההסננה השאתית בדופן הקיבה יכולה להתפשט לא רק ישירות דרך הדופן, אלא גם דרך צינורות הלימפה בתת-רירית, והיא יכולה להיות מוקדית או תסחיפית. לכן, בדיקת השוליים אינה מבטיחה כריתה בגבול בריא.
- הסמיכות האנטומית של הקיבה לטחול, ללבלב, לכבד ולכלי הדם החיוניים באזור שער הכבד והצליאק מונעת ביצוע כריתה עם גבול ביטחון נרחב. במקרים שבהם יש כבר חדירה דרך הנסיובית, או הסננה לקשריות הלימפה האחור-צפקיות, ספק רב אם אפשר בכלל לקוות לכריתה רדיקלית.
- קשה, ולפעמים בלתי אפשרי, לבצע דיסקציות קפדניות של האזור האחור-צפקי ברום הבטן, בפרט באזור שמסביב הצליאק trunks (הקשה מבחינה אנטומית). לכן, אם יש חדירה נרחבת לקשריות הלימפה האזוריות הללו, או לקשריות שער הכבד, יהיה כל ניתוח פליאטיבי בלבד.
טיפול כירורגי
הניתוח המומלץ כיום הוא כריתה כמעט שלמה של הקיבה Subtotal gastrectomy. בניתוח משחררים את הליגמנט הגסטרוהפטי ואת הליגמנט הגסטרוקולי, וקושרים את כלי הדם הגדולים של הקיבה. את עורק הקיבה השמאלי יש לקשור ביציאתו מה-Celiac plexus. קו חיתוך בקיבה עובר באזור החיבור האזופגוגסטרי על העקומה הקטנה לעבר העקומה הגדולה בקו ישר (כריתה של 85% מהקיבה), ובתריסריון 4 ס"מ מהשוער. יש לשמור על Short gastric vessels בעקומה הגדולה, כדי לשפר את אספקת הדם לגדם. כמו-כן, יש לכרות את הפדר הגדול והפדר הקטן בדרך זו ניתן לסלק את השאת והניקוז הלימפתי הראשוני שלה, ניתוח זה נקרא (D1) - Radical subtotal gastrectomy.
בחולים בעלי שאתות הממוקמות גבוה יותר יש צורך לכרות חלק גדול יותר מהקיבה (Near total gastrectomy) ואז פוגעים ב-Short gastric artery. לפעמים יש לכרות גם את הטחול ואת זנב הלבלב. במצב זה אספקת הדם הנותרת לקיבה היא דרך כלי דם קטנים מהוושט.
את הניתוח אפשר לסיים על-ידי שחזור בעזרת Gastroduodenostomy או Gastroenterostomy antecolic or retrocolic. מומלץ לבצע את ההשקה לפני הכרכשת, כדי למנוע קיבוע של ההשקה, היכולה להיחסם אם השאת חוזרת.
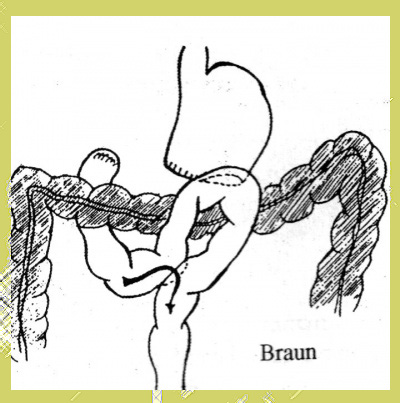
בחולים שבהם בוצעה השקה לפני הכרכשת רצוי להוסיף השקה בין ה-Efferent loop וה- Afferent loop, כדי למנוע זרם מרה חוזר לקיבה והקאות מרתיות (Braun anastomosis - איור 24.3). כאשר החולה שוכב, השקה בין הקיבה למעי הדק היא מעל לקיבה, ולכן המרה המגיעה מה-Afferent loop נשפכת לקיבה וגורמת להקאות מרתיות. חולים שבהם לא בוצעה ההשקה בין שתי לולאות המעי צריכים להימצא ככל האפשר בתנוחת ישיבה כדי למנוע זרם חוזר של המרה.
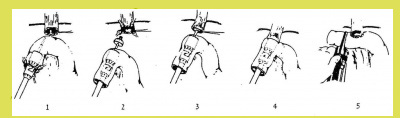
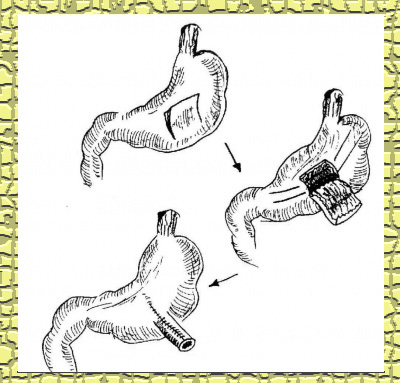
בחולים שבהם השאת היא באזור הקרדיה מבצעים Proximal gastrectomy, הכוללת כריתת החלק הקריבני של הקיבה (פונדוס וגוף), השארת החלק הרחיקני והשקה בין החלק הרחיקני של הקיבה לוושט (Esophagogastrostomy). במקצת החולים, בעלי שאת ממארת המפושטת בכל דופן הקיבה, או מרביתה, צריך לבצע כריתת קיבה שלמה (Total gastrectomy). בניתוח זה כורתים את כל הקיבה, כך שהקיבה מנותקת מהוושט ומהתריסריון. התריסריון נסגר בטכניקות שתוארו לעיל. הוושט מחובר למעי הדק. הטכניקה כיום לביצוע הניתוח כוללת שימוש במכלבים אוטומטיים, ומתוארת באיור 25.3.
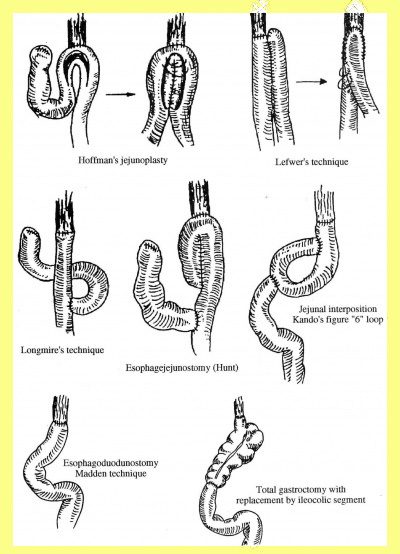
טכניקות שונות ליצירת מיכל במקום הקיבה שנכרתה מתוארות באיור 26.3.
ההוריות לכריתה שלמה של הקיבה מסוכמות בטבלה 6.3.
| 1 | Leather-bottle and diffuse gastric cancer |
| 2 | Large infiltrating gastric sarcoma |
| 3 | Diffuse adenomatous polyposis |
| 4 | Carcinoma involving the proximal half including those near the cardia, invading the fundus |
| 5 | Zollinger-Ellison syndrome |
| 6 | Gastric erosions with bleeding |
בשנים האחרונות פורסמו כמה סדרות מיפאן, שתיארו כריתת קיבה שלמה, לכל החולים הלוקים בשאת ממאירה של הקיבה, עם תוצאות טובות, מבחינת ההיוותרות בחיים. בניתוחים אלה מבצעים, מלבד כריתת הקיבה, גם כריתה של הטחול, רוב הלבלב ורקמת השומן ובלוטות הלימפה באזור שער הטחול, סביב הלבלב ולאורך ה- celiac trunk והוותין (Extended radical total gastrectomy - (D1-3. לגבי גישה נרחבת זו קיימים חילוקי דעות בספרות המערבית. במרכזים שונים במערב שבו ניסו את הגישה היפנית הנרחבת לא הצליחו לחזור על התוצאות המדווחות על-ידי היפנים ובמחיר הרבה יותר גבוה של תחלואה ותמותה בתר ניתוחית (טבלה 7.3).
| British trail | Dutch trail | |||
| mortality | morbidity | mortality | morbidity | |
|---|---|---|---|---|
| 28% | 6% | 4% | 25% | D1 |
| 46% | 13% | 10% | 43% | D2 |
בחלק מהחולים כריתה שלמה של הקיבה - כטיפול בשאתות ממאירות בקיבה - אינה מקנה בהכרח פרוגנוזה טובה יותר, אולם כרוכה בשכיחות גבוהה של תמותה ניתוחית וסיבוכים בתר-ניתוחיים. קיימים דיווחים בספרות, שהיוותרות בחיים 5 שנים לאחר כריתת קיבה שלמה בשאתות של הקרדיה טובה יותר מאשר בחולים שעברו Proximal gastrectomy.
ההמלצה לכריתת הטחול בשאתות הפונדוס והקרדיה מעוררת ספקות. הטחול הינו איבר בעל ערך רב מבחינה חיסונית (אימונולוגית) וחשוב במניעת זיהומים אחר הניתוח. נדיר שהטחול עצמו נגוע. סילוקו מומלץ במרבית המקרים בגלל הסננה שאתית בשומן ובקשריות הלימפה שבשער הטחול וליד הלבלב, המופיעה ב-40%-20% משאתות גוף או רום הקיבה. במקרים אלה אין טעם לכרותו בלא כריתת זנב הלבלב ובלא דיסקציה של הקשריות האחור-צפקיות. יעילותם של ניתוחים אלה לא הוכחה ביחס לכריתות שמרניות יותר.
בחולים בעלי סיכון ניתוחי גבוה ושאת בקרדיה או בחולים שבהם השאת בקרדיה לא ניתנת לכריתה, אפשר להכניס תותב צלסטין (Celestine) בזמן הניתוח או בדרך אנדוסקופית, על מנת לאפשר להם לאכול ולבלוע את הרוק.
השיטות הניתוחיות לטיפול בסרטן הקיבה מסוכמות בטבלה 8.3
| טבלה 8.3: Surgical Management of Gastric Carcinoma |
|---|
Palliative Procedure
|
|
Definitive Surgical Procedure
radical sub-total gastrectomy (D1 resection)
radical sub-total gastrectomy (D1 resection)
|
Endoscopic Mucosal Resection (EMR)
בשנים האחרונות מדווח על שיטה חדשה של טיפול בשאתות ממאירות בקיבה והיא כריתת הרירית והתת רירית דרך גסטרוסקופ (EMR). בתחילת התהליך מזריקים נוזל בתת רירית, מרימים אותה ולאחר מכן כורתים את הרירית בשולים בריאים (R0). רק שאת ממאירה בקיבה המוגבלת לרירית ולתת רירית בעלות התמיינות טובה ולכן סיכוי נמוך לגרורות ושקוטרן קטן מ-3 ס"מ הן אלה שניתן לכורתן בשיטת ה-EMR. ניסיון רב הצטבר בקרב האנדוסקופיסטים היפנים ששם אבחון המחלה בשלביה המוקדמים שכיחה, מה שאין כן במדינות המערב. ב-70% מהחולים המועמדים ל-EMR מושגת כריתה שלמה (R0). ב-3% יופיעו סיבוכים כמו דימומים או פרפורציות.
פרוגנוזה
התוצאות גרועות יחסית. רק 15% מהחולים ייוותרו בחיים לאחר 5 שנים. 28% מהחולים מאובחנים בשלב שבו לא ניתן לנתחם, עקב התפשטות המחלה. ב-36% מהחולים יבוצעו ניתוחים פליאטיביים בלבד, ורק ב-36% מהחולים יבוצעו ניתוחים שייעודם להשיג ריפוי מלא. רק ב-20% מאלה אפשר להשיג ריפוי מלא. הטיפולים הקרינתיים והכימיים לא הוסיפו הרבה להיוותרות בחיים של חולים אלה. שיעור התמותה הניתוחית (30 יום לאחר הניתוח) הוא 2%-1% בכריתה תת-שלמה של הקיבה, או 7%-3% בכריתה שלמה.
ההיוותרות בחיים תלויה בהתפשטות השאת, ואפשר לחלקה ל-5 דרגות:
- דרגה 0: שאת מוגבלת לרירית בלבד ולא מערבת את בלוטות הלימפה.
- דרגה 1: שאת המוגבלת לדופן, עם או בלי בלוטות נגועות הסמוכות לקיבה.
- דרגה 2: שאת המוגבלת לדופן עם בלוטות רחיקניות נגועות או שאת העוברת את הדופן, עם או בלי בלוטות קריבניות נגועות.
- דרגה 3: שאת הפורצת את הדופן עם בלוטות רחיקניות נגועות.
- דרגה 4: שאת עם גרורות רחיקניות.
לגבי כל קבוצה כזו יש חלוקה נוספת:
- כריתה תת-שלמה מרפאת.
- כריתת-קיבה שלמה מרפאת.
- כריתה פליאטיבית.
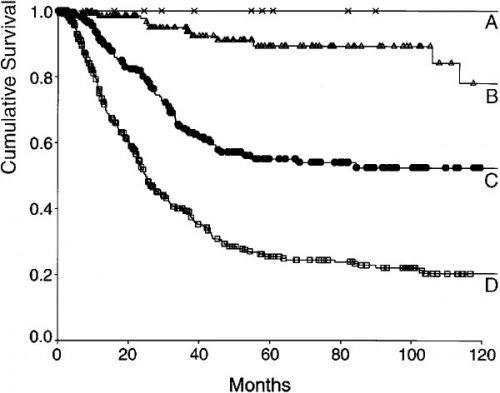
יש מתאם בין הדירוג שצוין בניתוחים מרפאים לבין ההיוותרות בחיים (גרף 1.3). בדרגה 0 שיעור ההיוותרות בחיים לאחר 5 שנים הוא 0.9%, בדרגה 1 - 60%-40%, בדרגה 2 - 30%-15%, בדרגה 3 - 10% ובדרגה 4 - 3%. לגבי כריתות פליאטיביות, אין הבדל בין הקבוצות ושיעור ההיוותרות בחיים לאחר שנתיים הוא כ-20%. נראה כי כריתות פליאטיביות משיגות הישרדות טובה יותר מאשר מעקפים.
בסדרה של Kim וחבריו (יפן) שיעור ההיוותרות בחיים לאחר 5 שנים בדרגה 1 (TNM) היה 98%; בדרגה 2 - 72%; בדרגה 3 - 31%; בדרגה 4 - 10%. הפרוגנוזה הטובה ביותר היא במקרים הבאים:
- השאת מאובחנת בשלב מוקדם (ה-Early carcinoma מבטיחה הישרדות בחיים יותר מ-5 שנים ב-29% מהחולים).
- בחולים ללא בלוטות נגועות.
- בחולים שבוצעה בהם כריתת-קיבה שלמה או תת-שלמה מרפאת.
הגישות לכריתות מרפאות ופליאטיביות
כמחצית החולים מתגלים כבר בשלב אל-נתיח, וכ-80% מהם נפטרים בתוך שנתיים. במקרים המתגלים מאוחר, כאשר השאת מתגלית כגוש נימוש ברום הבטן, וניכרת כבר התפשטות גרורתית נרחבת, או חדירה נרחבת לקשריות הלימפה האזוריות, ההיוותרות בחיים הממוצעת היא 4 חודשים, וכמעט כל החולים נפטרים בתוך שנה. אך במקרים המוקדמים יחסית, כאשר השאת ניתנת לכריתה שלמה, לפי דעתו של המנתח (כריתה מרפאה), גם אז במקרים רבים התפשט התהליך ושיעור ההיוותרות בחיים לשנתיים הוא 47%, ו-20% ל-5 שנים. לרוע המזל, שאתות אלו, רובן מסוג האדנוקרצינומה, משתפרות אך מעט על-ידי טיפולים קרינתיים, ואין לצפות לשיפור פליאטיבי של ממש בטיפול בשאתות שאינן ניתנות לכריתה. לטיפולים כימותרפיים השפעה גדולה יותר, אך גם הם מאכזבים מאוד. התרופה המקובלת ביותר, Fluorouracil, או Xeloda הניתנת דרך הפה משיגה תגובה חיובית רק ב-22% מהמקרים, אך השיפור זמני בלבד ומתבטא בהקטנת מסת השאת ו/או הגרורות, ולעתים בהפחתת הכאב, אך אין עמו הארכת משך ההיוותרות בחיים. גם במתן תרופות אחרות כגון Mitomycin, או צירופים של Fluorouracil עם CCNU, מושגת תגובה ב-24% עד 35% מהמקרים וההיוותרות הממוצעת אינה מתמידה יותר מ-5 חודשים. מכאן, שהטיפולים הכימותרפיים מסוגלים להקטין את מסת השאת ואולי לשפר זמנית את איכות החיים, אך לא להאריך את חיי החולים.
רק הטיפול הכירורגי יש בו כדי להעניק לחולה זיק של תקווה להבראה, בשלבים המוקדמים של סרטן הקיבה (Early carcinoma), וסיכוי לחיות מספר שנים באיכות סבירה במקרים של התפשטות סרטנית מוגבלת. בשני המקרים הטיפול הכירורגי חייב לכלול כריתה של מרבית הקיבה או כולה עם השאת בגבול בריא, ואם אפשר גם את האיברים הנגועים שניתנים לכריתה בסביבתה. הצורך בכריתה במקרים אלה אינו מוטל בספק, ואולם מידת הכריתה של הקיבה, הכדאיות שבכריתת איברים סמוכים נגועים, הצורך בדיסקציה מדויקת ככל האפשר של קשריות הלימפה האזוריות, ומידת הסיכון והנזק הכרוכים בניתוח רדיקלי, כל אלה שנויים במחלוקת. יתר על כן, בקרב קבוצת החולים הניתוחיים והאל-ניתוחיים יש קבוצה גדולה של חולים שניכרת בהם בבירור התפשטות גרורתית מוגבלת, או מפושטת במתינות, וכריתה פליאטיבית של השאת נעשית מתוך ידיעה ברורה שההקלה היא לזמן מוגבל בלבד, ומתוך מודעות שהניתוח כרוך בתחלואה רצינית ובתמותה בשיעורים גבוהים הנעים בסדרות שונות בין 8% ל-23%. כאן נטוש הוויכוח על התועלת והכדאיות שבביצוע ניתוחי הכריתה, מול פעולות פליאטיביות אחרות, כגון השקה עוקפת (Bypass), או ביצוע גסטרוסטומיה. ויכוח זה מתחדד יותר ומפצל את המנתחים לפעלתנים ולמתונים. הפעלתנים מבצעים כריתות נרחבות לשם הקלה, ואילו המתונים ממליצים על כריתות פליאטיביות רק כאשר מתאפשרת כריתה חלקית או תת-שלמה של הקיבה, אך לדעתם יש להימנע מכריתות קיבה שלמות או קריבניות הכרוכות בהשקות הוושט. יש מנתחים הממליצים רק על פעולות ניתוחיות מיקטיות להקלה.
יש מנתחים המבצעים כריתות נרחבות מאוד, הכוללות כריתה רדיקלית של הקיבה יחד עם בלוטות הלימפה האזוריות, ובאם יש צורך אף כריתת הטחול, הלבלב וחלק מהכבד. אפשר לדון בשאלה אם כריתות אלה - Extended total gastrectomy - מקלות יותר מאשר כריתות פליאטיביות שמרניות, אך אין זו כריתה מרפאת, במקרים שבהם השאת מפושטת. הדוגלים בניתוחים נרחבים אלה בשלבים מתקדמים מדווחים על שיפור בשיעור ההיוותרות בחיים של חולים אלה - 19%, לעומת 10% בניתוחים שמרניים יותר, אבל במחיר של תמותה ניתוחית בשיעור 22% לעומת 13% בכריתות תת-שלמות. מקומם של ניתוחים אלה הוא במקרים נבחרים כאשר השאת קטנה ונמצאו קשריות לימפה יחידות נגועות באזור הטחולי-לבלבי בלבד. כדאיותן של הכריתות הפליאטיביות במקרים של שאתות הקיבה, גם במקרים שבהם ברור שאין אפשרות לסלק את כל השאת, תיבחן ב-3 מישורים:
- אפשרות להארכת החיים.
- אפשרות למניעת תמותה ותחלואה גבוהה בניתוח זה, יחסית לאותם סיבוכים בניתוחי המעקף.
- השגת שיפור באיכות החיים לאותה תקופה שנותרה לחולה, ומניעת סיבוכים הצפויים בעתיד.
ההיוותרות בחיים בחולים הלוקים בסרטן אל-נתיח של הקיבה היא כ-6 חודשים בממוצע. בניתוחי מעקף - ההיוותרות בחיים אינה משתנה, ורק מקרים יחידים נותרים בחיים שנה לאחר הניתוח. ניתוחים אלה מועילים בפתרון סיבוכי השאת רק ב-80% מהחולים. בכריתות פליאטיביות מדווחים מחברים שונים על היוותרות ממוצעת של 14.6 חודשים. 16% נותרו בחיים יותר משנתיים ו-7% יותר מ-3 שנים.
כריתות פליאטיביות בשלבים מתקדמים של המחלה כרוכות בשיעור תמותה ניתוחית גבוה של 23%-8%. ואולם על שיעור תמותה זהה דיווחו מחברים שונים גם בניתוחי מעקף. לכן, אם כי החולים בשתי הקבוצות אינם אותם חולים, משתמע שניתוח המעקף אינו בטוח יותר מכריתה פליאטיבית.
איכות החיים של חולים לאחר כריתה פליאטיבית טובה יותר מזו של חולים לאחר ניתוחי מעקף. ואולם היכולת לחזור לאחר הניתוח לאכילה רגילה ולדיאטה רגילה מוגבלת בשני הניתוחים לכ-60% מהחולים. התסמינים הקליניים של קשיי בליעה, כאבים ברום הבטן, בחילה, הקאות, שיהוקים, חוסר תיאבון וכוי, חמורים יותר לאחר ניתוחי מעקף מאשר לאחר ניתוחי כריתה פליאטיבית. התחלואה המיידית והסיבוכים המוקדמים זהים בשני הניתוחים. בניתוחי הכריתה נמנעים סיבוכים רבים הנובעים מעצם קיום השאת בקיבה, כגון דימום חד עם שיחרה, או הקאות דמיות, התנקבות וסתימת המעבר בקיבה.
כריתה פליאטיבית חלקית או תת-שלמה עדיפה מכל ניתוח המותיר את השאת הראשונית של הקיבה במקומה, גם אם לא סולקה כל שאת הנראית לעין. כל זאת, כל עוד מדובר בכריתות רחיקניות, שאינן דורשות השקות מסוכנות עם הוושט, והחולה במצב כללי טוב, שאין בו סיכון גבוה בגלל מחלות נלוות. לא כן המצב במקרים של סיכון ניתוחי גבוה, או בחולים שבהם הכרחי לכרות את הקיבה בשלמותה. במקרים אלה הסיכון אינו מוצדק, ואינו מתאזן על-ידי התועלת הזמנית המצופה מהניתוח.
גסטרוסטומיה
ההזנה האנטרלית היא השיטה המועדפת בחולים הלוקים בתת- תזונה על רקע ירידה בכושר הבליעה או כהקלה בשאת לא-נתיחה של הוושט או הקרדיה. באופן מסורתי, הפתרון המוצע לבעיה זו הוא הכנסת מחדר אף-קיבה (זונדה) ולהאכיל את החולים דרכו. ההחדרה יכולה להיות באופן עיוור או בעזרת גסטרוסקופ. המחדר בדרך כלל אינו נוח ומהווה מטרד לחולה ובני משפחתו, ולכן במסקנות "החברה לגסטרואנטרולוגיה" מומלץ להשתמש במחדרים אלה לתקופה של לא יותר מ-30 יום. בחולים הזקוקים להזנה ממושכת יש לתת את המזון דרך גסטרוסטומיה או ג'גונוסטומיה. הגסטרוסטומיה יכולה להתבצע באופן כירורגי בדרך אנדוסקופית או רנטגנית.
בשיטה הכירורגית נכנסים לבטן בחתך אמצעי עליון בהרדמה מקומית או כללית. מזהים את גוף הקיבה ומחדירים לתוכו צנתר, מקבעים אותו לדופן הקיבה ומעבירים אותו דרך חתך נפרד בדופן הבטן לעור. השיטות לביצוע גסטרוסטומיה מסוכמות באיורים 27.3 ו-28.3.
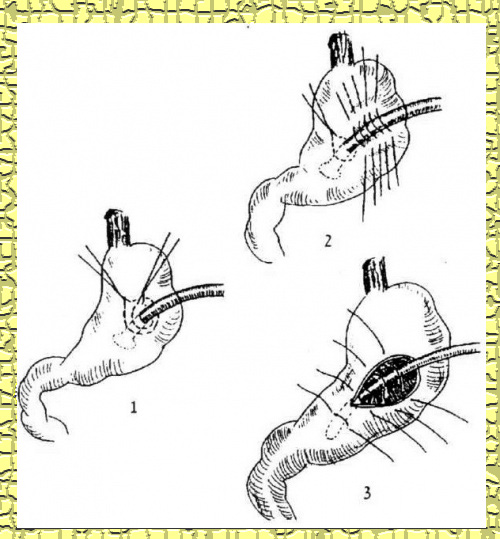
1) Stomm's gastrostomy לאחר יצירת נקב בקיבה (גוף) מחדירים צנתר פצר ותופרים סביבו את דופן הקיבה בתפר "שק טבק" את הצנתר מעבירים דרך דופן הבטן, בסוף הניתוח מקבעים את הקיבה לדופן הבטן.
2) Witzal Gastrostomy לאחר החדרת הצנתר לקיבה "עוטפים" את הצנתר על-ידי דופן הקיבה;
3) Morwedeis Gastrostomy לאחר פתיחת הדופן השרירית של הקיבה יוצרים תעלה סוב מוקוזלית שבה מוליכים את הצנתר אל תוך הקיבה ומעליו תופרים את הדופן השרירית. בשיטה זו שיעור הדליפות מהקיבה קטן יותר
בשיטה האנדוסקופית בעזרת הגסטרוסקופ מצמידים את דופן הקיבה אל דופן הבטן ומאירים את המקום. מחדירים דרך העור מחט מיוחדת המחוברת לחוט ארוך. את החוט מושכים בעזרת הגסטרוסקופ ומחדירים צנתר לקיבה העובר מהקיבה דרך דופן הבטן לעור בטכניקה מיוחדת הנקראת פיום קיבה מלעורי בעזרת הגסטרוסקופ – PEG (Percutaneous endoscopic gastrostomy).
בשיטה הרנטגנית, כמו בגישה האנדוסקופית, הגישה היא מלעורית. מנפחים את הקיבה דרך זונדה, מזריקים מעט חומר ניגוד ותחת שיקוף מוליכים מחט לתוך הקיבה. המחט מקבעת את הקיבה לדופן הבטן ובעזרת טרוקרים ומרחיבים מחדירים את הצנתר דרך העור לקיבה.
שאתות ממקור סטרומלי של הקיבה והמעי - GIST Tumor
עד שנת 1990 כל הגידולים הלא-אפיתליאלים של מערכת העיכול נקראו Gastro Intestinal Stromal Tumors (GIST). מקור הגידולים נחשב שריר חלק והם השתייכו לקבוצת הליומיוסרקומות, וזאת למרות העובדה שרק לעתים רחוקות הופיעו באופן ברור סימנים להתמיינות (דיפרנציאציה) של שריר. בהיסטולוגיה נראו גידולים עם תאים כישוריים וכולם טופלו בצורה שווה ונחשבו בעלי אותה פרוגנוזה. בשנות ה-90 האונקולוגים הבחינו בשיעורי תגובה נמוכים לטיפולים כימותרפיים (על בסיס Doxorubicin) בליומיוסרקומות של מעי לעומת ליומיוסרקומות ממקורות אחרים (הרחם, הגפיים וכדומה). אז החל תהליך הגדרת הפנוטיפ של הגידולים בעזרת בדיקות אימונו- היסטו-כימיות. נמצא שחלק מגידולים אלה לא נצבע עם נוגדן 100S (נוגדנים נגד שריר או תאי שוון). כ-75% נמצאו חיוביים ל-34CD ול-117CD או c-Kit. המולקולה (או אנטיגן) CD117 היא חלק מקולטן ה- c-Kit . הקולטן c-Kit הוא קולטן מסוג טירוזין קינז ונוצר על-ידי פרוטואונקוגן c-Kit הנמצא בכרומוזום 4, לפי הצביעות אימונו- היסטוכימיות. התאים האנטרסטיציאלים של קאגל (Interstitial cells of cajal) מהווים מרכיב חשוב בהתפתחות השאתות הסטרומליות. תאים אלה הנמצאים בין סיבי העצב של מערכת אוטונומית לבין סיבי השריר החלק של המעי הם תאי "קוצב" של מערכת העיכול. בצביעות אימונו-היסטוכימיות הם מראים תכונות המאפינות גידולים סטרומאלים של מערכת העיכול והם c-Kit חיובים.
ניתן היה לחלק את הגידולים הסטרומאלים של מערכת העיכול לכאלה הנצבעים ל-c-Kit ונקראים חיוביים (80%) ולכאלה שלא נצבעים ל-c-Kit ונקראים שליליים (20%). לפי המבנה המיקרוסקופי וצביעות אימונו-איסטוכימיות ניתן לחלק את גידולי רקמת החיבור של מערכת העיכול ל: GIST ממקור תאים אינטרסטיציאלים של קאגל שהם c-Kit חיוביים, ולליומיוסרקומות וליומיומה - ממקור של שריר c-Kit שליליים. בעבודה רטרוספקטיבית משוודיה הראו ש-27% מהחולים שאובחנו בעבר כסרקומות ממקור שריר היו כיום מאובחנים עם GIST.
גידולי ה-GIST הם הגידולים הסטרומאלים השכיחים ביותר של מערכת העיכול. הסיבה המדויקת להופעת GIST אינה ידועה. גידולים אלה נדירים ובישראל מאובחנים מדי שנה עשרות בודדות של חולים במחלה זו. הלוקים בהם הם גברים ונשים מעל גיל 50 ללא סיפור משפחתי ולעיתים עם סיפור של שאתות שפירות של מעטפת מערכת העצבים. כ-60% מתגלים בקיבה, השאר עשויים להופיע גם במקומות נוספים במערכת העיכול, החל מהוושט וכלה בפי הטבעת. בכ-27% מהחולים נמצא גידולים נוספים. השילוב המוכר יותר הוא השילוש (טריאדה) על שם Carney הכוללת GIST, פראגנגליומה וכונדרומה של הריאה.
פתולוגיה
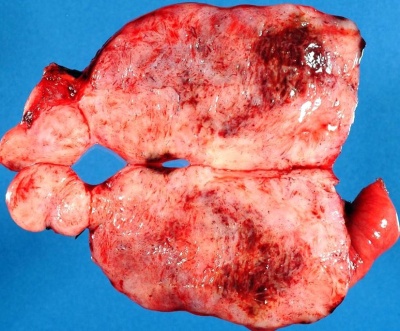
גידולים אלה מופיעים כגושים הבולטים אל תוך נהור המעי (גוש בתת רירית) או לתוך חלל הבטן (אקסטראלומינרית), מוגבלים היטב, עשירים בכלי דם, בעלי מבנה פריך עם מרכז נמקי (תמונה 17.3).
קיימים שלושה סוגים הסטולוגיים: (1) ב-70% מהשאתות נמצא תאים כישוריים (Spindle Cell Type), (2) ב-20% מהשאתות נמצא תאים אפיתליואידים (Epithelioid type) השכיחים יותר באומנטום ובמזנטריום. רובם c-Kit שלילים ובעלי פרוגנוזה גרועה יותר, (3) ב-10% נמצא תאים מעורבים.
תסמינים קליניים
בשלבים הראשונים של התפתחות הגידול (2 ס"מ <) אין שום תסמינים ולכן המחלה לרוב מאובחנת בשלביה היותר מתקדמים. חלק מהחולים מתגלה באופן אקראי בזמן ניתוח או בבדיקת הדמיה כמו CT או גסטרוסקופיה. התסמינים הם לא ספציפים: גוש באזור הבטן ללא כאב או רגישות כלשהי (40%), כאב או אי נוחות באזור הבטן (20%), דימום ממערכת העיכול (40%), הקאות, חולשה, עייפות, חום גבוה ואנמיה.
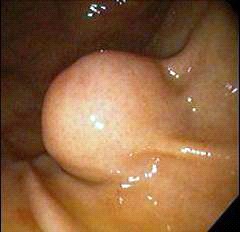
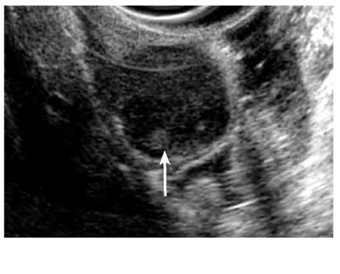
אבחנה
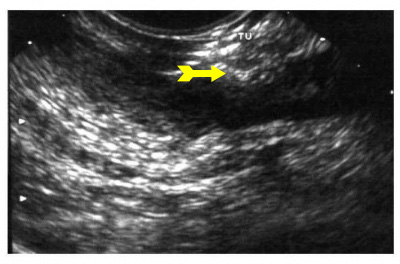
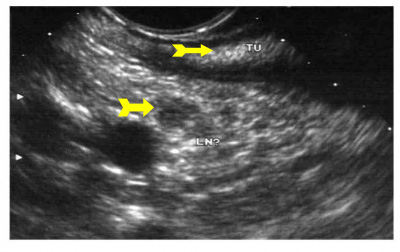
אמצעי האבחנה המקובלים הם: אנדוסקופיה (תמונה 18.3), אולטראסאונד בעיקר אנדוסקופי, (תצלום 27.3), טומוגרפיה ממוחשבת (CT), PET-CT, הדמיה בתהודה מגנטית (MRI) וביופסיה (מדידת הכמות של טאירזין קינז על-ידי שימוש בנוגדן 117 CD). ביצוע ביופסיה טרום ניתוחית (תחת US או CT) הוא נושא שנוי במחלוקת: קיימת סכנה של דימום והתפרקות הגידול, אבחנה של GIST ב- FNA קשה והאפשרות שהדגימה תילקח מהחלק הנמקי של הגידול שלא נותנת אבחנה אינם תומכים בלקיחת דגימה לפני ניתוח. יש מקום לביצוע ביופסיה טרום ניתוחית במקרים בהם הגוש חשוד ללימפומה או יש צורך בתשובה פתולוגית לפני החלטה למתן טיפול נאואדגובנטי (neoadjuvant therapy).
כדי להגדיר את הגידול כ-GIST הגידול צריך להיות c-Kit חיובי או שקיימת מוטציה פעילה בגנים KIT או PDGFRA.
ה-GIST מתנהג בצורה שונה מיתר הסרקומות: הוא שולח גרורות בעיקר לכבד ופחות לבלוטות לימפה ולא שולח גרורות לריאות (מיקום השכיח בליומיוסרקומה).
שכיחות הפיזור הגרורתי ומידת הממאירות תלויה ב:
- מספר מיטוזות
- גודל הגידול בזמן האבחנה
- מיקומו של הגידול. לגידולים בקיבה פרוגנוזה טובה ביחס לגידולים במעי הדק, לגידול קטן מ-5 ס"מ בקיבה וקטן מ-2 ס"מ במעי הדק פרוגנוזה טובה. לכל ה-GIST פוטנציאל ממאיר, פרט לגידולים הקטנים מ- 1 ס"מ. הישרדות בחיים לחמש שנים בכל הקבוצה היא 48%-28%. ההישרדות הממוצעת של חמש שנים לאחר כריתה שלמה של גידול ראשוני בודד היא 65%-55%. בגידול גרורתי או חוזר ההישרדות הממוצעת היא של 12-9 חודשים. הישנות מקומית או גרורות נמצא ב-90%-40% (ממוצע 50%) מהחולים אשר טופלו ניתוחית.
הטיפול ב-GIST
הטיפול הכירורגי, כלומר כריתת השאת, הוא הטיפול המועדף בלוקים ב-GIST.80% מחולי ה-GIST ניתנים לכריתה בניתוח הראשון. כאשר תוחלת החיים הממוצעת לחמש שנים בחולים לאחר כריתה שלמה היא 65%-48%. לכן כריתה שלמה של השאת היא החשובה ואילו לשוליים - מרחק מהגידול אינו עקרוני.
כריתה כזו ניתן להשיג על-ידי כריתה סגמנטרית של האיבר ממנו נוצר הגידול יחד עם הגידול עצמו (En-block resection), ללא צורך בשוליים כירורגיות רחבות אלא שוליים נקיות מגידול (קשה בגידולים > 10 ס"מ). טכניקה ניתוחית מדויקת ועדינה חשובה למניעת התפרקות (הגידולים פריכים) הגידול ופיזורו בחלל הצפק. אין צורך בכריתה מונעת של בלוטות הלימפה, אולם אם הבלוטות חשודות יש לבצע כריתה של בלוטות מקורבות.
הישנות מקומית או גרורות נמצא בכ-50% בתוך 5 שנים, כאשר רוב ההישנויות מתרחשות תוך 24-7 חודשים, רק כ-10% מהחולים נשארים ללא מחלה במעקב ממושך. הסיכוי להישנות תלויה ב: (1) גורמי סיכון (גודל, מיקום, אינדקס מיטוטי), (2) התפרקות של הגידול בניתוח, (3) שוליים מעורבים מיקרוסקופיות על-ידי גידול (4) מיקום ראשוני - חלל הצפק וכבד. תפקיד הכירורגיה במחלה חוזרת לא ברור. כריתת גרורות (Metastasectomy) בחולים נבחרים יכולה להאריך חיים (Survival) בגידולים עם התמיינות (דיפרנציאציה) טובה. כריתת גרורות בכבד - הישרדות ממוצעת ללא מחלה של 12 חודשים.
בשנת 2000 החלה תקופה חדשה בטיפול בחולים עם GIST בשלב לא נתיח, גרורתי או מפושט.
שימוש מוצלח ב- Glivec (Imatinib Mesylate) פתח תקופה חדשה של טיפול תרופתי במחלה.
אין יותר צורך בכריתות ניתוחיות נרחבות (Debulking) אשר בוצעו בעבר, וזאת עקב היעדר טיפול תרופתי תחליפי (אלטרנטיבי) - פרט למקרים עם עמידות לטיפול ב- Glivec. אולם יעילות התרופה מוגבלת לטווח ארוך עקב תנגודת משנית המופיעה בחלק מהחולים וגורמת להתלקחות של המחלה (Late relapses). בטיפול ב- Glivec נראה ב: 1% תגובה מלאה, ב-67% תגובה חלקית, ב-16% מחלה יציבה לאורך זמן וב-15% חוסר יעילות.
זמן ממוצע עד לתגובה היה 13 שבועות, משך התגובה הממוצע הוא כ-118 שבועות. בחלק מהחולים מופיעה עמידות מיידית או מאוחרת לטיפול ובחלקם הגיבו באופן אטי לאורך הזמן (מצדיק טיפול ממושך). תגובה טובה מאוד מדווחת בחולים עם מוטציה באקסון 11 עם הישרדות חציונית בחיים (Median survival) של 4.8 שנים. 68% מהחולים נפטרו ממחלה מתקדמת. כריתה ניתוחית שלמה נשארת הטיפול היחיד לריפוי חולי GIST (25%). לרוב החולים מוטציה באקסון 11 ולהם הסיכוי הטוב ביותר להגיב לטיפול בGlivec, לעומת חולים עם מוטציה באקסונים 9, 13, 17 - שלהם סיכוי פחות טוב להגיב לתרופה.
במסגרת הטיפול והמעקב יש לבצע CT ו FDG-PET - מוקדם בתחילת הטיפול (תוך 24 שעות PET ותוך חודש CT). ב-CT מבוצע מעקב אחרי הקטנה בקוטר השאת שיכול להישאר יציב או לגדול בתחילת טיפול, הופעת Cystic degeneration הגורמת לירידה בצפיפות (Hounsfield unit-density) והקטנת הווסקולריזציה (Enhancament) של הגידול. ב-PET נראה הקטנת בקליטה של FDG.
חשיבות המעקב היא שניתן להעריך אובייקטיבית ובמדויק את התגובה, ולכן לגלות מוקדם יותר את חזרת הגידול.
חלק מהחולים עמידים לתרופה. העמידות יכולה להיות ראשונית: מוגדרת כהמשך התפתחות המחלה למרות מתן הGlivec בפעם הראשונה למשך שישה חודשים, או שניונית: מתפתחת לאחר תקופה של תגובה לטיפול. עמידות יכולה להיות חלקית: מספר גרורות גדלות והיתר נשלטות על ידי התרופה, או עמידות רב מוקדית: כל הגרורות גדלות. בחולים עם עמידות אפשר לנסות לטפל על-ידי הגברת מינון התרופה או מתן תרופות נוגדות טירוזין קינז חדשות כמו Sunitinib malate PK787, ואחרות.
ראו גם
- לנושא הקודם: שאתות תוך-דופניות של הקיבה - Intramural gastric neoplasms
- לנושא הבא: לימפומה של הקיבה - היבטים כירורגיים - Gastric lymphoma - surgical aspects
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הצפק
- לפרק הבא: כירורגיה של המעי הדק
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק