לימפומות אינדולנטיות - התקדמות מהירה בדרך לפתרון הלימפומות הזוחלות - Indulent lymphomas
הופניתם מהדף לימפומות אינדולנטיות לדף הנוכחי.
| לימפומות אינדולנטיות - התקדמות מהירה בדרך לפתרון הלימפומות ה"זוחלות" | ||
|---|---|---|
| Indolent lymphoma | ||
| ||
לימפומה פוליקולרית במח העצם
| ||
| שמות נוספים | Low-grade lymphoma | |
| יוצר הערך | ד"ר חוה פרי ופרופסור עירית אביבי | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – לימפומה
לימפומות אינדולנטיות מהוות כ-35–40 אחוזים מסוגי מחלת לימפומה שאינה הודג'קין - NHL (Non-Hodgkin's lymphoma). תתי-הסוגים הנפוצים ביותר בה הם לימפומה פוליקולרית, לוקמיה לימפוציטית כרונית/לימפומה של לימפוציטים קטנים ולימפומה של האזור המרג'ינלי[1]. המוטציות המעורבות בהתפתחות לימפומה אינדולנטית ונרכשות בעת התפתחות התאים הלימפטיים, פוגעות ביכולת התאים לעבור מוות תאי מתוכנן ובמידה פחותה גם ביכולתם להתרבות בצורה מהירה ובלתי מבוקרת, דבר המסביר את ההתקדמות האיטית המאפיינת לימפומות אלו.
הגדלה קלה של בלוטות לימפה, בהיעדר תסמינים סיסטמיים כגון חום, הזעות לילה וירידה במשקל (תסמיני B) תיתכן חודשים ואף שנים טרם האבחנה. בעת האבחנה המחלה לרוב מפושטת ועשויה להתייצג כבעלת קצב התקדמות איטי וללא צורך בטיפול במשך תקופה ארוכה, או כבעלת מאפיינים אגרסיביים יותר: מסת מחלה גדולה וקצב התקדמות מהיר הדורשים טיפול מוקדם[1].
לימפומה פוליקולרית
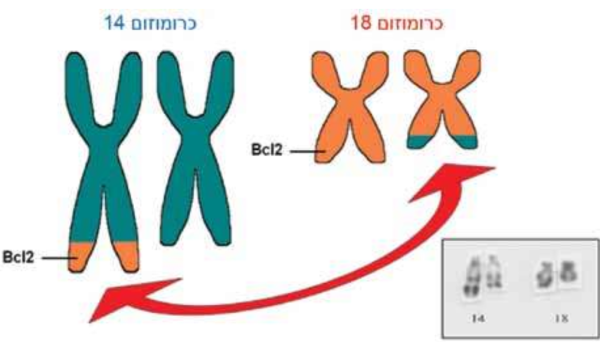
לימפומה פוליקולרית מהווה כחמישית מהלימפומות המאובחנות במדינת ישראל ובעולם המערבי, והיא הלימפומה השכיחה ביותר מהלימפומות האינדולנטיות. השינוי הגנטי השכיח בתאים אלו הוא טרנסלוקציה בין מקטעי כרומוזומים 14;18 הגורמת לעלייה בביטוי החלבון האנטי אפופטוטי Bcl2 ולחיות ממושכת של התאים (תרשים 1). התאים אינם מתרבים במהירות, ולפיכך המחלה מתפתחת באיטיות ומאובחנת, ב-75–80 אחוזים מהמקרים, בשלב מתקדם. רק במיעוט החולים המחלה מאובחנת בשלב מוקדם, כשהיא מערבת אתר מחלה יחיד[1].
יש שונות רבה במהלך הקליני של החולים: חלקם נהנים ממהלך איטי של מחלתם במשך שנים רבות, בעוד אחרים סובלים מלימפומה שמתקדמת במהירות ואף מהתמרה (טרנספורמציה) של מחלתם ללימפומה אגרסיבית - סיבוך שמתרחש בכ-20 אחוזים מהחולים בתוך חמש שנים מאבחון מחלתם (ובכ-30 אחוזים בתוך 10 שנים).
בעת האבחנה מבוצעות בדיקות FDG-PET/CT, Fluorodeoxyglucose-Positron Emission Tomography/Computed Tomography, (או בדיקת CT בלבד) וביופסיית מח עצם במטרה להעריך את שלב המחלה. אלה, בנוסף לבדיקות דם, יסייעו להעריך את סיכויי התקדמות המחלה במשך השנים[2] (טבלה 1). מדד FLIPI (Follicular Lymphoma International Prognostic Index) (טבלה 2) ורמת Beta-2-microglobulin מהווים מדדים פרוגנוסטיים מקובלים בלימפומה פוליקולרית[3][4].
ההחלטה לגבי הצורך בטיפול נשענת על כמה גורמים: שלב המחלה (מעורבות אתר בודד או שני אתרים לעומת מחלה המערבת מספר אתרים רב יותר), התסמינים עמם התייצג המטופל בעת אבחון מחלתו, גודלן של הבלוטות המעורבות וקצב צמיחתן.
|
לימפומה פוליקולרית בשלב מוקדם מגיבה היטב לקרינה מקומית, המביאה במרבית המקרים לריפוי[5], אך בשלב מתקדם, הלימפומה לרוב אינה ניתנת לריפוי, ולא הוכח כי טיפול בחולים ללא תסמינים מביא לשיפור בהישרדות בהשוואה לחולים שטופלו רק בעת התקדמות מחלתם. לפיכך, מקובל לעקוב אחר חולים אלו (watch & wait) ולטפל רק אם מתפתחים תסמינים או שמסת המחלה גדולה או גדלה במהירות[6][7] .
הטיפול בלימפומה פוליקולרית בשלב מתקדם מבוסס על כימו-אימונותרפיה: טיפול המשלב כימותרפיה ונוגדן, ריטוקסימאב (Rituximab ,Mabthera), המכוון נגד החלבון CD20 שמבוטא על פני תאי הלימפומה, משרה תגובה חיסונית נגד התאים ומשמידם. הטיפולים הכימו-אימונותרפיים משפרים משמעותית את התגובה לטיפול, משך התגובה והישרדות החולים, לעומת כימותרפיה בלבד[1]. משלבים כימותרפיים מקובלים, הניתנים עם ריטוקסימאב, כוללים CHOP (ציקלופוספאמיד, דוקסורוביצין, הידרוכלוריד, וינקריסטין ופרדניזון), CVP (ציקלופוספאמיד, וינקריסטין ופרדניזון), בנדמוסטין או כלורמבוציל[8][9][10]. במקרים מסוימים ניתן לשקול טיפול בריטוקסימאב בלבד[1][11].
| Factors (1 point for each variable present)[3] |
|---|
|
| Risk category (factors)[3] |
|
- Solal-Celigny P, Roy P, Colombat P, et al. Follicular lymphoma international prognostic index. Blood.2004;104:1258-1265[3]
בחולים שהשיגו תגובה לטיפול ניתן לשקול המשך טיפול בריטוקסימאב (טיפול "אחזקה") אשר מאריך את משך התגובה[1].
דור חדש של נוגדנים המכוונים נגד תאי B נמצא בשלבים שונים של מחקר, בהם גזיבה (Gazyva, Obinutuzumab) נוגדן המכוון אף הוא נגד CD20 ונמצא יעיל בטיפול בחולי לימפומה פוליקולרית, כולל חולים שהיו עמידים לטיפול בריטוקסימאב[12].
תרופות נוספות שנמצאו יעילות בטיפול בלימפומה פוליקולרית נשנית הן לנלידומיד (Lenalidomid, Revlimid) המשרה הרג תאי הגידול לצד שפעול תאי מערכת החיסון שבסביבתם, אידלליסיב (Idelalisib, Zydelig) המעכבת את האנזים פוספטידיל אינוזיטול-3-קינאז ובכך חוסמת אותות שחיוניים להישרדות תאי הלימפומה, וכן מעכב 2-BCL (ונטוקלקס, Venetoclax)[13].
חולים עם לימפומה פוליקולרית נשנית, בפרט אלו שמחלתם עברה התמרה ללימפומה אגרסיבית, מועמדים לעיתים להשתלת מח עצם עצמית. השתלה מתורם נשקלת על פי רוב בחולים אשר מחלתם נשנתה זמן קצר מסיום קווי טיפול קודמים[1].
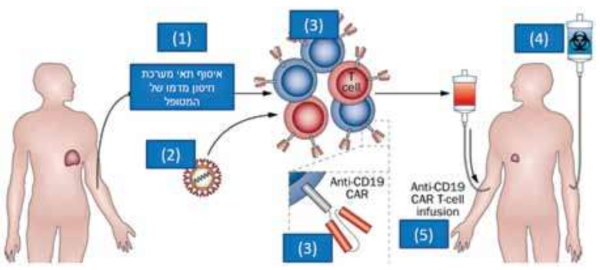
בחולים הסובלים מלימפומה, תאי מערכת החיסון של המטופל "תשושים" (Exhausted) ואינם מסוגלים לתקוף את תאי הלימפומה ולהשמידם. בטיפול חדשני הקרוי "Chimeric Antigen Receptor - CAR T cells", מוצאים תאי T של המטופל מגופו ועוברים שינוי גנטי שבעקבותיו הם מציגים חלבון ייחודי שחלקו רצפטור תא ה-T וחלקו החוץ-תאי פועל כנוגדן ונקשר ספציפית לתאי B. בעקבות קישור תא T התוקף לתאי הלימפומה חלה הפעלה של התא התוקף כך שיתקוף סלקטיבית את תאי המחלה. טיפול זה מוצע במרכזים מחקריים בודדים בעולם ומשמש לטיפול בחולים שמחלתם נשנתה על אף מספר קווי טיפול.
דווח שטיפול ב-CAR הביא לתגובות טובות בקבוצה קטנה של חולי לימפומה פוליקולרית אשר מחלתם נשנתה.
לימפומה מרג'ינלית
לימפומה של האזור המרג'ינלי (Marginal zone lymphoma - MZL), היא הסוג השלישי בשכיחותו של NHL.
ישנם שלושה סוגים של MZL (טבלה 3 מציגה את מאפייני הלימפומה המרג'ינלית לסוגיה השונים):
- לימפומה אקסטרה-נודלית (Extranodal MZL, EMZL)
- לימפומה טחולית (Splenic MZL, SMZL)
- לימפומה נודלית (Nodal MZL, NMZL)
| MZL סוג | EMZL | SMZL | NMZL |
|---|---|---|---|
| גיל חציון | 60 | 65 | 60-50 |
| פתוגנזה | הליקובקטר פילורי, קמפילובקטר ג'ג'וני, כלמידיה פסיטקי ובורליה בורגדורפרי | לרוב לא ידוע הפטיטיס C | לא ידוע הפטיטיס C |
| מאפיינים קליניים | לרוב מחלה באתר אחד אקסטראנודלי | ספירת דם לא תקינה ספלנומגליה | מעורבות בלוטות מפושטת |
- Zinzani PL. The many faces of marginal zone lymphoma. Hematology Am Soc Hematol Educ Program. 2012;2012:426-32[14]
MZL אקסטרה-נודלית (EMZL)
EMZL, הנקראת גם MALT lymphoma (Mucosa-associated lymphatic tissue), היא לימפומה המתפתחת באזורים לימפואידיים ברקמות ריריות, אקסטרנודליות. סוג זה הוא השכיח ביותר בקבוצה, ומהווה 50–70 אחוזים מכלל ה-MZL. הקיבה היא האיבר המעורב ביותר, אך תיתכן מעורבות בלוטות הרוק, בלוטות הדמעות, ארובת העין, עור, הריאה ועוד. הגידול נשאר לרוב ממוקם אך עשוי להתפשט סיסטמית ואף לעבור התמרה ללימפומה אגרסיבית[15][14]. לימפומה זו מהווה 5 אחוזים מכל מקרי ה-NHL וכ-50 אחוזים מכל מקרי הלימפומה בקיבה.
התפתחות לימפומת MALT תוארה במקרים רבים כקשורה לנוכחות גירוי כרוני, לרוב חיידקי או אוטואימוני. הדוגמה השכיחה לכך היא הקשר בין גסטריטיס כרונית הנגרמת על ידי הליקובקטר פילורי (HP) והתפתחות MALT בקיבה[14].
הטיפול ב-Gastric MALT: הטיפול נקבע על פי שלב המחלה ונוכחות או היעדר החיידק HP במטופל. קו הטיפול הראשון בחולים בשלב מחלה מוקדם הוא טיפול להכחדת החיידק (אנטיביוטיקה במשולב עם Proton Pump Inhibitor - PPI) הן בחולים שנמצאו חיוביים ל-HP והן בחולים בהם לא הוכחה נוכחותו, כיוון שחלק משמעותי מחולים אלה מגיבים גם הם לטיפול זה. בחולים שלא הגיבו לטיפול האנטיביוטי המשולב, ובחולים שבהם תאי המחלה מבטאים טרנסלוקציה מסוג (11;18) T ולפיכך סיכוייהם להגיב לטיפול זה נמוכים, ניתן לטפל בטיפול קרינתי מקומי או בריטוקסימאב (לבד או בשילוב עם כימותרפיה). חולים עם מחלה בשלב מתקדם בהם נמצא HP מטופלים להכחדת המחלה וממשיכים במעקב הדוק. אם מתפתחים תסמינים או שיש עדות להתקדמות המחלה, יינתן טיפול בריטוקסימאב בשילוב עם כימותרפיה או ריטוקסימאב בלבד[4][15][14].
הטיפול ב-Non-Gastric MALT: קרינה מקומית היא טיפול הבחירה במרבית המקרים בהם המחלה ממוקמת. במחלה בשלב מתקדם מקובל לטפל בדומה לחולי לימפומה פוליקולרית: בחולים ללא תסמינים שמחלתם יציבה ניתן להסתפק במעקב, ואילו בחולים בעלי תסמינים שמחלתם מתקדמת או כשעומס הלימפומה גדול, הטיפול הוא כימו-אימונותרפיה (ריטוקסימאב בשילוב עם כלורמבוציל/CVP/CHOP/בנדמוסטין/Purine analogues) או ריטוקסימאב בלבד, בעיקר בחולים שמצבם הכללי ירוד[4][15][16].
(SMZL) טחולית MZL
מחלה זו מערבת לרוב את הטחול, בלוטות הלימפה שבשער הטחול, מח העצם והדם הפריפרי, והיא מהווה פחות מ-5 אחוזים מכלל ה-NHL. זוהה קשר בין התפתחות MZL טחולית לבין הימצאות נגיף הפטיטיס C, ומשערים כי אנטיגנים של הנגיף מהווים גירוי אימונולוגי מתמשך המעורר התפתחות המחלה. נמצא גם מתאם בין מקרים של MZL טחולית להימצאות Mixed cryoglobulinemia. החולים מתייצגים לרוב עם ספלנומגליה, לימפוציטוזיס וציטופניות (לרוב עקב היפרספלניזם). לימפאדנופתיה, מעורבות איברים אקסטרה-לימפטיים ותסמיני B אינם שכיחים. הטיפול ב-MZL טחולית, באמצעות ריטוקסימאב או כריתת טחול, ניתן בעיקר למטופלים הסובלים מהגדלת טחול משמעותית, תסמינים סיסטמיים וציטופניות משמעותיות[17][18]. מטופלים ללא תסמינים זקוקים לרוב למעקב בלבד. למטופלים עם הפטיטיס C, ניתן לתת טיפול אנטי-ויראלי, אשר דווח כיעיל בחלק ניכר מהחולים[17].
(NMZL) נודלית MZL
NMZL מהווה כ-1 אחוז בלבד מכל מקרי ה-NHL. מרבית המטופלים הם ללא תסמינים בזמן האבחנה, על אף שהם מתייצגים עם מחלה מתקדמת. הטיפול מבוסס על המתווה שתואר בלימפומה פוליקולרית, כשבחולים בהם המחלה מוגבלת ניתן לטפל בקרינה, ובחולים שהמחלה אובחנה אצלם בשלבים מתקדמים ההחלטה אם לעקוב או לטפל מותנית בנוכחות או בהיעדר תסמינים, עומס המחלה וקצב התקדמותה[15][17].
לסיכום
הלימפומות האינדולנטיות מתאפיינות לרוב בהתפתחות איטית, ולכן הן מאובחנות, ברוב המקרים, בשלב מתקדם. המהלך הקליני נע בין מהלך איטי הנמשך שנים רבות, לבין לימפומה שמתקדמת במהירות ואף עוברת התמרה ללימפומה אגרסיבית. במחלה מוגבלת ניתן לטפל בקרינה, ואילו אחרי חולים ללא תסמינים שמחלתם מתקדמת ניתן לעקוב ולטפל רק אם הם מפתחים תסמינים או שמסת מחלתם גדולה או גדלה במהירות. הטיפול במקרה זה הוא כימו-אימונותרפיה.
תרופות חדשות המשפיעות על התאים שבסביבת הלימפומה או על תהליכים בתא הממאיר וכן טיפולים המגייסים את מערכת החיסון למלחמה בלימפומה כבר אושרו או נמצאים בשלבים שונים של מחקר קליני.
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 Gribben JG. How I treat indolent lymphoma. Blood. 2007 June 1;109(11):4617-26.
- ↑ Cheson BD, Fisher RI, Barington SF, et al. Recommendations for initial evaluation, staging and relapse assessment of Hodgkin and non-Hodgkin Lymphoma: The Lugano classification. J Clin Oncol. 2014 September 20; 32(27):3059-67
- ↑ 3.0 3.1 Solal-Celigny P, Roy P, Colombat P, et al. Follicular lymphoma international prognostic index. Blood. 2004;104:1258-1265
- ↑ 4.0 4.1 4.2 Zelenetz AD, Gordon LI, Wierda WG, et al. NCCN clinical practice guidelines in oncology: non¬Hodgkin’s lymphomas. Version 4, 2014. Available at: http://www.nccn.org/professionals/ physician_gls/PDF/nhl.pdf
- ↑ MacManos MP and Hoppe RT. Is radiotherapy curative for stage I and II low-grade follicular lymphoma? Results of a long-term follow-up study of patients treated at Stanford University. J Clin Oncol. 1996 April;14(4):1282-1290
- ↑ Brice P, Bastion Y, Lepage E, et al., Comparison in low-tumor-burden follicular lymphomas between an initial no-treatment policy, prednimustine, or interferon alfa: a randomized study from the Groupe d'Etude des Lymphomes Folliculaires. Groupe d'Etude des Lymphomes de l'Adulte. J Clin Oncol. 1997;15:1110-1117
- ↑ Advani R, Rosenberg SA, Horning S. Stage I and II follicular non-Hodgkin's lymphoma: long-term follow-up of no initial therapy. J Clin Oncol. 2004;22:1454-1459
- ↑ Marcus R, Imrie K, Belch A, et al. CVP chemotherapy plus rituximab compared with CVP as first-line treatment for advanced follicular lymphoma. Blood. 2005;105:1417-1423
- ↑ Czuczman MS, Grillo-Lopez AJ, White CA, et al. Treatment of patients with low-grade B-cell lymphoma with the combination of chimeric anti-CD20 monoclonal antibody and CHOP chemotherapy. J Clin Oncol. 1999;17:268-276
- ↑ Friedberg JW. The emerging role of bendamustine in follicular lymphoma. Leuk Lymphoma. 2009 March;50(3):317-18
- ↑ Davis TA, Grillo-Lopez AJ, White CA, et al. Rituximab anti CD20 monoclonal antibody therapy in non¬Hodgkin's lymphoma: Safety and efficacy of re¬treatment. J Clin Oncol. 2000; 18:3135-43
- ↑ Salles GA, Morschhauser F, Solal-Celigny P et al. Obinutuzumab (GA101) in patients with relapsed/ refractory indolent non-Hodgkin lymphoma: Results from the phase II GAUGUIN study. J Clin Oncol. 2000; 18:3135-43
- ↑ Bachy E, Salles G. Are we nearing an era of chemotherapy-free management of indolent lymphoma? Clin Cancer Res. 2014 October 15; 20(20):5226-39
- ↑ 14.0 14.1 14.2 14.3 14.4 Zinzani PL. The many faces of marginal zone lymphoma. Hematology Am Soc Hematol Educ Program. 2012;2012:426-32
- ↑ 15.0 15.1 15.2 15.3 Vannata B, Stathis A, Zucca E. Management of the marginal zone lymphomas. Cancer Treat Res. 2015 February 7;165:227-49
- ↑ Luminari S, Goldaniga M, Cesaretti M, et al. A phase II study of bendamustine in combination with rituximab as initial treatment for patients with indolent non- follicular non-Hodgkin’s lymphoma. Leuk Lymphoma. 2015 Sep 17:1-31. [Epub ahead of print]
- ↑ 17.0 17.1 17.2 Reid R, Friedberg JW. Management of marginal zone lymphoma. Oncology. 2013 September; 27(9): 840-44
- ↑ Olzewski AJ, Ali S. Comparative outcomes of Rituximab-based systemic therapy and splenectomy in splenic marginal zone lymphoma. Ann Hematol. 2014 March;93(3):449-58
המידע שבדף זה נכתב על ידי ד"ר חוה פרי - המערך ההמטולוגי והשתלות מח עצם, המרכז הרפואי תל אביב, ופרופסור עירית אביבי - המערך ההמטולוגי והשתלות מח עצם, המרכז הרפואי תל אביב והפקולטה לרפואה ע"ש סאקלר, אוניברסיטת תל אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק