מלנומה בעין - Eye melanoma
| מלנומה בעין | ||
|---|---|---|
| Eye melanoma | ||
| ||
| יוצר הערך | ד"ר שחר פרנקל | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מלנומה
מבוא
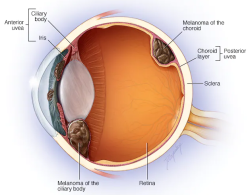
מלנומה ממאירה יכולה להופיע במספר תצורות בעין ובסביבתה. ניתן למצוא מלנומה עורית בעור העפעפיים כבכול מקום אחר בעור הגוף. מלנומה יכולה להופיע על פני שטח גלגל העין, בציפוי המוקוזלי של העין הנקרא לחמית (Conjunctiva). סוג זה דומה מאוד למלנומה העורית במאפייניו הגנטיים ובאופן הפיזור הגרורתי לבלוטות לימפה מנקזות סמוכות (בלוטות זקיף) ומשם לאתרים מרוחקים. הסוג השכיח ביותר הוא מלנומה תוך-עינית בענביה (Uveal Melanoma - UM), שהיא השכבה האמצעית בקיר העין וכוללת את הקשתית (Iris), גוף העטרה (Ciliary body) והדמית (Choroid). סוג זה של מלנומה שונה לחלוטין במאפייניו ממלנומה עורית (וממלנומה של הלחמית), עם מוטציות שונות (אין מוטציה ב-BRAF או ב-NRAS), ופיזור גרורתי שונה (המטוגני - בראש ובראשונה לכבד). התצורה האחרונה היא מלנומה בארובת העין, מאחורי העין. זוהי תצורה נדירה ביותר, וכאשר היא מופיעה היא לרוב גרורה ממלנומה עורית. נדירה עוד יותר, ברמה של מקרים בודדים בספרות הרפואית, היא מלנומה ראשונית בארובת העין.
מלנומה של הענביה - UM
זהו הגידול הראשוני התוך-עיני השכיח ביותר במבוגרים, ובישראל יש כ-6.7 מקרים חדשים למיליון מדי שנה באוכלוסייה היהודית, וכ-1.7 מקרים חדשים למיליון באוכלוסייה הערבית[1]. לא ידוע על גורמי סיכון ל-UM, גם לא חשיפה לקרינה על-סגולה (UV - Ultra Violet).
לכ-85 אחוזים מהמלנומות של הענביה יש מוטציות ב-GNAQ או ב-GNA11. בנוסף, לכ-75 אחוזים מה-UM יש מוטציה באחד משלושת הגנים הבאים: BAP1, SF3B1 ו-EIF1AX. יש לכך גם משמעות פרוגנוסטית כאשר גידולים עם מוטציה ב-BAP1 ישלחו גרורות בשלב מוקדם, גידולים עם מוטציה ב-SF3B1 ישלחו גרורות בשלב מאוחר, ונדיר למצוא מחלה גרורתית במטופלים שבמלנומה שלהם יש מוטציה בגן EIF1AX. מעניין להזכיר כי גם נגעים מלנוציטריים לפטומנינגאלים נושאים מוטציות ב-11/GNAQ וכן ב-SF3B1 או ב-EIF1AX.
דרכים מולקולריות נוספות לקביעת הפרוגנוזה כוללות אפיון השינויים הכרומוזומליים החלים בגידולים (מונוזומיה של כרומוזום 3, תוספת 6q ואובדן 8q הם כולם סמנים פרוגנוסטיים גרועים), וכן שינויים בתבנית ביטוי הגנים (Gene Expression Profile - GEP). בעזרת ה-GEP חולקו מלנומות הענביה לשתי קבוצות עיקריות 1 Class ו-2 Class, עם פרוגנוזה טובה (ללא גרורות כלל) ופרוגנוזה רעה, בהתאמה. כל אחת משתי הקטגוריות הללו חולקה לשתי קבוצות - Class 1A ו-Class 1B וכן Class 2A ו-Class 2B. מחקרי השוואה שונים מצאו התאמה בין קבוצות אלו ובין מוטציות ב-EIF1AX ,SF3B ,BAP1.
כדי להגיע לדגימות אלו דרושה ביופסיה מתוך הגידול, שנעשית בעולם בעיקר לצרכים פרוגנוסטיים או מחקריים. דווקא בנגעים הקטנים יותר, כאשר רוצים לדעת אם מדובר בנבוס (שומה) גדול או במלנומה קטנה, יעילות לקיחת דגימה ייצוגית בביופסיה היא נמוכה. עם זאת, במקרים חריגים בהם יש קושי להגיע לאבחנה קלינית, ביופסיה עשויה לעזור.
האבחנה נעשית בדרך כלל בבדיקה שגרתית לבעיות עיניים אחרות, או בשל תלונות על הפרעות בראייה. האבחנה מבוססת על בדיקה קלינית בשילוב ממצאי בדיקת אולטראסאונד (US). יש להבדיל בין UM ובין גידולים שפירים בעין, כגון נקודות חן וגידולי כלי דם (המנגיומות), ולכך דרוש ניסיון קליני. צילומים נוספים אינם הכרחיים לאבחנה, אלא לצורך מעקב בלבד. לפעמים צילום מסוג [[Optical Coherence Tomography) [[OCT) יכול לעזור להבדיל בין UM ובין גרורות בשכבת הדמית של העין על ידי הבחנה בין פני שטח חלקים (UM) לפני שטח לא סדירים (גרורה). על פי מדידת קוטר הגידול וגובהו ניתן לחלק את הגידולים לקבוצות - דירוג (Staging) שנקבע באיגוד האמריקני AJCC (American Joint Committee on Cancer). חלוקה זו לקבוצות קושרה גם היא לפרוגנוזה, אך אין לה משמעות טיפולית. בבואנו לטפל בגידול תוך-עיני ממאיר כ-UM, עלינו להעמיד בפני המטופל את מטרות הטיפול בסדר העדיפויות הבא: שמירה על החיים, העין והראייה. כדי להציל חיים, יש לעיתים להקריב את העין. אך בכל מקרה בו אפשר להציל את העין, נעשה זאת, וגם ננסה ככל האפשר לשמר את הראייה.
ישנן שיטות שונות לטיפול ב-UM, והן נקבעות בהתאם לגודל הגידול ולמיקומו, אך גם על פי גורמים אחרים, כגון מצב הראייה, מצב הבריאות הכללי של המטופל וממצאים אחרים בעין. הטיפול השכיח ביותר ב-UM הוא הקרנה של הגידול במינונים גבוהים מאוד, שכן ה-UM אינה רגישה לקרינה במינונים המקובלים בגידולים אחרים. דרכי ההקרנה האפשריות הן הקרנה מקומית - ברכיתרפיה - באמצעות לוחית רדיואקטיבית המוצמדת ללובן העין מעבר לגידול (תמונה מספר 1), או הקרנה חיצונית ממוקדת, למשל על ידי רדיוכירורגיה סטראוטקטית (Stereotactic Radiosurgery) בעזרת מאיץ קווי, הקיים במרכזים רפואיים מובילים בישראל ומחוץ לה ומשמש במקור להקרנת גידולי מוח. לעיתים אין ברירה אלא לעקור את העין הנגועה (אנוקלאציה).
הטיפול הנפוץ ביותר ב-UM הוא הברכיתרפיה, המאפשרת טיפול ממוקד בגידול עם פגיעה מועטה ברקמות הסובבות אותו בתוך העין, בדגש על פגיעה ברשתית, בעצב הראייה ובעדשה.

A. לוחית 106-Ru עשויה מכסף ומצופה על פני המשטח הפנימי שלה בחומר רדיואקטיבי בפיזור אחיד. יש לוחיות עגולות וכן לוחיות עם חלק חסר להתאמה בצמוד ללימבוס או עם שנץ כפי שנראה בתמונה, שניתן להכניס אליו את עצב הראייה, להקרנה בצמוד לעצב.
B. לוחית זהב על בסיס הלוחיות שהיו בשימוש במחקר ה-COMS ובתוכה חומר פלסטי/סיליקוני בו משובצים "זרעי" היוד הרדיואקטיבי. ניתן לשבץ זרעים בעוצמות שונות ועל פי צורת הגידול ומשך הזמן שרוצים להקרין.
C. מודל עין ועליו שני סוגי הלוחיות להשוואת צורתן וגודלן היחסי. קל יותר להשתיל את לוחיות הרוטניום הדקות יותר.
החומרים הרדיואקטיביים הנפוצים ביותר בשימוש בברכיתרפיה הם (106-Ruthenium) Ru ו-(1–125) Iodine. לרוטניום הפולט קרינת בטא (אלקטרונים) טווח חדירה קצר, ולכן יש מומחים שאינם משתמשים בו לגידולים בגובה של יותר מ-5 מילימטר. לעומתם, יש מומחים המדווחים על הצלחה טיפולית טובה גם בגידולים גבוהים יותר אפילו עד מעל ל-10 מילימטר גובה[2]. יוד רדיואקטיבי פולט קרינת גמא וחודר לעומק ניכר, ולכן הוא גם מגיע במינון גבוה לעומק הגידול, אך מסיבה זו הוא גם גורם לפגיעה רבה יותר ברקמות התוך-עיניות כגון העדשה, הרשתית ועצב הראייה. זו הסיבה שאפשר לשמר את הראייה טוב יותר בשימוש בלוחיות של רוטניום[3]. סיבה נוספת היא שבשימוש בלוחיות רוטניום אפשר להצמיד את הלוחית לקיר העין ללא שוליים בצד הגידול הקרוב לפובאה (מרכז הראייה) או לעצב הראייה, ועדיין להשיג שליטה טובה על הגידול תוך צמצום הפגיעה בראייה, דבר שאינו אפשרי בשימוש בלוחיות יוד[4].
יש המוסיפים לברכיתרפיה טיפול חימום באמצעות לייזר (Transpupillary Thermotherapy - TTT) לחלק הפנימי של הגידול, כדי להשלים את מינון הקרינה של הלוחית הרדיואקטיבית המקרינה מבחוץ - שיטת הסנדוויץ'. ה-TTT, שנוסה במקור כטיפול ראשוני, הוכח כלא יעיל כטיפול יחיד, גם לא בגידולים קטנים, וגם אלו שהביאו אותו לעולם משתמשים בו רק כטיפול נוסף. גם היעילות כטיפול סנדוויץ' לא הוכחה באופן משכנע, ובמרבית המרכזים לא משתמשים בשיטה זו. בדומה, גם טיפול בלייזר בשיטת Photodynamic Therapy - PDT לא הוכח כיעיל נגד מלנומה UM.
תופעות לוואי נוספות של הטיפול הקרינתי במלנומה הן איסכמיה של הרשתית המובילה להפרשת VEGF (Vascular Endothelial Growth Factor) ולצמיחת כלי דם לא תקינים על פני הקשתית וזווית הלשכה הקדמית, כך שפתחי הניקוז של הנוזל התוך-עיני נסתמים והלחץ התוך-עיני עולה (Neovascular Glaucoma - NVG). מצב זה עלול להיות בלתי הפיך, ולהוביל לעליית לחץ תוך-עיני ולערכים גבוהים מאוד עם הופעת כאבים עזים בעין וסביבה, עד כדי התחננות של המטופל לעקירת העין. תופעת לוואי זו שכיחה יותר בהקרנות חיצוניות מאשר בברכיתרפיה. אם מטפלים בתופעה זו בזמן, ניתן בחלק מהמקרים לטפל בהזרקות של נוגדנים נגד VEGF ולהשיג את ה-NVG לאחור. תופעת לוואי אחרת המופיעה בהקרנת גידולים באזור גוף העטרה, היא הופעת תמס קיר העין. לעיתים המצב ניתן לתיקון, ולעיתים הוא מוביל לעקירת העין.
האנוקלאציה, שהייתה הדרך השכיחה ביותר לטיפול ב-UM עד סוף שנות השבעים של המאה ה-20, משמשת כטיפול ראשוני בגידולים גדולים מאוד, הן בקוטרם והן בגובהם, שבהם הסיכוי להצלחה בהקרנה נמוך, וגם כשיש תגובה טובה לקרינה, החומר הנמקי של הגידול המוקרן עלול להוביל לסיבוכים המצריכים את הוצאת העין.
כריתה של גידול מתוך העין נעשית לפעמים בגידולים של הקשתית וגידולים - Irido ciliary. כריתת מלנומה כורואידלית נעשית במרכזים בודדים בעולם באופן שגרתי, ובמספר מקומות נוספים, כמו בית החולים הדסה, במקרים חריגים. בדרך כלל כריתת מלנומה כורואידלית נעשית לאחר טיפול קרינתי ראשוני בברכיתרפיה.
הצלחת הטיפול נמדדת בהפסקת גדילת הגידול, צמצום גודלו ושינוי במאפייני הרקמה ב-US, כך שתדמה יותר לנקודת חן. ההצלחה מושגת בכ-90 אחוזים מהמטופלים לאחר ברכיתרפיה. היתר יעברו ברכיתרפיה חוזרת, הקרנה חיצונית או עקירת העין. עם זאת, עדיין יכולות להופיע גרורות.
על פי ההערכות, UM שולח גרורות לעיתים עוד לפני הביקור הראשון במרפאה. גידולים בקשתית כמעט לעולם אינם שולחים גרורות. גידולים בגוף העטרה שולחים יותר גרורות מחלקם היחסי מתוך סך המלנומות של הענביה, ככל הנראה בשל זמן גדילה ארוך יותר לפני שניתן לשים אליהן לב במיקומן המוסתר.
גרורות מגיעות בראש ובראשונה לכבד, אך יכולות להישאר שם כפיזור מיקרוסקופי רדום למשך שנים ארוכות. עובדה זו נקבעה לאחר אבחון גרורות שנים לאחר עקירת העין, מה שלא יכול להותיר שארית גידול ראשוני בגוף. השיא בהדסה היה אבחון גרורות 17 שנה לאחר הטיפול בגידול הראשוני, אך בעולם יש דיווחים על הופעת גרורות גם לאחר למעלה מ-20 שנה, ולפיכך דרוש מעקב חצי שנתי קבוע לכל החיים. לאחר ההופעה בכבד, מלנומה של הענביה יכולה להגיע לאיברים נוספים, אך בעיקר לריאות. לאחר הריאות הגידול יכול להתפזר למקומות אחרים בגוף, בדרך כלל בשלב הסופני של המחלה. בניגוד למלנומה עורית בה גרורות במוח הן דבר שבשגרה, נדיר ביותר, ברמה של תיאורי מקרה, למצוא פיזור גרורות ראשוני למוח ממלנומה של הענביה. לכן הדמיית ראש אינה חלק מהמעקב השגרתי הקבוע.
גרורות של UM יכולות להופיע ללא קשר למצב העין והראייה. אין טיפול יעיל לגרורות, ובסטטיסטיקה העולמית תוחלת החיים מהופעת גרורות עומדת על 12-7 חודשים בלבד. גרורות מופיעות באחד משני אופנים: מספר מצומצם של גרורות בודדות, ופיזור מיליארי של שפע גידולים קטנים על פני כל הכבד. לא ידוע מה מוביל לשתי צורות הופעה שונות אלו. גרורות בודדות ניתן לעיתים לכרות, פעולה היכולה להאריך משמעותית את תוחלת חיי המטופלים, פי 3–4 לעומת מצבים בהם לא ניתן לכרות את הגרורות[5][6]. אנו עוקבים גם אחר מטופלים ששרדו למעלה מ-10 שנים לאחר הופעת גרורות ולאחר כריתה וטיפולים כימיים. עם זאת, כאמור, מרבית הגרורות אינן מגיבות לכימותרפיה. ניסיונות שונים להשתמש בתרופות אימונותרפיות לוויסות התגובה הדלקתית וטיפולים מכווננים (ממוקדי מטרה, ביולוגיים) שונים, אכזבו ויש קושי לצרף חולי UM גרורתיים למחקרים רבים לטיפול במלנומה עורית. לפיכך, אנו עמלים במעבדה על פיתוח טיפול מכוונן חדש, בתקווה להביא מזור למטופלינו. במקביל אנו חוקרים סמנים ביולוגיים שונים בסרום לצורך אבחון מוקדם של הגרורות, בתקווה שאבחון מוקדם עם עומס גידולי מופחת יוביל לטיפול טוב יותר בגרורות.
מלנומה של הלחמית
השכבה הרירית (מוקוזה) המצפה את גלגל העין והצד הפנימי של העפעפיים היא הלחמית, ויכולים להופיע בה נגעים פיגמנטיים שפירים, טרום-ממאירים וממאירים. בנגעים השפירים אנו כוללים נקודות חן (נבוסים), נבוסים מודלקים של בני נוער (Inflamed Juvenile Conjunctival Nevi - IJCN) המופיעים על רקע אלרגי, פיגמנטציה המופיעה באנשים כהי עור (Complexion related melanosis), וכן הופעת מלנוזיס לחמיתי (Primary Acquired Melanosis - PAM). PAM שפיר לא יכלול בתוכו אטיפיה תוך-אפיתליאלית. כאשר PAM כולל בתוכו אטיפיה כזו, הוא הופך לנגע טרום-ממאיר עם כ-25 אחוזים סיכון להתמרה סרטנית למלנומה, שמצדה כוללת כ-25 אחוזי תמותה. כדי להבדיל בין שני סוגי PAM אלו, חייבים לקחת ביופסיה לאבחון היסטולוגי. גם עבור IJCN וגם עבור PAM יש יתרון בכך שאת האבחון יעשה פתולוג עיניים המודע לדקויות באבחנות אלו. מלנומה של הלחמית יכולה לצמוח מתוך PAM עם אטיפיה, או להופיע כגידול ראשוני על פני העין.
נגעים ממקור מלנוציטרי בלחמית העין אינם תמיד מייצרים מלנין, ולכן לעיתים הנגעים גדולים יותר ממה שנראה קלינית לעין הבודק. לעיתים קרובות הנגעים גם מפושטים מאוד על פני שטח הלחמית ואינם מאפשרים כריתה מלאה. תחום אונקולוגיית העין חלוק בגישה הנובעת מכך. יש המחזיקים בדעה שיש לבצע כריתות עם שוליים רחבים, להרוס את השוליים הניתוחיים בהקפאה, ולהשתמש בשתל אמניוטי לעזור לעין להחלים מהניתוח הרדיקלי. אנו מחזיקים בגישה ההפוכה, המצמצמת את הנזק המקומי ומתאימה טיפול משלים לכירורגיה על פי מידת החומרה ההיסטופתולוגית. טיפולים משלימים אלו כוללים שימוש בכימותרפיה מקומית בטיפות לנגעים טרום-ממאירים, ובהקרנה מקומית (ברכיתרפיה) למיטת הכריתה של מלנומה ממאירה עם לוחיות רוטניום שהוזכרו למעלה. רופאי הדסה (פרופ' י' פאר ופרופ' י' פרוכט) היו חלוצים בעולם בשימוש בכימותרפיה מקומית לגידולי פני שטח העין עם טיפול בטיפות מיטומיצין. חומר זה משמש לגידולים אפיתליאליים ולגידולים מלנוציטריים (במינון גבוה יותר). אך שימוש חוזר במיטומיצין במספר מחזורים רב עלול להוביל לדיכוי תאי האב (Stem cells) המחדשים את ציפוי שטח העין, ובמיוחד את ציפוי הקרנית. נזק זה עלול להוביל לאובדן שקיפות הקרנית, לפגיעה בראייה, ולעיתים אף לאובדן העין.
מלנומה בלחמית הטרסלית (Tarsal conjunctiva melanoma) המצפה את פנים העפעף עלולה להיות קשה לטיפול כירורגי. פותחה בארץ שיטה ייחודית בעולם לטיפול בברכיתרפיה ללחמית הטרסלית, שיטה שנמצאה יעילה נגד מספר סוגי גידולים במיקום זה, כולל לגידולים בעור העפעף מבחוץ. אנו יוצרים מעין כריך בו העפעף עם הגידול הוא המילוי, והפרוסות העוטפות הן הלוחית הרדיואקטיבית מצד אחד של העפעף, ולוחית דמי הבולמת את הקרינה בצדו השני של העפעף.
מיקום מלנומה בלחמית הטרסלית או באזור הקרונקולה (caruncule, "הכרית" בקצה הלחמית ליד האף) הוא גורם סיכון גבוה לפיזור גרורתי. מלנומה לחמיתית מתפשטת בפיזור לימפטי אל הבלוטות המנקזות את הלחמית: הבלוטות הפרוטידיות (פרה- אוריקולריות) והתת-לסתיות, ומהן אל כל הגוף. מומלץ לבדוק את בלוטות זקיף אלו לאתר פיזור גרורתי בשלב מוקדם. הטיפול במלנומה לחמיתית הוא כריתה עם השלמה של ברכיתרפיה מעל מיטת הגידול. אם מופיע פיזור גרורתי ניתן לטפל כמו במלנומות מוקוזליות אחרות.
מלנומה של עור העפעפיים
מלנומה עורית לכל דבר ועניין. מבחינת המיקום, זוהי הופעה לא שכיחה של מלנומה בכלל ובאזור העין בפרט. הייחודיות במיקום זה היא שבגידולים קטנים ניתן לטפל בכריתה מקומית, ובגידולים בינוניים ניתן לטפל בברכיתרפיה בשיטה הייחודית שפיתחנו ושהוזכרה למעלה לגבי גידולים בלחמית הטרסלית.
מלנומה ארובתית - Orbital melanoma
ארובת העין כוללת שומן ארובתי השומר על העין מפני חבלות מעצמות הארובה בתוכה היא יושבת, שרירים המזיזים את העין ועצבים. נדיר למצוא במיקום זה מלנוציטים בכלל ומלנומה בפרט. אם כבר יש מלנומות באזור זה, הן יהיו בדרך כלל גרורות של מלנומה עורית ממקום אחר בגוף, שאינו סביב העין. קיים קושי להגיע לגידולים בניתוח, ולכן טיפולים לאזור זה יהיו מבוססים על קרינה חיצונית או על טיפול תרופתי סיסטמי.
ביבליוגרפיה
- ↑ Iscovich J, Abdulrazik M, Pe'er J. Posterior uveal malignant: temporal stability and ethnic variation in rates in Israel. Anticancer Res. 2001 Mar- Apr;21(2B):1449-54
- ↑ Kaiserman N, Kaiserman I, Hendler K, et al. Ruthenium-106 plaque brachytherapy for thick posterior uveal melanomas. Br J Ophthalmol. 2009 Sep;93(9):1167-71. Epub 2009 Jun 30
- ↑ Damato B, Patel I, Campbell IR, et al. Visual acuity after Ruthenium (106) brachytherapy of choroidal melanomas. Int J Radiat Oncol Biol Phys. 2005 Oct 1;63(2):392-400
- ↑ Russo A, Laguardia M, Damato B. Eccentric ruthenium plaque radiotherapy of posterior choroidal melanoma. Graefes Arch Clin Exp Ophthalmol. 2012 Oct;250(10):1533-40. Epub 2012 Feb 23
- ↑ Frenkel S, Hendler K, Pe'er J. Uveal melanoma in Israel in the last two decades: characterization, treatment and prognosis. Isr Med Assoc J. 2009 May;11(5):280- 5
- ↑ Frenkel S, Nir H, Hendler K, et al. Long-term survival of uveal melanoma patients after surgery for liver metastases. Br J Ophthalmol. 2009 Aug;93(8):1042- 6. Epub 2009 May 7
המידע שבדף זה נכתב על ידי ד"ר שחר פרנקל - מנהל המעבדה לאונקולוגיה של העין, רופא בכיר בשירות גידולי העיניים, אגף עיניים, המרכז הרפואי הדסה, ירושלים


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק