מערכת המשלים ומחלות כליה - The complement system and renal diseases
הופניתם מהדף מערכת המשלים ומחלות כליה - Complement and renal diseases לדף הנוכחי.
| מערכת המשלים ומחלות כליה | ||
|---|---|---|
| Complement and renal diseases | ||
| ||
| יוצר הערך | ד"ר נועם טראוב, פרופ‘ מנחם שלזינגר, פרופ‘ אבישלום פומרנץ | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – מערכת המשלים, פגיעה כלייתית
חקר מערכת המשלים גרם לשינוי בהבנה של תהליכי מחלה שונים, בהם התהליכים הפתופזיולוגיים (Pathophysiology) של מחלת הכליה Membranoproliferative Glomerulonephritis (MPGN), ועשוי לסייע בעתיד לאבחנה של מחלות שונות ולפיתוחן של תרופות חדשות.
מערכת המשלים
שמה של מערכת המשלים נגזר מתפקידה - השלמת פעילות הנוגדנים בהרג חיידקים. במשך הזמן נמצאו תפקידים נוספים למערכת, בהם סילוק של קומפלקסים חיסוניים (Immune complex) מהגוף.
הפעלה
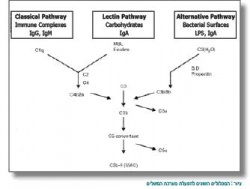
מערכת המשלים מורכבת מחלבונים רבים שנמצאים בנסיוב (Serum) בצורה בלתי פעילה. הפעלתה של המערכת יכולה להיעשות באמצעות שלושה מסלולים (Pathway): המסלול הקלאסי (Classical), מסלול לקטין קושר המאנוז (Mannose-binding lectin) והמסלול החליפי (Alternative)[1], [2]. שלושת המסלולים מובילים אל מסלול משותף שמטרתו להביא לסילוק של אנטיגנים (Antigen) זרים, כולל הרג של חיידקים בגוף (ראו איור משמאל).
המסלול הקלאסי - Classical pathway
מסלול זה מורכב מחלבונים C1-C9 (Complement 1-9).
המסלול מתחיל כאשר חלבון C1 נקשר לנוגדנים המוצמדים לאנטיגן על תא החיידק. C-reactive protein (CRP) יכול גם הוא להפעיל את C1, במקום הנוגדנים. הפעלה של C1 גורמת לשרשרת פעולות שבה נחתכים החלבונים C2, C4 ו-C3 (בסדר זה). C3b, תוצר הפירוק של C3, פותח את המסלול המשותף לכל מסלולי המשלים ומוביל ליצירת ה-Membrane attack complex שמביא להרס דופן החיידק.
מסלול לקטין קושר המאנוז - Mannose-binding lectin pathway
חלבון ה-Lectin נקשר אל Mannose המצוי על דופן תא החיידק. לאחר הקישור, פרוטאז (Protease) המצוי עליו (Mannose-binding protein-Associated Serine Protease 2, MASP2) פועל בדומה ל-C1, וגורם לביקוע של C4 ובהמשך ליצירה של C3b.
המסלול החליפי - Alternative pathway
המסלול מתחיל מביקוע עצמוני (Spontaneous) של C3 בפלזמה (Plasma). C3b נקשר אל פקטור (Factor) B, שמוביל ליצירה של C3b נוסף, המשמש במסלול המשותף במערכת המגבירה את עצמה.
בקרה
כדי שמערכת אנזימטית (Enzymatic) כה פעילה תפעל בצורה טובה, יש צורך בחלבונים שיהיו אחראיים לבקרה של מערכת המשלים. מבין אנזימי הבקרה השונים, נזכיר את C1 Inhibitor, שמבקר את שפעול מערכת המשלים מיד בהתחלה, ואת החלבונים (פקטורים) H ו-I שמשתתפים בוויסות המסלול החליפי.
C3b עשוי לגרום ללולאה (Loop) המגבירה את פעילות המערכת. כדי למנוע הגברה אינסופית של המערכת, דבר העלול להביא להרס של תאי המאכסן, יש מערכת הגורמת לפירוק של C3b לחלבונים בלתי פעילים. פקטורים H ו-I הם הגורמים להרס של C3b. פקטור H נקשר ל-C3b שעל גבי תאי המאכסן בזיקה (Affinity) גבוהה יותר מאשר פקטור B, וכך מונע הרס של תא המאכסן.
חסר של פקטור H עלול לגרום להפעלה בלתי מרוסנת של מערכת המשלים ולתגובת חיסון עצמי (Autoimmune reaction), שמתבטאת למשל ב-MPGN (ראו להלן) או בתסמונת המוליטית-אורמית (Hemolytic-Uremic Syndrome, HUS). דווח על מקרה שבו חולה כליות עם חסר תורשתי של פקטור H, עבר השתלה משולבת של כליה וכבד, ובעקבותיה התחיל לייצר פקטור H אשר מנע את הישנות המחלה בכליה המושתלת[3].
ליקויים וחסרים
במצב רגיל, אחראית מערכת המשלים לפינויים של קומפלקסים חיסוניים (למשל נוגדנים הקשורים לדופן של חיידק). במידה והיא נכשלת בכך, עלולים קומפלקסים חיסוניים אלו, להביא להפעלה מתמדת של המשלים ולמצב של דלקת מתמשכת. הדבר קורה למשל בזיהומים כרוניים (Chronic) כגון: HCV (Hepatitis C Virus), דלקת זיהומית של פנים הלב (Infective endocarditis)[4], Shunt nephritis - נפריטיס הקשורה בנקז לחדרי המוח[5], או במחלות שבהן יש נוגדנים המכוונים כנגד הגוף (Autoantibodies), כמו למשל מחלת Goodpasture, שבה הנוגדנים מכוונים כנגד קרום הבסיס (Basement membrane) של פקעיות הכליה (Glomerulus) והריאות.
חסר של מרכיבי משלים יגרום לנטייה לזיהומים, מחלות חיסון עצמי ומחלות של קומפלקסים חיסוניים. נמצא, כי אנשים עם חסר תורשתי של מרכיבי המשלים C1q ,C1r ,C1s ,C4 ,C2, נמצאים בסיכון ללקות בזאבת אדמנתית מערכתית (SLE ,Systemic Lupus Erythematosus)[6] ובמחלות חיסון עצמי אחרות. נראה כי המצאות פקטורים אלו מגנה מפני התפתחות SLE.
בתוך כך, פותחה השערת ה-Waste disposal המנסה להסביר תופעה זו ואחרות[2]. לפי השערה זו, מרכיבי המשלים נקשרים, במצב רגיל, אל תאים שעברו מוות תאי מתוכנן (Apoptosis), ובכך גורמים לפינויים מהגוף.
מחד גיסא, היעדר תגובה זו יגרום להצטברות של מרכיבי תא ומרכיבי גרעין מפורקים, ולתגובת חיסון עצמי הכוללת יצירת נוגדנים נגד אותם מרכיבים, ובכך יביא החסר במשלים להופעה של מחלות חיסון עצמי, כגון SLE. מאידך גיסא, בזמן מחלת SLE פעילה יש צריכה מוגברת של מרכיבי משלים, המתבטאת ברמות משלים נמוכות בדם.
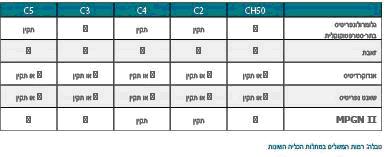
רמות נמוכות של C3 ו-C4 נמצאו בחולי SLE בעת שסבלו ממחלה כלייתית פעילה[7], (ראו טבלה). כמו כן, נמצאו רמות נמוכות של C3 ו-CH50 בחולי SLE בשנתיים שלפני הופעת הנפריטיס[8].
רמות נמוכות של משלים (Hypocomplementemia) אופייניות גם לגלומרולונפריטיס בתר-סטרפטוקוקלית (Post-Streptococcal Glomerulonephritis, PSGN). במחלה זו, רמות המשלים לרוב חוזרות לנורמה בתוך 8 שבועות, אולם לעתים נשארות הרמות הנמוכות בדם לתקופה ממושכת יותר[9]. הנפריטיס ב-Henoch-Schönlein Purpura (HSP) דומה לזו של PSGN[10], ורמות המשלים (CH50 ,C3 ,C4) הנמוכות ב-HSP חוזרות לנורמה בתוך 5 שבועות.
מערכת המשלים ומחלות כליה
מערכת המשלים נמצאה קשורה למחלות כליה רבות[11]. זאת ניתן להבין בזוכרנו שהכליה היא איבר עשיר בכלי דם, ולתוך פקעית הכליה מתנקזים מרכיבי משלים רבים וכך היא חשופה להשפעתם. תאי הכליה עשויים לייצר בעצמם מרכיבי משלים[12], [13], וכך עלולים לתרום להיווצרות דלקת בכליה.
פקטורים נפריטיים
פקטורים נפריטיים (Nephritic Factors) הם נוגדני IgG (Immunoglobulin G) שמגנים על מערכת המשלים מפני פירוק (Degradation). בעשותם זאת, הם מביאים להגברה של פעולת המשלים ובכך לירידה של רמת C3 בפלזמה. פקטורים אלה כוללים:
- נוגדנים כנגד C1q - תוארו ונמצאו קשורים לנפריטיס בחולי SLE[14]
- C4NeF (C4 Nephritic Factor) - נוגדן IgG נוסף, נקשר אל C4b2a [אנזים (Enzyme) ה-Convertase של המסלול הקלאסי][15] ומייצב אותו, ובכך מאריך את זמן מחצית החיים שלו. הוא תואר ב-PSGN וכן ב-SLE. הצריכה המוגברת של C3 במחלות אלו עשויה להיות מוסברת על ידי פקטור זה, על ידי קומפלקסים חיסוניים או על ידי שניהם
- C3NeF (C3 Nephritic Factor) - גורם נפריטי שתואר במסלול החליפי, נקרא גם 'הפקטור הנפריטי של מסלול ההגברה' (Nephritic Factor of the amplification loop, NFa). נוגדן זה מייצב את האנזים C3bBb, ה-Convertase של המסלול החליפי[16]. המצאותו נמצאה קשורה ל-MPGN וכן ל-Partial Lipodystrophy. במחקר אחד נמצאה פעילות של C3NeF בלפחות 60 אחוז מחולי MPGN, דבר שהביא לרמות נמוכות של C3 ושל CH50[17]. אולם, פקטור זה נמצא גם במחלות אחרות של פקעיות הכליה, בכללן נפריטיס של SLE (Lupus nephritis)[18] ו-PSGN[19], ואף באנשים בריאים
- NFt (Nephritic Factor of the terminal pathway) - הפקטור הנפריטי של המסלול הסופי (ראו להלן)
Membranoproliferative Glomerulonephritis (MPGN)
MPGN מהווה כ-10-5 אחוזים ממקרי התסמונת הנפרוטית (Nephrotic syndrome) בילדים. מצב זה יכול להיות עלום (Idiopathic) או משני למחלות אחרות.
MPGN מתבטא בדרך כלל כתסמונת נפרוטית עם מרכיב נפריטי (Nephritic) ושתן דמי (Hematuria). המהלך הקליני הוא של התקדמות איטית אך מתמדת לעבר מחלת כליה סופנית (End Stage Renal Disease, ESRD).
במיקרוסקופ האור (Optical microscope), מתאפיין MPGN בהיפרצלולריות (Hypercellularity) [בשל שגשוג (Proliferation) של תאים במזנגיום (Mesangium)], בעיבוי קרום הבסיס של פקעית הכליה (Glomerular Basement Membrane, GBM), וכן בהגברה של המשתית המזנגיאלית (Mesangial matrix). כאשר בוחנים את דגימות הרקמה (Biopsy) במיקרוסקופ אלקטרונים (Electron microscope, EM), מתגלה תת-חלוקה של MPGN לשלושה סוגים:
- MPGN סוג I מתאפיין בהכפלת קרום הבסיס שליד נימי הדם (Capillary), וכן במשקעים תת-אנדותליאליים (Subendothelial deposits), שבהם ניתן למצוא את C1q ,C4, C3 וכן את IgG
- MPGN סוג II מתאפיין במשקעים דמויי עניבה ב-GBM הנראים ב-EM. משום כך, סוג זה נקרא גם Dense Deposit Disease (DDD)[20]. בחולי DDD ניתן למצוא רמות נמוכות של C3, אך רמות תקינות של C4. כמו כן, ניתן למצוא אצלם רמות נמוכות של פקטור B ושל Properdin, שהם מרכיבים של המסלול החליפי. ביותר מ-70 אחוז מהחולים בסוג זה של MPGN ניתן למצוא את C3NeF, שהוא, כאמור, נוגדן שנקשר ל-C3bBb. קישור זה מייצב את Convertase זה של C3, מגן עליו מפני פירוק אנזימטי (Enzymatic degradation) ובכך גורם לביקוע מתמיד של C3
- MPGN סוג III הוא נדיר, ומהווה שילוב של מאפייני הסוגים I ו-II
MPGN יכול להיות משני למצבי מחלה שונים ובכלל זה, מצבים כרוניים הקשורים בקומפלקסים חיסוניים [SLE, HBV (Hepatitis B Virus), HCV, דלקת פנים הלב, מורסות (Abscess) כרוניות, בילהרציה (Schistosomiasis)], ממאירויות, Partial Lipodystrophy ומצבים תורשתיים של חסר במרכיבי מערכת המשלים.
המשותף לכל המצבים התורשתיים של חסר במרכיבי המשלים שנמצאו קשורים ל-MPGN, הוא פגיעה בתפקוד של פקטור H. כאמור, פקטור זה מונע הפעלת-יתר של מערכת המשלים ליד תאי המאכסן, לכן פגיעה בתפקודו תביא בהכרח להפעלת-יתר של המערכת ולירידה ב-C3. המצבים התורשתיים הללו הם[21]: חסר הומוזיגוטי (Homozygote) של פקטור H, מחלת Marder [חסר הטרוזיגוטי (Heterozygote) של אתר הקישור לפקטור H על C3b], הימצאות נוגדן המעכב את פקטור H או פקטורים נפריטיים.
מבין הפקטורים הנפריטיים הקשורים לMPGN, ציינו כבר את C3NeF (NFa). פקטור נפריטי נוסף הוא NFt, שאחראי לרמות המשלים הנמוכות ב-MPGN סוג III (רמות נמוכות של C3 ,C5 ופקטורים נוספים של המסלול הסופי של מערכת המשלים). ייתכן וזה ה-Convertase של C5. על אף היותו קשור ל-MPGN סוג III, NFt נמצא בכ-20 אחוז מהסובלים מ-MPGN סוג I.
ביבליוגרפיה
- ↑ Walport MJ. Complement (First of two parts) N Engl J Med 2001;344:14:1058-1066
- ↑ 2.0 2.1 Walport MJ. Complement (Second of two parts) N Engl J Med 2001;344:1140-1144
- ↑ Remuzzi G, Ruggementi P, Codazzi D, et al. Combined liver and kidney transplantation for familial haemolytic uraemic syndrome. Lancet 2002;359:1671-1672
- ↑ Messias-Reason IJ, Hayashi SY, Nisihara RM, Kirschfink M. Complement activation in infective endocarditis: correlation with extracardiac manifestations and prognosis. Clin Exp Immunol 2002;127:310-315
- ↑ Haffner D, Schindera F, Aschoff A, et al. The clinical spectrum of shunt nephritis. Nephrol Dial Transplant 1997;12:1143-1148
- ↑ Pickering MC, Botto M, Taylor PR, et al. Systemic lupus erythematosus, complement deficiency, and apoptosis. Adv Immunol 2001;76:227-324
- ↑ Ho A, Barr SG, Magder LS, Petri M. A decrease in complement is associated with increased renal and hematologic activity in patients with systemic lupus erythematosus. Arthritis Rheum 2001;44(10):2350-2357
- ↑ Wada Y, Ito S, Ueno M, et al. Renal outcome and predictors of clinical renal involvement in patients with silent lupus nephritis. Nephron Clin Pract 2004;98(4):105-111
- ↑ Deodoglu IO, Springate JE, Waz WR, et al. Prolonged hypocomplementemia in poststreptococcal acute glomerulonephritis. Clin Nephrol 1996;46(5):302-305
- ↑ Motoyama O, Iitaka K. Henoch-Schonlein purpura with hypocomplementemia in children. Pediatrics International 2005;47:39-42
- ↑ Trouw LA, Seelen MA, Daha MR. Complement and renal disease. Molecular Immunology 2003;40:125-134
- ↑ Sheerrin NS, Sacks SH. The local production of complement in the pathogenesis of renal inflammation. Nephrologie 1999;20:377-382
- ↑ Zhou W, Marsh JE, Sacks SH. Intrarenal synthesis of complement. Kidney International 2001;59:1227-1235
- ↑ Horvath L, Czirjak L, Fekete B, et al. High levels of antibodies against C1q are associated with disease activity and nephritis but not with other organ manifestations in SLE patients. Clin Exp Rheumatol 2001;19:667-672
- ↑ Daha MR, van Es LA. Relative resistance of the F-42 stabilized classical pathway C3 convertase to inactivation by C4-binding protein. J Immunol 1980;125:2051-2054
- ↑ Daha MR, Fearon DT, Austen KF. C3 nephritic factor (C3NeF): stabilization of fluid phase and cell-bound alternative pathway convertase. J Immunol 1976;116:1-7
- ↑ Schwertz R, Rother U, Anders D, et al. Complement analysis in children with idiopathic membranoproliferative glomerulonephritis: a long-term follow-up. Pediatr Allergy Immunol 2001;12:166-172
- ↑ Walport MJ, Davies KA, Botto M, et al. C3 nephritic factor and SLE: report of four cases and review of the literature. Q J Med 1994;87:609-615
- ↑ Fremeaux-Bacchi V, Weiss L, Demouchy C, et al. Hypocomplementemia of poststrptococcal acute glomerulonephritis is associated with C3 nephritic factor (C3NeF) IgG autoantibody activity. Nephrol Dial Transplant 1994;9:1747-1750
- ↑ Walker DW. Dense deposit disease: new insights. Curr Opin Nephrol Hypertens 2007;16:204-212
- ↑ West CD, McAdams AJ. The alternative pathway C3 convertase and glomerular deposits. Pediatr Nephrol 1999;13(5):448-453
המידע שבדף זה נכתב על ידי ד"ר נועם טראוב, היחידה למחלות כליה, בית החולים מאיר, כפר סבא; פרופ‘ מנחם שלזינגר, מנהל מח’ ילדים ואימונולוגיה קלינית, בית החולים ברזילי, אשקלון; פרופ‘ אבישלום פומרנץ, מנהל היחידה למחלות כליה בילדים והמרפאה לאי שליטה על מתן שתן, בית החולים מאיר, מרכז רפואי ספיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק