הבדלים בין גרסאות בדף "נוגדנים לקולטן של Phospholipase A2 receptor antibodies - phospholipase A2"
| שורה 63: | שורה 63: | ||
==החיוניות של מדד נוגדנים כנגד PLA2R להערכת הטיפול המתאים ב-IMN== | ==החיוניות של מדד נוגדנים כנגד PLA2R להערכת הטיפול המתאים ב-IMN== | ||
| + | התרפיה העיקרית ב-30 השנים האחרונות התבססה על דיכוי בלתי-ספציפי של מערכת החיסון, שנקבעה באופן אמפירי בשימוש משולב של ציקלופוספמיד וסטרואידים. כתוצאה מחסר של מדד ביולוגי רלוונטי של אימונו-פתולוגיה, נעשה שימוש ברמיסיה של פרוטאינוריה כמדד של תוצא דומיננטי. למרות שתכשירים לא-ספציפיים אלה יכולים להתברר כיעילים למניעה של התקדמות המחלה ב-60-80% מהמטופלים, טיפול זה גובה תשלום יקר בתחלואה ואף בתמותה כתוצאה מהגברת הסיכון להדבקות בפתוגנים שונים, ממאירות, ואירועים קרדיו-וסקולריים. רוב המטופלים חווים מהלך מחלה מחזורית של רמיסיות ומשברים, בהם מתבקש טיפול של דיכוי של מערכת החיסון, כאשר חלק מהמטופלים מראים עמידות לטיפול האחרון. נתונים אלה מחייבים צורך בטיפול משופר, עם שימוש בתכשירים מכוונים וספציפיים, והתנהלות טיפולית הולמת יותר על בסיס של מדד-ביולוגי רלוונטי. | ||
| + | |||
| + | הנוגדן החד-שבטי [[rituximab]], הספציפי לאנטיגן CD20 על תאי B, הוא התכשיר הראשון המייצג דור חדש של תרפיה מדכאת-חיסון, שהראה תוצאות מבטיחות בניסויים קטנים בכך שהצליח להשרות רמיסיה של תסמונת נפרוטית ב-2/3 של המטופלים עם MN ראשוני או אידיופטי. Ruggenenti וחב' ב-J Am Soc Nephrol משנת 2015, פרסם נתונים חשובים מניסוי עם 101 מטופלים עם MN, בו הוא עשה שימוש ב-rituximab והסתבר שהשפעת תכשיר זה הייתה דומה באלה עם נוגדנים anti-PLA2R כמו גם באלה ללא נוגדנים. מחקרים קודמים הראו שכמעט 50% מהמטופלים עם MN ראשוני-אידיופטי, בהם לא נמצאו נוגדנים ל-PLA2R, ניתן היה לזהות ב-basement membrane הגלומרולרי, משקעי קומפלקסים המכילים PLA2R (על פי Svobodova וחב' ב-Nephrol Dial Transplant משנת 2013). כלומר יתכן שבמקרים האחרונים, ריבוי של קולטן לפוספוליפאזה A2 במשקעים בממברנת הגלומרולי, גורם לכך שרוב או כל הנוגדנים לקולטן זה נספחים אליו, ולכן אלה נגרעים מהפלזמה. | ||
| + | |||
| + | במטופלים עם רמות נמוכות של נוגדנים כנגד PLA2R בבסיס הטיפול, היעלמות מוחלטת של נוגדנים אלה לאחר 6 חודשים של טיפול ב-rituximab, מנבאת באופן חזק רמיסיה. לעומת זאת, הופעה מחודשת של הנוגדנים בצירקולציה, מצביעה על relapse צפוי. הקשר הגנטי בין PLA2R ו-HLA DQA1 ל-MN אידיופטי מאוד חזק (Stanescu וחב' ב-N Eng J Med משנת 2011). קשר זה הוכח במטופלים סיניים (Lv וחב' ב-J Am Soc Nephrol משנת 2013), וגם במטופלים בארה"ב (Saeed וחב' ב-Genes Immun משנת 2014), ושני מחקרים אלה מראים קשר חזק בין הסטאטוס של anti-PLA2R לבין SNPs או single-nucleotide polymorphisms בגן האמור. | ||
| + | |||
| + | ==מגבלות השיטה== | ||
גרסה מ־07:35, 30 במרץ 2019
| מדריך בדיקות מעבדה | |
| נוגדנים לקולטן של phospholipase A2 | |
|---|---|
| Phospholipase A2 receptor antibodies | |
| שמות אחרים | נוגדנים לקולטן של phospholipase A2 |
| מעבדה | אימונולוגיה בדם |
| תחום | אבחון של גלומרולונפריטיס על רקע membranous nephropathy ומעקב אחר מהלך המחלה. |
| טווח ערכים תקין | בשיטת ELISA-תוצאה שלילית כאשר <14 RU/mL; תוצאה גבולית כאשר > or =14-<20 RU/mL; תוצאה חיובית כאשר > or =20 RU/mL. בשיטת כימות אחרת של רמת הנוגדנים כנגד PLA2R סף הנורמה העליון הוא 0.91 מיקרוגרם/מיליליטר. בשיטת Immunofluorescence Assay (IFA) תוצאה תקינה היא תוצאה שלילית. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הבדלה בין membranous nephropathy ראשונית (אידיופתית) לבין membranous nephropathy שניונית.
membranous nephropathy
המפגע הכלייתי הידוע כ-membranous nephropathy (להלן NM) הוא הנפוץ ביותר בתרחיש של תסמונת נפרוטית (nephrotic syndrome) במבוגרים, בנוסף ל-focal segmental glomerulosclerosis (או FSGS) (על פי Beck וחב' ב-N Eng J Med משנת 2009, ו-El Husseini וחב' ב-Am J Nephrol משנת 2016). בערך 80% מהמקרים הם idiopathic membrane nephropathy (להלן IMN), ו-20% מהמקרים הם secondary membrane nephrpopathy (להלן SMN) (Couser ב-Clin J Am Soc Nephrol משנת 2017, ו-Ravindra וחב' ב-Ind J Nephrol משנת 2016). למרות שתרפיה עם תכשירים מדכאי מערכת החיסון, מוכחת כיום כיעילה בהתנהלות עם מטופלים הסובלים מ-IMN (Bech וחב' ב-Clinical Journal of the Am Soc Nephrol משנת 2014), חשוב לציין שמספר מטופלים סובלים מאירועים חמורים לאחר סוג טיפול כזה (Pavenstadt ב-Nephrologe משנת 2016). לכן נחוץ לטפל בערך בשליש מהמטופלים בטיפול שמרני כדי להימנע מאירועים ממאירים העלולים להיגרם על ידי דיכוי מערכת החיסון (Stahl וחב' ב-Dtsch Medl Wochenschr משנת 2011).
מפגע ה-MN מתאפיין על ידי דלקת ורגישות-יתר של פקעיות הכליה (glomerulitis) ושל האינטרסטיציום (nephritis) (על פי Ronco ו-Debiec ב-Nat Rev Nephrol משנת 2012, Glassock ב-Conrib Nephrol משנת 2013). בצפון אירופה השכיחות השנתית של MN היא 5-10 מקרים למיליון (McQuarrie וחב' ב-Nephrol Dial Transplant משנת 2010). מפגע זה נגרם על ידי תגובה אימונולוגית המאופיינת על ידי שקיעה של קומפלקסים אימוניים ב-basement membrane של הגלומרולות, מה שגרם להפחתת הפעילות של הכליות ברוב המקרים. עם התקדמות המחלה, התעבות של הממברנה הבסיסית יכולה להיראות במיקרוסקופ אור, וכך בתחילה הוגדר המפגע כ-"membranous glomerulonephritis" (על פי Beck ו-Salant ב-Kidney Int משנת 2010). המשקעים האימוניים פוגעים בחדירות של הלולאות הקפילריות מה שגורם לפרוטאינוריה, ולעתים קרובות לתסמונת נפרוטית המתבטאת בהיפו-אלבומינמיה, היפרליפידמיה ובצקת (Scheidat ו-Stahl ב-Internist משנת 2003).
נוגדנים כנגד הקולטן לפוספוליפאז A2
בארה"ב בערך 1/3 ממקרי התסמונת הנפרוטית מיוחסים ל-membranous nephropathy. ברבע מהמקרים של MN, המחלה מופיעה באופן שניוני להשפעות של טיפולים תרופתיים, או למחלות אחרות כגון SLE, הפאטיטיס B או הפאטיטיס C, עגבת, תירואידיטיס, או ממאירויות שונות. שאר המקרים נחשבים ראשוניים, אם כי מבחינה קלינית, MN ראשוני או שניוני אינם ניתנים להבדלה. שני הסוגים האמורים מאופיינים על ידי התדרדרות הדרגתית לתסמונת נפרוטית במהלך של חודשים אחדים, בדרך כלל עם לחץ-דם תקין, ותפקוד כליות שמור.
הצורה הראשונית של המחלה מאופיינת על ידי עיבוי של הממברנה הבסיסית של פקעית הכליה כתוצאה מקישור של IgG ושל C3 לממברנה זו. בערך 70% מהמקרים כרוכים עם נוגדנים עצמיים הנקשרים ל-PLA2R, שהם ברובם מסוג IgG4. כיוון שנוגדנים אלה אינם מתגלים ברוב המכריע ברוב הסוגים של MN שניוני, ניתן להשתמש בבדיקה זו להבדיל בין 2 סוגי MN העיקריים.
רמות הנוגדנים כנגד PLA2R יכולות לשמש לצורך ניטור התגובה לתרפיה. השינוי ברמת הנוגדן בדרך כלל מקדים את השינוי בסטאטוס הקליני. ברוב המקרים רמות נוגדנים אלה תואמות את פעילות המחלה, ואת הסיכון להישנותה לאחר שתילת כליות (Schlumberger וחב' ב- Autoimmun Rev משנת 2014). במהלך טיפול במחלה, רמות הנוגדנים בדרך כלל יורדות לפני הרמיסיה של הפרוטאינוריה. לאחר הטיפול בערך 50% מאלה שהם שליליים לבדיקת הנוגדנים כנגד PLA2R, נשארים ברמיסיה לתקופה של 5 שנים, אך אלה הנותרים חיוביים לנוגדנים כנגד PLA2R, חווים relapse תוך שנתיים.
רמת הנוגדנים כנגד PLA2R ורמיסיה ספוטנית
הקולטן של M type phospholipase A2 (להלן PLA2R), הוא אנטיגן ספציפי ב-IMN, ונוגדנים כנגד PLA2R מופיעים בערך ב-70% מהמאובחנים עם IMN (Kao וחב' ב-J Am Soc Nephrol משנת 2015, Szymanski וחב' ב-Journal of Clinical Aphresis משנת 2017, ו-Prabhu וחב' ב-Nephrology משנת 2016). למרות שהערך האבחוני של נוכחות נוגדנים כנגד PLA2R ב-IMN מקובל כיום (Pang וחב' ב-Medicine משנת 2017, Van De Logt וחב' ב-Kid Int משנת 2015, ו-Seitz-Polski וחב' ב-J Am Soc Nephrol משנת 2016), לא ברורה נוכחות נוגדנים אלה על הפרוגנוזה של המפגע. ניסויים אחדים אף הראו שנוכחות נוגדנים אנטי-PLA2R בעת אבחון המפגע, עשויים לנבא רמיסיה ספונטנית (Radice וחב' ב-Autoimmun Rev משנת 2016, Jullien וחב' ב-Clin Kidney J משנת 2017, Hoxha וחב' ב-Clin J Am Soc Nephrol משנת 2014, ו-Kim וחב' ב-American Journal of Nephrology משנת 2015). Hofstra ו-Timmermans הציעו שרמיסיה ספוטנית שכיחה יותר באלה עם IMN שטיטר הנוגדנים כנגד PLA2R בנסיוב שלהם נמוך יותר (Hofstra וחב' ב-J Am Soc Nephrol משנת 2012, ו-Timmermans וחב' ב-Am J Nephrol משנת 2015). אך כיוון שבניסויים אלה מספר המטופלים היה קטן, קשה להגיע למסקנה באשר לקשר בין טיטר הנוגדנים כנגד PLA2R לבין ההסתברות לרמיסיה בחולים אלה (Oh וחב' ב-PLos One משנת 2012, ו-Pourcine וחב' באותו כתב עת משנת 2017).
Wu וחב' פרסמו ב-Medicine משנת 2018 מטה-אנליזה שהתייחסה לרמת הנוגדנים כנגד PLA2R להסתברות לרמיסיה ספונטנית במטופלים עם IMN. נסקרו חמישה ניסויים שכללו במקובץ 190 משתתפים, ונמצא שאלה ממשתתפי הניסוי שנמצאו חיוביים לנוכחות נוגדנים אלה בעת שאובחן בהם IMN, נמצאו במתאם שלילי לגבי ההסתברות של רמיסיה ספונטנית (RR=0.69, p=0.001). מסקנת מטה-אנליזה זו היא שאי-נוכחות נוגדנים ל-PLA2R מגבירה את הסיכוי לרמיסיה ספונטנית, בהשוואה לאלה בהם נמצאים נוגדנים אלה. לכן, כדי להימנע מאירועים ממאירים שעלולים להתרחש בטיפול עם תכשירים מדכאי-חיסון, כדאי לנקוט בטיפולים שמרניים באלה הנמצאים שליליים לנוכחות בנוגדנים האמורים בעת האבחון של IMN.
בעוד שכּשל כלייתי נמצא מתרחש בשכיחות נמוכה יותר באלה עם רמת anti-PLA2R נמוכה, הרי שרמיסיות ספונטניות פחות שכיחות באלה עם רמות גבוהות של נוגדנים anti-PLA2R. מספר מחקרים דיווחו שמטופלים על ידי תרפיה מדכאת חיסון הראו כצפוי ירידה ברמת הנוגדנים כנגד PLA2R, ושרמת נוגדנים אלה עולה בעת רמיסיה (Beck וחב' ב-J Am Soc Nephro משנת 2011, Hoxha וחב' ב-Nephrol Dial Transplant משנת 2011, Stahl וחב' ב-N Eng J Med משנת 2010, ו-Hofstra וחב' ב-Nat Rev Nephrol משנת 2013). נתונים נוספים מצביעים על כך שבמטופלים חיוביים לנוגדנים כנגד PLA2R, מדידת רמת הנוגדנים בסיום תקופת הטיפול עשויה לנבא את מהלך המחלה בהמשך (Beck וחב' ב-Clin J Am Soc Nephrol משנת 2014). כמו כן, El Zoghby וחב' דיווחו ב-Am J Transplant משנת 2009, ש-IMN מתרחש ב-40% לכל היותר מבין אלה שעברו השתלת כליה. הסיכון להישנות המחלה גדול יותר כאשר נוגדנים עצמיים כנגד PLA2R מתגלים לפני ההשתלה.
MN אחראי בערך ל-20% מהמקרים של תסמונת נפרוטית במבוגרים. בערך שליש מאלה עם MN, יתדרדרו בהמשך לפתח אי-ספיקה כלייתית סופנית תוך 10 שנים (Steinman וחב' ב-Nephrol News Issues משנת משנת 2003). שליש אחר של אלה עם MN יפתחו פרוטאינוריה כרונית ותסמונת נפרוטית, ואילו שליש נוסף ייהנו מרמיסיה ספונטנית. MN יכול להופיע כתולדה של מספר מצבים קליניים כגון זיהומים (הפאטיטיס B ועגבת), לופּוס סיסטמי, סרטן, וטוקסיות של תרופות. כאשר MN מופיע ללא תלות בתמונות ידועות אחרות, ההתייחסות אליו היא כאל primary MN , אשר באופן היסטורי כונה idiopathic MN (או IMN) דהיינו ללא סיבה אטיולוגית ידועה. מדובר במחלה אוטו-אימונית בה נוגדנים מגיבים עם אנטיגן אינטרינסי על פני הפּדוֹציטים הגלומרולריים, ויוצרים משקעים של קומפלקסים אימוניים על דופן הקפילרות הגלומרולריות. ידוע שנוגדנים עצמיים בצירקולציה המכוונים כנגד קולטן M type על פני הפּודוציט המשמש את האנזים המופרש phospholipase A2, מופיעים ב-70-80% מאנשים מאובחנים עם IMN (על פי מחקרו המקורי והמכונן של Beck משנת 2009 שהתפרסם ב-N Eng J Med).
העיקרון של מדידת נוגדנים כנגד PLA2R בשיטת TRFIA (time-resolved fluoroimmunoassay)
נוגדנים רקומביננטיים כנגד PLA2R נוצרו על ידי שיבוט בתאי 293T. נוגדנים ממקור עז כנגד IgG אנושי סומנו עם +Euronium3. הריכוז האופטימלי של האנטיגן PLS2R לציפוי פלטות מיקרו-טיטר היה בערך 5 מיקרוגרם/מ"ל. ההוספה של מגביר פלואוסצנטי הביאה לחיזוק הפלואורסצנציה המקורית פי מיליון, ושיפרה את הרגישות ואת טווח הגילוי בשיטה זו של הנוגדנים מסוג IgG כנגד PLA2R. מכשיר AutoDELFIA1235 של חברת Perkin Elmer, שימש למדידת הפלואורסצנציה +Euronium3 בבארות של פלטת המיקרוטיטר. תחום המדידה של IgG כנגד PLA2R בשיטת TRFIA היה 0.02-340 מיליגרם/ליטר. ה-intra CV נקבע כ-3.2%, וה-inter CV נקבע כ-5.6%.
כימות אולטרה-רגיש של רמת נוגדנים כנגד PLA2R כמדד אבחוני ופרוגנוסטי של idiopathic membranous nephropathy
בסין, אחוז המקרים של MN גדל במהירות בקרב אלה עם גלומרולופתיה ראשונית (או אידיופתית) מ-7.1% בשנת 2000, ל-22.7% בשנים 2009-2011 (Pan וחב' ב-Conrtib Nephrol משנת 2013). מפגע MN שכיח בגברים פי-2 יותר מאשר בנשים והוא מופיע בבני 50 שנה ומעלה ב-30.6% מהמקרים, כאשר באלה בני 60 שנה ומעלה, הוא מהווה את הסיבה העיקרית ל-MN אידיופתי. האבחון המסורתי של MN התבצע בעזרת ביופסיה כלייתית, כאשר 75% מהמקרים היו אידיופתיים (IMN), ושאר המקרים היו משניים לזיהומים (דוגמת הפאטיטיס B), מסיבה אוטו-אימונית (דוגמת לופוס), השפעת תרופות (דוגמת NSAIDs), או משניים לממאירויות (Feng וחב' ב-Oncotarget משנת 2016, Lefaucheur וחב' ב-Kidney Int משנת 2006). המחקרים המקוריים של Hoxha ,Hofstra ,Beck וחבריהם, הראו שנוגדנים עצמיים כנגד PLA2R הופיעו ב-52-82% מהמאובחנים עם IMN. אך לא נמצאו או שהיו מאוד לא שכיחים באלה עם MN משני (Segarra-Medrano וחב' ב-Nefrologia משנת 2014).
גם Dou וחב' ב-Int Urol Nephrol משנת 2016, הדגימו את דרגות הדיוק, הרגישות והספציפיות הגבוהות של בדיקה זו לאבחון IMN. אך מה שלא הובהרה לחלוטין היא מידת המתאם בין טיטר הנוגדנים ל-PLA2R ודרגת המחלה (Kim וחב' ב-Am J Nephrol משנת 2015, Wei וחב' באותו כתב עת משנת 2016, Lin וחב' ב-Zhonghua Nei ke Sa Zhi משנת 2015, ו-Ruggenenti וחב' ב-J Am Soc Nephrol משנת 2015). אי הוודאות הזו יכולה להיות מוסברת חלקית בכך בהבדלים בין שיטות המדידה של טיטר הנוגדנים הללו, וגם בעיתוי השונה של נטילת הדם על ידי החוקרים השונים. לכן בחרו Zhang וחב' ב-Sci Rep משנת 2017, למדוד את הנוגדנים כנגד PLA2R בשיטת TRFIA או Time-resolved fluoroimmunoassay, שהיא שיטה חדשה לאנליזה של המתאם בין רמת הנוגדנים האמורים לבין המדדים הקליניים של מאובחנים עם IMN.
בניסוי האחרון נמדדה בשיטת TRFIA רמת אימונוגלובולין IgG כנגד PLA2R בנסיוב של 172 מטופלים, מהם 69 עם IMN, וכן 9 עם MN משני ו-94 מאובחנים עם גלומרולונפריטיס מסיבות אחרות, וכקבוצת ביקורת נוספת שמשו 286 אנשים בריאים לחלוטין. רמות של נוגדנים אנטי-PLA2R בנסיוב של המתנדבים הבריאים היו בין 0.09-0.91 מיקרוגרם/מיליליטר, וכיוון שכך החליטו בעלי המחקר לקבוע את רף הנורמה העליון על רמת נוגדנים של 0.91 מיקרוגרם/מיליליטר. עם סף נורמה זה רגישות הבדיקה נקבעה כ-84.06% לאבחון של IMN. כאשר הוגבה סף הנורמה העליון לריכוז נוגדנים של 2.025 מיקרוגרם/מיליליטר, הרגישות לאבחון IMN אמנם פחתה ל-71.01%, אך הספציפיות של האבחון הגיעה ל-100%. במאובחנים עם IMN רמת הנוגדנים מסוג IgG כנגד PLA2R, הייתה גבוהה יותר באופן משמעותי בהשוואה לרמתם במאובחנים עם MN משני. היה מתאם שלילי בין רמת נוגדנים אלה לבין תפקוד הכליות (GFR), דהיינו ככל שרמת הנוגדנים הייתה גבוהה יותר, ה-GFR היה נמוך יותר, כמו גם רמת אלבומין בנסיוב שכן אחוז גבוה של חלבון זה הופרש בשתן. כצפוי, ככל שרמת הנוגדנים הייתה גבוהה יותר כך גם נרשמה עלייה ברמת קראטינין בנסיוב, וירידה בשיעור רמיסיה מוחלטת. מובהק לא פחות היה הממצא שככל שרמת הנוגדנים ל-PLA2R הייתה גבוהה יותר, הפרוגנוזה של אלה עם IMN הייתה גרועה יותר.
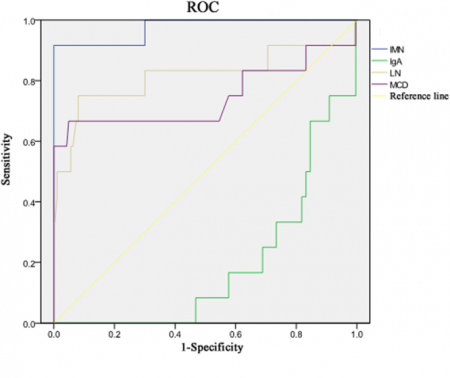
פירוט של תוצאות הניסוי של Zhang וחב': הרמה הממוצעת של נוגדנים מסוג IgG כנגד PLA2R בנסיוב של מתנדבים בריאים הייתה 0.5 מיקרוגרם/מיליליטר. כאמור, בקבוצת ה-IMN רגישות השיטה הייתה של 84.06%, בעוד שרגישותה בקבוצת המאובחנים עם minimal change disease או MCD הייתה 58.33%, בקבוצת ה-lupus nephritis או LN הרגישות הייתה 50%, בקבוצת המאובחנים עם IgA nephropathy הרגישות הייתה 41.82%, ואילו באלה עם נפרופתיות מסיבות אחרות הרגישות הייתה 40%. אנליזה של עקומת ROC או receiver-operating-characteristics של נוגדנים מסוג IgG כנגד PLA2R, הבדילה בין IMN (עם 0.975), לופוס נפריטיס (0.815), מחלת שינוי מינימלי או MCD (עם 0.745), ו-IgA nephropathy (עם 0.191).
המתאם של רמות נוגדנים מסוגIgG כנגד PLA2R עם המאפיינים הקליניים
הרמה הממוצעת של נוגדנים אלה בחולי IMN היא 8.78 מיקרוגרם/מיליליטר במחקרם של Zhang וחב', ואילו באלה עם SMN רמה ממוצעת של 0.99 מיקרוגרם/מיליליטר. לעומת זאת, לא היה הבדל משמעותי בין רמות הנוגדנים האלה בין השלבים II ,I או III של המחלה. דגימות נסיוב וביופסיות כליה היו זמינות מ-63 מתוך 69 משתתפי הניסוי עם IMN, והם נלקחו בעת ובעונה אחת, ממטופלים ללא טיפול בקורטיקו-סטרואידים או בתכשירים מדכאי-חיסון. מבין 63 הנבדקים, ב-47 נמצאו הנוגדנים האמורים הן בנסיוב, כמו גם נמצאה בביופסיות צביעה חיובית כנגד PLA2R. ב-6 מהנבדקים נמצאו נוגדנים בנסיוב, אך הייתה צביעה שלילית של הביופסיות, ו-6 מהמשתתפים נמצאו שליליים לנוגדנים בנסיוב וחיוביים לצביעה בביופסיה, ו-4 נבדקים היו שליליים בשתי הקטגוריות. הרגישויות של מציאת נוגדנים חיוביים בנסיוב או צביעת PLA2R בביופסיות היו 84.13% ו-80.95%, בהתאמה.
הטיטר של נוגדנים ל-PLA2R נמצא בתאום שלילי עם התפקוד הכלייתי (GFR), כאשר מטופלים חיוביים עם רמת נוגדנים מעל 0.91 מיקרוגרם/מיליליטר היו שונים משמעותית מאלה עם ערכים נמוכים של נוגדנים anti-PLA2R, ביחס למפגעים קליניים כגון פרוטאינוריה של 24 שעות (4.56 לעומת 3.03 גרם/24 שעות, p=0.013), ואלבומין בפלזמה (21.45 לעומת 26.21 גרם/ליטר, p=0.025).
בעוד שהגישה הטיפולית באלה עם MN שניוני לתרחישים בולטים מתמקדת באותם תרחישים, הרי שאלה עם IMN בדרך כלל מטופלים עם תכשירים מדכאי חיסון. עם זאת מספר קטן של מטופלים עם מחלת MN משנית לתרחישים ידועים נמצאים גם הם חיוביים לנוגדנים עצמיים כנגד PLA2R, אם כי המשמעות הקלינית של ממצא זה אינה ברורה (Beck ו-Salant ב-J Clin Invest משנת 2014, Gunnarsson וחב' ב-Am J Kidney Dis משנת 2012, Qin וחב' ב-J Am Soc Nephrol משנת 2011, ו-Hofstra וחב' ב-Clin J Am Soc Nephrol משנת 2014). רמות של נוגדנים בצירקולציה כנגד PLA2R מראות מתאם עם פעילות המחלה, כפי שהדבר נמדד עם דרגת הפרוטאינוריה. רמת anti-PLA2R נמצאה בעלת ערך של ניבוי מהלך המחלה ותוצאותיה (Kanigicheria וחב' ב-Kidney Int משנת 2013, ו-Hoxha וחב' ב-J Am Soc Nephrol משנת 2014).
נוגדנים בנסיוב כנגד PLA2R הנמדדים בשיטת TRFIA ופרוגנוזה גרועה בקרב מטופלים עם IMN
כדי להעריך את הקשר בין הטיטר של נוגדן כנגד PLA2R לבין הממצאים הקליניים והתוצאים הקליניים, חולקו משתתפי הניסוי לשתי קבוצות מבחינת טיטר הנוגדנים, כאשר ריכוז נוגדנים של 2.025 מיקרוגרם/מיליליטר שימש כריכוז סף בין רמת נוגדנים גבוהה ונמוכה: קבוצה A (41 נבדקים) עם טיטר נוגדנים גבוה וקבוצה B עם טיטר נוגדנים נמוך. בקבוצה A הייתה רמת אלבומין בנסיוב נמוכה משמעותית מאשר בקבוצה B (3.093 לעומת 3.580 גרם/דציליטר, p=0.048), כתוצאה מתפקוד כליות ירוד יותר (GFR של 77.76 לעומת 107.67 מ"ל/דקה/1.73מ2, p=0.005), עם פרוטאינוריה גבוהה יותר (2.34 לעומת 1.22 גרם/יום, p=0.031), וריכוז קראטינין בנסיוב גבוה יותר (87.87 לעומת 67.64 מיקרומול/ליטר, p=0.049). מטופלים עם טיטר גבוה של נוגדנים כנגד PLA2R היו בעלי רמיסיה קלינית נמוכה יותר (51.22% לעומת 82.35%, p=0.027).
אחד היתרונות של גילוי נוגדנים כנגד PLA2R הוא בכך שהופעת נוגדנים אלה בנסיוב או היעלמותם, מקדימה את ההופעה או ההתפוגגות של התסמינים הקליניים (Brenchley ב-J Am Soc Nephrol משנת 2015). וכך רמות הנוגדנים הללו פחתו לפני שפחתה דרגת הפרוטאינוריה, כאשר ברוב המטופלים הפכו שליליים בבדיקת הנוגדנים 6-9 חודשים לפני רמיסיה מוחלטת של פרוטאינוריה שהתרחשה רק לאחר 12-24 חודשים. מחקר אירופי על MN הראה קשר בין רמות גבוהות של נוגדנים ל-PLA2R בעת אבחון המחלה, לסיכוי מופחת של רמיסיה ספונטנית (Hofstra וחב' ב-J Am Soc Nephrol משנת 2012). מחקר Manchester הראה שרמות גבוהות של anti-PLA2R היו במתאם עם תוצאים קליניים גרועים 5 שנים מהאבחון (Kanigicheria וחב' ב-Kidney Int משנת 2013). תוך שימוש בפרוטוקול תקני של immunosuppression, נמצא שהכישלון להסב מטופלים לשליליים מבחינת הנוגדנים ל-PLA2R על ידי דיכוי המערכת החיסונית, כרוך בשיעור גבוה של הישנות המחלה (relapse) (על פי Bech וחב' ב-Clin J Am Soc Nephrol משנת 2014). מחקר רב-מוסדי בגרמניה אישר באופן ברור שרמת anti-PLA2R היא גורם סיכון בלתי-תלוי לכך שלא ניתן לקבל רמיסיה בפרוטאינוריה (Hoxha וחב' ב-J Am Soc Nephrol משנת 2014). עיכוב בטיפול להפחתת רמת anti-PLA2R, עלול לסכן פעילות הכליות (Hoxha וחב' ב-Clin J Am Soc Nephrol משנת 2014). ניסויים אלה התבצעו בשיטת ELISA שהתבררה כמדויקת וקלה יותר לביצוע מאשר שיטת Western blotting (על פי Dahnrich וחב' ב-Clin Chim Acta משנת 2013).
החיוניות של מדד נוגדנים כנגד PLA2R להערכת הטיפול המתאים ב-IMN
התרפיה העיקרית ב-30 השנים האחרונות התבססה על דיכוי בלתי-ספציפי של מערכת החיסון, שנקבעה באופן אמפירי בשימוש משולב של ציקלופוספמיד וסטרואידים. כתוצאה מחסר של מדד ביולוגי רלוונטי של אימונו-פתולוגיה, נעשה שימוש ברמיסיה של פרוטאינוריה כמדד של תוצא דומיננטי. למרות שתכשירים לא-ספציפיים אלה יכולים להתברר כיעילים למניעה של התקדמות המחלה ב-60-80% מהמטופלים, טיפול זה גובה תשלום יקר בתחלואה ואף בתמותה כתוצאה מהגברת הסיכון להדבקות בפתוגנים שונים, ממאירות, ואירועים קרדיו-וסקולריים. רוב המטופלים חווים מהלך מחלה מחזורית של רמיסיות ומשברים, בהם מתבקש טיפול של דיכוי של מערכת החיסון, כאשר חלק מהמטופלים מראים עמידות לטיפול האחרון. נתונים אלה מחייבים צורך בטיפול משופר, עם שימוש בתכשירים מכוונים וספציפיים, והתנהלות טיפולית הולמת יותר על בסיס של מדד-ביולוגי רלוונטי.
הנוגדן החד-שבטי rituximab, הספציפי לאנטיגן CD20 על תאי B, הוא התכשיר הראשון המייצג דור חדש של תרפיה מדכאת-חיסון, שהראה תוצאות מבטיחות בניסויים קטנים בכך שהצליח להשרות רמיסיה של תסמונת נפרוטית ב-2/3 של המטופלים עם MN ראשוני או אידיופטי. Ruggenenti וחב' ב-J Am Soc Nephrol משנת 2015, פרסם נתונים חשובים מניסוי עם 101 מטופלים עם MN, בו הוא עשה שימוש ב-rituximab והסתבר שהשפעת תכשיר זה הייתה דומה באלה עם נוגדנים anti-PLA2R כמו גם באלה ללא נוגדנים. מחקרים קודמים הראו שכמעט 50% מהמטופלים עם MN ראשוני-אידיופטי, בהם לא נמצאו נוגדנים ל-PLA2R, ניתן היה לזהות ב-basement membrane הגלומרולרי, משקעי קומפלקסים המכילים PLA2R (על פי Svobodova וחב' ב-Nephrol Dial Transplant משנת 2013). כלומר יתכן שבמקרים האחרונים, ריבוי של קולטן לפוספוליפאזה A2 במשקעים בממברנת הגלומרולי, גורם לכך שרוב או כל הנוגדנים לקולטן זה נספחים אליו, ולכן אלה נגרעים מהפלזמה.
במטופלים עם רמות נמוכות של נוגדנים כנגד PLA2R בבסיס הטיפול, היעלמות מוחלטת של נוגדנים אלה לאחר 6 חודשים של טיפול ב-rituximab, מנבאת באופן חזק רמיסיה. לעומת זאת, הופעה מחודשת של הנוגדנים בצירקולציה, מצביעה על relapse צפוי. הקשר הגנטי בין PLA2R ו-HLA DQA1 ל-MN אידיופטי מאוד חזק (Stanescu וחב' ב-N Eng J Med משנת 2011). קשר זה הוכח במטופלים סיניים (Lv וחב' ב-J Am Soc Nephrol משנת 2013), וגם במטופלים בארה"ב (Saeed וחב' ב-Genes Immun משנת 2014), ושני מחקרים אלה מראים קשר חזק בין הסטאטוס של anti-PLA2R לבין SNPs או single-nucleotide polymorphisms בגן האמור.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק