שאתות ממאירות בכבד - היבטים כירורגיים - Malignant liver tumors - surgical aspects
הופניתם מהדף סרטן בכבד היבטים כירורגיים לדף הנוכחי.
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הכבד | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – גידולי כבד
אפידמיולוגיה
השאתות הממאירות הראשוניות של הכבד הן נדירות בעולם המערבי. שכיחותן בארה"ב היא 0.3% ואילו באסיה השכיחות המדווחת היא 2.5%. למרות נדירות השאת, היא נחשבת לשאת קטלנית ביותר. המחלה שכיחה בחולי דלקת כבד נגיפית B ודלקת כבד נגיפית C. המחלה שכיחה יותר בגברים ובאיזורים שבהם המחלה שכיחה היחס הוא 1:6. בחלק העולם המערבי המחלה נדירה לפני גיל 40, ואילו באסיה ואפריקה היא שכיחה יותר בקרב צעירים מגיל 40. בילדים, ההפטובלסטומה מופיעה בגיל מתחת לשנתיים והיא השאת הממארת האפיתליאלית השכיחה ביותר בגילים אלה.
אטיולוגיה
קיימים מספר גורמי סיכון לפתח שאת ממארת ראשונית של הכבד. בין הגורמים הנמנים הם חולים עם:
- דלקת כבד נגיפית B או C כרונית, בסין שבה דלקת כבד נגיפית B היא השכיחה היא מהווה את הגורם מספר אחד להופעת Hepatocellular carcinoma (HCC) לעומת זאת בארה"ב שבה דלקת כבד נגיפית C היא היותר שכיחה היא מהווה את הגורם השכיח יותר.
- חולים עם שחמת הכבד על רקע אלכוהוליזם היא הגורם השכיח ביותר בארה"ב. כ- 5% מהחולים עם שחמת הכבד יפתחו שאתות בכבד.
- חולים עם מחלות מטבוליות כמו המוכרומטוזיס וטירוזינמיה מהווים קבוצת סיכון לפתח שאתות בכבד.
- שכיחות גבוהה של שאתות אלו נמצא גם בקרב אוכלוסיות בעיקר באסיה ואפריקה הצורכות בדיאטה שלהן כמויות של aflatoxin.
- סוכרת מסוג 2 (שכיחות גבוהה פי 2.5 עד 7).
- מחלת וילסון?
- הפטוצלולר אדנומה הגדולה מ- 6-8 ס"מ נחשבת לממארת.
פתולוגיה
מרבית השאתות הממאירות של הכבד (85-90%) מקורן בתאי הכבד - Hepatocellular carcinoma. שאתות אחרות כמו Cholangiocarcinoma, Angiosarcoma או Hepatoblastoma הן נדירות יותר. לרוב התת קבוצות של HCC התנהגות דומה מלבד משתי תת קבוצות מיוחדות:
- FLC (Fibrolamellar carcinoma) השכיחה בצעירים ובעלת פרוגנוזה טובה יותר משל HCC.
- Adenomatous hyperplasia. שהיא נגע קדם סרטני של HCC המופיע בנודולים רגנרטיבים של שחמת הכבד. בחולים אלה כריתה של הנגע מבשרת ריפוי מלא.
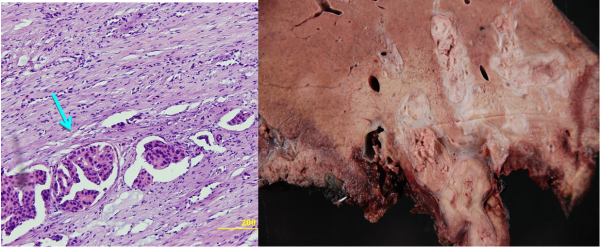
מבחינה פתולוגית שאתות אלה מופיעות לרוב כנגע בודד גדול נודולרי או כנגעים מרובים על פני הכבד כולו. ב- FLC הנגעים בדרך כלל בודדים (75%) ממוקמים באונה שמאלית בעיקר. שאתות ה- HCC הן בעלות מבנה טרבקולרי ועשירות בכלי דם ולעיתים קרובות פולשות לענפים של הווריד הפורטלי ואף לענפים של ורידי הכבד (תמונה 9.10).
השאתות הללו יכולות להתפשט ל:
- רקמת הכבד.
- לתוך הסינוסואידים ומשם למקומות נוספים בכבד.
- דרך הוורידים הפורטלים אל הווריד הפורטלי או דרך ורידי הכבד לווריד החלול התחתון ולעליה הימנית.
- דרך המערכת הלימפתית לאיברים מרוחקים.
תסמינים קליניים
לרוב החולים עם HCC יש סיפור של דלקת כבד נגיפית או שחמת כבד על רקע אלכוהולי. התמונה הקלינית היא של חולה בשחמת הכבד אשר באופן פתאומי מתחיל להתדרדר ומפתח:
- ירידה במשקל וחולשה (80%)
- כאבי בטן עמומים (50%), כאב חד יכול להופיע בדימום פתאומי של השאת לבטן
- מיימת (50-70%)
- צהבת (20-50%)
- אנמיה
- החמרה ביתר לחץ הדם הפורטלי עם הופעת דליות מדממות בוושט
- בחולים שאינם לוקים בשחמת הכבד ניתן לראות
- חוסר תיאבון
- ירידה במשקל
- כאבי בטן עמומים
- חום
- בצקות
- תסמינים פארא-נאופלסטיים כמו: היפוגליקמיה, היפרקלצמיה, אריטרוציטוזיס ועוד
- בבדיקה ניתן למצוא
- כבד מוגדל קשה ומגורגר
- מיימת
- בצקות ברגלים
- צהבת
- גוש בבטן
- תסמינים של חסימה של הוריד הנבוב התחתון
- גירוי צפקי בחולים עם דמם חד לחלל הבטן
- בהאזנה מעל הכבד אפשר לעיתים לשמוע אוושות
בילדים התסמין הראשון שמופיע הוא גוש בבטן. בילדים מבוגרים יותר היפרטרופיה של מחצית הגוף וסמנים לבגרות מינית מוקדמת מתוארים.
אבחנה
במעבדה נמצא לעיתים הפרעות בתפקודי הכבד שאינם ספציפיים. עליה ב- Alfa-feto-protein, המאפיינת בעיקר שאתות גדולות ופחות בולטת בקטנות, מרמזת על הופעה של שאת ראשונית בכבד. באפריקה ב- 75% מהחולים נמצא רמות מוגברות של סמן זה לעומת 30% בארה"ב או אירופה. אמצעי ההדמיה הם:
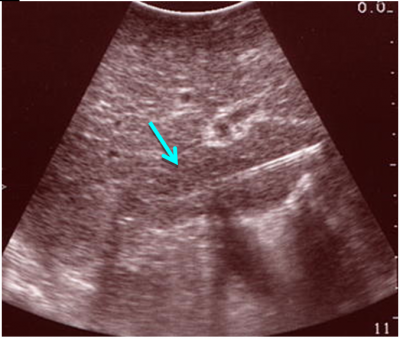
- US המראה שאת או מספר שאתות בכבד והוא כלי ראשוני לסקירה ומעקב (תצלום 29.10).
- CT המראה נגעים בכבד. בשאתות קטנות הרגישות של ה- CT ו- US זהה ולכן US משמש לסיקור באוכלוסיות בסיכון גבוה. בעזרת ה- CT ניתן לאתר גם נגעים מחוץ לכבד. ה- CT הספירלי מאפשר לנו לבצע שחזור כלי דם ולהדגים את עושר כלי הדם העוטפים את השאת. ההדגמה ב- CT היא תלת פאזית
- לפני הזרקת חומר ניגוד
- מיד אחריו
- מאוחר לאחר ההזרקה
- ה- HCC יכול להופיע
- כנגע בודד
- נגעים מרובים
- נגע בעל גבולות מטושטשים פולשניים
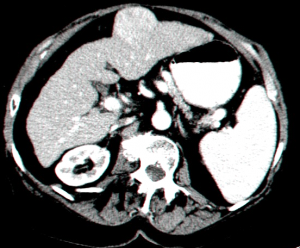
- בדרך כלל אין צורך בביופסיה מחטית של הנגע בתנאי שניתן לראות ב- CT מאפיינים קלאסיים ל- HCC. כיוון שה- HCC היא שאת מאוד וסקולרית הרי שהיא "נצבעת" מהר וחזק בשלב ההזרקה ויש שטיפה מהירה בשלב הפורטלי המאוחר (תצלום 30.10-33.10).
|
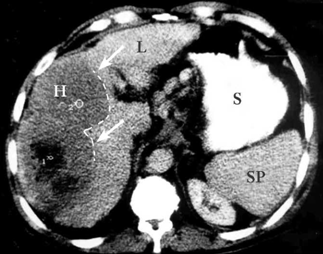
|
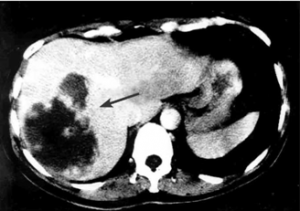
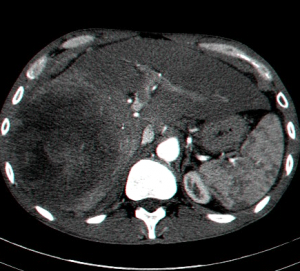
| תצלום 30.10: שאת בכבד הנראית ב- CT. מימין HCC הבולטת על פני הכבד. משמאל פגם מילוי בכבד כביטוי לשאת בכבד (החץ מצביע על השאת). | |
|---|---|
|
|
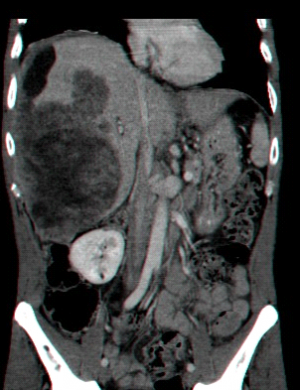
| תצלום 32.10: HCC החודרת לכלי דם ויוצרת קרישים בכלי דם ורידיים. | |
|---|---|
- CT עם CTAP) arterial portography) היא אחת השיטות הטובות לברור גושים בכבד. בשיטה זו מזריקים דרך עורק העורק המזנטרי העליון (SMA) חומר ניגוד ומבצעים סריקה מאוחרת של השלב הורידי. מכיוון שה- HCC איננה מסופקת על ידי מערכת השער נקבל צביעה של הכבד הבריא בעוד השאתות לא יצבעו ויופיעו כפגמי מילוי בכבד.
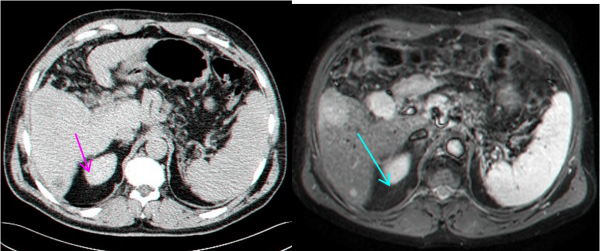
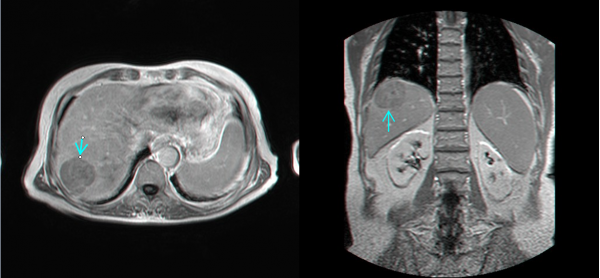
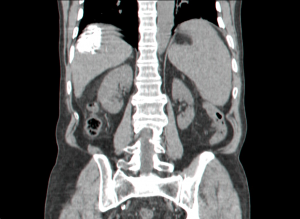
- MRI הוא אמצעי טוב להדגמת השאתות, מקומן האנטומי ויחסן לכלי הדם בכבד (תצלום 34.10). נמצא שה- MRI הוא יותר רגיש ויותר ספציפי ביחס ל- CT, אולם יותר יקר ממנו.
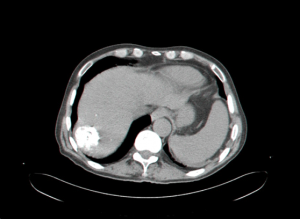
- ליפיודול הוא חומר שומני שעליו חיברו חומר ניגוד והוא נקלט היטב בשאתות מסוג HCC. יתרונו הוא בכך שהוא נשאר הרבה זמן בשאת ולכן ניתן להדגמה שוב ושוב בלא צורך להזריק חומר ניגוד. הזרקת ליפיודול יכולה לעזור לנו באבחון של שאתות בקטרים קטנים של מספר מ"מ (תצלום 35.10).
|
|
| תצלום 35.10: הדגמת השאת בכבד לאחר הזרקת ליפיודול הנקלט בשאת ונשאר בה ולכן מאפשר מעקב ממושך אחר הנגעים בכבד. | |
|---|---|
- ניקור כבד נותן לנו אבחנה הסטולוגית של הנגע. מכיוון שהשאתות הללו הן עשירות בכלי דם הרי שסכנת הדימום לאחר ביופסיה היא גדולה, לכן, בחולים המועמדים לכריתת השאת אין צורך לקבל אבחנה היסטולוגית לפני הניתוח. רק בחולים שלא מועמדים לניתוח והאבחנה הפתלוגית תאפשר תכנון טיפול טוב יותר, יעברו ביופסיה מחטית.
- חולים לפני ניתוח יעברו צילום חזה לשלילת גרורות בריאות אין צורך בבדיקות סיקור נוספות.
סווג שאתות הכבד
שאתות הכבד מסווגות בהתאם לשיטת ה- TNM. סווג השאתות מוצג בטבלה 5.10
| טבלה 5.10 : סווג לפי ה- TNM | |
|---|---|
| Tx | גודל שאת לא ידוע |
| T0 | אין עדות לשאת ראשונית |
| T1 | שאת קטנה מ- 2 ס"מ |
| T2 | שאת קטנה מ- 2 ס"מ עם פריצה לכלי דם או נגעים מרובים באונה אחת ללא פריצה לכלי דם או שאת הגדולה מ- 2 ס"מ ללא פריצה לכלי דם |
| T3 | שאת גדולה מ- 2 ס"מ עם פריצה לכלי דם או שאתות מרובות קטנות מ- 2 ס"מ עם פריצה לכלי דם או שאתות באונה אחת שאחת מהן גדולה מ- 2 ס"מ |
| T4 | שאתות מרובות ביותר מאונה אחת או שאתות החודרות לאחד מכלי הדם הגדולים |
| בלוטות | |
| Nx | לא ידוע |
| N0 | אין בלוטות נגועות |
| N1 | בלוטות נגועות |
| גרורות רחוקות | |
| גרורות | |
| Mx | לא ידוע |
| M0 | אין גרורות מרוחקות |
| M1 | יש גרורות מרוחקות |
הדרוג של השאתות מוצג בטבלה 6.10.
| טבלה 6.10: דרוג המחלה לפי ה- TNM | |||
|---|---|---|---|
| Stage 1 | T1 | NO | MO |
| Stage 2 | T2 | NO | MO |
| Stage 3 | T3 | NO | MO |
| T1-3 | N1 | ||
| Stage 4a | T4 | Any N | MO |
| Stage 4b | Any T | Any N | M1 |
טיפול
הכריתה הכירורגית של הנגע בכבד היא הטיפול היחיד שיכול להציע ריפוי מהמחלה. לפני הניתוח, יש לברר האם לחולה, הסובל בדרך כלל ממחלת כבד הפוגעת בתפקוד הכבד, יש מספיק רזרבות כבד כך שכריתת הכבד לא תגרום לו לאי ספיקת כבד ומוות. הערכת תפקוד הכבד יכולה להתבסס על הסיווג לפי Child-Pugh, שתוארה כבר קודם לכן ומבוססת על היכולת הסינטטית ויכולת סילוק הרעלים של הכבד. ככל שדירוג ה- Child גבוה יותר תפקוד הכבד פגוע יותר, חולים ב- Child C הם מועמדים גרועים לניתוח ובהם התמותה הניתוחית היא גבוהה מאוד, בעוד, שחולים עם Child A הם חולים עם רמת סיכון סבירה. היחס בין תפקוד הכבד לגודל הכבד יכול להיות מוערך על ידי מיפוי כבד עם N-pyridoxyl-5-methyltryptopan, כאשר משווים את כמות הקליטה בכל הכבד לקטע שיישאר לאחר הניתוח. הערכה וליומטרים – נפח הכבד הנותר – מחושבת בעזרת ה- CT, כאשר כל הכבד מסומן נערך חישוב של כל נפח הכבד ולאחר מכן מסומן על ה- CT הנפח שאמור להיות מוסר. היחס בינם נותן למעשה את הנפח השארי. בחולים עם כבד לא חולה ניתן להשאיר 30% מהנפח מבלי לגרום לאי ספיקה. בחולים עם מחלות כבד דרוש נפח גדול יותר לתפקוד. למרות היכולת להעריך של רזרבות הכבד נרשמה תמותה של 20% בחולים שעברו כריתות כבד עקב HCC וזאת עקב דימומים, אי ספיקת כבד ואלח דם. בהערכת החולה לפני ניתוח מלבד הערכה של Child יש להעריך מחלות נלוות אחרות מחלות לב, ריאות וכליות המעלים בצורה משמעותית את התמותה הניתוחית.
רק 10-30% מחולים עם HCC הם מועמדים לטיפול כירורגי. מאלה שנמצאו מתאימים לניתוח רק 50-75% יעברו ניתוח מרפא. חולים שבהם לא נבצע כריתות כבד הם:
- חולים עם מחלה חוץ כבדית
- חולים עם אי ספיקת כבד חמורה
- חולים שלאחר כריתת הכבד יישארו עם נפח כבד שאינו מאפשר תפקוד סביר
- שאתות אשר פרצו לווריד החלול התחתון או לווריד השער
בניתוח, לפני ביצוע כריתת הכבד יש לבצע סקירה מדוקדקת של הבטן לשלול גרורות בחלל הבטן, בבלוטות בשער הכבד או ב- Hepatoduodenal ligament. צריך לשחרר את הכבד כך שאפשר יהיה לבודקו מכל צדדיו. יש המוסיפים US תוך ניתוחי על מנת להגדיר טוב יותר את איזור הכריתה ולגלות גרורות שלא ידעו עליהן לפני כן. כריתת הכבד טוב שתיעשה במישורים אנטומיים. השולים הנדרשים הם של 1 ס"מ לפחות. לעיתים, יש להתפשר ברוחב השולים בחולים עם שחמת הכבד כשהמטרה היא להשאיר מספיק רקמת כבד שתאפשר לאחר הניתוח תפקוד סביר. מאידך גיסא, ניתוחים מיקטניים כמו כריתות יתד (wedge resection) אינם מומלצים. שיעור החזרות המדווח בחולים לאחר כריתות כבד נע בין 30% ל- 70%. השיעור גבוה יותר בחולים עם:
- חדירת השאת לכלי דם או לקפסולה שסביבם
- דרוג היסטולוגי גבוה
- שאת גדולה
- שאתות מרובות
חולים שאינם מועמדים לניתוח עקב רזרבת כבד נמוכה הם גם המועמדים להשתלת כבד. השתלות כבד לא העלו את שיעורי ההיוותרות בחיים ביחס לכריתות כבד והן עומדות על 15-30% לחמש שנים. בחולים עם HCC ושחמת הכבד השתלות כבד הביאו לשיפור בהישרדות ביחס לכריתות כבד. מחולים המועמדים להשתלות כבד אשר קיבלו לפני ההשתלה 3-4 מחזורי כימותרפיה נותרו בחיים שנה 91% מהחולים לעומת 43% שלא קבלו טיפול כימי לפני ניתוח. בחולים שלא ניתן לכרות את השאת, אפשר להורסה על ידי הקפאה או חימום. טיפול אחר שמוצע בספרות הוא הזרקה של אתנול לתוך השאת (PEI). חולים עם שאתות של פחות מ- 3 ס"מ ולא יותר משלוש שאתות ואינם מועמדים לניתוח הם המועמדים לטיפול באתנול.
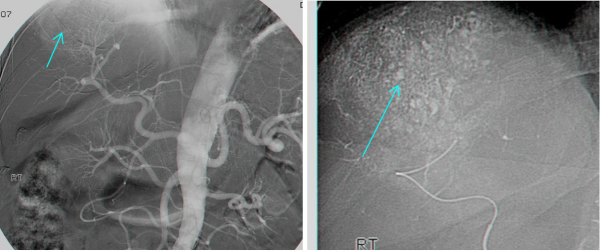
גישה טיפולית אחרת בחולים שלא ניתן לכרות בהם את השאת, היא קשירה של עורק הכבד המספק העיקרי של דם לשאת, או אמבוליזציה של כלי הדם של השאת באמצעים שונים. שיטת האמבוליזציה נקראת גם Transcatheter arterial chemoembolization (TACE) שבה מחדירים צנתר לאחד הענפים של עורק הכבד שמזין את השאת ודרכו מזריקים חומר מטרש כמו גלפום מעורב בחומר ניגוד (רדיואופקי) בעיקר ליפיודול וחומר ציטוטוקסי המקובל Cisplatin. התוצאות המדווחות אינן שונות מהתוצאות של כל טיפול תומך אחר (תצלום 36.10).
שיטה אחרת לטיפול ב- HCC היא על ידי Radiofrequency ablation (RFA) בשיטה זו משתמשים בגנרטור המייצר גל רדיו בעל תדירות גבוהה מאוד המועברת דרך מחט מיוחדת לשאת וגורמת לחימום השאת והריסתה. את המחט ניתן להחדיר לשאת דרך העור או דרך לפרוסקופ או בראיה ישירה בניתוח פתוח. שאתות מעל 5 ס"מ אינן מתאימות ל- RFA (תמונה 11.10 בהמשך).
ההיוותרות בחיים של חולים שלא עברו כריתות או טיפולים מקלים היא 3-4 חודשים בממוצע. 30% מהחולים שעברו כריתות כבד מוצלחות חיים 5 שנים. בילדים הפרוגנוזה טובה יותר. כאשר השאת מתגלית לפני גיל שנתיים - 75% חיים בממוצע 53 חודשים, ואחרי גיל שנתיים - 40% חיים בממוצע 81 חודשים.
גרורות בכבד
לאחר קשרי הלימפה, הכבד הינו האיבר הנפגע ביותר מגרורות. לכמחצית עד 2/3 מהחולים הנפטרים עקב שאתות של המעי יש גרורות בכבד. ממצא זה נכון גם לגבי חולים הנפטרים עקב שאתות של הלבלב, השחלות, השד, הריאות והכליות.
הגרורות מגיעות לכבד במספר דרכים:
- דרך מערכת השער.
- פיזור לימפתי.
- המערכת העורקית של הכבד.
- התפשטות ישירה.
הגרורה יכולה להימצא בזמן האבחון הראשוני של השאת - גרורה סינכרונית, או שנים לאחר אבחון השאת הראשונה - גרורה מטכרונית.
תסמינים קליניים
החולים מופיעים עם: כאבי בטן, ירידה במשקל וחוסר תיאבון.
אבחנה
במעבדה ניתן למצוא פוספטאזה בסיסית ו- CEA מוגברים. האבחנה נעשית בעזרת CT, אולטרה-סאונד של הכבד, מיפוי כבד, PET-CT וניקור הכבד. שיטה נוספת היא לפרוסקופיה וניקור ישיר דרך הלפרוסקופ או בעזרת האולטרה-סאונד הלפרוסקופי.
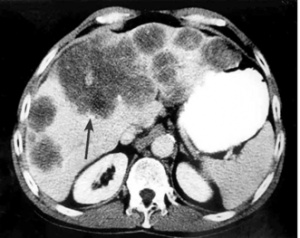
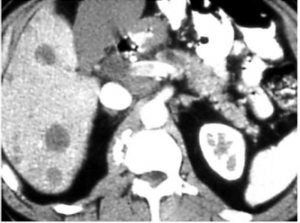
השיטות לאבחון גרורות בכבד הן: אולטראסאונד שבהכוונתו ניתן לבצע ניקור של הכבד ואבחנה של מהות הגוש. CT היא בדיקת הבחירה להדגמת גרורות בכבד ובהכוונתה ניתן לדגום את הגרורות (תצלום 37.10).
|
|
| תצלום 37.10: גרורות מרובות בכבד הנראות ב- CT (חץ). | |
|---|---|
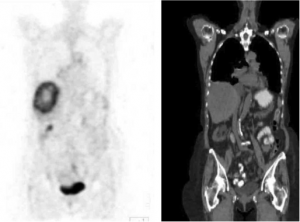
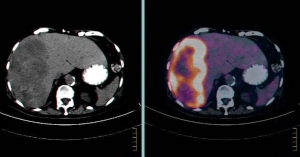
PET-CT הוא כלי חשוב לברור גרורות בכבד מכיוון שמרביתן קולטות FDG, קליטה שהיא אבחנתית לתהליך שאתי בכבד (תצלום 38.10). ה- PET עוזר גם בהגדרת מרחב המחלה בכבד. כל חולה המועמד לכריתת כבד צריך לעבור בדיקת CT תלת פאזי ו- PET-CT להערכת נגעים בכבד ולחיפוש נגעים מחוץ לכבד. רגישות ה- PET-CT היא כ- 90% והדיוק כ- 85%. כימותרפיה טרום ניתוחית מורידה את רגישות בדיקת ה- PET באופן משמעותי.
|
|
| תצלום 38.10: שני תצלומים משמאל - ב- CT נראה פגם מילוי בכבד. שני תצלומים מימין - הפגם "נצבע" על ידי FDG ממצא המעיד על תהליך פתולוגי בכבד. | |
|---|---|
טיפול
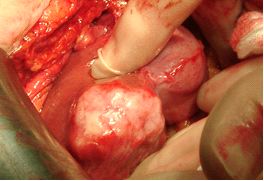
בגישה הטיפולית יש לחלק בין גרורות הניתנות לכריתה כירורגית לבין אלה שאינן ניתנות לכריתה. רק 30% מהגרורות לכבד ניתן לכרות כירורגית (תמונה 10.10).
גרורות הניתנות לכריתה הן:
- גרורות שהשאת הראשונית נכרתה בשלמות (RO).
- אין עדות לגרורות במקומות מרוחקים. נוכחות גרורות חוץ כבדיות נחשבה בעבר להורית נגד מוחלטת לכריתת גרורות בכבד. כיום, מחלה כזו הניתנת לכריתה, במיוחד אם היא בודדה, אינה מהווה הורית נגד לכריתת גרורות בכבד, ודווח בספרות על הישרדות ארוכת טווח בחולים שעברו כריתות משולבות.
- מצב החולה מאפשר כריתת כבד. תנאי הכרחי לבצוע כריתת כבד הוא שימור נפח מספיק של רקמת כבד. הנפח המזערי הדרוש תלוי גם באיכות הפרנכימה הנותרת (שחמת, פיברוזיס והסננה שומנית). במקרים נבחרים ניתן לשלב התערבויות טרום ניתוחיות כמו אמבוליזציה של וריד השער לאונה העומדת להיכרת, במטרה להשיג היפרטרופיה מפצה של האונה הנגדית, המאפשרת כריתת כבד נרחבת או טיפול כימי טרום ניתוחי המכוון להקטנת גרורות במקומות בעיתיים. כמו כן, ניתן לפצל כריתה מורכבת.
- כאשר קיימת גרורה בודדת או מספר גרורות באונה אחת. לעיתים גרורה ביותר מאונה אחת, כמו גרורות באונה שמאלית וסגמנט אחד ימני, עדיין אפשרית כריתה כירורגית.
מקובל כיום כי תוצאות עדיפות מושגות בכירורגיה אנטומית (כריתה לפי סגמנטים או אונות) לעומת כירורגיה משמרת לא אנטומית. עובדה זו לא הוכחה בעבודות שונות שהראו שמספיק שולים של 1-2 מ"מ מסביב לגרורה הנכרתת על מנת להשיג שליטה מקומית (Local control). גישה משמרת כבד זו מאפשרת הרחבת ההוריות לניתוח שימור טוב יותר של רקמת כבד ומהלך פשוט יותר בתר ניתוחי.
בחולים עם גרורות גדולות בכבד או חולים עם גרורות בשתי האונות מקובל לתת טיפול כימי טרום ניתוחי (Neoadjuvant) בהתאם למקור השאת. מכיוון שרוב הגרורות בכבד מקורם בכרכשת, הטיפול הניתן הוא משלבים כימותרפים כמו: 5Fluorouracil או Xeloda עם Leucovorin או Oxaliplatin או CP11 עם או ללא Bevacizumab. שיעורי התגובה הם טובים ובחלק מהחולים אפשר להשיג היעלמות קלינית ופתלוגית של הגרורות. הקטנת הגרורות הופכת חולים לא נתיחים לחולים שניתן לכרות את הגרורות בכבדם. היעלמות קלינית של הגרורות יוצרת בעיה של זיהוי איזור הכריתה הנדרש, מכיוון שאין שאת המכוונת את המנתח, ולכן לעיתים עדיף להשיג הקטנה של השאת לנתח ולהשלים לאחר הניתוח את הטיפול הכימותרפי. בחולים שהגיבו בנסיגה שלמה קלינית של הגרורות בעקבות כימותרפיה טרום ניתוחית מומלץ על כריתת אתר הגרורה. זאת מכיוון שחולים שלא נותחו אחר תגובה כזו רובם יפתחו הישנות מקומית בתוך מספר חודשים.
במספר עבודות במרכזים שונים אותרו גורמי סיכון להישנות לאחר כריתת גרורות מהכבד במטרת ריפוי. זוהו חמישה גורמים המנבאים פרוגנוזה:
- המרווח מההסתמנות ועד גילוי (יותר משנה)
- מספר הגרורות (יותר משלוש)
- גודל הגרורה הגדולה (מעל 5 ס"מ)
- רמת CEA מירבית (יותר מ- ng 200)
- ונוכחות בלוטות לימפה מעורבות בתכשיר המקורי.
כאשר כל חמשת הגורמים קיימים אחוז ההישרדות ירד ל- 14% לעומת 60% הישרדות לחמש שנים בחולים עם גורם אחד. חולים נתיחים אשר להם עד שני גורמים פרוגנוסטיים הם חולים המועמדים לכריתה כירורגית ללא כימותרפיה טרום ניתוחית. חולים נתיחים עם יותר משני גורמים הם מועמדים לכימותרפיה טרום ניתוחית.
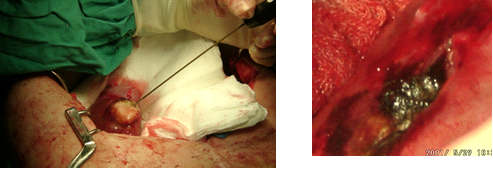
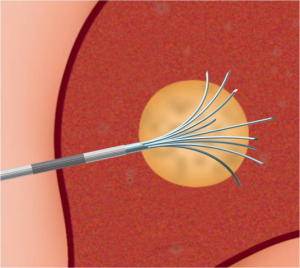
בחלק מהחולים ניתן לשלב את טיפול הכריתה עם טיפול הורס של גרורות (ראה טיפולים מקילים). בחולים עם גרורות בודדות באונה השנייה, או בחולים עם סיכון ניתוחי גבוה, ניתן להרוס את הגרורות על ידי אמצעים תרמיים. מצויות היום אלקטרודות מיוחדות שניתן לכוונן למרכז הנגע בכבד ודרכם להעביר אנרגיית חום על ידי חימום או גל רדיו (Radio frequency) או הקפאת השאת ובכך לחסל את גרורה (תמונה 11.10-12.10). בשיטות אלה ניתן להשתמש כאשר קוטר הגרורה קטן (פחות מ- 3 ס"מ) ובחולים עם גרורות בודדות. לעיתים, ניתן לשלב את הכריתה הכירורגית עם הרס תרמי של הגרורות, לדוגמה כריתת אונה מחד גיסא והרס תרמי של הגידול נותר מאידך גיסא.
|
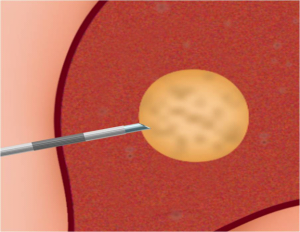
|
| תמונה 11.10: RFA . משמאל החדרת המחט לגידול. מימין פתיחת הזרועות דרכן יעברו גלי הרדיו ויהרסו את השאת. | |
|---|---|
התוצאות הטובות ביותר בכריתת גרורות בכבד מושגות בחולים בעלי שאת ראשונית בכרכשת. בממוצע, כ- 20% מהחולים העוברים כריתה מרפאה של גרורות בכבד חיים 5 שנים לפחות. רק חלק קטן מהחולים עונה לקריטריונים אלה. חולים שבהם לא ניתן לכרות את הגרורות יקבלו משלבים שונים של כימותרפיה. את הכימותרפיה אפשר לתת ישירות לגידול על ידי החדרת צנתר לעורק הכבד ודרכו להזליף את הטיפול הכימי ישירות לגידול או במתן טיפול סיסטמי. רוב החולים עם תהליכים משניים בכבד אינם מתאימים לכריתה כירורגית עקב מספר רב של גידולים, התפשטות לשתי האונות או תפיסת כלי דם ראשיים. חולים אלה יכולים להיעזר בטיפול במחלתם בשיטות זעיר פולשניות כמו טיפולים בגלי רדיו (Radiofrequency - RFA), גלי מיקרוגל או טיפול בלייזר היוצרים חום מקומי במרכז השאת ועקב כך גורמים לנמק של תאי השאת. סוג טיפולים אחר הוא הרס בקור (Cryoablation) או טיפול בכימואמבוליזציה שהינה שיטה בה מטפלים בכבד התרופות ציטוטוקסיות ההורסות את השאת, וחומרים המפקקים את כלי הדם ומונעים הספקת דם לשאת. בכל השיטות הללו נעזרים בהדמיה לאיתור השאת ולמיקום האלקטרודה במרכז השאת.
השימוש שנראה מבטיח, במשאבה המושתלת בעורק הכבד דרך ה-Gastroduodenal artery ומזליפה חומרים ציסטוטוקסיים בצורה מתמדת במשך חודשים או שנים - לא הוכיח את עצמו. האנומליות המרובות של העורק הזה מקשות עוד יותר על הצלחת הטיפול. לפני כל הכנסת צנתר כזה יש לבצע ארטריוגרפיה של עורק הכבד. שיטה חדשנית שבה מבודדים את הכבד על-ידי ניתוק זמני של כלי הדם בכבד והזלפת חומרים ציטוטוקסיים לכבד במנות גבוהות, או TNF, נראית מבטיחה.
פרוגנוזה
ההיוותרות בחיים תלויה במקור השאת. רוב החולים שלא מנותחים נפטרים תוך שנה לאחר האבחנה.
שאתות ממאירות בילדים
השאתות המקובלות הן Embrional hepatoma ,Malignant teratoma hepatoblastoma. כולן שאתות שגדלות לאט וניתנות לכריתה מרפאת. ההחלמה של הכבד לאחר כריתות נרחבות היא מצוינת והכבד יכול לחזור לגודל מתאים ולתפקד היטב, בטווח זמן קצר יחסית. לויקמיה ולימפומה פוגעות בכבד כחלק של המחלה הסיסטמית.
ראו גם
- לנושא הקודם: שאתות בכבד - היבטים כירורגיים - Liver tumors - surgical aspects
- לנושא הבא: המוביליה - Haemobilia
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הלבלב
- לפרק הבא: כירורגיה של הטחול
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק