עדכונים בטיפול בסרטן שד גרורתי בישראל - 2017 - Metastatic breast cancer - treatment - updates
הופניתם מהדף עדכונים בטיפול בסרטן שד גרורתי בישראל 2016 לדף הנוכחי.
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| עדכונים בטיפול בסרטן שד גרורתי בישראל 2017 | ||
|---|---|---|
| Metastatic breast cancer – treatment – updates - 2017 | ||
| ICD-10 | Chapter C 50. | |
| ICD-9 | 174
-175 |
|
| MeSH | D001943 | |
| יוצר הערך | ד"ר נעה אפרת (בן ברוך) | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן שד
סרטן שד גרורתי היא מחלה רבת פנים. מהלך המחלה יכול להיות אטי, עד כדי הפיכתה למחלה כרונית עם יכולת טיפולית ממושכת ולחילופין- מהלך מהיר, עם תגובה מזערית לטיפולים כימיים וביולוגיים (Chemical and Biological).
סל התרופות לסרטן שד ככלל, ולסרטן שד גרורתי בפרט, מבטא את המגוון הרב של טיפולים הקיימים למחלה זו והוא עשיר ומקיף את מרבית התרופות הרשומות ב-FDA (Food and Drug Administration) וב-EMEA (European Medicines Evaluation Agency).
בסקירה זו אפרט בקצרה את המהפכה השקטה שעובר הטיפול בסרטן שד גרורתי, את התרופות העיקריות שנכנסו לסל בשנים האחרונות ואת התרופות המועמדות לסל התרופות ב-2018.
אפיון סרטן שד וחשיבותו בקביעת מסכת טיפולית
הטיפול בסרטן שד גרורתי מסתמך על מאפיינים ביולוגיים של הגידול ובנוסף גם על משתנים רבים נוספים, בהם: מידת הפיזור הגרורתי, מידת ההפרעה לתפקודם של איברים חיוניים, תפקוד החולה, מחלות נוספות והעדפות החולה. קיימים קווים מנחים מקובלים לטיפול בסרטן שד גרורתי, שפורסמו על ידי ESMO (European Society for Medical Oncology), ASCO (American Society of Clinical Oncology) ו-NCCN (National Comprehensive Cancer Network)[1].
בזמן אבחון סרטן שד, נמדדים מספר מאפיינים ביולוגיים על ביופסיית (Biopsy) הגידול, וכן נבדקים גם מאפיינים מולקולריים (Molecular) בשיטות חדישות. בעזרת מאפיינים אלה, ניתן להעריך מהי יעילות הטיפולים השונים ולקבוע את מסכת הטיפול בעלת הסיכוי המרבי להשגת שליטה על המחלה הגרורתית.
שני מאפיינים עיקריים מהווים אבן בסיס בהחלטות טיפוליות:
- קיום ביטוי של קולטנים לאסטרוגן או פרוגסטרון (Estrogen Receptor ,Progeterone Receptor): לחולות עם קולטנים חיוביים להורמונים (Hormones), ניתן טיפולים אנטי הורמונליים כגון: Tamoxifen, Aromatase inhibitors או Fulvestrant (Faslodex). החידושים העיקריים בטיפול בחולות אלו, הם שילוב של תרופות ביולוגיות ספציפיות, יחד עם הטיפול ההורמונלי. שילובים אלה יכולים להביא להיפוך העמידות לטיפול הורמונלי [לדוגמה: טיפולים הורמונליים בשילוב עם מעכבי mTor (mammalian Target of rapamycin)] או לשיפור משך התגובה לטיפול הורמונלי [לדוגמה: שילוב עם מעכבי CDK4/6 (Cyclin-Dependent Kinases)]
- קיום ביטוי ביתר של הקולטן HER2 (Human Epidermal growth factor Receptor 2): לחולות עם ביטוי יתר של HER2, ניתן טיפול ספציפי כנגד HER2 כגון: נוגדנים [Trastuzumab (Herceptin, Kadcyla), Pertuzumab (Perjeta)] או מעכבי Tyrosine kinase ספציפיים (Lapatinib). החידושים העיקריים בטיפול בחולות אלו, הם שילוב של שני אופני דיכוי של HER2, כגון: שני נוגדנים או נוגדן ומעכב Kinase, וכניסתו לשימוש של נוגדן צמוד כימותרפיה (Antibody drug conjugates), בעל יעילות רבה ומיעוט תופעות לוואי
אצל חולות עם גידולים ללא ביטוי של קולטנים להורמונים או HER2 (Triple negative), אפשרות הטיפול העיקרית היא טיפול כימותרפי (Chemotherapy). ניסיון לשלב טיפול ביולוגי שאינו מכוון מטרה ספציפית לסרטן שד, כגון טיפול Anti angiogenic, לא הוביל לתוצאות חד-משמעיות.
מאפיין נוסף, החוצה את כל סוגי סרטן השד, הוא נשאות גנטית (Genetic) של מוטציות (Mutations) בגנים (Genes) BRCA1 ו-BRCA2. מוטציות אלו יכולות להיות מולדות או נרכשות, הנמצאות רק בגידול עצמו. מוטציות אלו פוגעות ביכולת התא הממאיר לתקן נזקי DNA דו-גדילי. לגידולים בעלי מוטציות ב-BRCA, רגישות רבה ביותר לטיפולים הפוגעים במנגנון של תיקון DNA, כגון: Platinum compounds (Cisplatin ו-Carboplatin) וכן לקבוצה של טיפולים ביולוגיים של מעכבי PARP (Poly ADP-Ribose Polymerase), הפוגעים ביכולת התא לתקן נזקי DNA חד גדילי.
כאשר התא אינו מסוגל לתקן נזקי DNA חד ודו גדילי, הוא עובר מוות תאי מתוכנן (Apoptosis) במנגנון שנקרא Synthetic lethality. לתרופות אלו יעילות בגידולים שונים הנושאים מוטציות ב-BRCA, ובשלב זה נמצאות בסל לטיפול אחזקתי בסרטן שחלה אצל נשים עם מוטציה ב-BRCA.
הודגם כי טיפול במעכבי PARP שונים הוא בעל משמעות גם אצל נשים עם סרטן שד גרורתי. תרופות אלו עדיין אינן מועמדות לכניסה לסל ב-2018, אך אנו תקווה כי התוצאות יבשילו לכדי רישום ומעמדות לסל בשנת 2019.
חידושים בטיפולים הורמונליים
החידושים העיקריים בטיפולים הורמונליים הם בפיתוח שילובים של טיפול הורמונלי מוכר עם טיפולים ביולוגיים, שמטרתם להפוך עמידות לטיפול או לשפר את יעילות הטיפול.
Everolimus (Afinitor)
אחת הבעיות המשמעותיות ביותר בטיפול בסרטן היא הופעת עמידות לתרופות. אחד המנגנונים העיקריים המעורבים בפיתוח עמידות היא הפעלת האנזים (Enzyme) mTor עם כל מסלול העברת האותות הנלווה אליו. בתאי סרטן שד, שפיתחו עמידות לטיפול הורמונלי, נראה שפעול יתר של המסלול PI3K/AKT/mTOR.
Everolimus (Afinitor) מוכרת שנים רבות כחלק ממסכת טיפול נוגד דחיית איברים מושתלים, ומנגנון הפעולה של תרופה זו כולל דיכוי של mTor. מחקר "בולרו 2"[2] בדק את היכולת של תוספת Everolimus לטיפול הורמונלי לשפר PFS (Progression-Free Survival, זמן התקדמות המחלה) ו-OS (Overall Survival, שיעורי ההישרדות) לעומת טיפול הורמונלי בלבד. 724 נשים עם סרטן שד גרורתי, שמחלתן התקדמה תוך כדי טיפול הורמונלי על ידי Non steroidal aromatase inhibitors, עברו באופן אקראי בין Exemestane (Aromasin, שהינו Steroidal aromatase inhibitor) + Everolimus [10 מיליגרם (מ"ג) ליום] לעומת Exemestane + אינבו. הודגם שיפור משמעותי ביותר ב-PFS מ-4.1 חודשים ל-Exemestane בלבד ל-10.6 חודשים לשילוב של Exemestane + Everolimus. לא נצפה שיפור משמעותי סטטיסטי ב-OS, אך כן הודגם שיפור מספרי של חיות חציונית של 26.6 חודשים ל-Exemestane לעומת 31 חודשים לשילוב.
לשילוב יש תופעות לוואי הדורשות מעקב צמוד וניהול קפדני. מרביתן מופיעות בחודשים הראשונים לטיפול. תופעות הלוואי כוללות Stomatitis, Pneumonitis, שינויים מטבוליים (Metabolic) ברמות סוכר ושומני הדם, נטייה לזיהומים ובעיות עוריות.
על סמך נתוני "בולרו 2" ונתוני מחקרים נוספים, Everolimus נמצאת בסל הבריאות משנת 2014 בהתוויה של טיפול בסרטן שד גרורתי עמיד לטיפולים הורמונליים, בשילוב עם Exemestane.
Fulvestrant (Faslodex)
Fulvestrant (Faslodex) היא מעכבת של הקולטן לאסטרוגן (ER), בעלת פעילות ייחודית. מנגנון הפעולה של Fulvestrant גורם להרס הקולטן (מנגנון הנקרא: Downregulation). כך, לאחר מתן Fulvestrant לתאי סרטן שד עם ביטוי של ER, נראה היעלמות של ביטוי ER בצביעות Immunohistochemistry.
פיתוח Fulvestrant כטיפול בסרטן שד גרורתי נמשך שנים רבות; הודגם כי יש לתת מנה כפולה, כולל מנת העמסה, לצורך השגת השפעה מרבית במחקר פאזה 3 "CONFIRM"[3]. Fulvestrant ניתנת במינון של 500 מ"ג בזריקה לתוך השריר, כל 28 ימים. בחודש הראשון ניתנת גם מנה נוספת של 500 מ"ג, שבועיים לאחר המתן הראשון. על סמך מחקר זה ומחקרים נוספים, Fulvestrant נמצאת בסל הבריאות כטיפול הורמונלי לסרטן שד גרורתי, במינון של 500 מ"ג עם מנת העמסה, לאחר כישלון של טיפול הורמונלי קודם לסרטן שד גרורתי וכן, לנשים שמחלתן נשנתה יותר משנה לאחר סיום טיפול הורמונלי משלים לסרטן שד מוקדם.
ב-2018 הוגשה בקשה להרחבת הסימן לשימוש ב-Fulvestrant כטיפול הורמונלי כקו טיפולי ראשון בסרטן שד גרורתי, לנשים שקיבלו טיפול הורמונלי משלים לסרטן שד מוקדם, ללא תלות בזמן וכן לנשים שאובחנו בשלב הגרורתי ולא קיבלו כל טיפול קודם. הבקשה להרחבת הסימן לשימוש מבוססת על שני מחקרים: "FIRST"[4] ו-"FALCON"[5].
במחקר פאזה 2 "FIRST"[4], 205 נשים עם סרטן שד גרורתי עם קולטנים חיוביים ו-HER2 שלילי טופלו באופן אקראי בין Fulvestrant 500 מ"ג לחודש, עם מנת העמסה, ל-Anastrozole (Arimidex) 1 מ"ג ליום כקו טיפולי ראשון; מרביתן לא קיבלו כל טיפול הורמונלי קודם. נצפה הבדל משמעותי ביותר ב-TTP (Time To Progression, משך זמן להתקדמות המחלה) בין Anastrozole (13 חודשים) ל-Fulvestrant (23 חודשים), כמו כן נמצא הבדל משמעותי בחיות חציונית בין Anastrozole (48 חודשים) לבין Fulvestrant (54 חודשים). אוכלוסיית החולות במחקר זה אינה מייצגת את אוכלוסיית החולות בישראל, היות שמרבית החולות עם סרטן שד גרורתי נחשפו לטיפול הורמונלי קודם, במסגרת טיפול משלים לסרטן שד מוקדם.
כדי לאמת את תוצאות מחקר "FIRST", תוכנן מחקר "FALCON"- מחקר פאזה 3, הבודק אוכלוסיה דומה למחקר "FIRST", כלומר: נשים עם סרטן שד גרורתי שלא קיבלו כל טיפול קודם[5]. 462 נשים עברו באופן אקראי בין טיפול ב-Fulvestrant ל-Anastrozole. הזמן להתקדמות המחלה היה ארוך יותר בקבוצת החולות שקיבלו Fulvestrant (16.6 חודשים) לבין זה של אלו שקבלו Anastrozole (13.8 חודשים). טרם פורסמו תוצאות של חיות (OS).
מעכבי CDK4/6 (Cyclin-dependent kinase 4/6)
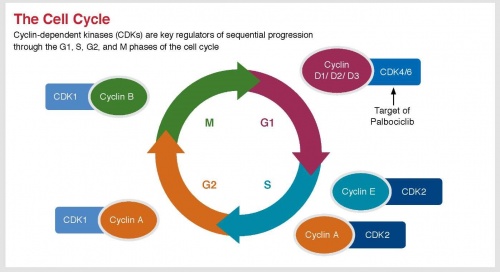
במסגרת מעגל חלוקת התא (תמונה מספר 1) יש חשיבות עליונה לתפקודן של CDKs) Cyclin-dependent kinases).
קינאזות אלו מהוות חלק ממערך אנזימים, החיוניים להתקדמות חלוקת התא בין שלביו השונים (G2 ,S ,G1 ו-S). עיכוב פעילותן של קינאזות אלו יכול להביא להיעצרות מעגל חלוקת התא ולדיכוי חלוקת תאי גידול ממאיר. קינאזות 4 ו-6 חיוניות למעבר מ-G1 ל-S: עיכוב CDK4/6 יביא לעצירת מעגל התא ב-G1 וימנע התקדמות לשלב S. פעילותן של תרופות מדכאות CDK4/6 מהווה הוכחת עיקרון זה (Proof of concept).
שלוש תרופות המעכבות CDK4/6 נמצאות בשלבי מחקר מתקדמים: Palbociclib (Ibrance), Ribociclib (Kisqali) ו-Abemaciclib[6],[7],[8],[9]. שתי הראשונות רשומות FDA והשלישית תירשם בזמן הקרוב.
Palbociclib
Palbociclib נרשמה ב-FDA בשנת 2015 כטיפול, בשילוב עם Letrozole, כקו טיפולי ראשון בחולות עם סרטן שד גרורתי ורצפטורים חיוביים וב-2016, בשילוב עם Fulvestrant, כטיפול בקווים מתקדמים יותר. Palbociclib ניתנת דרך הפה במינון של 125 מ"ג ליום, בתזמון יומי, למשך 3 שבועות עם שבוע הפסקה. התרופה נסבלת היטב עם רעילות מינימלית, הכוללת Neutropenia ותשישות. לא נצפו מאורעות של זיהומים הקשורים ל-Neutropenia במחקרים קליניים. האישור לטיפול בקו ראשון ניתן על סמך מחקר פאזה 2 "פלומה 1"[10], ואושר במחקר פאזה 3 "פלומה 2"[11].
במחקר "פלומה 1" טופלו 165 נשים עם סרטן שד גרורתי, ללא טיפול קודם למחלה גרורתית ולפחות שנה לאחר סיום של טיפול הורמונלי משלים לסרטן שד מוקדם. החולות עברו באופן אקראי בין טיפול על ידי Letrozole במינון של 2.5 מ"ג ליום לבין Letrozole+ Palbociclib (במינון ובתזמון כמפורט מעלה). ה-Primary end point של המחקר היתה PFS עם נקודות משניות של OS, משך תגובה ואחוזי תגובה לטיפול. המחקר כלל שתי קבוצות: בקבוצה הראשונה נכללו חולות ללא אפיון של סמנים ביולוגיים (Biomarkers) ובקבוצה השנייה נכללו חולות עם מאפיינים ביולוגיים שנחשבו למנבאי יעילות של Palbociclib (הגן CCND1 וכן הגברה ו/או אבדן של החלבון p16). לא נצפה כל הבדל בין הקבוצות ולכן בניתוח המחקר בוצע איחוד של שתי הקבוצות.
"פלומה 1" אישר את הנחת היסוד, ששילוב של Palbociclib עם Letrozole האריך באופן משמעותי את הזמן להתקדמות המחלה: מ-10 חודשים ל-20 חודשים. לא נצפה הבדל משמעותי בחיות החציונית, אם כי נצפה הבדל מספרי של 34 לעומת 30 חודשים.
מחקר "פלומה 2" הוא מחקר פאזה 3 זהה ל"פלומה 1". במחקר זה טופלו 666 נשים באקראיות של 2:1 על ידי Letrozole + Palbociclib (444 נשים) לעומת Letrozole + אינבו (222 נשים). גם במחקר פלומה 2 הודגם הבדל משמעותי ביותר בזמן להתקדמות המחלה בין החולות שקיבלו את השילוב לבין החולות שקבלו Letrozole בלבד, מ-14.5 חודשים ל-24.8 חודשים (HR=0.58; Confidence Interval ,CI=0.46-0.72, Hazard Ratio). נתוני חיות (OS) לא הוצגו עדיין, עקב חוסר זמן.
Palbociclib נבדקה במחקר "פלומה 3"[12], אצל 521 נשים עם סרטן שד בעל רצפטורים חיוביים ו-HER2 שלילי, שמחלתן התקדמה על טיפול הורמונלי קודם.
טיפול הורמונלי קודם הוגדר כטיפול הורמונלי למחלה גרורתית (עד שני קווי טיפול) או טיפול הורמונלי משלים, עם התקדמות המחלה, תוך כדי קבלת טיפול משלים. הטיפול שניתן במחקר "פלומה 3" היה 500 מ"ג Fulvestrant כל 4 שבועות, עם מנת העמסה ביום ה-14, בשילוב עם Palbociclib לעומת Fulvestrant באותו מינון, בשילוב עם אינבו.
347 נשים קיבלו Fulvestrant עם Palbociclib ו-174 נשים קיבלו Fulvestrant עם אינבו. גם במחקר זה הושגה המטרה הראשונית עם יותר מהכפלת ה-PFS מ-4.6 חודשים ל-Fulvestrant לבד ל-11.2 חודשים לשילוב. בנוסף, הודגמה במחקר שיפור באיכות חיי המטופלות שקיבלו את השילוב, לעומת Fulvestrant כתרופה בודדת.
על סמך מחקרים אלה ורישומה של Palbociclib על ידי ה-FDA, Palbociclib נרשמה בארץ לשתי ההתוויות בחודשים אלה ומוגשת להכללה בסל הבריאות של 2018, בהתוויה של קו טיפולי ראשון אצל נשים עם סרטן שד גרורתי בשילוב עם Letrozole וקו טיפולי מתקדם בשילוב עם Fulvestrant.
Ribociclib
Ribociclib נרשמה ב-FDA בשנת 2017, כטיפול בשילוב עם Letrozole כקו טיפולי ראשון בחולות עם סרטן שד גרורתי ורצפטורים חיוביים.
Ribociclib ניתנת דרך הפה במינון של 600 מ"ג ליום בתזמון יומי, למשך 3 שבועות עם שבוע הפסקה. בדומה ל-Palbociclib, התרופה נסבלת היטב עם רעילות מינימלית הכוללת Neutropenia ותשישות, ללא מאורעות של זיהומים הקשורים ל-Neutropenia. באחוז קטן של החולות נצפתה הארכה של מקטע QT, ונדרש ניטור אלקטרוקרדיוגרם (Electrocardiography, ECG) בחודשים הראשונים לטיפול.
Ribociclib נרשמה ב-FDA על סמך מחקר פאזה 3 "מונה ליזה 2"[13]. במחקר זה השתתפו 668 נשים שקיבלו Ribociclib עם Letrozole (334 נשים) או עם אינבו (334 נשים), כקו טיפולי ראשון למחלה גרורתית. גם כאן הושגה מטרת המחקר, כאשר השילוב הדגים הארכה משמעותית ב-PFS של 25.3 חודשים לעומת 16 חודשים ל-Letrozole בלבד. מחקר הבודק יעילות של Ribociclib בשילוב עם Fulvestrant כקו טיפול מתקדם סיים גיוס, ותוצאותיו יפורסמו בעתיד.
על סמך מחקר זה ורישומו על ידי ה-FDA, Ribociclib מועמדת לרישום בארץ להתוויה של קו טיפולי ראשון אצל נשים עם סרטן שד גרורתי בשילוב עם Letrozole, ומוגשת להכללה בסל הבריאות של 2018 להתוויה זו.
Abemaciclib
Abemaciclib היא השלישית ממשפחת מעכבי CDK4/6, שעדיין אינה רשומה ב-FDA. גם היא ניתנת דרך הפה, אך בשונה מ-Palbociclib ו-Ribociclib, היא ניתנת בתזמון יומי רציף במינון של 300 מ"ג ליום. פרופיל תופעות הלוואי של Abemaciclib שונה במקצת, יש פחות Neutropenia ויותר רעילות למערכת העיכול, המתבטאת בשלשולים.
מחקר "מונרך 3" הוצג בספטמבר 2017 בכינוס ESMO ועדיין לא פורסם, והוא מקביל באוכלוסיית החולות ל"פלומה 2" ו"מונה ליזה 2", כלומר: קו טיפול ראשון בשילוב עם Letrozole, לעומת אינבו אצל חולות עם סרטן שד גרורתי. גם כאן הושגה מטרת המחקר: PFS אצל חולות שקיבלו את השילוב עדיין לא נמדד, לעומת 14.7 חודשים אצל החולות שקיבלו Letrozole בלבד; הצפי הוא ל-PFS של כ-25 חודשים, לפחות, עם השילוב- משך זמן התואם את התוצאות שהושגו בשני המחקרים המקבילים.
Abemaciclib נבדקה במחקר "מונרך 2" כקו טיפול מתקדם, בשילוב עם Fulvestrant, בדומה למחקר "פלומה 3". גם כאן הושגה מטרת המחקר עם PFS לשילוב של 16.4 חודשים לעומת 9.3 חודשים ל-Fulvestrant לבד.
על סמך מחקרים אלה, Abemaciclib מוגשת להכללה בסל הבריאות של 2018, בהתוויה של קו טיפולי ראשון אצל נשים עם סרטן שד גרורתי בשילוב עם Letrozole וקו טיפולי מתקדם בשילוב עם Fulvestrant. זאת, לאחר רישומה ב-FDA ובארץ להתוויות אלו.
לשילוב של מעכבי CDK4/6 עם Letrozole משמעות רבה ביותר במסכת הטיפול אצל חולות עם סרטן שד גרורתי בעל רצפטורים חיוביים; אלו הן מרבית החולות עם סרטן שד גרורתי, ומתן השילוב מאפשר משך חיים ממושך יותר עם שליטה טובה ומיעוט תופעות לוואי לפני החמרה וצורך לעבור לקו טיפולי נוסף. כמו כן, בנוסף למשך תגובה ארוך יותר, לשילוב יש גם אחוז תגובה גבוה יותר מ-Letrozole כתרופה בודדת וכן מהירות תגובה גבוהה יותר. לא אחת נראה תגובות לשילוב תוך 6-4 שבועות מתחילת הטיפול, בעוד שעם Letrozole בלבד התגובה תיראה לאחר 3 חודשים ויותר.
חידושים בטיפולים כימיים
מרבית התרופות המפותחות היום הן תרופות ביולוגיות, בעלות מנגנון פעילות מולקולרי ייחודי, אך לצערנו רק למקצת מן הגידולים הממאירים אנו יכולים לזהות מטרות מולקולריות ולפתח תרופות ייעודיות. עקב כך, קיים צורך ברור בהמשך פיתוח תרופות כימותרפיות.
Eribulin
Eribulin היא תרופה ייחודית: אנלוג (Analog) סינתטי של Halichondrin B, שבודד מהספוג הימי: Marine sponge Halichondria okadai. Eribulin נקשרת לאתר ייחודי על Tubulin, מדכאת את הפולימריזציה (Polymerization) של המיקרוטובולים (Microtubules) ואינה מאפשרת מיטוזה (Mitosis), באופן בלתי הפיך. מנגנון הפעולה של Eribulin שונה מזה של Taxanes, ובתרביות רקמה מראה יעילות בתאים העמידים ל-Taxol.
Eribulin ניתנת במינון של 1.4 מ"ג/מ2 (מיליגרם למטר רבוע) בימים 8,1 כל 3 שבועות. הטיפול ניתן בעירוי מהיר של 5-2 דקות. תופעות הלוואי השכיחות הן: Peripheral neuropathy (כמו כל התרופות הכימותרפיות הפוגעות במיקרוטובולים), Neutropenia וחולשה.
שני מחקרים עיקריים מדגימים את פעילותה של Eribulin בחולות עם סרטן שד גרורתי, ובניתוח של אחד מהם מודגמת פעילות ייחודית אצל חולות עם סרטן שד מסוג Triple negative. במחקר הראשון, "EMBRACE"[14], טופלו 762 נשים עם סרטן שד גרורתי, שקיבלו לפחות 2 קווי טיפול קודמים למחלה גרורתית (טווח של 5-2 קווי טיפול קודמים). 508 נשים קיבלו Eribulin ו-254 קיבלו טיפול לפי בחירת הרופא המטפל, ללא מגבלה על סוג הטיפול. המטרה הראשונית של המחקר הייתה OS ואכן, מטרה זו הושגה כאשר אצל חולות שקיבלו Eribulin החיות החציונית עמדה על 13.1 חודשים, לעומת 10.6 חודשים אצל חולות שטופלו לפי בחירת הרופא המטפל. הבדל זה היה משמעותי סטטיסטית עם HR=0.81 ו- p value=0.041.
מחקר נוסף[15] בדק אוכלוסיית חולות דומה, עם מעט פחות קווי טיפול קודמים. הפעם הייתה מגבלה של עד 2 קווי טיפול לסרטן שד גרורתי, כאשר האקראיות בטיפולים הייתה בין Eribulin ל-Capecitabine (Xeloda). Eribulin במינון שנכתב מעלה ו-Capecitabine במינון של 2,500 מ"ג/מ2 ליום, בימים 14-1, כל 3 שבועות.
1,102 חולות עברו באקראי בין Eribulin ל-Capecitabine. במחקר זה לא נצפה כל הבדל במדדי PFS ו-OS בין Eribulin ל-Capecitabine: שיעור החיות החציוני היה 15.9 ו-14.5 חודשים, בהתאמה (HR=0.879, CI=0.770-1.003, p=0.056) ושיעור ה-PFS (בבחינה בלתי תלויה) עמד על 4.1 ו-4.2 חודשים עבור Eribulin ו-Capecitabine, בהתאמה (HR=1.079, CI=0.932-1.250, p=0.305). במחקר זה בוצע סיווג (Stratification) מראש לפי מצב הקולטנים.
במאמר שכלל את שני המחקרים בוצעה מטא-אנליזה (Meta analysis) לגבי יעילות Eribulin בתת אוכלוסיות שונות לפי מצב הקולטנים ו-HER2[16]. 1,062 חולות קיבלו Eribulin, 802 טופלו בקבוצת הבקרה. החיות החציונית עמדה על 15.8 חודשים עם Eribulin ועל 12.8 חודשים בקבוצת הבקרה (HR 0.85, p=0.003); ובייחוד אצל נשים עם סרטן שד מסוג Triple negative, התוצאות עמדו על חיות חציונית של 12.9 חודשים למטופלות על ידי Eribulin, לעומת 8.2 חודשים בקבוצת הבקרה (HR=0.74, p=0.006).
על סמך נתונים אלה, Eribulin רשומה במשרד הבריאות לטיפול בנשים עם סרטן שד גרורתי לאחר טיפול קודם ב-Anthracyclines ו-Taxanes. Eribulin הוכנסה לסל ב-2016, לחולות עם סרטן שד מסוג Triple negative, ומוגשת לסל 2018 לטיפול בנשים עם סרטן שד גרורתי עם HER2 שלילי ורצפטורים, כקו טיפולי שני ומעלה.
ביבליוגרפיה
- ↑ Cardoso, F., et al., ESO-ESMO 2nd international consensus guidelines for advanced breast cancer (ABC2)dagger. Ann Oncol, 2014. 25(10): p. 1871-88.
- ↑ Baselga, J., et al., Everolimus in postmenopausal hormone-receptor-positive advanced breast cancer. N Engl J Med, 2012. 366(6): p. 520-9.
- ↑ Di Leo, A., et al., Final overall survival: fulvestrant 500 mg vs 250 mg in the randomized CONFIRM trial. J Natl Cancer Inst, 2014. 106(1): p. djt337.
- ↑ 4.0 4.1 Ellis, M.J., et al., Fulvestrant 500 mg Versus Anastrozole 1 mg for the First-Line Treatment of Advanced Breast Cancer: Overall Survival Analysis From the Phase II FIRST Study. J Clin Oncol, 2015.
- ↑ 5.0 5.1 Robertson, J.F.R., et al., Fulvestrant 500 mg versus anastrozole 1 mg for hormone receptor-positive advanced breast cancer (FALCON): an international, randomised, double-blind, phase 3 trial. Lancet, 2016. 388(10063): p. 2997-3005
- ↑ Bilgin, B., et al., A current and comprehensive review of cyclin-dependent kinase inhibitors for the treatment of metastatic breast cancer. Curr Med Res Opin, 2017.: 33(9): p. 1559-1569.
- ↑ Griggs, J.J. and A.C. Wolff, Cyclin-Dependent Kinase 4/6 Inhibitors in the Treatment of Breast Cancer: More Breakthroughs and an Embarrassment of Riches. J Clin Oncol, 2017. 35(25): p. 2857-2859.
- ↑ Kwapisz, D., Cyclin-dependent kinase 4/6 inhibitors in breast cancer: palbociclib, ribociclib, and abemaciclib. Breast Cancer Res Treat, 2017.
- ↑ I Wander, S.A., E.L. Mayer, and H.J. Burstein, Blocking the Cycle: Cyclin-Dependent Kinase 4/6 Inhibitors in Metastatic, Hormone Receptor-Positive Breast Cancer. J Clin Oncol, 2017. 35(25): p. 2866-2870.
- ↑ Finn, R.S., et al., The cyclin-dependent kinase 4/6inhibitor palbociclib in combination with letrozole versus letrozole alone as first-line treatment of oestrogen receptor-positive, HER2-negative, advanced breast cancer (PALOMA-1WRIO-18): a randomised phase 2 study. Lancet Oncol, 2015. 16(1): p. 25-35.
- ↑ Finn, R.S., et al., Palbociclib and Letrozole in Advanced Breast Cancer. N Engl J Med, 2016. 375(20): p. 1925¬1936.
- ↑ Turner, N.C., et al., Palbociclib in Hormone-Receptor- Positive Advanced Breast Cancer. N Engl J Med, 2015. 373(3): p. 209-19.
- ↑ Hortobagyi, G.N., et al., Ribociclib as First-Line Therapy for HR-Positive, Advanced Breast Cancer. N Engl J Med, 2016. 375(18): p. 1738-1748.
- ↑ Cortes, J., et al., Eribulin monotherapy versus treatment of physician's choice in patients with metastatic breast cancer (EMBRACE): a phase 3 open-label randomised study. The Lancet, 2011. 377(9769): p. 914-923.
- ↑ Kaufman, P.A., et al., Phase III open-label randomized study of eribulin mesylate versus capecitabine in patients with locally advanced or metastatic breast cancer previously treated with an anthracycline and a taxane. J Clin Oncol, 2015. 33(6): p. 594-601.
- ↑ Twelves, C., et al., Efficacy of eribulin in women with metastatic breast cancer: a pooled analysis of two phase 3 studies. Breast Cancer Res Treat, 2014. 148(3): p. 553-61.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר נעה אפרת (בן ברוך) - מנהלת המכון האונקולוגי, המרכז רפואי קפלן, רחובות


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק