ניהול היריון ולידה בזיהומים מסכני אם ועובר - נייר עמדה
הופניתם מהדף Parvo Virus לדף הנוכחי.
|
| |
|---|---|
| נייר עמדה מספר 25 - ניהול היריון ולידה בנוכחות זיהומים מסכני אם ועובר, נוהל הטיפול בנשים הרות נשאיות של HIV | |
| ניירות עמדה של האיגוד הישראלי למיילדות וגינקולוגיה | |
| תחום | מיילדות |
| האיגוד המפרסם | החברה הישראלית לרפואת האם והעובר החברה הישראלית לחקר ומניעת מחלות המועברות במגע מיני החברה הישראלית לכשל חיסוני נרכש - איידס האיגוד למחלות זיהומיות בישראל |
| קישור | באתר האיגוד הישראלי למיילדות וגינקולוגיה |
| תאריך פרסום | אוגוסט 2025 |
| יוצר הערך | פרופ' טל בירון שנטל פרופ' רינת גבאי בן זיו פרופ' חן סלע פרופ' לירן הירש פרופ' גלי פריאנטה ד"ר דנה ויטנר ד"ר הדר רוזן ד"ר גיל שכטר מאור פרופ' מאיה וולף פרופ׳ מיכל פישל ברטל |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – היריון, לידה, HIV - נגיף הכשל החיסוני האנושי
נוהל הטיפול בנשים הרות החיות עם HIV
הקדמה
נכון לשנת 2022 היו רשומים 8,735 אנשים החיים עם HIV/איידס בישראל. בשנת 2023 דווח על 400 מקרים חדשים בישראל, ירידה לעומת 2022, אז התגלו כ-457 מקרים חדשים. בין השנים 2015 ל-2022 היו בין 2–6 מקרים של העברה ורטיקאלית מאם לילוד בשנה.
(הנתונים מתוך: HIV/איידס בישראל, דו״ח אפידמיולוגי תקופתי 1981–2022, משרד הבריאות)
סיכון למעבר לילוד
מטרת הטיפול האנטירטרוויראלי באישה הרה החיה עם HIV היא למזער את הסיכון להעברת הנגיף ליילוד, לשמור על בריאות האם ולהפחית העברה לבני זוג נוספים.
עיקר ההעברה לילוד מתרחשת במהלך הלידה. העברה במהלך ההיריון היא נדירה. שיעור ההעברה מאם ליילוד בהיריון ולידה באישה שאינה מטופלת עלול להגיע ל-15–30 אחוזים, כאשר בעזרת אבחנה וטיפול מתאימים ניתן להוריד את שיעור ההעברה הוורטיקאלית לפחות מ-1 אחוזים.
בדיקת סקר
בהתאם לחוזר משרד הבריאות מספר 2/2022, יש לסרוק את כל הנשים בהיריון בכל היריון ל-HIV. את הבדיקה יש לבצע בשליש הראשון להיריון. יש ליידע את האישה כי אחת מבדיקות השגרה המבוצעות היא HIV. אם האישה מתנגדת לביצוע הבדיקה, יש ליידע אותה כי קיים טיפול לנשים המתגלות כחיוביות היכול למנוע את ההעברה מהאם לילוד, וגם לשמור על בריאותה שלה. מחלת HIV שאינה מטופלת גורמת, בסופו של דבר, למות החולה כתוצאה מכשל חיסוני.
במקרה של תוצאה של בדיקה ראשונה חיובית או לא ודאית, על הרופא/ה המטפל/ת להפנות בהקדם האפשרי להמשך בירור וטיפול באחת ממרפאות HIV על פי בחירת האישה ההרה. טיפול מוקדם במהלך ההיריון מעלה את הסיכוי כי הנגיף לא יועבר לילוד, ומעלה משמעותית את הסיכוי כי האם לא תפתח סיבוכים הקשורים למחלת האיידס. כמו כן, הטיפול מונע הדבקה של בני הזוג.
בנשים הנמצאות בסיכון גבוה (לדוגמה: נשים שמקיימות יחסי מין תמורת תשלום, נשים עם פרטנרים מיניים מרובים במהלך ההיריון, נשים שבן זוגן המיני מקיים יחסי מין עם פרטנריות/ים נוספים במהלך ההיריון, או נשים שמשתמשות בסמים), מומלץ לבצע בדיקת סריקה חוזרת ל-HIV בשבוע 28–32 ושוב בלידה.
PrEP
בזוגות בהם אחד מבני הזוג מאובחן עם HIV ואילו השני לא, והם מעוניינים בהיריון, יש לוודא השגת דיכוי נגיפי מקסימלי (2 מדידות של עומס נגיפי בלתי מדיד (Undetectable) בהפרש של 3 חודשים), וזאת על מנת להפחית סיכון להעברה לבן הזוג וכן למנוע העברה ורטיקאלית בהיריון. ניתן לשקול מתן PrEP לבת הזוג (Pre-Exposure Prophylaxis) השלילית, בעיקר במצבים בהם בן הזוג אינו נוטל טיפול תרופתי או שאינו מקפיד לקבל טיפול או לעבור ניטור רפואי – זאת בהתייעצות עם מומחה HIV.
המלצות למעקב ההיריון
מומלץ שהמעקב יתבצע על ידי צוות הכולל מומחה למחלות זיהומיות/אימונולוגיה ו/או מרפאה ייעודית ל-HIV ומרפאה לרפואת האם והעובר.
בדיקות ההיריון
- בדיקות סקירה תבוצענה ללא שינוי
- מומלץ לבצע חיסונים, סקר סרולוגי למחלות זיהומיות ותרבית שתן בהתאם לנייר העמדה על בדיקות שגרה בכל היריון (נייר עמדה מספר 6)
- אין מניעה לבצע חיסונים כמקובל בהיריון
- דיקור מי שפיר: במידת האפשר, מומלץ לדחות את הדיקור עד להתחלת טיפול משולב והיעלמות העומס הנגיפי. יש להימנע ככל הניתן מלבצע את דיקור מי השפיר דרך השליה
טיפול ומעקב בהיריון
יש להתחיל טיפול אנטי-רטרוויראלי לכל הנשים בהיריון החיות עם HIV, על פי אמות הטיפול המקובלות במבוגרים החיים עם HIV, וללא קשר לרמות העומס הנגיפי או CD4. הטיפול יימשך למשך כל ההיריון, וכמקובל בזמן הלידה, ומומלץ להמשיך את הטיפול לאחר הלידה לזמן בלתי מוגבל. גם הילוד צריך לקבל טיפול מונע לאחר לידתו. בחירת פרוטוקול הטיפול המועדף לנשים הרות תתבצע בתיאום עם מומחה ל-HIV ובהתאם למצבים הקליניים השונים ולשבוע ההיריון.
- יש למדוד רמות HIV RNA בפלזמה במפגש הראשון להיריון, וכן כל 2–4 שבועות לאחר התחלת (או החלפת) הטיפול, עד לקבלת רמות שאינן ניתנות למדידה (undetectable)
- לאחר הגעה לעומס נגיפי בלתי מדיד ניתן לעקוב אחר רמות HIV RNA בפלזמה אחת ל-3 חודשים
- בדיקה נוספת בשבוע 34–36 להיריון על מנת לקבל החלטה מושכלת לגבי אופן היילוד
- CD4 – יש למדוד רמות לכל הנשים בתחילת מעקב ההיריון. יש לחזור על רמות CD4 על פי המלצת המומחה ל-HIV שעוקב אחר האישה
ירידת מים מוקדמת
אופן הניהול המיטבי בירידת מים מוקדמת בנשים החיות עם HIV אינו ברור ויש לשקול את החשש מהעברה ורטיקאלית אל מול סיבוכי פגות. קיימת עדות לכך שכאשר ההרה מטופלת בטיפול אנטירטרוויראלי במהלך ההיריון, עם עומס נגיפי נמוך וטיפל מונע במהלך הלידה, אין עלייה בשיעור ההעברה הורטיקאלית גם במקרי ירידת מים מוקדמת .
במקרים אלו מומלץ ניהול פרטני בליווי מומחה HIV, כאשר בגיל היריון מוקדם לפני שבוע 34, במטופלת עם טיפול מתאים ועומס נגיפי נמוך ניתן לשקול טיפול שמרני.
ניהול הלידה
מרבית מקרי ההדבקה מתרחשים בלידה עצמה ומיעוטם בשליש האחרון של ההיריון, לכן רצוי לתכנן בצורה מיטבית את אופן היילוד, ואת הטיפול באם. יש ליידע רופא יילודים בכל לידה של הרה שחיה עם HIV.
אופן היילוד
ניהול לידה על סמך העומס הנגיפי אשר נמדד בשבוע 34–36:
- אם העומס הנגיפי מתחת ל-50 עותקים למיליליטר
- ניתן לאפשר לידה נרתיקית
- יילוד יזום לפני שבוע 40 לא הוכח כמפחית סיכון להעברה ורטיקאלית
- משך ירידת המים בנשים עם עומס נגיפי נמוך אינו קשור לעלייה בהעברה ורטיקאלית
- אין צורך במתן AZT (Zidovudine) פרופילקטי תוך-ורידי
- בנשים עם עומס נגיפי מעל 50 אך מתחת ל-1000 עותקים למיליליטר ניתן לאפשר לידה נרתיקית. אין חובה לתת Zidovudine מניעתי בזמן הלידה, אך מומלץ להתייעץ עם מומחה ל-HIV לגבי ההמלצות באופן פרטני
- בכל מקרה יש להמשיך את הטיפול הקבוע האנטירטרוויראלי אותו מקבלת האישה גם סביב הלידה
- לנשים עם עומס נגיפי מעל 1000 עותקים למיליליטר בסמוך למועד הלידה, או בנשים שלא ידוע מהו העומס הנגיפי בסמוך ללידה:
- מומלץ לתכנן ניתוח קיסרי לשבוע 38–39 להיריון
- יש להתחיל טיפול תוך-ורידי ב-Zidovudine שלוש שעות לפני תחילת הניתוח הקיסרי
- Zidovudine ניתן תוך-ורידית, מנת העמסה במינון 2 מיליגרם/קילוגרם במשך שעה, ובהמשך 1 מיליגרם/קילוגרם/שעה עד הלידה
| Treatment and VL status of the mother | Received antepartum ART with no adherence concerns | * No antepartum ART*
| ||
| Undetectable
VL(<50 copies/mL) within 4 weeks of delivery |
Detectable (>50 copies/mL) but <1000 copies/mL within 4 weeks of delivery | >1000 copies/mL within 4 weeks of delivery | ||
| Risk for HIV transmission | * Low risk | High risk | High risk | High risk |
| Preferred delivery mode | Determined by obstetric indications | Determined by obstetric indications | Scheduled cesarean delivery at 38 weeks | Individualized based on HIV viral level (If known) and presentation* |
| Intrapartum antiretrovirals | Continue baseline ART regimen | * continue baseline ART regimen
|
* continue baseline AR־ regimen
|
continue baseline ART regimen if receiving ART
|
| Other intrapartum interventions | Avoid fetal scalp electrodes | * Avoid artificial rupture of membranes
|
Avoid fetal scalp electrodes | * Avoid artificial rupture of membranes (If
not undergoing cesarean)
|
| Infant antiretroviral prophylaxis* | 2 to 4 weeks of zidovudine | Presumptive HIV therapy | Presumptive HIV therapy | Presumptive HIV therapy |
הנחיות כלליות לטיפול במהלך לידה נרתיקית
- מומלץ להימנע מפקיעת קרומים יזומה או משימוש בניטור פנימי המחובר לקרקפת העובר
- עדיפות להימנע מלידה מכשירנית
- יש להימנע מטפול במטרגין אצל נשים עם PPH (Post Partum Hemorrhage) המטופלות בתכשיר אנטי-רטרוויראלי ממשפחת ה-Protease inhibitor בשל סיכון מוגבר לוזוקונסריקטציה בשילוב התרופות
הטיפול התרופתי במהלך הלידה
- טיפול תוך ורידי ב-Zidovudine מומלץ לנשים החיות עם HIV אשר העומס הנגיפי בפלסמה שלהן הוא מעל 1000 עותקים למיליליטר
- נשים המטופלות טיפול אנטי-רטרוויראלי משולב, ימשיכו טיפול זה ככל שניתן במהלך הלידה ולפני ניתוח קיסרי על פי המלצות מומחה ל-HIV
- בכל מקרה של עומס נגיפי מעל 50 עותקים מומלץ להתייעץ עם מומחה HIV
המלצות לטיפול ומעקב במשכב הלידה
- יש להימנע מהנקה. נשים החיות עם HIV זכאיות לקבל תרכובת מזון לתינוקות (תמ״ל) ללא עלות במהלך 12 חודשים שלאחר הלידה. על הרופא/ה המטפל/ת במרפאת HIV ליידע אישה הרה על הזכות לקבלת אספקה שוטפת של תמיליליטר וכן להפנות לאגף התזונה/מזון של הקופה המבטחת לקבלת הדרכה על מימוש זכות זו
- אם האישה בכל זאת מעוניינת בהנקה, בתנאי שהיא נמצאת במעקב קבוע עם היענות טובה לטיפול ומעקב, והעומס הנגיפי בדמה בלתי מדיד בבדיקות עוקבות, ניתן לדון באופן פרטני עם האישה על האפשרות להניק תוך כדי הסבר על הסיכון שקיים בכך
- לכל אישה מומלץ להמשיך ולקחת טיפול אנטי-רטרוויראלי לאחר הלידה ובמשך כל החיים
- יש להפנות את האם והתינוק למרכז HIV להמשך טיפול ומעקב
מקורות
- Panel on Treatment of HIV During Pregnancy and Prevention of Perinatal Transmission. Recommendations for the Use of Antiretroviral Drugs During Pregnancy and Interventions to Reduce Perinatal HIV Transmission in the United States. Department of Health and Human Services. Available at https://clinicalinfo.hiv.gov/en/ guidelines/perinatal. Updated Dec 30th 2021
- Silverman, N. S. )2018(. Labor and Delivery Management of Women with Human Immunodeficiency Virus Infection. Obstetrics and Gynecology, 132)3(, E131-E13
- EACS )EUROPEAN AIDS CLINICAL SOCIETY( guidelines - 2024 https://eacs.sanfordguide.com/eacs-part1/ art/eacs-pregnancy-and-hiv
- Recommendations for the Use of Antiretroviral Drugs During Pregnancy and Interventions to Reduce Perinatal HIV Transmissions in the United States, 2024 *https://clinicalinfo.hiv.gov/en/guidelines/perinatal/ whats-new
- חוזר משרד הבריאות -02/2022 - נוהל אבחון מוקדם של האישה בגיל הפוריות הנושאת HIV והטיפול בה
- ACOG committee opinion 751: Labor and delivery management of women with Human Immunodeficiency Virus
הרפס בהיריון
מבוא
נגיפי ההרפס סימפלקס (Herpes simplex virus – HSV) מסוג 1 ו-2 שייכים למשפחת נגיפי ההרפס (DNA), החבויים בצורה לטנטית במאכסן. שפעול הנגיף לעיתים אל-תסמיני ואינו מלווה במחלה קלינית. השפעול הוא ספונטאני או עקב לחץ נפשי, מאמץ גופני, חשיפה לקרינת UV, נזק לרקמה או דיכוי חיסוני, אך לא תמיד ניתן לזהות גורם כלשהו.
בזיהום בהרפס גניטלי ראשוני יופיעו נגעים אופייניים, לעומת זיהום חוזר/משופעל שבו ייתכנו נגעים שיהיו קשים לזיהוי ולאבחון קליני. נגיפי ההרפס אינם טרטוגנים.
הסיבוך החמור ביותר של הרפס גניטלי בהיריון הוא המחלה בילוד (Neonatal Herpes) לאחר הלידה, שלה שלושה סוגי התבטאויות אפשריים (רירית ועור, מערכת עצבים מרכזית או זיהום סיסטמי), המתבטאת במעורבות משמעותית של מערכת העצבים המרכזית בכ-50 אחוזים מהנדבקים. התמותה מגיעה לכדי 30 אחוזים, ו-40 אחוזים מהשורדים ילקו בחסרים נוירולוגיים למרות טיפול אנטי-ויראלי.
הזיהום הגניטלי האימהי מסווג לפי סרולוגיה ומבחני גילוי הנגיף
- ראשוני (primary): אירוע ראשון של זיהוי הנגיף במערכת הגניטליה באישה שהייתה לה סרולוגיה שלילית ל-HSV-1 ו-HSV-2 בתחילת הזיהום
- אירוע ראשון אבל לא ראשוני (non-primary first episode): זיהום עם נגיף הרפס מסוג אחד בנוכחות נוגדנים לנגיף ההרפס השני
- חוזר/שפעול (reactivation): לאישה סרולוגיה חיובית לאותו נגיף שזוהה מנגע במערכת הגניטלית
אבחון נוכחות נגיף ההרפס
- PCR: בדיקת HSV PCR היא שיטה רגישה יותר לאישור זיהום HSV בנגעים. אבחון מוקדם על ידי מבחני HSV PCR עשוי גם להפחית הדבקה בזיהום אסימפטומטי
- סרולוגיה של נגיף ה-HSV: הנוגדנים מתפתחים תוך 6–12 שבועות מזיהום ראשוני ונשארים למשך כל החיים. התגובה החיסונית היא ייחודית לסוג הנגיף, וניתן לזהות באופן נפרד נוגדנים חדשים לסוג אחד של נגיף בנוכחות נוגדנים קיימים לנגיף מהסוג השני (מבוסס על זיהוי גליקופרוטאין G ייחודי על מעטפת הנגיפים). נוכחות נוגדנים ל-HSV-2 מצביעה בדרך כלל על זיהום גניטלי, היות שברוב המקרים HSV-2 מועבר במגע מיני. קיימת בדיקה סרולוגית ל-HSV1/2-IgG, אשר מבדילה בהדבקה בין שני הנגיפים, ובדיקה סרולוגית בלתי ספציפית ל-HSV-IgM/IgG, אשר אינה מבדילה בין שני סוגי הנגיפים, אולם מסוגלת לזהות הדבקה לאחרונה באמצעות הדגמת IgM
המעבר לילוד
המעבר השכיח הוא בתהליך הלידה בשל הפרשת הנגיף בתעלת הלידה מנגע פעיל או מהפרשה אל-תסמינית של הנגיף (asymptomatic viral shedding). הדבקת הילוד לא תתרחש ברוב המקרים במהלך ההיריון אלא במעבר בתעלת הלידה. שער הכניסה של הנגיף לילוד הוא דרך העיניים, הנזופרינקס ודרך פגמים בשלמות העור/הסיכוי להפרשת הנגיף בלידה נמוך ודומה בנשים עם זיהום סימפטומטי ובאלו עם מחלה אסימפטומטית.
הסיכון להדבקת יילוד
- אצל נשים עם זיהום ראשוני בשליש השלישי להיריון מופרשת הכמות המרבית של הנגיף בתעלת הלידה, ואז הסיכון לזיהום הילוד מקסימלי ומגיע לכ-30–50 אחוזים
- בנשים עם זיהום ראשוני במחצית הראשונה של ההיריון, וכן במקרה של זיהום חוזר בהיריון, הסיכון נמוך יותר ועומד על כ-1 אחוז
- ב-non-primary first episode הסיכון להעברה מעט נמוך יותר מאשר בהדבקה ראשונית, אך גבוה יותר מאשר בזיהום חוזר
- בזיהום חוזר הסיכון למחלה בילוד עולה אם הנגיף הנוכח בתעלת הלידה הוא מסוג HSV1 (15 אחוזים עבור HSV1 מול 0.01 אחוזים עבור HSV2). לעומת זאת, המחלה בילוד שנחשף ל-HSV1 קלה יותר ומוגבלת לעור ולריריות, ומערבת פחות את מערכת העצבים המרכזית
לפיכך עמדת האיגוד
- סריקה שגרתית של אוכלוסיית הנשים בגיל הפוריות ובזמן היריון: בשל השכיחות הגבוהה של סרולוגיה חיובית לנגיף, ובשל חוסר המתאם בין סרולוגיה ומחלה חוזרת, אין מקום לבדיקת סקר שגרתית בהיריון באוכלוסיית הנשים הבריאות
- הטיפול בהרפס סימפלקס סימפטומטי במהלך ההיריון: מטרת הטיפול בהרפס גניטלי היא הקלה סימפטומטית, ריפוי מהיר יותר של נגעים וקיצור זמן הפרשת הנגיף. הטיפול הוא אמבולטורי ופומי, למעט במקרה של סיבוכים סיסטמיים (pneumonitis, HSV disseminated hepatitis, CNS involvement). יש להתחיל בטיפול מייד עם ביסוס החשד הקליני, ואין להמתין לתרביות, PCR או סרולוגיה. התכשירים האנטי-ויראליים (אציקלוויר, ואלאציקלוויר) עוברים שלייה. לא נמצאו להם השפעות טרטוגניות
| הוראה | אציקולוויר פומי | ואלאציקלוויר פומי |
| זיהום ראשוני או אירוע ראשון | 400 מיליגרם כל 8 שעות למשך 7–10 יום | 1 גרם כל 12 שעות למשך 7–10 יום |
| זיהום חוזר סימפטומטי | 400 מיליגרם כל 8 שעות למשך 5 ימים | 500 מיליגרם כל 12 שעות למשך 3 ימים או 1 גרם פעם ביום לחמישה ימים |
| זיהום חוזר בנשים עם HIV או מדוכאת חיסון | 400 מיליגרם כל 8
שעות למשך 5 עד 10 ימים |
1 גרם פעמיים ביום למשך 5–10 ימים |
| טיפול מדכא יומי | 400 מיליגרם כל 8 שעות משבוע 36 עד ללידה | 500 מיליגרם כל 12 שעות משבוע 36 עד ללידה |
שיטות למניעת הדבקה בילוד בנגיף ההרפס סימפלקס
- טיפול מדכא אנטי-ויראלי: אין מספיק מידע על מנת לבסס טענה שטיפול זה יפחית היארעות הדבקת הילוד. בנשים עם הרפס גניטלי סימפטומטי ראשוני או חוזר, התחלת טיפול משבוע 36 תוריד את הצורך ביילוד קיסרי, כי תפחית את הימצאות הנגעים ואת נוכחות הנגיף בתרביות PCR בזמן הלידה. לעומת זאת, אין מספיק מידע על מנת להמליץ באופן גורף על טיפול זה בהיריון בכל אישה אסימפטומטית עם נוגדנים ל-HSV2. ההחלטה על טיפול מונע תינתן בצורה פרטנית בכל מקרה לגופו
- בזמן לידה בנשים המדווחות על הרפס גניטלי בעבר או מחלה אצל בן הזוג יש:
- לשאול באופן מכוון לגבי סימפטומים גניטליים בהווה
- לבצע בדיקה גופנית של תעלת הלידה לזיהוי נגעים של הרפס. לציין שיש מגבלות לבדיקה פיזיקלית לניבוי חיובי או שלילי לנוכחות הנגיף בתעלת הלידה
- לבצע סריקה ל-HSV מהילוד, על פי ההנחיות הקליניות המוכרות
המלצה ללידה בניתוח קיסרי במקרים הבאים
התוויה יחסית:
- זיהום ראשוני או non-primary first episode בטרימסטר שלישי, ללא קשר לסימפטומים או סימנים בזמן התחלת הלידה
התוויה מוחלטת:
- זיהום פעיל, כולל פרודרום אופייני בזמן התחלת הלידה
- בכל מקרה של ירידת מים במועד בנוכחות מחלה גניטלית פעילה
- במקרה של ירידת מים מוקדמת (PPROM):
- יש לשקול את הסיכון לסיבוכי פגות אל מול הסיכון להעברה ורטיקלית של HSV ליילוד
- לא קיימת הוריה לגיל היריון מסוים טרם המועד בו מומלץ להתקדם ליילוד בירידת מים מוקדמת עם זיהום פעיל ב-HSV (נייר עמדה)
- בכל מקרה של מחלה אימהית או חשד לכך, יש ליידע את רופא הילודים
- לבצע סקר ל-HSV מהילוד, על פי ההנחיות הקליניות המוכרות
- פעולות פולשניות:
- בהיעדר נגעים פעילים אין מניעה מלידה מכשירנית (שולפן ריק או מלקחיים), ואין מניעה מניטור פנימי (scalp electrode)
לאחר הלידה
- בנשים עם מחלה פעילה אין למנוע מגע עם הילוד, אך יש להקפיד על רחיצת ידיים לפני כן ולהימנע ממגע עם רוק במקרה של HSV1 או מגע עם נגעים אימהיים כלשהם
- ההנקה מותרת (ללא קשר לטיפול באציקלוויר או אלציקלוויר)
בכל אישה עם הרפס גניטלי יש לבצע סקר למחלות המועברות במגע מיני לרבות HIV, עגבת, זיבה וכלמידיה.
מקורות
1. Brown, Z.A., et al., The acquisition of herpes simplex virus during pregnancy. NEngl J Med, 1997. 337)8(: p. 509-15.
2. Brown, Z.A., et al., Neonatal herpes simplex virus infection in relation to asymptomatic maternal infection at the time of labor. N Engl J Med, 1991. 324)18(: p. 1247-52. LEVEL I
3. Prober, C.G., et al., Use of routine viral cultures at delivery to identify neonates exposed to herpes simplex virus. N Engl J Med, 1988. 318)14(: p. 887-91. LEVEL Iia
4. Dan, M., et al., Prevalence and risk factors for herpes simplex virus type 2 infection among pregnant women in Israel. Sex Transm Dis, 2003. 30)11(: p. 835-8.LEVEL IIa
5. Brown, Z.A., et al., Genital herpes complicating pregnancy. Obstet Gynecol, 2005. 106)4(: p. 845-56. LEVEL I
6. Hollier, L.M. and G.D. Wendel, Third trimester antiviral prophylaxis for preventing maternal genital herpes simplex virus )HSV( recurrences and neonatal infection.Cochrane Database Syst Rev, 2008)1(: p. CD004946. LEVEL I
7. Gardella, C., et al., Poor correlation between genital lesions and detection of herpes simplex virus in women in labor. Obstet Gynecol, 2005. 106)2(: p. 268-74. LEVELII 8. Management of Herpes in Pregnancy, ACOG Practice Bulletin, Obstet gynecol 2007, 109: 1489-1498
זיהוי וטיפול בעגבת בהיריון
הקדמה
עגבת (סיפיליס) היא מחלה סיסטמית הנרכשת במגע מיני ונגרמת על ידי הספירוכטה Treponema pallidum.
על בסיס הממצאים הקליניים מחלקים את המחלה לארבעה שלבים:
עגבת ראשונית – מאופיינת בנוכחות כיב (chancre) באזור ההדבקה, והגדלה של בלוטות לימפה אזוריות. לעיתים קרובות שלב זה אינו מזוהה, מאחר שהכיב אינו כואב ועלול להיות נסתר (בתוך הנרתיק, הפה או הרקטום).
עגבת שניונית – מחלה סיסטמית הכוללת פריחה, נגעים עוריים, קונדילומטה לטה, לימפאדנופאתיה כללית, וכן זיהום במערכת העצבים המרכזית (מנינגיטיס, פגיעה בעצבים קרניאליים, שבץ, הפרעה בתפקוד מנטלי, איבוד שמיעה והפרעות בראייה).
עגבת לטנטית – זיהום ללא ממצאים קליניים או סימפטומים; האבחנה היא סרולוגית בלבד. עגבת לטנטית מוקדמת מוגדרת כאשר קיים תיעוד כי ההדבקה או השינוי הסרולוגי התרחש במהלך השנה האחרונה.
עגבת שלישונית (מאוחרת) – מצב נדיר. מחלה פרוגרסיבית הפוגעת במערכות גוף רבות, כולל נוירוסיפיליס, פגיעה קרדיאלית וגרנולומות אינפלמטוריות באיברים שונים כמו שלד ועור.
עגבת בהיריון
- הדבקה עוברית מתרחשת בדרך כלל מאוחר בהיריון, אולם הודגמה כבר בשבוע 8–9 להיריון
- הדבקה עוברית שכיחה יותר בעגבת אימהית מוקדמת, וכאשר כייל התבחין הלא-ספציפי (non-treponemal) גבוה. הדבקה זו עלולה להתבטא גם כ-congenital syphilis – מחלה הכרוכה במגוון תוצאים משמעותיים במוח, עיניים, אוזניים, עצמות ועוד
- הממצאים הסונוגרפיים והמומים העובריים האופייניים להדבקה בעגבת הינם, בין השאר: שליה מעובה, ריבוי מי שפיר, הידרופס, מיימת, בצקת תת-עורית, הפטומגליה. כמו כן ייתכנו שינויים בעצמות, כגון עיכוב בצמיחה, אי-סדירות והקשתה. בנוסף תיתכן אנמיה עוברית
- מתוארת עלייה בשיעור הפלות, לידה מוקדמת, ריבוי מי שפיר, הידרופס ו-IUFD
אבחנה של הדבקה בעגבת נעשית על ידי בדיקות סרולוגיות המתבצעות במעבדות מאושרות ועל פי הנחיות משרד הבריאות.
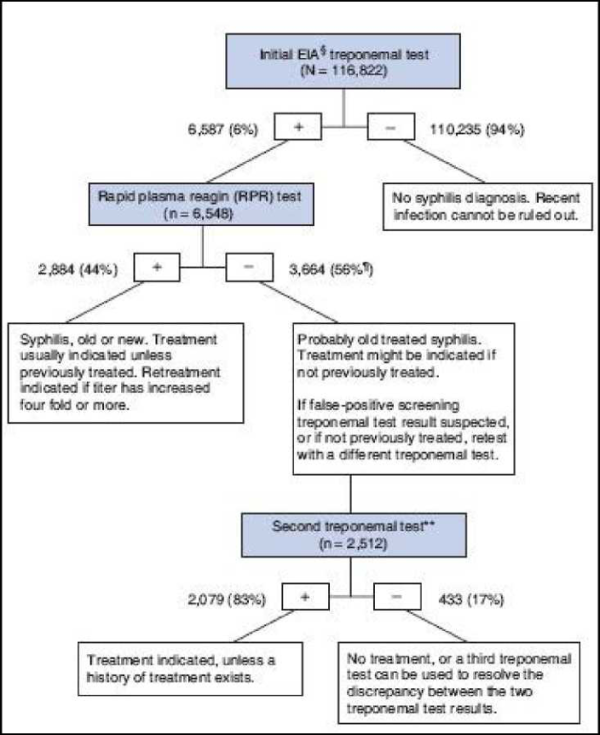
מעבדה הבודקת נסיוב של נבדקת חשודה בהידבקות בעגבת תבצע תבחיני סיקור בשתי שיטות:
- תבחין סרולוגי ספציפי (treponemal, כלומר ספציפי לאנטיגנים של חיידק העגבת):; A. TPHA – Treponema pallidum particle hemagglutination assay B. ELISA – Enzyme Linked Immunosorbent Assay תבחינים אלו הם ספציפיים יותר, כלומר לתוצאה חיובית יש positive predictive value גבוה, במיוחד אם שני תבחינים ספציפיים הם חיוביים. לאחר הדבקה בעגבת תבחינים אלו נשארים חיוביים לתמיד, על פי רוב, ולכן אינם מסוגלים להבדיל בין מחלה פעילה, מחלת עבר או מחלה שטופלה, ואינם יכולים לשמש למעקב אחר הצלחת הטיפול. במעבדות רבות קיים שימוש בתבחין treponemal chemiluminescent נוסף (לדוגמה: chemiluminescent immunoassay, CMIA/CIA). תבחין זה פשוט לביצוע ורגיש מאוד, ולכן משמש כבדיקת סקר, אולם הוא בעל ספציפיות מעט נמוכה יותר. אי לכך, תוצאה חיובית בבדיקת סקר כגון CMIA מחייבת אשרור בבדיקות ספציפיות נוספות. עד לקבלת תוצאותיהן ניתן להתייחס לתוצאות בדיקת הסקר על פי רמת החשד הקלינית והאפידמיולוגית
- תבחין סרולוגי לא-ספציפי וכמותי (non-treponemal, תבחין שעושה שימוש באנטיגנים שאינם של חיידק העגבת). כייל הנוגדנים של תבחינים אלה נמצא בקורלציה לפעילות המחלה. הכייל עולה לאחר ההדבקה ויורד לאחר טיפול, או עם הזמן כאשר המחלה עוברת למצב לטנטי: A. VDRL (Venereal Disease Research Laboratory) B. RPR (Rapid Plasma Reagin)
כאשר התגובה חיובית באחת השיטות, חובת המעבדה לשלוח את הדגימה לאימות במרכז הארצי לעגבת באבו כביר.
| פרשנות | תבחין לא ספציפי
(VDRL, RPR) |
תבחין ספציפי
TPHA, (ELISA) |
| שלילי לעגבת | שלילי | שלילי |
| חיובי לעגבת פעילה. מידת הפעילות מבוטאת בכייל התבחין הלא ספציפי | חיובי | חיובי |
| עגבת בעבר או עגבת לטנטית לעיתים | שלילי או חיובי בכייל נמוך | חיובי |
| תוצאה חיובית-כוזבת לעגבת, לעיתים נדירות אבחנה מאוד מוקדמת | חיובי | שלילי |
לפיכך המלצות האיגוד הישראלי למיילדות וגינקולוגיה הן
המלצות לאבחון
- יש לבצע לכל הנשים ההרות בדיקת סקר נוגדנים לעגבת באחת השיטות בתחילת ההיריון
- בנשים הנמצאות בסיכון גבוה (לדוגמה: נשים שמקיימות יחסי מין תמורת תשלום, נשים עם פרטנרים מיניים מרובים במהלך ההיריון, או נשים שבן זוגן המיני מקיים יחסי מין עם פרטנריות/ים נוספים במהלך ההיריון, או נשים שמשתמשות בסמים), מומלץ לבצע בדיקת סקר חוזרת בשבוע 28–32 ושוב בלידה
- בנשים שלא נבדקו בבדיקת סקר במהלך ההיריון, יש לבצע בדיקת סקר בלידה
- בנשים שקיים תיעוד ברור על הדבקה בעבר שטופלה כיאות, יש לצפות כי התבחינים הספציפיים יהיו חיוביים, אולם התבחינים הבלתי-ספציפיים יהיו שליליים או חיוביים בכייל נמוך וללא עלייה יחסית לבדיקות קודמות. במקרים אלו ניתן להתייחס כאל "צלקת סרולוגית"
- כאשר תוצאת המבחן הלא-ספציפי שלילית אין צורך לחזור על טיפול. כאשר תוצאת המבחן הלא-ספציפי חיובית בכייל נמוך או גבולית, יש להתייעץ עם מומחה למחלות זיהומיות ולוודא כי לא מדובר בהדבקה חוזרת
- תבחין לא-ספציפי יכול להיות חיובי כוזב במצבים קליניים שונים, כגון מחלות אוטואימוניות, גיל מבוגר ושימוש בסמים. קבלת תשובת תבחין ספציפי שלילי, המאומת בשתי בדיקות שונות, מעידה על היעדר הידבקות בעגבת, גם אם בבדיקות נמצא תבחין לא-ספציפי חיובי
המלצות לטיפול
- נשים הרות צריכות לקבל טיפול אנטיביוטי בהתאם לשלב המחלה בו הן נמצאות. הטיפול האנטיביוטי בפניצילין יעיל במניעה של העברת הזיהום לעובר ובטיפול בעובר. לאחר טיפול בעגבת ראשונית ושניונית יש לצפות כי בדיקות סרולוגיות חוזרות כעבור 3–6 חודשים ידגימו ירידה (פי 4) בכייל הנוגדנים של התבחין הלא-ספציפי. יש להשתמש באותו תבחין (VDRL או RPR) לצורך מעקב אחר כייל הנוגדנים. היעדר ירידה מספקת ברמת הנוגדנים עשוי להעיד על כישלון בטיפול התרופתי או הידבקות חוזרת
- כאשר אבחנה של עגבת נעשתה החל משבוע 18 להיריון, מומלץ לבצע בירור להידבקות עוברית ולהפנות למכון אולטרה-סאונד לאבחון מומים אופייניים, לשלילת הידרופס או הפטוספלנומגליה, ולבצע מעקב במרפאת היריון בסיכון, משולבת עם מומחה מחלות זיהומיות
- הטיפול בעגבת כרוך בסיכון לתגובת Jarisch-Herxheimer, המופיעה לרוב בעקבות טיפול בעגבת ראשונית או שניונית. מצב זה עלול להתבטא בחום גבוה, כאבי ראש ושרירים, צירים מוקדמים, תוך 24 שעות ממתן הטיפול. יש ליידע את המטופלת ולהפנותה לבית חולים בכל מקרה של חום וצירים מוקדמים, או הפחתה בתנועות העובר, כיוון שקיים סיכון ללידה מוקדמת ומצוקה עוברית. לנשים הרות המאובחנות עם עגבת יש להמליץ על בדיקת נשאות ל-HIV, הפטיטיס B, הפטיטיס C ובדיקת שתן/צוואר רחם לזיבה (גונוריאה) וכלמידיה. יש להפנות את בני הזוג המיניים לטיפול בעגבת. על פי רוב יש לטפל בבני הזוג גם אם תוצאות בדיקות סרולוגיות שלהם שליליות (מחשש להדבקה טרייה שטרם התבטאה סרולוגית)
- עגבת היא מחלה מחויבת דיווח על פי פקודת בריאות העם. יש להעביר דיווח שמי ללשכת הבריאות המחוזית ולציין כי מדובר באישה הרה
- במועד לידה יש ליידע את רופאי היילודים לגבי הדבקה בעגבת בהיריון
פרוטוקול טיפול בעגבת
טיפול אנטיביוטי בעגבת בהיריון הוא עם פניצילין בלבד. אין טיפול אחר שהוכחה יעילותו בהיריון.
- עגבת ראשונית/שניונית, עגבת לטנטית מוקדמת: Single dose of IM Benzathine penicillin G 2.4 MU – יש הממליצים בנשים הרות על מתן מנה נוספת שבוע לאחר המנה הראשונה
- עגבת לטנטית מאוחרת: IM Benzathine penicillin G 2.4 MU אחת לשבוע למשך 3 שבועות. חשוב לשמור על רצף מתן הזריקות. חולה עם עגבת לטנטית מאוחרת, או חולה עם עגבת המלווה בסימפטומים וסימנים לפגיעה נוירולוגית (הפרעה בתפקוד הקוגניטיבי, חסרים מוטוריים או סנסוריים, מנינגיטיס, חרשות) או פגיעה אופטלמית (iritis, uveitis), או מי שלא הגיב כצפוי לטיפול בירידת כייל הנוגדנים של התבחין הלא-ספציפי, צריכים לעבור הערכה נוירולוגית שעשויה לכלול בדיקת נוזל שדרה (Lumbar puncture), בהתייעצות עם מומחית למחלות זיהומיות
טיפול בנוירוסיפיליס
Aqueous crystalline penicillin G 18–24 MU/day, administered as 3–4 MU IV every 4h or continuous infusion, for 10–14 days.
נשים הרות עם עגבת המדווחות על "רגישות לפניצילין" – יש למצות כל אפשרות למתן טיפול בפניצילין. ברוב הנשים הללו ניתן להשתמש בפניצילין לאחר קבלת אנמנזה מפורטת על האלרגיה, ובהתייעצות עם מומחה באלרגיה או במחלות זיהומיות. בשאר הנשים יש לבצע דסנסיטיזציה ובהמשך טיפול בפניצילין.
שימוש בטטרציקלין אינו מומלץ בנשים הרות. שימוש באריתרומיצין או אזיתרומיצין לא הוכח כמרפא זיהום אימהי או כיעיל בטיפול בעובר. יש הממליצים שימוש בצפטריאקסון (Ceftriaxone) (לצורך טיפול בזיהום אימהי או מניעה של זיהום קונגניטלי), אולם טיפול זה לא הוכח.
ביבליוגרפיה
- השנתון הסטטיסטי לישראל, למ"ס, מאגר הנתונים OECD לשנת 2010, למ"ס
- נוהל משרד הבריאות: חוזר המחלקה למעבדות 2008/02
- מכתב משרד הבריאות, שירותי בריאות הציבור, המחלקה למעבדות מיום 30.7.12 בנושא: "שינוי שיטת הבדיקה המשמשת את המעבדה המרכזית לעגבת" וכן מכתב משרד הבריאות, שירותי בריאות הציבור, המחלקה למעבדות מיום 08.01.13 בנושא: "תבחינים סרולוגיים לאבחון עגבת ושליחת דגימות למרכז הארצי"
- CDC sexually transmitted disease infections guidelines. MMWR Recomm Rep 2021;704 https://www.cdc.gov/std/treatment-guidelines/syphilis-pregnancy.htm
- USPSTF Recommendation: Screening for Syphilis Infection in Pregnant Women JAMA. 2018;320)9(:911-917. doi:10.1001/jama.2018.117
- UK national guidelines on the management of syphilis 2015. Int J STD AIDS. 2016 May;27)6(:421-46
נגיף ה-PARVO בהיריון
Parvo B19 הוא נגיף בעל שרשרת DNA בודדת ממשפחת Parvoviridae. במבוגרים ההדבקה היא בדרך כלל אסימפטומטית, ובילדים המחלה קלה ומוגבלת וידועה גם כ"המחלה החמישית". לאחר הדבקה בנגיף רמת IgM מגיעה לשיא תוך 28 ימים מהחשיפה, ויורדת באופן מהיר לרמות אפסיות תוך 2–3 חודשים. נוגדני ה-IgG מופיעים עם התחלת הפריחה האופיינית לנגיף בשבוע השלישי לתחלואה. הופעת הפריחה מסמלת למעשה את היעלמות הנגיף מהדם ואת הפסקת הפרשתו למערכת הנשימה – כלומר החולה אינו מדבק יותר. הנוגדנים מסוג IgG נשארים בדם שנים ארוכות ומקנים, ככל הנראה, הגנה מלאה מפני זיהומים חוזרים.
שער הכניסה של הנגיף אל תאי-האב האדומים והטסיות הוא קולטן המכונה גלובוזיד (Globoside), הידוע יותר כקבוצת הדם מסוג P. קבוצת האנשים שחסרה את הקולטן לעולם לא תידבק בווירוס ותהיה חסינה כנגדו.
נשים בהיריון הנושאות את הקולטן תהיינה חשופות לזיהום. הנגיף עלול לעבור את השליה ולגרום לפגיעה עוברית, בעיקר בייצור במח העצם ובכבד העוברי שהוא אתר המטופואזיס עיקרי. כתוצאה מכך עלולה להיגרם השפעה ציטופטית בעובר בצורת המוליזה וטרומבוציטופניה. נוכחות הקולטן בתאים עובריים נוספים (תאי אנדותל, סינוביום, מיוציטים וטרופובלסט) תחמיר את הנזק הצפוי. הסתמנות המחלה העוברית היא בצורת aplastic crisis.
הדבקה ורטיקלית מתרחשת רק ב-30 אחוזים ממקרי ההידבקות האימהית. למעט כך הווירוס איננו טרטוגני לעובר, אולם אם נלווית אנמיה קשה והידרופס תיתכן סקוולה נוירולוגית בשל כך, ולכן יש לשקול הדמיה מוחית בעוברים אלו. כמו כן תיתכן מיוקרדיטיס העלולה להוביל לקרדיומיופתיה בהמשך.
בעת הדבקה עוברית רק ב-9 אחוזים מהם תתבטא פגיעה כלשהי. הסיכון לעובר הוא מקסימלי כאשר ההדבקה מתרחשת בשליש השני. למרות זאת, הסיכון הכולל להתפתחות הידרופס פטליס על רקע זיהום בנגיף הוא נמוך ביותר ועומד על 2 ל-10,000 הריונות. חציון ההיארעות של הידרופס קורה 3 שבועות לאחר ההדבקה, ו-95 אחוזים מהמקרים מתרחשים עד 8 שבועות מההדבקה. ב-95 אחוזים בעוברים הידרופיים יש טרומבוציטופניה נלווית, וחמורה ב-46 אחוזים מהמקרים, ויש לקחת זאת בחשבון בעת ביצוע עירוי תוך-רחמי.
בעת חשד להדבקה בנגיף, לפי סיפור קליני או משפחתי או בעת הופעת סימני הידרופס בעובר, יש לבצע בירור סרולוגי. המחלה מאובחנת על ידי נוכחות נוגדנים ספציפיים IgM, IgG בדם האם, או זיהוי דנ״א ויראלי בדם האימהי, העוברי או במי השפיר. אולם לא קיימת אינדיקציה לדיקור מי שפיר לצורך אבחנה, ובירור זה יבוצע רק במקרה של צורך בעירוי תוך-רחמי.
יש להפנות לבירור ומעקב על מנת לשלול סימני אנמיה עוברית החל מאבחון ההדבקה, ואחת לשבועיים ועד 12 שבועות לאחר ההדבקה. יש לשלול אנמיה באמצעות דופלר של MCA (Middle Cerebral Artery), וכן סימנים של הידרופס וקרדיומגליה, ולשקול עירוי תוך-רחמי במקרים בהם אובחנה אנמיה עוברית משמעותית.
יש להשלים בדיקת אקו לב עובר.
מניעה ראשונית אינה אפשרית (אין חיסון).
מניעה שניונית היא זיהוי מוקדם של הדבקה בנשים ללא נוגדנים לווירוס. מקור הזיהום האימהי העיקרי הוא חשיפה לילד חולה. על פי כן עמדת האיגוד היא כי אין המלצה לסקר כללי לאוכלוסיית נשים הרות, אלא במקרים של חשד קליני גבוה להדבקה, למשל בעקבות חשיפה.
ביבליוגרפיה
- Van Gessel P, Gaytant MA, Vossen A.C.T.M, Galama K.M.D,Ursem N.T.C., Steegers E.A.P., Wildschut. H.I.J. Incidence of parvovirus B19 infection among an unselected population of pregnant women in the Netherlands:A prospective study . European Journal of Obstet &Gynecology and Reproductive Biology 128:46-9, 2006 ) Level III(
- Dijkmans AC, de Jong EP, Dijkmans BAC, Lopiore E, Vossen A, Walther FJ, Oepkes D. Parvovirus B19 in preganncy: prenatal diagnosis and management of fetal complications . Review . Current Opinion 24)2(: 95-100, 2012) Level III(
- ISUOG
טוקסופלסמוזיס בהריון
מבוא
טוקסופלזמוזיס הוא תהליך זיהומי הנגרם על ידי טפיל תוך-תאי מסוג פרוטוזואה בשם Toxoplasma gondii, שהמאכסן הטבעי שלו הוא ממשפחת החתולים. כדי להוות גורם מזהם בבני אדם, הטפיל חייב להשלים את מחזור החיים שלו לציסטה (oocysts sporulated) בחיה נגועה (בדרך כלל חתול), שהיא הצורה המידבקת.
זיהום ראשוני הוא בדרך כלל אסימפטומטי בילדים ובמבוגרים בריאים עם מערכת חיסונית תקינה, והללו אף אינם בסיכון לסיבוכים ארוכי טווח. בהדבקה ראשונית החיסון הנרכש נשמר לאורך כל החיים, ולכן הדבקה חוזרת וריאקטיבציה היא ללא משמעות קלינית.
דרכי ההדבקה הם באמצעות מים מזוהמים או מזון מזוהם (מוצרי בשר או ירקות ופירות שהיו במגע עם צואת חיה נגועה או קרקע מזוהמת), או אכילת בשר שלא בושל דיו מחיה נגועה, או בצורה נדירה על ידי שאיפת הציסטות המכילות את הטפיל מחיה נגועה. תיתכן גם הדבקה מבני אדם דרך איברים שהושתלו, או על ידי הדבקה אנכית מאם לעובר. הטפיל מסוגל לעבור דרך השליה ובכך מעלה את הסיכון לסיבוכי היריון.
רוב הנשים שנדבקו יהיו אסימפטומטיות בהיריון, וכך גם הילודים, אצלם לא יופיעו תסמינים מיד לאחר הלידה אלא במהלך חייהם. שיעור ההדבקה האנכית הכללית לאחר זיהום ראשוני הוא כ-40 אחוזים, עם שכיחות משתנה במהלך ההיריון: שיעור ההדבקה נמוך בשליש הראשון (15 אחוזים), אך כרוך ביותר פגיעה בעובר, וגבוה בשליש השלישי (60 אחוזים), אך כרוך בפגיעה קטנה יותר בעובר.
הדבקת העובר יכולה להתבטא בהפלה או בפגיעה בכבד ובמערכת העצבים המרכזית של העובר, במוח ובעיניים. פגיעה שכזאת עלולה להוביל למות העובר ברחם או לתחלואה משמעותית, המתבטאת במהלך הילדות כפיגור שכלי, התכווצויות, חירשות ועיוורון.
שיעור הנשאות לטוקסופלזמה בישראל הוא בין 13–40 אחוזים בטווח גילאים בין 19 ל-45, ועולה עם הגיל, זאת בהתבסס על תבחין Feldman-Sabin. בישראל, שכיחות הזיהום הראשוני המשוער בהיריון מוערכת בכ-4.1–6 אחוזים. מהנתונים של המעבדה המרכזית של משרד הבריאות קיים שיעור נמוך ביותר בארץ של עדות להדבקה במי שפיר באישה שעברה הדבקה ראשונית בהיריון.
לפיכך, עמדת האיגוד היא
בהתבסס על מחקרים שבוצעו במדינות אחרות עם שכיחות זיהום נמוכה כמו בישראל נמצא שאין מקום לסקר האוכלוסייה הכללית של נשים בגיל הפיריון או ילודים, ועל כן אין המלצה לביצוע בדיקת סקר לטוקסופלזמוזיס בישראל. יש לבצע בדיקה סרולוגית לטפיל על בסיס חשד קליני בלבד.
היות שרוב הנשים הן שליליות לנוגדני טוקסופלזמה הגישה היעילה ביותר למניעת מחלה מולדת היא מניעה ראשונית. המניעה הראשונית כוללת שמירה על כללי היגיינה: רחיצת ידיים לאחר מגע עם חיות או עם צואתם והימנעות מאכילת בשר נא וירקות ופירות לא שטופים. באזורים אנדמיים מומלץ בישול המזון עד לפחות 66 מעלות צלזיוס או הקפאה למשך 24 שעות לפחות.
אבחנה
האבחון הוא סרולוגי: רמת נוגדני ה-IgG יותר ספציפית לעומת בדיקת ה-IgM לקביעת עיתוי הזיהום, וזאת כיוון שרמת ה-IgM היא בעלת ערך מוגבל הן מבחינת הספציפיות הנמוכה והן מבחינת הימצאות ארוכת טווח של הנוגדן בדם (עד 10–13 חודשים). אין נתונים לגבי משמעות העלייה בכייל הנוגדנים לצורך קביעת עיתוי הזיהום.
כדי לאמת הדבקה ראשונית יש להתבסס על תבחין Feldman-Sabin הספציפי לטוקסופלזמוזיס. אם הבדיקה חיובית יש לשלוח לאימות למעבדה המרכזית בנס-ציונה. עלייה פי 4 או יותר בכייל הנוגדנים, בשתי בדיקות חוזרות, או ערך הגבוה מ-250 יחידות בינלאומיות מחשידים להידבקות במחלה, ואז יש להמליץ על טיפול מונע לאם.
אם יש חשד להדבקה בהיריון, לפי נוכחות IgM חיובי בנוכחות IgG שלילי או עדות ל-seroconversion, יש להתחיל טיפול עד לקבלת תשובות VIDAS הספציפי לטוקסופלזמוזיס.
ניתן לבצע זיהוי ישיר של הטפיל במקרים ייחודיים על ידי ביצוע דיקור מי שפיר לזיהוי DNA של הטפיל על ידי real-time PCR במי השפיר. הבדיקות הסרולוגיות הספציפיות ובדיקת מי שפיר מתבצעות במעבדה המרכזית של משרד הבריאות שבאבו כביר.
האינדיקציה לביצוע דיקור מי שפיר קיימת רק כאשר יש עדות ברורה למחלה ראשונית אימהית או ממצאים אופייניים בעל-קול לעובר. את דיקור מי השפיר יש לבצע לפחות 4 שבועות מההדבקה ולאחר שבוע 18 להיריון. PCR שלילי במי שפיר אינו שולל לחלוטין הדבקה עוברית, ועל כן מומלץ להמשיך בכל מקרה טיפול אנטיביוטי – בספירמיצין או טיפול משולש כפי שמפורט בהמשך – ומעקב סונוגרפי אחר סימני הדבקה.
טיפול
קיימות 2 גישות מקובלות:
- טיפול בספירמיצין/רובמיצין (Rovamycine 1.5 million IU), לאם בהיריון – 2–3 tabs ×2/day – מוריד את שיעור ההדבקה העוברית. יש להתחיל את הטיפול מיד עם אבחנת ההדבקה האימהית ולהמשיך לאורך כל ההיריון. אם יש הוכחה להדבקה עוברית, טיפול משולב בפירימטמין (Pyrimethamine) במינון 50 מיליגרם פעם ביום, וסולפדיאזין (Sulfadiazine) במינון 1 גרם 3 פעמים ביום, מוריד את שיעור ההדבקה ואת חומרת התחלואה. יש להוסיף לטיפול חומצה פולינית 50 מיליגרם לשבוע. לציין כי פירימטמין היא תרופה עם סיכוי לטרטוגניות ואינה מומלצת לפני שבוע 14 להיריון
- גישה נוספת היא טיפול משולש מיד עם אבחון טוקסופלזמה ועד לדיקור, המוריד שיעורי הדבקה מ-30 אחוזים ל-17 אחוזים. אם הדיקור שלילי ניתן להמשיך ספירמיצין בלבד. במצב זה, אם לא מבוצע דיקור, ניתן לשקול להמשיך טיפול משולש
מעקב אחר העובר במקרי הדבקה עוברית
- מעקב אחת לחודש לסקירה מכוונת לרבות מוח, עיניים ומעקב גדילה
- יש לשקול MRI (Magnetic Resonance Imaging) מוח עובר
- יש ליידע את המטופלות כי גם במקרה של מעקב תקין ב-30 אחוזים ייתכן סקוולה ארוכת טווח לעובר בייחוד כוריורטיניטיס העלולה לפגוע בראייה
מקורות
- Dan Miron, Raul Raz, Antony Luder. Congenital Toxoplasmosis in Israel: To Screen or Not to Screen. IMAJ 4:119-122, 2002 )Level III(
- Wallon M, Frank J, THulliez P, Huissoud C, Peyron F, Garcia-Meric P, Kieffer F. Accuracy of Real time polymerase chain reaction for Toxoplasma Gondii in amniotic fluid. Obstet Gynecol 115)4(: 727-33, 2010. )Level III(
- Roman E, Zamir CS, Riklis I, Ben-David H: Congenital toxoplasmosis-prenatal aspects of toxoplasma gondii infection. Reprod Toxicol 21:458-72, 2006 )Level III(
- ISUOG Practice Guidelines: role of ultrasound in congenital infection Ultrasound Obstet Gynecol 2020
נגיף הואריצלה בהיריון
מבוא
נגיף הוריצלה זוסטר ממשפחת ההרפס הוא הגורם למחלת אבעבועות רוח (וריצלה) ולהרפס זוסטר (shingles). ההידבקות היא טיפתית ובמגע ישיר עם נוזלי השלפוחית. זיהום ראשוני מתאפיין בחום, חולשה ופריחה מגרדת המתפתחת לפריחה מקולופפולרית שהופכת לשלפוחיתית, מלווה בתחושת עקצוץ, כאשר בהמשך מופיעים גלדים לפני הריפוי. תקופת הדגירה היא 1–3 שבועות. המחלה מידבקת מאוד 48 שעות לפני הופעת הפריחה, וממשיכה להיות מידבקת עד שכל הנגעים הגלידו. המחלה שכיחה בילדים, כך שמרבית האוכלוסייה היא בעלת נוגדני IgG לנגיף הווריצלה.
הידבקות ראשונית בווריצלה בהיריון עלולה לגרום לתחלואה ותמותה אימהית, וכרוכה בשיעור מוגבר של פנאומוניה, הפטיטיס ואנצפליטיס. וריצלה מולדת יכולה להתפתח אם מופיע זיהום ראשוני במחצית הראשונה של ההיריון, אך הסיכון להידבקות העובר נמוך מ-2 אחוזים וקטן עוד יותר בהמשך ההיריון. הפגיעה האופיינית בווריצלה מולדת כוללת: מומי עיניים (מיקרואופטלמיה, כוריורטיניטיס, קטרקט), היפופלזיה של הגפיים והפרעות נוירולוגיות (מיקרוצפליה, אטרופיה קורטיקלית, פיגור שכלי).
הופעה של אבעבועות רוח סביב הלידה או מייד לאחר הלידה כרוכה בסיכון מוגבר להתפתחות מחלה קשה, הכרוכה בסיכון לתחלואה ותמותה עקב היעדר חיסון מספק בילוד. המעבר לילוד ייתכן דרך השליה, זיהום עולה מהנרתיק או במגע ישיר עם שלפוחיות לאחר הלידה. בעבר דווח על תמותה של 30 אחוזים, אולם כיום, עם השיפור בטיפול, שיעור התמותה כ-7 אחוזים.
לפיכך המלצות האיגוד הן
מניעה
- בחשד לחשיפה לווריצלה יש לברר את מצבה החיסוני של האם לפי אנמנזה ו/או בדיקת דם לסרולוגיה
- בחשד לחשיפה לווריצלה, אם לא ידוע המצב החיסוני, יש לעשות מאמץ לבצע בדיקת נוגדנים לווריצלה בכדי לראות האם יש צורך במתן טיפול מונע. אם לא ניתן לקבל מידע לגבי רמת הנוגדנים תוך 96 שעות מההדבקה, מומלץ לטפל ב-VZIG (Varicella Zoster Immunoglobulin). ניתן לטפל עד 10 ימים מהחשיפה
- בנשים בגיל הפיריון לא מחוסנות וללא נוגדנים יש לשקול לחסן לווריצלה בין ההיריונות. החיסון אסור בהיריון מאחר שהוא חיסון חי מוחלש
הידבקות בווריצלה בהיריון
- יש ליידע את ההרה כי המחלה מידבקת ועלולה לגרום לסיבוכים עובריים ואימהיים (דלקת ריאות, אנצפליטיס ובמקרים נדירים מוות)
- ההחלטה לגבי אופן הטיפול התרופתי באציקלוויר – פומי או תוך-ורידי – או ההחלטה על מקום הטיפול בהרה, בביתה או בבית חולים (בבידוד), תיעשה בהתאם למצבה
- אם ההידבקות במחלה היא במחצית הראשונה של ההיריון, יש ליידע שהסיכון לפתח וריצלה מולדת הוא נמוך ביותר. מומלץ להפנות לבדיקות הדמיה מכוונות של העובר לפחות לאחר 5 שבועות מההידבקות
- דיקור מי שפיר לזיהוי הנגיף אינו מומלץ
- יש לדווח לרופא ילודים ומומחה למחלות זיהומיות בכל מקרה בו הרה מפתחת אבעבועות רוח בטווח של 7 ימים סביב הלידה
- יש להימנע מיילוד אלקטיבי (במידת האפשר) לפרק זמן של 7 ימים לאחר הופעת הפריחה העורית
- הופעה של הרפס זוסטר בהיריון או סביב הלידה אינה מסכנת את העובר המוגן על ידי נוגדנים אימהיים
מקורות
- Royal College of Obstetricians and Gynaecologists Green-top Guideline No. 13 Chickenpox in pregnancy
- Management of Varicella Infection in pregnancy SOGC Clinical Practice Guideline, J. Obstet. Gynecol. Can 2018
- Varicella Vaccine- Q As about Pregnancy: http//:www.cdc/gov/vaccines/vpd-vac/varicella


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק