סוכרת מסוג 1 - Type 1 diabetes
הופניתם מהדף Type 1 Diabetes לדף הנוכחי.
| סוכרת מסוג 1 | ||
|---|---|---|
| Type 1 Diabetes | ||

| ||
| שמות נוספים | סוכרת נעורים | |
| ICD-10 | Chapter E 10. | |
| ICD-9 | 250.01 | |
| MeSH | D003922 | |
| יוצר הערך | פרופ' משה פיליפ וד"ר רויטל נימרי
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סוכרת מסוג 1
שמות שונים שימשו בעבר לתיאור סוכרת המתרחשת בגיל הילדות וההתבגרות וביניהם סוכרת נעורים, סוכרת התלויה באינסולין וסוכרת קטוטית. החל ב-1998 (על פי המלצות WHO - World Health Organization) מקובל לסווג את מחלת הסוכרת על פי התהליך הגורם למחלה, וסוכרת זו זכתה למינוח - סוכרת מסוג 1.
ערך מורחב – סוכרת מסוג 1 בגיל הרך - Toddlers Diabetes
סוכרת מסוג 1 שכיחה ביותר בגיל הילדות והנעורים. מחלה כרונית וחסרת ריפוי זו מתפתחת בדרך כלל אצל אנשים שהרקע הגנטי שלהם מגביר את סיכונם ללקות בה, לאחר מפגש עם גורם סביבתי הגורם להפעלת מערכת החיסון בגופם, שתוקפת את התאים מייצרי האינסולין שבלבלב והורסת אותם. הרס התאים מוביל לחסר של אינסולין ולמצב חירום מטבולי, הדורש אבחון וטיפול דחוף. רוב חולי הסוכרת מסוג 1 מאופיינים, על כן, בחוסר אינסולין ובתלות מוחלטת בטיפול בו.
הטיפול בחולה נתפר אישית ומורכב ממתן אינסולין, תזונה נכונה, סדר יום מתאים ופעילות גופנית.
הטיפול דורש צוות רב-מקצועי, הכולל תמיכה פסיכולוגית. את הטיפול, במיוחד בילדים ובמתבגרים, יש לבצע במרכזים רפואיים המתמחים בכך.
העשורים הקרובים הם עידן התקווה לריפוי הסוכרת. הכנסת דרכי הניטור החדשות והחיישנים ושילובם עם משאבת אינסולין, יהוו בעתיד חלק סטנדרטי מהטיפול בסוכרת, ויש לשער כי יגרמו למהפך בחיי חולי הסוכרת. הריפוי והמניעה אמנם נמצאים במרחק של שנים אבל הצעדים הראשונים כבר כאן.
אפידמיולוגיה
סוכרת מסוג 1 היא אחת המחלות הכרוניות השכיחות בקרב ילדים ומתבגרים, ומהווה 10 אחוזים מכלל מקרי הסוכרת. היא יכולה להופיע בכל גיל, אך רוב מקרי הסוכרת בגיל הילדות והנעורים הם של סוכרת מסוג 1. ההיארעות (מספר מקרים חדשים בשנה) של סוכרת מסוג 1 איננה אחידה על פני הגלובוס, ומשתנה במקומות שונים בעולם. במדינות במזרח, כגון סין ויפן, ההיארעות נמוכה (0.57 מקרים ל-100,000 לשנה), ואילו בארצות כמו פינלנד וסרדיניה השכיחות גבוהה מזו פי 100 (49 מקרים ל-100,000 לשנה).[1] היארעות מחלת הסוכרת במדינת ישראל היא כ-12 מקרים חדשים בשנה לכל 100,000 ילדים ומתבגרים מתחת לגיל 18. ההיארעות שונה בקרב העדות השונות: היא גבוהה ביותר בקרב יהודים ממוצא תימני ואתיופי ונמוכה ביותר בקרב האוכלוסייה הערבית בישראל.
בניגוד למחלות אוטו-אימוניות אחרות, השכיחות של סוכרת מסוג 1 שווה בין המינים, ויש נטייה קלה לשכיחות גבוהה יותר בקרב בנים. היארעות המחלה נמצאה גבוהה יותר בחודשי שנה מסוימים (סתיו וחורף), וישנן אף עדויות לקשר בין חודש הלידה לשכיחות המחלה.
שתי תקופות גיל בעלות שכיחות גבוהה יותר יחסית של סוכרת מסוג 1. הראשונה, גיל הילדות המוקדמת (חמש-שבע שנים), התואם את זמן החשיפה והתחלואה המוגברת של מחלות זיהומיות נגיפיות. השנייה, בעלת שכיחות גבוהה יותר בגיל ההתבגרות המינית, כנראה על רקע העלייה בעמידות לאינסולין הקשורה לתקופה זו של החיים.
בעשור האחרון של המאה העשרים נראתה עלייה בהיארעות המחלה בכל העולם בשיעור של 5-2 אחוזים לשנה. העלייה בשכיחות בולטת ביותר בקרב קבוצת הגיל הצעירה מתחת גיל חמש שנים. נתונים אלה יכולים לרמוז על קיום גורם סביבתי חדש, או לשקף את העלייה במשקל של האוכלוסייה, כגורמים התורמים לפיתוח הסוכרת.
אטיולוגיה
סוכרת מסוג 1 נגרמת עקב התקפה אוטו-אימונית של תאי ביתא בלבלב, המתווכת על ידי תאי T של המערכת החיסונית. עדות לחשיבות של תאי T כגורם המרכזי בפתוגנזה של מחלת הסוכרת נתמכת גם על ידי תיאור מקרה של ילד החולה במחלה אימונית – א-גאמא-גלובולינמיה (חוסר יכולת מולדת לפתח נוגדנים), שחלה בסוכרת מסוג 1. הפעלה שגויה של המערכת האימונית כלפי מרכיבים עצמיים זו גורמת לתהליך דלקתי באיי הלבלב, וגם לתגובה של יצירת נוגדנים על ידי תאי B של המערכת האימונית כנגד מרכיבים של תאי ביתא בלבלב. נוגדנים אלה ניתנים לזיהוי בסרום: נוגדנים כנגד איי הלבלב (ICA), נוגדנים כנגד אינסולין (IAA), נוגדנים כנגד החלבון Glutamic Acid Decarboxylase (GAD) ונוגדנים כנגד החלבון tyrosine phosphatase IA2 (IA-2AA). בנוכחות נוגדנים אלה משתמשים בסרום לזיהוי של התהליך האוטו-אימוני, לעתים אף שנים לפני ההופעה הקלינית של המחלה. נוכחות שילובים שונים של נוגדנים אלה בסרום, משקפת שלבים שונים בהרס הלבלב ותלויה בגיל החולה.
עדות נוספת לתהליך אוטו-אימוני כגורם למחלת הסוכרת מסוג 1 משתקף מהנטייה של חולים אלה לפתח מחלות אוטו-אימוניות נוספות, כולל מחלת השימוטו (10 אחוזים), כרסת (מחלת צליאק) (4 אחוזים) ובשכיחות נמוכה יותר מחלת אדיסון (2 אחוזים), בהרת (ויטיליגו), מיאסטניה גרביס ועוד.
המודל להתפתחות סוכרת מסוג 1
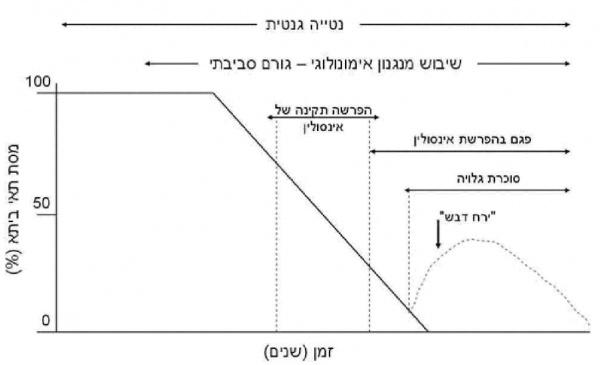
בשנות ה-80 תואר המודל להתפתחות סוכרת מסוג 1.[2] מודל זה מניח, כי בשלב ראשון כל אדם נולד עם דרגה מסוימת של נטייה גנטית לפתח סוכרת מסוג 1, בחלק הנטייה גבוהה ובחלק נמוכה. השלב השני של התפתחות המחלה דורש חשיפה לגורם סביבתי, המשנה את תפקוד המערכת האימונית, וכך גורמת לתחילת המתקפה האימונית, שסופה הרס תאי ביתא של הלבלב. ההרס המתמשך של תאי ביתא מוביל לאיבוד הדרגתי של יכולת הפרשת אינסולין: בתחילה, נפגע השלב הראשון של שחרור אינסולין (שחרור של אינסולין שכבר אגור בלבלב כתגובה לגירוי של עליית סוכר בדם), אחר כך, הופעה גלויה של סוכרת, כאשר יתרת יכולת ההפרשה יורדת מתחת לסך קריטי (20 אחוזים), ובשלב האחרון, ברוב חולי הסוכרת, חסר מלא של אינסולין. תקופת ירח דבש מופיעה זמן קצר לאחר האבחנה הקלינית ותחילת הטיפול באינסולין, כאשר הלבלב ׳נח׳ ויכול להפריש מעט אינסולין. יש לציין, כי קצב איבוד תאי ביתא של הלבלב יכול להיות איטי או מהיר, ולהימשך שבועות, חודשים או שנים.
הגורם הגנטי
סוכרת מסוג 1 איננה בעלת תורשה גנטית מובהקת, אינה מתאימה לאף צורת הורשה מנדליאנית ידועה והגנטיקה של המחלה הנה רבת-גורמים. אצל 10 אחוזים בלבד מהחולים החדשים בסוכרת מסוג 1 נמצאו קרובי משפחה נוספים הסובלים מסוכרת דומה, לעומת 90 אחוזים במקרה של סוכרת מסוג 2.
הקשר המשפחתי מתבטא בעלייה מסוימת בסיכון של קרובי משפחתו של החולה לחלות במחלה, לעומת האוכלוסייה הכללית. בתוך המשפחות, הנטייה תלויה בדרגת הזהות הגנטית עם בן המשפחה החולה. הסיכון הגבוה ביותר נצפה בקרב תאומים זהים. במעקב ארוך טווח נמצא סיכון עד 70 אחוזים לפתח סוכרת. לאחים יש ממוצע סיכון נמוך יותר (6 אחוזים), אך עדיין גבוה מהשכיחות המדווחת באוכלוסייה הכללית בארצות הברית - 0.4 אחוזים. השוני בסיכון לפתח סוכרת גם תלוי במין ההורה החולה בסוכרת. ילדים לאם סוכרתית בעלי סיכון של 2 אחוזים לפתח סוכרת, לעומת 7 אחוזים בילדים לאב חולה בסוכרת.
במחקרים מרובים ניסו לפצח את הנטייה הגנטית לפתח את מחלת הסוכרת, וידועים למעלה מ-25 אתרים גנטיים שנמצאו קשורים לסיכוי לפתח סוכרת. הגנים החשובים ביותר התומכים בנטייה לפתח את המחלה הנם הגנים לסיווג רקמות הממוקמים בכרומוזום 6 בקומפלקס Human Leukocyte Antigen (HLA), המהווים 60-40 אחוזים מהנטייה לפתח סוכרת. מביניהם חשובים במיוחד הגנוטיפים DQ-DR, הקשורים לתהליך האימוני המציג את האנטיגן הזר לתאי T של המערכת החיסונית, ובכך מאפשרים הפעלה של המערכת כנגד אנטיגנים עצמיים, או גורמים להפרעה בתהליך התגובה האימונית. היכולת של מערכת סיווג הרקמות להציג אנטיגן תלויה בהרכב חומצות האמינו שמהן היא בנויה. שינוי, ולו של חומצה אמינית אחת, עלול להעלות או להוריד את האופייניות בה הן נקשרות לאנטיגנים עצמיים, ולפיכך להשפיע על הסיכוי לפתח סוכרת מסוג 1. רוב החולים בסוכרת מסוג 1 נושאים DR3 או DR4, ואילו 0602*DQB1 מגן מפני התפתחות של סוכרת מסוג 1 ונמצא בפחות מאחוז מהחולים. את ההבדלים בהיארעות סוכרת מסוג 1 באוכלוסיות השונות בעולם ניתן לייחס, בחלקם, לסיכון או להגנה הטמונים במבנה הגנטי שלהם.
אולם, ישנם גם גנים מחוץ למערכת סיווג הרקמות שנמצאו קשורים לנטייה לפתח סוכרת. ביניהם אזור הגן לאינסולין, הנמצא בזרוע הקצרה של כרומוזום 11, המהווה כ-15 אחוזים מהנטייה לפתח סוכרת. פולימורפיזם (שונות בין בני אדם במספר חזרות של חומצות אמינו) באזור המפעיל את הגן קובע עלייה בסיכון לפתח סוכרת או הגנה מפני התפתחות המחלה בתלות במספר החזרות. גנים נוספים בעלי תרומה קטנה יותר, כגון SUMO4 ,PTPN22 ,CTLA4, הם בעלי תפקיד ברגולציה של המערכת האימונית.
הגורם הסביבתי
חשיבות המרכיב הסביבתי בתהליך התפתחות סוכרת מסוג 1 מודגמת בצורה המשכנעת ביותר אצל תאומים זהים. תוצאות מחקרים אפידמיולוגים בתאומים אלה הראו, שהסיכוי לפתח סוכרת אצל תאום זהה גנטית לחולה סוכרת הוא 35-15 אחוזים, ועל כן מרמז כי על מנת לחלות בסוג זה של סוכרת נדרש פקטור תורם נוסף שאיננו גנטי.
השונות הגיאוגרפית בהיארעות של מחלת הסוכרת והעלייה בשכיחות הסוכרת בשנים האחרונות גם הן לא יכולות להיות מוסברות על בסיס גנטי בלבד. מהגרים מאזורים בעלי שכיחות נמוכה של סוכרת רוכשים את השכיחות של המקום החדש בטווח זמן קצר. כך, שעדויות אלו תומכות במרכיב סביבתי כגירוי המוביל לתהליך האוטו-אימוני באנשים בעלי נטייה גנטית לפתח סוכרת. יתרה מכך, ניתן למצוא עדות לנוכחות של נוגדנים למרכיבי לבלב כבר בגיל הינקות, עוד לפני התפתחות הסוכרת, אשר מעלה את האפשרות שישנם גורמים סביבתיים טרום-לידתיים וגורמים סביבתיים בילדות המוקדמת המגרים להתפתחות המחלה. אמנם, במספר מחקרים אפידמיולוגים נמצא כי גורמים סביבתיים אשר התרחשו טרום הלידה או בשלב מוקדם אחריה, נמצאו כמעלים קלות את הסיכוי לפתח סוכרת. חלק מהחוקרים הראו קשר למשקל לידה נמוך (קשור למסה קטנה יותר של תאי ביתא), למשך הריון, לגיל מתקדם של האם (מעל 35 שנה), לקדם רעלת הריון או רעלת הריון (חוסר סבילות אימונולוגית אם-עובר), לצהבת של היילוד (בעיקר אם היא על רקע חוסר התאמה בסוגי הדם) ולתסמונת מצוקה נשימתית ביילוד. הגורמים הראשונים והנחקרים ביותר, שהועלו כגורמים סביבתיים מוקדמים, הנם מחלות זיהומיות (נגיפיות) ותזונה. נציין, שנכון להיום אין עדות ישירה לאף אחד מגורמים אלה כגורם ישיר להתפתחות סוכרת (למעט סוכרת הנגרמת מזיהום מולד באדמת, שנעלמה עם החיסון למחלה).
נגיפים
נגיפים שונים הואשמו בהשתתפות בתהליך המוביל לסוכרת מסוג 1 (קוקסקי-וירוס, רוטה-וירוס, חזרת, דלקת כבד נגיפית מסוג סי, CMV (Cytomegalovirus), EBV (Epstein–Barr Virus) ועוד), אך העיקריים שבהם שייכים לקבוצת האנטרו-וירוסים. על פניו נראה הקשר הגיוני. במחקרים בבעלי חיים נמצא, שנגיפים יכולים לגרום באופן ישיר להרס תאי ביתא, או בדרך עקיפה לשפעול המנגנון האימוני כנגד תאים אלה. בבני אדם עדיין לא הוכח קשר זה. בנוסף, האללים של מערכת סיווג הרקמות, הקובעים את הנטייה לפתח סוכרת, קשורים גם לתהליך ההגנה של הגוף מפני נגיפים. התבנית העונתית של סוכרת (חורף וסתיו) מתאימה גם לשיא בשכיחות של מחלות נגיפיות, כמו גם לשיא של גיל ההופעה הראשון של סוכרת (חמש-שבע שנים).
הנגיפים מהווים כר נרחב למחקר, מתוך מחשבה שזיהוי של גורם נגיפי כגורם לסוכרת יאפשר פיתוח חיסון שימנע את הופעת המחלה. יש לציין, כי באחד המחקר שפורסמו בנושא לא נמצא קשר בין חיסוני ילדות לסיכוי לפתח סוכרת בקרב קבוצה גדולה של אחים לחולי סוכרת.
תזונה
גם גורמים תזונתיים הוערכו כגורמים בהתפתחות של סוכרת מסוג 1. חשיפה מוקדמת לחלב פרה הואשמה כגורם סביבתי בהתפתחות מחלת הסוכרת ונחקרה בשנים האחרונות במחקרים מעבדתיים וקליניים שונים. גרשטיין הציג סיכום תוצאות המחקרים שבוצעו עד כה והראה קשר חלש, אך משמעותי סטטיסטית, בין התפתחות סוכרת מסוג 1 לבין תקופת הנקה קצרה וחשיפה מוקדמת לחלב פרה (לפני גיל שלושה-ארבעה חודשים).[3] הסברה, שעדיין לא הוכחה באופן סופי ומשכנע, היא כי אצל תינוקות חדירות רירית דופן המעי גדולה יותר מאשר בגיל מאוחר. לפי תיאוריה זו, חשיפה מוקדמת לחלבוני חלב פרה גורמת למעבר חלבוני החלב מהמעי לגוף התינוק ללא פירוקם המלא, ושם מעוררים החלבונים הזרים את המערכת החיסונית, דבר שמוביל בסופו של תהליך להרס התאים יוצרי האינסולין המצויים בלבלב. תמיכה לתיאוריה זו נמצאה בשורה של תוצאות מחקרים שהצביעו על אנטיגן משותף לחלבון חלב הפרה ולחלבונים המוצגים על גבי ממברנת תאי הביטא. במספר מחקרים נמצא גם קשר בין חשיפה מוקדמת לגלוטן ולדגנים (לפני גיל שלושה חודשים) לבין הנטייה לפתח סוכרת, אך עדיין דרושים מחקרים נוספים. השכיחות הגבוהה של סוכרת בארצות כמו פינלנד מעלה את האפשרות של קשר בין חוסר חשיפה לשמש ורמות נמוכות בדם של ויטמין D לבין סיכון לפתח סוכרת מסוג 1. במחקרים בבעלי חיים נמצאה עדות לכך שוויטמין D מדכא את המערכת החיסונית וחסר שלו מאפשר, על כן, שפעול של המערכת ועלייה בסיכון לפתח סוכרת.
ניטרטים הם חומרים מחמצנים הנמצאים במזונות רבים, כולל במי שתייה, בריכוזים שונים. במספר מחקרים נמצא קשר בין כמות הניטרטים במים לבין הסיכון לפתח סוכרת.
תיאוריית ההיגיינה
לבסוף, השכיחות העולה של היארעות מחלת הסוכרת היוותה את הבסיס לתיאוריית ההיגיינה. על פי תיאוריה זו, השיפור בתנאים הסניטריים גורם לחשיפה פחותה לגורמים זיהומיים ולחוסר הבשלה של המערכת האימונית, ועל כן לעלייה בסיכון לפתח סוכרת מסוג 1. ההוכחות לנכונות תיאוריה זו עדיין דלות.
קליניקה
באופן טיפוסי, חולי הסוכרת מסוג 1 מפתחים תסמינים של צמא, שתייה מרובה (פולידיפסיה), השתנה לעתים קרובות (פוליוריה), כולל התעוררויות רבות לצורך השתנה בלילה, בריחת שתן מתוך שינה, הרטבת לילה אצל ילד שלא סבל מתופעה זו קודם לכן, ירידה במשקל, דרגות שונות של שינוי בתיאבון - ממוגבר ועד העדר תיאבון, לעתים עייפות מוגברת וחולשה, כאבי בטן, בחילות, ובילדות יכולה להופיע פטרת בנרתיק. בתינוקות הביטוי של המחלה יכול להיות חבוי ולהתבטא בחוסר שגשוג, החלפת חיתולים תכופה ואי-שקט.
חמצת קטוטית סוכרתית (DKA - Diabetic Ketoacidosis) עדיין מהווה את הביטוי הראשון למחלה ב-40-20 אחוזים מהמקרים. בחולים אלה מופיעים סימנים של התייבשות, הקאות, נשימת קוסמאול (נשימות עמוקות ומהירות) או שינוי במצב ההכרה.
לאחרונה מאובחנים חולים בשלב של סוכרת "שקטה", כלומר, בשלב המוקדם של המחלה. לרוב, מקרים אלה מאובחנים על ידי בני משפחה שכבר חולה בסוכרת, על ידי קלינאי המזהה דרגת חשד גבוהה או בבדיקת שגרה של סוכר בצום.
אבחנה
בכל מקרה של חשד קליני לסוכרת מסוג 1 יש להשלים את האבחנה במהירות וללא כל עיכוב, שכן יש חשיבות עליונה בהתחלה מוקדמת ככל האפשר של טיפול באינסולין. זיהוי מהיר וטיפול מוקדם ימנעו התפתחות של חמצת קטוטית סוכרתית. במצבים אלה על הקלינאי לבדוק מיידית את רמת הסוכר בדם ו/או בשתן, לאישור של המחלה או לשלילתה. את הבדיקה יש לבצע בו ביום, ואין להשהותה עד ליום המחרת, או עד אחרי חופשת סוף השבוע. ברוב המקרים, ובעיקר בגיל הילדות וההתבגרות, האבחנה מיידית וברורה ואיננה מצריכה בדיקות נוספות.
הבחנה בין שני סוגי הסוכרת
בשנים האחרונות ישנה עלייה בשכיחות סוכרת מסוג 2 בקרב ילדים ומתבגרים, בצמוד לעלייה העצומה בשכיחות ההשמנה בקבוצת הגיל הצעירה. ההבחנה בין שני סוגי הסוכרת אינה קלה תמיד, במיוחד אצל מתבגרים או מבוגרים צעירים הסובלים מהשמנת יתר. בלא מעט מקרים תתבהר האבחנה רק לאחר כמה חודשים מאבחון הסוכרת. במקרים אלה התסמינים הקליניים, השמנת יתר, סיפור משפחתי, נוכחות של אקנטוזיס (התכהות של העור כעדות לעמידות לאינסולין), ונוגדנים למרכיבי לבלב (אם כי קיימים מאמרים המטילים ספק אף בכך) יכולים לתרום לאבחנה בין שני סוגי הסוכרת.
טיפול
גילוי האינסולין ב-1921 הפך את הסוכרת ממחלה חשוכת מרפא למחלה כרונית עם סיבוכים ארוכי טווח מיקרו ומקרו-וסקולריים.
הטיפול בסוכרת מסוג 1 מבוסס על מתן אינסולין, הניתן בזריקות או בהזלפה תת-עורית. עיקרון הטיפול מורכב ממתן אינסולין ברמה בסיסית – אינסולין בזאלי, בכמות המספיקה לדיכוי תהליך יצירת הסוכר בכבד (גלוקוניאוגנזיס) ולדיכוי של יצירת גופי הקטו (קטוגנזיס), ומתן אינסולין בעת הארוחות – בולוס, לדיכוי עליית הסוכר הצפויה בעקבות הארוחה.
תוצאות מחקר DCCT - Diabetes Control and Complications Trial,[4] שפורסם ב-1993, הדגימו לראשונה כי איזון הדוק של רמות הסוכר, כפי שמתבטא בהמוגלובין מסוכרר (HBA1C), יכול להקטין את הסיבוכים ארוכי הטווח של המחלה (רטינופתיה סוכרתית, נפרופתיה סוכרתית, נוירופתיה סוכרתית) או לדחות אותם, ולאחרונה עלתה גם עדות לירידה בסיבוכים הקרדיו-וסקולריים. ירידה של 1 אחוז בהמוגלובין מסוכרר מורידה את הסיכון לסיבוכי סוכרת ב-50-20 אחוזים. במחקר זה הודגם הצורך החד-משמעי לשליטה מטבולית ופיזיולוגית ככל האפשר, והוטבע המינוח "לחשוב כמו לבלב". עם זאת, תוצאות המחקר הראו יחס הפוך בין האיזון המטבולי לבין שכיחות אירועי היפוגליקמיה קשים, אשר התרחשו פי שניים-שלושה יותר בקרב קבוצת הטיפול האינטנסיבי. כך שהיפוגליקמיה מהווה אחד מהמכשולים להשגת איזון טוב. רק כ-5 אחוזים מהחולים שטופלו בזרוע האינטנסיבית במחקר DCCT, הצליחו להשיג רמת המוגלובין מסוכרר של 7 אחוזים ומתחת. יתרה מכך, נתונים ממרכזי סוכרת המטפלים בילדים הראו, שרמת ההמוגלובין המסוכרר הממוצע של החולים עדיין רחוקה מרמת היעד. נתונים אלה מדגישים, שמתן אינסולין הוא רק חלק מהפתרון המלא של הטיפול בחולי סוכרת מסוג.
משאבות אינסולין
מתן אינסולין בצורה רציפה בעזרת משאבת אינסולין מחקה את הדרך הטבעית בגוף למתן של אינסולין: קצב בזאלי ומתן של בולוסים לפני ארוחות. לפיכך, מבחינה תיאורטית, חולה המחובר למשאבת אינסולין אינו מחויב בסדר יום קבוע ובארוחות בזמנים קבועים. השימוש במשאבה יעיל, אם כן, במיוחד לאנשים שאין להם אפשרות לשמור על סדר יום קבוע. מתבגרים רבים מוצאים את השימוש במשאבה מתאים יותר לאורח החיים אותו הם מנהלים, ומדווחים על שיפור באיכות חייהם.
יתרונות הטיפול במשאבה הינם ירידה בהמוגלובין מסוכרר, ירידה בסיכון לאירועי היפוגליקמיה ושיפור באיכות חיים. החסרונות: בעיות טכניות (חסימה, דליפה, סוללות ועוד), סיבוכים עוריים (זיהום, אלרגיה, איבוד מקומי של שומן) ואירועים של חמצת סוכרתית על רקע תזוזה של הפרפרית שגורמת להפסקה בהזלפת האינסולין. קיים, על כן, צורך בניטור צמוד (מספר רב יותר של בדיקות סוכר ביממה) כדי להימנע מסכנת חמצת. לאחרונה הודגם במספר מחקרים, כי משאבת אינסולין יכולה להוות אפשרות טובה ובטוחה לטיפול בסוכרת בילדים בגיל הרך. שימוש במשאבת האינסולין במרכז המתמחה בכך יכול להביא לשיפור באיזון המטבולי ובאיכות חיי החולים.[5]
השימוש במשאבות האינסולין נמצא בעלייה בשנים האחרונות, במקביל לשכלול המשאבות והציוד הנלווה אליהן. משאבות האינסולין מאפשרות לחולה לקבוע את מינוני האינסולין הבזאלי ואף לשנותם כל שעה, וכך יכול החולה להתאים את כמות מתן האינסולין ותזמונו לצרכיו המשתנים, וכל זאת ללא צורך בזריקות חוזרות.
הצוות הרפואי מנסה להתאים את סוג האינסולין, את המינון ואת תזמון זריקות האינסולין לגיל החולה, לסדר יומו, לארוחותיו ולפעילות הגופנית.
רוב חולי הסוכרת מטופלים כיום בשלוש-ארבע זריקות אינסולין ביום לפחות, או במשאבת אינסולין. הטיפול באינסולין אינדיווידואלי, ועליו להיתמך בחינוך הולם לטיפול במחלת הסוכרת. שמירה קפדנית על סדר היום ועל הארוחות, פעילות גופנית מסודרת ובדיקות עצמוניות של רמת הסוכר בדם מספר פעמים ביום, מקלות על השגת איזון מטבולי, אך קשות להשגה אצל ילדים ומתבגרים. הדיאטה בסוכרת צריכה להיות מותאמת גם היא, באופן פרטני, לצורכי הגדילה וההתפתחות של הילד או המתבגר.
סוגים שונים של אינסולין
הכניסה של טכניקות מולקולריות גנטיות חדשות בעשור האחרון אפשרה ייצור אינסולינים בעלי תכונות פרמקולוגיות שונות, שהשימוש המשולב בהם מאפשר חיקוי של הפעולה הפיזיולוגית של הלבלב, המושתתת על הפרשת רמה בסיסית קבועה ויציבה של אינסולין לאורך כל היממה, ועליות מהירות וקצרות טווח של רמות האינסולין בזמן הארוחות. האינסולינים ארוכי הטווח מסוג גלרגין [Glargine (Lantus)] ודטמיר [Detemir (Levemir)], הנספגים באיטיות ובצורה קבועה, מייצרים רמת אינסולין בסיסית יציבה ונטולת שיא לאורך היממה, מאפשרים גמישות בזמני הארוחות ומקטינים שכיחות של אירועי היפוגליקמיה. אינסולינים מהירי פעולה מסוג ליספרו [Lispro (Humalog)], אספרט [Aspart (Novorapid)] וגלוליזין [Glulisine (Apidra)], נספגים תוך כעשר דקות מההזרקה, מייצרים במהירות רמה גבוהה של אינסולין בדם בשעתיים לאחר הארוחה, ודועכים מהר לאחר שעתיים. השימוש המשולב באינסולין מהיר וארוך טווח מאפשר חיקוי המודל "בזאל-בולוס", עליו מושתתת משאבת האינסולין. סוג טיפול זה מהווה, משום כך, "משאבה ללא משאבה".
נסיון לפיתוח אמצעי למתן אינסולין ללא צורך בהזרקה
חולה סוכרת מודד את רמות הסוכר לפחות ארבע פעמים ביום ומזריק שלוש-ארבע זריקות אינסולין ביום, משמע 240 דקירות בחודש, 3,000 בשנה. על כן, עדיין מחפשים את הדרך הטובה ביותר למתן ההורמון ללא צורך בזריקה. ניסיונות ראשונים החלו כבר בדרך לפיתוח תכשיר אינסולין פומי, ניסיונות הפיתוח מתרכזים במציאת הדרך לשמירה על האינסולין מפני האנזימים המעכלים במעי ובמעבר האינסולין אל זרם הדם דרך רירית המעי. דרך נוספת שנבדקת, הנה מתן אינסולין במדבקה דרך העור. ניסיונות ראשונים בבני אדם תוארו בהצלחה חלקית. לאחרונה אושר השימוש באינסולין בשאיפה למבוגרים חולי סוכרת מסוג 1 ומסוג 2. אינסולין הניתן בשאיפה לחולי סוכרת מסוג 1 יכול לשמש כתחליף לזריקות הבולוס, אך לא כתחליף לצורך במתן אינסולין בזאלי. לפיכך, חולי סוכרת סוג 1 המקבלים אינסולין בשאיפה עדיין יידרשו למתן זריקה של אינסולין ארוך טווח.
ניטור
הזרוע השנייה בטיפול בסוכרת היא מדידה של רמות הסוכר, כאשר תוצאות מחקרים רבים מדגימות, כי בדיקות מרובות לאורך היממה, המלוות כמובן, בתגובה טיפולית מתאימה, משפרות את איזון הסוכרת.
המכשירים כיום דורשים כמות מזערית של דם, מספקים רמת סוכר תוך 15-5 שניות, בדרגת דיוק טובה (10 אחוזים טווח טעות). אך למרות שכלולם של מדי הסוכר החדשים, עדיין כל מדידה מחייבת דקירה. כמו כן, אין מכשירים אלה מאפשרים ניטור ממושך של רמות הסוכר לאורך היממה, ואינם נותנים מענה לשאלות יומיומיות איתן מתמודדים החולים כגון: האם רמת הסוכר שלי נמוכה בשעה שלוש בלילה? איך פיצה משפיעה על רמת הסוכר שלי? איך הכדורסל משפיע על רמת הסוכר שלי? כמה פעמים ביום יש לי ערכים גבוהים או נמוכים? האם תיקנתי (בהזרקת אינסולין) יותר מדי? פחות מדי?
מזה כשלושים שנה נעשה מאמץ לפיתוח חיישנים שימדדו רמות סוכר לכל אורך היממה. שני העשורים האחרונים היוו פריצת דרך ובמהלכם מנסות חברות שונות לפתח חיישני סוכר בטכנולוגיות שונות.
ההתפתחות בתחום התוכנה מאפשרת היום גם פריקת נתונים למחשב ישירות ממדי הסוכר וממשאבות האינסולין. הנתונים ניתנים לתצוגה גרפית ולפילוחים שונים: רמות סוכר לאורך היממה, הצגה גרפית בצורת תרשים עמודות או עוגה של אחוז הערכים מעל או ליעד או מתחתיו לאורך היממה, כמות ומספר הבולוסים, היחס בולוס-בזאל ועוד. נתונים אלה מאפשרים הדרכה טובה יותר של החולים ותיקון נקודות כשל בטיפול.
בתחום משחקי המחשב, ניתן למצוא משחקים שמטרתם חינוך והגברת מוטיבציה אצל ילדים לביצוע מדידות סוכר. במסגרת המשחק יכולים המשתתפים לנחש את רמות הסוכר רק לאחר הזנה של שלוש בדיקות אמת ממד הסוכר. תוצאות מחקר שבו נבדקה השפעת השימוש במשחק, הראו כי הקבוצה שהשתמשה בו ביצעה יותר מדידות סוכר מקבוצת הביקורת ושיפרה את איזון הסוכרת.
ההתפתחות המהירה של תחום התוכנה יצרה את "מחשב הבולוסים הקוסם" (Bolus Wizard Calculator), המשמש היום כמרכיב אינטגרלי של חלק ממשאבות האינסולין. החולה מזין למחשב את רמת הסוכר בדמו ואת כמות הפחמימות שבכוונתו לאכול. המחשב ממליץ לחולה על מינון בולוס האינסולין הרצוי, וזאת על פי הנתונים שהוזנו, תוך לקיחה בחשבון של גורמי התיקון האישיים לחולה (שהוזנו למחשב מבעוד מועד), וכן את כמות האינסולין שנשארה בגוף החולה מבולוסים קודמים שניתנו.
החזון לשנים הקרובות הוא שילוב הטכנולוגיות שתוארו עד כה ליצירת לבלב מלאכותי, ועל ידי כך יצירת "ריפוי טכנולוגי" של הסוכרת: לבלב מלאכותי כזה יתקבל על ידי חיישן, מחשב ומשאבה - ש"ידברו" ביניהם וישדרו נתונים בזמן אמת זה לזה. שתי מערכות כאלו נמצאות בפיתוח: האחת מערכת חיצונית והשנייה מערכת מושתלת. בניסיונות ראשונים הצליחו ליצור שילוב טכנולוגי שתפקד כלבלב מלאכותי למשך מספר ימים והצליח לאזן את החולה בזמן צום, אך לא הצליח עד כה לאזן את רמות הסוכר של חולים בצורה יעילה לאחר ארוחות.
מבט לעתיד
ההצלחה של השתלת איי לבלב, תוך שימוש בפרוטוקול שפותח באדמונטון שבקנדה, חידשה את ההתעניינות בהשתלה של תאים מייצרי אינסולין כטיפול דפיניטיבי לסוכרת.[6] אחת הבעיות העיקריות הנה חסר בתרומות של איי לבלב. חסר זה העלה את הצורך בחיפוש של מקורות חלופיים לתאי לבלב. המטרה לכוון ולהכריח תאים ממקורות שונים להפוך לתאים מייצרי אינסולין. מקורות תאיים שיכולים להתמיין ולהפוך לתאים מייצרי אינסולין כוללים תאי כבד, טחול ותאי אב עובריים. במחקרים נוספים השתמשו בטכנולוגיה של השתלת גן מייצר אינסולין או מייצר חומרים שימנעו את התגובה האימונית כלפי תאי לבלב מושתלים.[7] במשך השנים נערכו ניסיונות בהשתלת איי לבלב העטופים בממברנות חצי-חדירות המגנות על איי הלבלב מפני ההתקפה הצפויה של מערכת החיסון. ממברנות אלו מפרידות בין איי התורם והמערכת האימונית של הנתרם, אך עם זאת מאפשרות מעבר של חמצן וחומרים נוספים הדרושים לחיות השתל.[8]
מניעה
מאמץ רב מושקע לאורך השנים גם בתחום מניעת הסוכרת, ולחלופין, הארכת תקופת ירח הדבש, שבה קיימת עדיין רזרבת אינסולין עצמוני.
הארכת תקופת ירח הדבש
תחום אחד הנו יצירת חיסונים, אשר ישרו סבילות של המערכת החיסונית בגוף כלפי איי הלבלב וכך יימנע תהליך הרס איי הלבלב. דוגמאות למחקרים אלה: מחקר בחיסון ה-DiaPep - פפטיד שהדגים במודל חיות יכולת של עיכוב התהליך האימוני, ולפיכך של הופעת הסוכרת. פפטיד זה ניתן לקבוצה קטנה של חולים חדשים בסוכרת מסוג 1, במטרה להאריך את תפקוד תאי הביתא שלהם. הממצאים הראשוניים העלו את הרושם כי במבוגרים (ולא בילדים) גרם הפפטיד לשארית תפקודית של הפרשת אינסולין טובה במעט יותר מאשר בקבוצת הביקורת. במחקר נוסף, שכלל מספר משתתפים קטן בקרב מבוגרים חולי סוכרת מסוג 1, ניתן חיסון 1-GAD, והתוצאות הצביעו על האטה בקצב איבוד יכולת הפרשת אינסולין מתאי ביתא בקרב הקבוצה שחוסנה. בנוסף פורסם, כי טיפול בעזרת נוגדנים כנגד CD3 האט את קצב איבוד תאי ביתא של הלבלב והביא לשיפור באיזון המטבולי בחולי סוכרת "חדשים".
מחקרים הממוקדים במניעת סוכרת
במחקר 1-Diabetes Prevention Trial) DPT) נבדק אם מינון קטן של אינסולין בזריקות, או דרך הפה, יכול למנוע או לדחות התפתחות של סוכרת מסוג 1 באוכלוסייה בסיכון לפתח סוכרת. תוצאות המחקר היו מאכזבות ואופציה טיפולית זו נזנחה.
במחקר הרב-מרכזי ENDIT (European Nicotinamide Diabetes Intervention Trial), נבדק אם מתן של ניקוטינאמיד (Nicotinamide) (המעודד תיקון דנ"א (DNA) בתאי ביתא של הלבלב) מונע או מאט התפתחות סוכרת בקרב קרובי משפחה מדרגה ראשונה. גם במחקר זה התוצאות היו מאכזבות. במחקר TRIGR (Trial to Reduce IDDM in the Genetically at Risk) נבדק אם הזנת תינוקות בתחליפי חלב מעלה את הסיכון לפתח סוכרת מסוג 1. במחקר הראשוני שבוצע נמצאו תוצאות מעודדות, לפיהן מתן חלב אם בינקות מונע סוכרת. המחקר נמשך גם כיום ובודק אם הימנעות מחלב פרה לפני גיל חצי שנה תמנע התפתחות סוכרת בגיל העשרה.
פרוגנוזה
אורח חיים בסוכרת מסוג 1
בטיפול בילד או במתבגר החולה בסוכרת מסוג 1, הצוות המטפל עושה כל מאמץ לאזן את ערכי הסוכר בדם, תוך ניסיון להמשיך ולאפשר לחולה לנהל אורח חיים רגיל ככל האפשר. מיד לאחר האבחנה נעשה מאמץ לאפשר לחולה לקבל את הטיפול ואת החינוך לטיפול בסוכרת באופן אמבולטורי. הצוות מעודד את הילד לחזור ולהשתלב בלימודים מוקדם ככל האפשר, להשתתף בשיעורי ספורט, בטיולי בית הספר ובחוגים שונים. הצבא בישראל מאפשר לחולי סוכרת מסוג 1 הרוצים בכך, להתנדב לשירות פעיל במדים. לאחרונה אף נשקלת בצבא האפשרות לגייס את חולי הסוכרת במסגרת גיוס חובה. יחד עם התמיכה והעידוד להשתלבות חברתית מלאה ככל האפשר, החינוך שניתן לצעירים חולי סוכרת מסוג 1 מדגיש את כללי הבטיחות ואת הדרכים למניעת סיבוכים מיידיים, כהיפוגליקמיה או חמצת קטוטית.
חמצת קטוטית סוכרתית
חמצת קטוטית סוכרתית - Diabetic Ketoacidosis) DKA) הינה מצב מטבולי מסכן חיים, המהווה את סיבת המוות העיקרית מסוכרת מסוג 1. מצב זה עדיין מהווה את הביטוי הראשון למחלה ב-40-20 אחוזים מהמקרים. חולים אלה מאובחנים בשלב שבו התפקוד של תאי ביתא חסר בצורה חמורה יותר, כך שביטוי המחלה מלווה בהפרעה מטבולית וחמצת. חולים אלה מאופיינים בחסר אינסולין חמור, ובשלב זה המנגנונים המטבוליים משתמשים בפירוק השומן והטריגליצרידים ליצירת גופי קטו לשם אספקת אנרגיה. התייבשות (דהידרציה) ופרפוזיה נמוכה לרקמות מובילות גם למרכיב של חמצת לקטית. בחולים אלה מופיעים סימנים של התייבשות, הקאות, נשימת קוסמאול (נשימות עמוקות ומהירות) או שינוי במצב ההכרה, ונדרשים אשפוז וטיפול מיידי. הטיפול ההתחלתי במצב זה כולל הזלפת נוזלים, ניטור סימנים חיוניים, טיפול מתאים בחסרים של נוזלים ואלקטרוליטים, ומתן של אינסולין כמרכיב העיקרי לתיקון ההפרעה המטבולית.
דגלים אדומים
ביבליוגרפיה
- ↑ LaPorte R, Matsushima M, Chang Y. Prevalence and incidence of insulin-dependent diabetes. In Diabetes in America, second edition, ed. NDDG NIH 1995:37-46.
- ↑ Eisenbarth GS. Type 1 diabetes mellitus: A chronic autoimmune disease. N Engl J Med, 1986;314:1360-1368.
- ↑ Gerstein HC. Cow's milk exposure and type 1 diabetes mellitus: a critical overview of the clinical literature. Diabetes Care, 1994;17:13-19.
- ↑ The Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med, 1993;329:977-986.
- ↑ Nimri R, Weintrob N, Benzaquen H et al.flnsulin pump therapy in youth with type 1 diabetes mellitus: A retrospective paired study. Pediatrics, 2006;117:2126-2131.
- ↑ Shapiro AM, Lakey JR. Future trends in islet cell transplantation. Diabetes Technol Ther, 2000;2:449-452.
- ↑ Lee HC, Kim SJ, Kim KS, et al. Remission in models of type 1 diabetes by gene therapy using a single-chain insulin analogue. Nature, 2000;23:483-488.
- ↑ Sambanis A: Engineering challenges in the development of an encapsulated cell system for treatment of type 1 diabetes. Diabetes Technol Ther, 2000;2:81-89.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי פרופ' משה פיליפ, מנהל המכון לאנדוקרינולוגיה וסוכרת, המרכז הארצי לסוכרת נעורים, מרכז שניידר לרפואת ילדים בישראל, פתח-תקוה, הפקולטה לרפואה ע"ש סאקלר אוניברסיטת ת״א; ד"ר רויטל נימרי, המכון לאנדוקרינולוגיה וסוכרת, המרכז הארצי לסוכרת נעורים, מרכז שניידר לרפואת ילדים בישראל, פתח-תקוה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק