הבדלים בין גרסאות בדף "המדריך לטיפול בסוכרת - כבד שומני - קשר לסוכרת מסוג 2 ודרכי טיפול - Fatty liver disease and type 2 diabetes - treatment methods"
(←סיכום) |
|||
| (127 גרסאות ביניים של 5 משתמשים אינן מוצגות) | |||
| שורה 1: | שורה 1: | ||
| − | {{ | + | {{Sub Chapter |
| + | |Book=המדריך לטיפול בסוכרת | ||
| + | |Chapter number=4 | ||
| + | |Sub Chapter number=3 | ||
| + | }} | ||
{{ספר| | {{ספר| | ||
| − | |שם הספר= [[המדריך לטיפול בסוכרת]] | + | |שם הספר= [[המדריך לטיפול בסוכרת]] |
| − | |תמונה=[[קובץ:מדריךסוכרת.jpg| | + | |תמונה=[[קובץ:מדריךסוכרת.jpg|200px]] |
| − | |שם המחבר= | + | |שם המחבר= פרופסור שירה זלבר-שגיא, ד"ר חני ישועה, דנה איבנקובסקי-וכקמן, ד"ר מאיה מרגלית, פרופסור אורן שבולת |
|שם הפרק= '''כבד השומני - הקשר לסוכרת מסוג 2 ודרכי טיפול''' | |שם הפרק= '''כבד השומני - הקשר לסוכרת מסוג 2 ודרכי טיפול''' | ||
|עורך מדעי= | |עורך מדעי= | ||
|מאת=[[המועצה הלאומית לסוכרת]], {{ש}}משרד הבריאות | |מאת=[[המועצה הלאומית לסוכרת]], {{ש}}משרד הבריאות | ||
|מוציא לאור= | |מוציא לאור= | ||
| − | |מועד הוצאה= | + | |מועד הוצאה=2022 |
| − | |מספר עמודים= | + | |מספר עמודים=614 |
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | {{הרחבה| | + | {{הרחבה|כבד שומני וסוכרת}} |
| − | מחלת הכבד השומני | + | הצטברות שומן בתוך תאי הכבד נקראת [[Hepatic steatosis]] וכאשר היא עולה על 5 אחוזים מוגדרת התופעה כ[[כבד שומני]] (Hepatic steatosis, Fatty liver) נובע מצירוף של עודף יצור שומן (ליפוגנזה), הגעה מוגברת של [[טריגליצרידים - Triglycerides|טריגליצרידים]] מרקמת שומן פריפרי לכבד ותזונה עתירת שומן. גורמים אלה מובילים ל"הצפת" הכבד בשומן, בכמות העולה על יכולת הוצאתו. |
| + | |||
| + | [[NAFLD]]) Nonalcoholic Fatty Liver Disease) (מחלת הכבד השומני - מכ"ש), הוכרה כמחלה המהווה נטל רפואי רב משקל בשל הימצאותה הגבוהה באוכלוסייה הכללית, בשל היותה גורם סיכון משמעותי להתפתחות נזק כבדי ובשל הקשר לתחלואה נלווית. מכ"ש מוכרת כמחלת הכבד השכיחה ביותר בעולם{{הערה|שם=הערה1|Loomba R, Sanyal AJ. The global NAFLD epidemic. Nature reviews Gastroenterology & hepatology. 2013;10(11):686-90}}, הימצאותה המוערכת באוכלוסייה הבוגרת היא 20–30 אחוזים ברוב המחקרים{{הערה|שם=הערה2|Zelber-Sagi S, Nitzan-Kaluski D, Halpern Z, Oren R. Prevalence of primary non-alcoholic fatty liver disease in a population-based study and its association with biochemical and anthropometric measures. Liver Int. 2006;26(7):856-63}} ודווח אף על 46 אחוזים בארצות הברית{{הערה|שם=הערה3|Williams CD, Stengel J, A sike MI, Torres DM, Shaw J, Contreras M, et al. Prevalence of nonalcoholic fatty liver disease and nonalcoholic steatohepatitis among a largely middle-aged population utilizing ultrasound and liver biopsy: a prospective study. Gastroenterology. 2011;140(1):124-31}} המצאות מכ"ש בקרב הסובלים מ[[השמנה - Obesity|השמנה]] מגיעה ל-70–80 אחוזים{{הערה|שם=הערה2}} ול-50–74 אחוזים בחולי [[סוכרת מסוג 2 - Type 2 diabetes|סוכרת מסוג 2]]{{הערה|שם=הערה3}}. | ||
| + | |||
| + | בעבר הקרוב נחשב כבד שומני לממצא מקרי ללא משמעות קלינית. אולם נכון ל-2022 ברור שכ-10–20 אחוזים מהסובלים מכבד שומני עלולים לפתח [[NASH]]) Non-Alcoholic Steato-Hepatitis) (כבד שומני דלקתי - כש"ד), שעשוי להוביל להצטלקות (פיברוזיס) ועד ל[[שחמת הכבד|שחמת]] על סיבוכיה, כולל [[סרטן כבד]] ראשוני. | ||
| + | |||
| + | בנוסף, כבד שומני נחשב למרכיב הכבדי של [[הסינדרום המטבולי]] וכגורם סיכון מוקדם ל[[סוכרת]] ול[[מחלת לב איסכמית]]. במטא-אנליזה נמצא כי מכ"ש מגביר את הסיכון למחלת לב פי 2 (95% רווח בר סמך 2.3-1.8){{הערה|שם=הערה4|Musso G, Gambino R, Cassader M, Pagano G. Meta-analysis: natural history of non-alcoholic fatty liver disease (NAFLD) and diagnostic accuracy of non-invasive tests for liver disease severity. Ann Med. 2011;43(8):617-49}}. בנוסף, הודגם כי מכ"ש מגביר את הסיכון לסוכרת פי 3.5 (95% רווח בר סמך 5.4-2.3) באופן בלתי תלוי בגורמי סיכון ידועים אחרים{{הערה|שם=הערה4}}. מחקרים נוספים הדגימו קשר בין כבד שומני לבין גידולים מחוץ לכבד, בעיקר במערכת העיכול{{הערה|שם=הערה5|Hudng KW, Leu HB, Wang YJ, Luo JC, Lin HC, Lee FY, et al. Patients with nonalcoholic fatty liver disease have higher risk of colorectal adenoma after negative baseline colonoscopy. Colorectal Disease. 2013;15(7):830-5}}{{הערה|שם=הערה6|Allen AM, Hicks SB, Mar a KC, Larson JJ, Therneau TM. The risk of incident extrahepatic cancers is higher in non-alcoholic fatty liver disease than obesity—A longitudinal cohort study. Journal of hepatology. 2019;71(6):1229-36}}. | ||
| + | |||
| + | == גורמי סיכון עיקריים לכבד שומני == | ||
| + | כבד שומני הוא מחלה מולטיפקטוריאלית שגורמיה ידועים רק בחלקם. בין גורמי הסיכון החשובים ביותר נכללים [[תנגודת לאינסולין - Insulin resistance|תנגודת לאינסולין]] ועלייה בשומן בטני עם עלייה ברמת [[לפטין - Leptin|לפטין]] וירידה ברמת ה[[אדיפונקטין - Adiponectin|אדיפונקטין]]. הקשר החזק של מכ"ש עם תנגודת לאינסולין ועם הסינדרום המטבולי תועד בהרחבה בספרות ויש ראיות לכך כי תנגודת לאינסולין קיימת גם בחולי מכ"ש רזים ולא סוכרתיים{{הערה|שם=הערה7|Kim CH, Younossi ZM. Nonalcoholic fatty liver disease: a manifestation of the metabolic syndrome. Cleve Clin J Med. 2008;75(10):721-8}}. כמות גבוהה של שומן בטני מהווה גם היא גורם סיכון למכ"ש עקב השפעתה על ויסות השומן בכבד והתגלתה כגורם סיכון חשוב גם בבעלי משקל תקין{{הערה|שם=הערה8|Stefan N, Kantartzis K, Haring HU. Causes and metabolic consequences of Fatty liver. Endocr Rev. 2008;29(7):939-60}}. גורם סיכון נוסף, ידוע פחות הוא [[עלייה במשקל|עליית משקל]]. במחקר מעקב בן 7 שנים נמצא כי עליית משקל של 3–5 קילוגרם היא גורם קובע בהיארעות של כבד שומני חדש או ברמיסיה של כבד שומני קיים, ללא קשר למשקל התחלתי{{הערה|שם=הערה9|Zelber-Sagi S, Lotan R, Shlomai A, Webb M, Harrari G, Buch A, et al. Predictors for incidence and remission of NAFLD in the general population during a seven-year prospective follow-up. J Hepatol. 2012;S6(5):1 l45-51}}. | ||
| + | |||
| + | קיימת הסכמה רחבה כי גורמים התנהגותיים מעורבים בפתופזיולוגיה של כבד שומני כשההיבטים החשובים ביותר הם צריכת אנרגיה מופרזת, הרכב [[תזונה - Nutrition|תזונה]] לקוי ואורח חיים יושבני המהווה גורם סיכון בפני עצמו לכבד שומני. | ||
| + | |||
| + | == מאפיינים קליניים ואבחון של כבד שומני == | ||
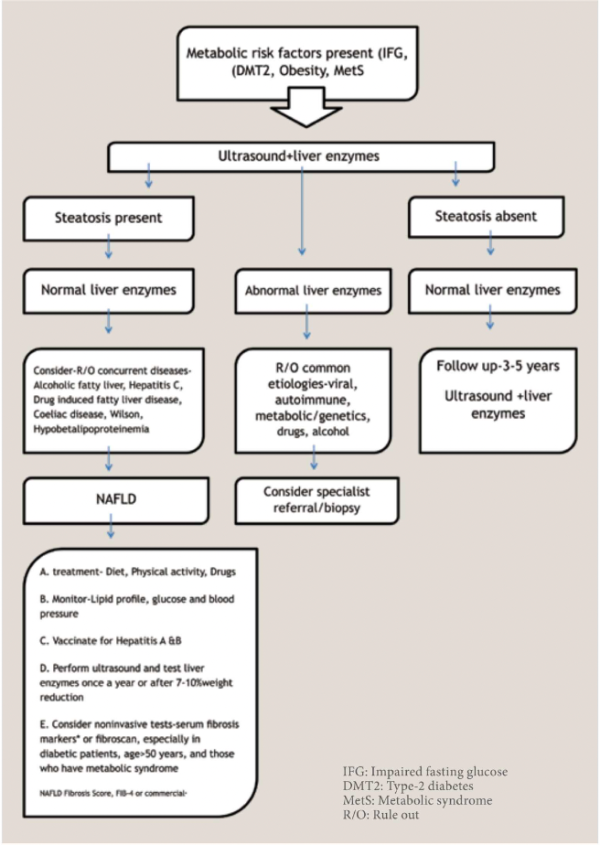
| + | מרבית המטופלים הם א-תסמיניים, ורוב המקרים של כבד שומני מתגלים באקראי בעת ביצוע בדיקת [[אולטרסאונד]] (סונר) או כשמודגמת [[אנזימי כבד|הפרעה באנזימי הכבד]] בבדיקות דם שגרתיות. הפרעה באנזימי כבד תופיע בכ-10 אחוזים מהמטופלים עם כבד שומני ומתאפיינת לרוב בעלייה קלה עד בינונית בטרנסאמינזות עם יחס [[אספרטאט טרנסאמינאזה - Aspartate transaminase|AST]]/[[אלנין טרנסאמינאזה - Alanine transaminase|ALT]]{{כ}} (Aspartate Transaminase/Alanine Transaminase) של פחות מ-1. תיתכן גם עלייה ב-[[גמא-גלוטאמיל טרנספראזה - Gamma glutamyl transferase|GGT]]{{כ}} (Gamma Glutamyl Transferase) ובשכיחות נמוכה יותר גם בפוספטזה הבסיסית ([[ALK]]). לא נמצא קשר בין רמת האנזימים לחומרת המחלה ההיסטולוגית{{הערה|שם=הערה10|Vernon G, Baranova A, Younossi ZM. Systematic review: the epidemiology and natural history of non-alcoholic fatty liver disease and non-alcoholic steatohepatitis in adults. Aliment Pharmacol Ther.34(3):274-85}}. ירידה בספירת שורות הדם (בעיקר [[תרומבוציטופניה - Thrombocytopenia|תרומבוציטופניה]]), [[היפואלבומינמיה]] או הארכת זמן פרותרומבין ([[זמן פרותרומבין - Prothrombin time|PT]]{{כ}}, Prothrombin Time) עשויים לרמז על נוכחות שחמת כבד. | ||
| + | |||
| + | במטופלים ללא הפרעה באנזימי כבד בהם התגלה כבד שומני באקראי בסונר והם א-תסמינים מבחינת מחלות כבד וללא אנמנזה של [[צריכת אלכוהול מוגזמת|צריכת אלכוהול מופרזת]] או נטילת [[תרופות]] היכולות לגרום לכבד שומני, ניתן להסיק שמדובר במכ"ש. | ||
| + | |||
| + | [[קובץ:Fatty diabetes 1.png|מרכז|ממוזער|600 פיקסלים|'''תרשים 1. מאפיינים קליניים ואבחון של כבד שומני'''.]] | ||
| + | |||
| + | הסבירות למכ"ש עולה בנוכחות הסינדרום המטבולי הכולל השמנת יתר, רמת סוכר גבוהה בצום, סוכרת או [[דיסליפידמיה]]. אם קיימת הפרעה באנזימי כבד, האבחנה של כבד שומני תתבצע רק לאחר שלילת סיבות משניות אחרות להפרעה באנזימים, כמקובל בספרות, ובעיקר שלילת [[זיהום]] בנגיף [[הפטיטיס B|דלקת הכבד מסוג B]] או [[הפטיטיס C|C]]{{הערה|שם=הערה11|Pratt DS, Kaplan MM. Evaluation of abnormal liver-enzyme results in asymptomatic patients. N Engl J Med. 2000;342(17):1266-71}}. | ||
| + | |||
| + | === ביופסית כבד ואמצעי אבחון לא פולשניים === | ||
| + | על אף חסרונות הבדיקה (ביניהם עלות, שונות דגימה, תחלואה ואף תמותה הקשורות בפרוצדורה){{הערה|שם=הערה12|Chalasani N, Younossi Z, Lavine JE, Charlton M, Cusi K, Rinella M, et al. The diagnosis and management of nonalcoholic fatty liver disease: Practice guidance from the American Association for the Study of Liver Diseases. Hepatology. 2018;67(1):328-57}}, ביופסיית כבד היא עדיין הדרך האמינה ביותר לאבחון של כש"ד ופיברוזיס במטופלים עם מכ"ש. יש לשקול ביופסיה בחולים עם מכ"ש ב-3 מצבים עיקריים: | ||
| + | |||
| + | # במטופלים בהם נותרה שאלה אבחנתית אם מדובר בכש"ד או בכש"ד בלבד (לאור ההיארעות הגבוהה של מכ"ש, לא נדיר למצוא מכ"ש במטופלים עם מחלות כבד אחרות) - לדוגמה מטופלים עם הפרעה ניכרת באנזימי הכבד, עם כייל גבוה של [[נוגדנים]] אוטואימוניים, ללא [[תסמונת מטבולית]] וכיוצא בזה; | ||
| + | # לאישוש חומרת הפגיעה ההיסטולוגית בכבד; | ||
| + | # בגיוס לניסויים קליניים | ||
| + | |||
| + | קיימים גם אמצעים לא חודרניים להעריך את חומרת ההצטלקות הכבדית, שהיא המדד היחיד שנקשר לתחלואה ותמותה כבדית ול[[השתלות כבד - Liver transplantation|השתלת כבד]] במטופלים עם מכ"ש{{הערה|שם=הערה13|Angulo P, Kleiner DE, Dam-Larsen S, Adams LA, Bjornsson ES, Charatcharoenwitthaya P, et al. Liver Fibrosis, but No Other Histologic Features, 1s Associated With Long-term Outcomes of Patients With Nonalcoholic Fatty Liver Disease. Gastroenterol- ogy. 2015;149(2):389-97 e10}}{{הערה|שם=הערה14|Ekstedt M, Hagstrom H, Nasr P, Fredrikson M, Stal P, Kechagias S, et al. Fibrosis stage is the strongest predictor for dis- ease-specific mortality in NAFLD after up to 33 years of follow-up. Hepatology. 201S;61(5):1547-54}}. אמצעים אלו משמשים לסיווג חולים לכאלו המצויים בסיכון גבוה לפיברוזיס משמעותי (F3 - פיברוזיס מתקדם, או F4 - שחמת), שיש להפנות לבירור כבדי שיכלול בחלק לא מבוטל מהמקרים גם ביופסיית כבד, ולכאלו המצויים בסיכון נמוך לפיברוזיס משמעותי (F0 או F1), שאינם זקוקים לבירור כזה. האמצעים הבלתי פולשניים הנהוגים כוללים אלגוריתמים מנבאים המבוססים על בדיקות מעבדה (כגון NAFLD Fibrosis Score - NFS{{כ}}, Fibrosis 4 - FIB4{{כ}} ו-Enhanced Liver Fibrosis (ELF) score) ובדיקות הדמיה המעריכות את אלסטיות הכבד, שמהן בדיקת ה[[Fibroscan|פיברוסקן]] - Vibration Controlled Transient Elastography) VCTE), היא הנפוצה והנחקרת ביותר. חשוב להדגיש, שבדיקות אלה תוקפו בהשוואה לביופסיית כבד; מכיוון שקיימות מגבלות לביופסיית כבר כסטנדרט להשוואה (כגון שונות דגימה, מהימנות בתוך הבודק ובין בודקים), ישנו ערך מקסימום אינהרנטי למידת הדיוק של בדיקות אלה. | ||
| + | |||
| + | '''אלגוריתמים מעבדתיים:''' מבין האלגוריתמים המעבדתיים המנבאים, FIB4 וה-NAFLD Fibrosis Score (NFS) נחקרו באופן נרחב באוכלוסיות מגוונות, והם מומלצים להערכה מוקדמת של מטופלים עם גורמי סיכון מטבוליים ומכ"ש{{הערה|שם=הערה12}}{{הערה|שם=הערה15|McPherson S, Anstee QM, Henderson E, Day CP, Burt AD. Are simple noninvasive scoring systems for fibrosis reliable in patients with NAFLD and normal ALT levels? Eur J Gastroenterol Hepatol. 2013;2S(6):652-8}}{{הערה|שם=הערה16|lmajo K, Kessoku T, Honda Y, Tome no W, Ogawa Y, Mawatari H, et al. Magnetic Resonance Imaging More Accurately Clas- sifies Steatosis and Fibrosis in Patients With Nonalcoholic Fatty Liver Disease Than Transient Elastog raphy. Gastroenterology. 2016;150(3):626-37 e7}}{{הערה|שם=הערה17|Ratziu V, Bellentani S, Cortez-Pinto H, Day C, Marchesini G. A position statement on NAFLD/NASH based on the EASL 2009 | ||
| + | |||
| + | special conference. J Hepatol. 2010;53(2):372-84}}. אלגוריתמים אלו, המבוססים על פרמטרים קליניים ומעבדתיים פשוטים וניתנים לחישוב בקלות, בסיוע מחשבונים אינטרנטיים, ב-Point of care, הודגמו כמנבאים תמותה (Overall), תמותה קרדיווסקולרית ותמותה הקשורה בכבד (Liver-related mortality) בחולים עם מכ"ש. | ||
| + | |||
| + | FIB4 מבוסס על גיל, AST ,ALT ורמת טסיות, ומתאפיין ב-0.8< (Area under the receiver Operating characteristic (AUROC (שטח מתחת לעקומה, כמה שהוא יותר גבוה וקרוב ל-1 כך הרגישות והסגוליות, כלומר תוקף הבדיקה טוב יותר). לאבחנה של פיברוזיס בדרגה של F3 או F4. | ||
| + | |||
| + | ה-NFS מתבסס על גיל, [[BMI]] (Body Mass Index) ,ALT ,AST, נוכחות/העדר [[Impaired fasting glucose]] או סוכרת, ורמת [[אלבומין]]. במטא-אנליזה של 13 מחקרים לגבי NFS, שכללה 3,064 חולים עם מכ"ש, דווח על 0.85 AUROC לניבוי פיברוזיס מתקדם{{הערה|שם=הערה4}}. אלגוריתם מעבדתי נוסף שקיים באופן מסחרי, כרוך בעלות, ומבוסס על בדיקות שאינן מבוצעות באופן רוטיני (Procollagen III amino terminal peptide, [[חומצה היאלורונית]] ו-Tissue inhibitor of matrix metalloproteinase) הוא ה-(panel ELF (Enhanced Liver Fibrosis, שדווחו לגביו במטופלים עם מכ"ש AUROC, רגישות וסגוליות 0.90, 0.80 ו-0.90, בהתאמה, לאיתור פיברוזיס מתקדם{{הערה|שם=הערה18|Guha IN, Parkes J, Roderick P, Chattopadhyay D, Cross R, Harris S, et al. Noninvasive markers of fibrosis in nonalcoholic fatty liver disease: Validating the European Liver Fibrosis Panel and exploring simple markers. Hepatology. 2008;47(2):455-60}}. בדיקת ה-ELF אושרה לשימוש מסחרי באירופה ונכנסה להמלצות ה-NICE לשלילת פיברוזיס מתקדם במטופלים עם מכ"ש; נכון לתחילת 2021, היא אינה בשימוש נרחב בישראל. | ||
| + | |||
| + | ב-FIB4 וב-NFS מוגדרים שני ערכי סף (cut-off); מטופלים בעלי ציון נמוך מערך הסף הנמוך 1.3> ל-FIB4 ו-1.455-> בבדיקת ה-NFS{{הערה|שם=הערה4}}{{הערה|שם=הערה19|Kaswala DH, Lai M, Afdhal NH. Fibrosis Assessment in Nonalcoholic Fatty Liver Disease (NAFLD) in 2016. Dig Dis Sci. 2016;61(5):1356-64}} הם בסיכון נמוך לפיברוזיס מתקדם, אינם זקוקים להערכה הפטולוגית באותה נקודת זמן, ומומלץ לחזור בהם על ההערכה כעבור שנתיים לפי המלצות האיגוד האירופי. במטופלים בעלי ציון גבוה מערך הסף הגבוה (2.67< בבדיקת ה-FIB4 ו-0.676< בבדיקת ה-NFS{{הערה|שם=הערה4}}{{הערה|שם=הערה19}}) קיים חשד לפיברוזיס מתקדם או שחמת, ויש להפנותם להערכה הפטולוגית (הערך הספציפי לחולים עם מכ"ש הוא מעל 2.67 לחשד לפיברוזיס מתקדם). בכ-30–50 אחוזים מהמטופלים מתקבל ערך שהוא בין ערך הסף הנמוך לערך הסף הגבוה; במקרים אלו נדרשת הערכה נוספת כדי לקבוע את דרגת הסיכון, ומומלץ להפנות את המטופל להערכה הפטולוגית. ב-ELF panel קיימים ערכי סף בדומה ל-FIB4 וה-NFS, אך בהנחיות ה-NICE נקבע ערך סף אחד (10.51) לניבוי פיברוזיס מתקדם; במטופלים מבוגרים שבהם תוצאת הבדיקה נמוכה מ-10.51 קיימת המלצה למעקב על ידי בדיקת ELF חוזרת לאחר 3 שנים{{הערה|שם=הערה20|NACE guideline ”Non-alcoholic fatty liver disease (NAFLD): assessment and management.“ Published b July 2016}}. | ||
| + | |||
| + | '''(Vibration Controlled Transient Elastography (VCTE - פיברוסקן:''' קיימים מספר סוגים של בדיקות מבוססות פרמטרים פיזיקליים להערכת אלסטיות הכבד, כגון Vibration Controlled Transient Elastography (VCTE){{כ}}, (Acoustic Radiation Force Impulse (ARFI ו-Magnetic Resonance Elastography ([[MRE]]). מביניהן, בדיקת VCTE היא הבדיקה הזמינה והנפוצה ביותר{{הערה|שם=הערה21|Vuppalanchi R, Siddiqui MS, Van Natta ML, Hallinan E, Brandman D, Kowdley K, et al. Performance characteristics of vibra- tion־controlled transient elastography for evaluation of nonalcoholic fatty liver disease. Hepatology. 2018;67(1):134-44}}{{הערה|שם=הערה22|Kwok R, Choi KC, Wong GL, Zhang Y, Chan HL, Luk AO, et aL Screening diabetic patients for non-alcoholic fatty liver disease with controlled attenuation parameter and liver stiffness measurements: a prospective cohort study. Gut. 2016;65(8):1359-68}}{{הערה|שם=הערה23|Tapper EB, Castera L, Afdhal NH. FibroScan (vibration-controlled transient elastography): where does it stand in the United States practice. Clin Gastroenterol Hepatol. 2015;13(1):27-36}}{{הערה|שם=הערה24|Kwok R, Tse YK, Wong GL, Ha Y, Lee AU, Ngu MC, et al. Systematic review with meta-analysis: non-invasive assessment of non-alcoholic fatty liver disease-the role of transient elastography and plasma cytokeratin-18 fragments. Aliment Pharmacol Ther. 2014;39(3):254-69}}. ה-VCTE מבוסס על עקרונות של אלסטוגרפיה על קולית, ומבוצע על ידי מכשיר פיברוסקן (חברת Echosens). תוצאת הבדיקה, LSM{{כ}} (Liver Stiffness Measure), נמדדת בקילו-פסקל (KPa). בדיקת ה-VCTE תוקפה על פני ספקטרום רחב של מחלות כבד כרוניות ונמצאה עם רמת דיוק גבוהה. יתרונות הבדיקה כוללים: בדיקה קצרה וקלה לביצוע, נסבלת היטב על ידי הנבדקים, ומעריכה נפח כבד גדול פי 100–200 לעומת ביופסיית כבד. במטא-אנליזה של 9 מחקרים על TE שכללו 1,047 חולים עם מכ"ש, רמת הדיוק הייתה בינונית עבור 2 ≤ F (רגישות וספציפיות 79 אחוזים ו-75 אחוזים בהתאמה), וטובה מאוד עבור F3 ו-F4 (רגישות וספציפיות של 85 אחוזים ו-85 אחוזים, בהתאמה, עבור F3; רגישות וספציפיות 92 אחוזים ו-92 אחוזים, בהתאמה, עבור F4{{הערה|שם=הערה24}}). יתרון נוסף של בדיקת הפיברוסקן הוא שברוב המכשירים מתאפשרת מדידה בו זמנית של ערך ה-CAP{{כ}} (Controlled Attenuation Parameter), שנותן הערכה כמותית של השומן בכבד{{הערה|שם=הערה22}}. | ||
| + | |||
| + | === הגישה לשימוש באמצעי אבחון לא פולשניים === | ||
| + | מרבית האמצעים הלא פולשניים שתוארו מתאפיינים בערך מנבא שלילי (NPV - Negative Predictive Value) גבוה להיעדר פיברוזיס מתקדם, ובערך מנבא חיובי (PPV - Positive Predictive Value) טוב במידה פחותה לניבוי פיברוזיס מתקדם; לאור זאת, מדובר בכלים המאפשרים לסווג באופן אמין מטופלים לקבוצת סיכון נמוך ולהתריע אודות מטופלים עם סיכון גבוה למחלה מתקדמת, שבהם נדרש בירור נוסף. היכולת להבחין באמצעות אמצעים אלו בדרגות פיברוזיס שאינן בקצוות, לדוגמה - בין פיברוזיס בדרגה F2 (פיברוזיס משמעותי), F1, או F0 (העדר פיברוזיס) מוגבלת. | ||
| + | |||
| + | חישוב ה-FIB4 או ה-NFS יכול להתבצע במסגרת הרפואית שבה מתקיים המעקב הרגיל אחר המטופל עם סוכרת או סינדרום מטבולי (רפואה ראשונית, מרפאת סוכרת). לפי הנחיות האיגוד האירופי, במטופלים ללא הפרעה באנזימי הכבד עם תוצאת FIB4 או NFS המעידה על סיכון נמוך מומלץ לחזור על בדיקת אנזימי הכבד ועל FIB4 או NFS כעבור שנתיים. מטופלים עם הפרעה באנזימי הכבד או עם תוצאת FIB4 או NFS שהיא מעל לערך הסף התחתון יש להפנות לבירור במרפאת כבד. מטופלים עם תוצאת FIB4 או NFS שהיא Indeterminate יופנו על פי רוב לבדיקה לא פולשנית נוספת, כגון VCTE; גישה זו נתמכת על ידי מחקרים שהדגימו ששילוב של גישות לא פולשניות מעלה את דיוק הניבוי{{הערה|שם=הערה25|Tsochatzis EA, Newsome PN. Non-alcoholic fatty liver disease and the interface between primary and secondary care. Lancet Gastroenterol Hepatol. 2018;3(7):509-17}}{{הערה|שם=הערה26|Petta S, Vanni E, Bugianesi E, Di Marco V, Camma C, Cabibi D, et al. The combination of liver stiffness measurement and NAFLD fibrosis score improves the noninvasive diagnostic accuracy for severe liver fibrosis in patients with nonalcoholic fatty liver disease. Liver Int. 2015;35(5):1566-73}}. במטופלים שבהם הבדיקה השנייה מעידה על סיכון נמוך לפיברוזיס מתקדם הגישה דומה למטופלים שבהם נמצא סיכון נמוך בבדיקת ה-FIB4 או ה-NFS. הגישה למטופלים עם עדות בבדיקה בלתי פולשנית לפיברוזיס מתקדם היא אינדיבידואלית ומותאמת לנתונים הקליניים של המטופל. כשהבדיקה המעידה על פיברוזיס מתקדם היא FIB4 או NFS, בחלק מן המקרים תבוצע בנוסף בדיקה לא פולשנית מקו שני (VCTE); עם זאת, לאור ספציפיות ו-PPV תת-אופטימלי של כל האמצעים הלא פולשניים, בהתחשב במשמעות של אבחנה של שחמת כבד למטופל ובמשאבים הנדרשים למעקב אחר מטופל עם שחמת ובהינתן המידע הנוסף שניתן לקבל מביופסיה, מקובל לנקוט בגישה מתירנית בהפניית מטופלים אלו לביופסיית כבד. | ||
| + | |||
| + | מצטברות עדויות שאמצעי אבחון לא פולשניים יכולים גם לנבא תוצאים קליניים (Clinical outcomes) במטופלים עם מכ"ש. בהקשר זה, השכיחות המצטברת (Cumulative probability) של תמותה או השתלת כבד נמצאה קשורה בציון ה-FIB4 ו-NFS{{הערה|שם=הערה27|Angulo P, Bugianesi E, Bjornsson ES, Charatcharoenwitthaya P, Mills PR, Barrera F, et al. Simple noninvasive systems predict long-term outcomes of patients with nonalcoholic fatty liver disease. Gastroenterology. 2013;145(4):782-9. e4}} עם ערך ניבויי דומה לשל ביופסיית כבד{{הערה|שם=הערה28|Hagstrom H, Nasr P. Ekstedt M, Hammar U, St3l P, Hultcrantz R, et al. Fibrosis stage but not NASH predicts mortality and time to development of severe liver disease in biopsyproven NAFLD. J Hepatol. 2017;67:1265-73}}; ערכי סף של ELF נמצאו מנבאים התקדמות לשחמת כבד ולאירוע דקומפנסציה של שחמת{{הערה|שם=הערה29|Sanyal AJ, Harrison SA, Ratziu V, Abdelmalek MF, Diehl AM, Caldwell S, et al. The natural history of advanced fibrosis due to nonalcoholic steatohepatitis: data from the simtuzumab trials. Hepatology. 2019;70(6):1913-27}} ו-VCTE נמצא מנבא שרידות כוללת (Overall survival) ושרידות ללא תמותה מסיבוכי מחלת כבד{{הערה|שם=הערה30|Boursier J, Vergniol J, Guillet A, Hiriart J-B, Lannes A, Le Bail B, et al. Diagnostic accuracy and prognostic significance of blood fibrosis tests and liver stiffness measurement by FibroScan in non-alcoholic fatty liver disease. Journal of hepatology. 2016;65(3):570-8}}. בעבודה נוספת הראו Sanyal וחבריו שערכי ELF ,NFS ,FIB4 ו-VCTE ב-baseline ושינוי בערכי NFS ו-VCTE לאורך תקופת המעקב קשורים לתוצאים קליניים הקשורים בשחמת: [[מיימת]], דמם משני ל[[יתר לחץ דם פורטלי]], [[אנצפלופתיה כבדית]], ציון 15 ≤ MELD או השתלת כבד או מוות{{הערה|שם=הערה31|Sanyal AJ, Anstee QM, Trauner MH, Lawitz EJ, Abdelmalek MF, Ding D, et al., editors. CIRRHOSIS REGRESSION IS ASSOCIATED WITH IMPROVED CLINICAL OUTCOMES IN PATIENTS WITH NONALCOHOLIC STEATOHEPATITIS (NASH). HEPATOLOGY; 2020: WILEY 111 RIVER ST, HOBOKEN 07030-5774, NJ USA}}. | ||
| + | |||
| + | == יחסי הגומלין בין כבד שומני וסוכרת == | ||
| + | מכ"ש וסכרת הן שתי מחלות מטבוליות שכיחות היכולות ללגרום באופן סינרגיסטי להגברת הסיכון לסיבוכים מטבוליים. גורמים המנבאים מעבר מהשמנה כבדית פשוטה (סטאטוזיס) למצב דלקתי-צלקתי בחולי מכ"ש הינם: גיל מבוגר, השמנת יתר, יחס ALT/AST גבוה מ-1 ונוכחות סוכרת{{הערה|שם=הערה32|Angulo P, Keach JC, Batts KP, Lindor KD. Independent predictors of liver fibrosis in patients with nonalcoholic steatohepati- tis. Hepatology. 1999,30(6):! 356-62}}. Younossi וחבריו העריכו על סמך מטא-אנליזה שמכ"ש מתקיימת בכ-55 אחוזים מחולי סוכרת{{הערה|שם=הערה33|Younossi ZM, Golabi P, de Avila L, Paik JM, Srishord M, Fukui N, et al. The global epidemiology of NAFLD and NASH in pa- tients with type 2 diabetes: A systematic review and meta-analysis. J Hepatol. 2019;71(4):793-801}}. הם גם מצאו שכיחות גבוהה יותר של דלקת וצלקת כבדית בחולים סוכרתיים עם כבד שומני, לעומת חולים ללא סוכרת עם כבד שומני. השכיחות של שחמת בחולים עם סוכרת וכבד שומני, הייתה 25 אחוזים לעומת 10 אחוזים בחולים עם כבד שומני ללא סוכרת. בנוסף, שיעורי התמותה מסיבות כבדיות היו גבוהים באופן משמעותי בחולי הסוכרת, לעומת חולים ללא סוכרת{{הערה|שם=הערה34|Younossi ZM, Gramlich T, Matteoni CA, Boparai N, McCullough AJ. Nonalcoholic fatty liver disease in patients with type 2 diabetes. Clin Gastroenterol Hepatol. 2004;2(3):262-5}}. מקובל לחשוב שהקשר בין שתי המחלות הוא דו-כיווני כאשר מכ"ש היא גורם סיכון לסיבוכים מטבוליים וסוכרת מסוג 2, באופן עצמאי מגורמי סיכון ידועים אחרים{{הערה|שם=הערה35|Targher G, Corey KE, Byrne CD, Roden M. The complex link between NAFLD and type 2 diabetes mellitus - mechanisms and treatments. Nat Rev Gastroenterol Hepatol. 2021}}. | ||
| + | |||
| + | מחקרים פרוספקטיביים מהשנים האחרונות תומכים בכך שכבד שומני מקדים סוכרת, אפילו באנשים ללא [[עודף משקל]]{{הערה|שם=הערה36|Fukuda T, Hamaguchi M, Kojima T, Hashimoto Y, Ohbora A, Kato T, et al. The impact of non-alcoholic fatty liver disease on incident type 2 diabetes mellitus in non-overweight individuals. Liver international: official journal of the International Associ- ation for the Study of the Liver. 2016;36(2):275-83}} ואף הועלתה הצעה כי נסיגה של כבד שומני מפחיתה סיכון להיארעות סוכרת{{הערה|שם=הערה37|Yamazaki H, Tsuboya T, Tsuji K, Dohke M, Maguchi H. Independent Association Between Improvement of Nonalcoholic Fatty Liver Disease and Reduced Incidence of Type 2 Diabetes. Diabetes Care. 2015;38(9):1673-9}}. לעומת זאת, נוכחות סוכרת בחולי מכ"ש נקשרה להתקדמות מהירה של פיברוזיס ותחלואה חוץ כבדית קשה יותר{{הערה|שם=הערה38|Mantovani A, Scorletti E, Mosca A, Alisi A, Byrne CD, Targher G. Complications, morbidity and mortality of nonalcoholic fatty liver disease. Metabolism. 2020;111 S:154170}}. | ||
| + | |||
| + | הסיבה לממצאים הקליניים וההיסטולוגים הקשים יותר בחולים סוכרתיים אינה ברורה, אך קשורה כנראה למצב דלקתי כרוני, עקה חמצונית ושחרור יתר של [[ציטוקינים]] הרעילים לכבד. ההסבר לכך הוא שהצטברות שומן בכבד מעכבת את העברת האותות הקשורים ל[[אינסולין - Insulin|אינסולין]] בתאי הכבד וגורמת לתנגודת כבדית לאינסולין עם פגיעה בדיכוי ייצור [[גלוקוז]] אנדוגני (גלוקונאוגנזה). חולים עם סוכרת ומחלת כבד נמצאים גם בסיכון גבוה יותר להתפתחות סרטן כבד ראשוני{{הערה|שם=הערה39|Bugianesi E, Vanni E, Marchesini G. NASH and the risk of cirrhosis and hepatocellular carcinoma in type 2 diabetes. Curr Diab Rep. 2007;7(3):175-80}}. | ||
| + | |||
| + | == כבד שומני כגורם סיכון למחלות לב == | ||
| + | מרבית החולים עם מכ"ש לא ימותו ממחלות כבד אלא ממחלות כלי דם ולב (מכ"ל) (Cardio-Vascular Diseases - CVD). מקובל לקבוע שכ-40 אחוזים ממקרי המוות בחולי מכ"ש הם תוצאה של מכ"ל (אחריהן: סרטן במקום השני, ומחלות כבד במקום שלישי){{הערה|שם=הערה38}}. | ||
| + | |||
| + | מספר מחקרים אפידמיולוגים הראו כי כבד שומני הוא גורם סיכון עצמאי ל[[מחלה טרשתית]]. בסקר שכלל 3,166 מטופלים הסובלים מסוכרת, נמצאה שכיחות גבוהה יותר ל[[מחלת לב כלילית]] (27 אחוזים לעומת 18 אחוזים), מחלת כלי דם מוחיים (20 אחוזים לעומת 13 אחוזים) ו[[מחלת כלי דם היקפית]] (15 אחוזים לעומת 10 אחוזים) בחולים הסובלים מסוכרת וכבד שומני לעומת חולים עם סוכרת בלבד{{הערה|שם=הערה40|Targher G, Bertolini L, Padovani R, Rodella S, Tessari R, Zenari L, et al. Prevalence of nonalcoholic fatty liver disease and its association with cardiovascular disease among type 2 diabetic patients. Diabetes Care. 2007;30(5):1212-8}}. במחקרים נוספים נמצאה עלייה בשכיחות פגיעה כלייתית ופגיעה עינית בחולי סוכרת עם כבד שומני לעומת חולי סוכרת ללא כבד שומני{{הערה|שם=הערה41|Targher G, Bertolini L, Rodella S, Zoppini G, Lippi G, Day C, et al. Non-alcoholic fatty liver disease is independently associated with an increased prevalence of chronic kidney disease and proliferative/laser-treated retinopathy in type 2 diabetic patients. Diabetologia. 2008;51(3):444-50}}. מחקרים נוספים תמכו בקשר בין כבד שומני להתפתחות מחלת לב, כולל מחקר פרמינגהם (Framingham) שהראה קשר לסמנים תת-קליניים של מחלת לב בקרב אנשים עם כבד שומני{{הערה|שם=הערה42|Mellinger JL, Pencina KM, Massaro JM, Hoffmann U, Seshadri S, Fox CS, et al. Hepatic steatosis and cardiovascular disease outcomes: An analysis of the Framingham Heart Study. Journal of hepatology. 2015;63(2):470-6}}. מחקר מטא-אנליזה שכלל 16 מחקרים עם 34,000 משתתפים הראה שמכ"ש קשור לאירועים קרדיווסקולריים קטלניים ולא קטלניים ושעוצמת הקשר התגברה עם עלייה בחומרת מכ"ש גם לאחר תקנון גורמי סיכון קלאסיים למכ"ל{{הערה|שם=הערה43|Targher G, Byrne CD, Lonardo A, Zoppini G, Barbui C. Non-alcoholic fatty liver disease and risk of incident cardiovascular disease: A meta-analysis. J Hepatol. 2016;65(3):589-600}}. | ||
| + | |||
| + | מחקר דומה, שבדק התפתחות מכ"ל בחולי מכ"ש שהוכחה בביופסיה, מצא אף הוא קשר מובהק בין חומרת הפיברוזיס הכבדי לבין התפתחות אירועים קרדיו-ווסקולרים{{הערה|שם=הערה44|Henson JB, Simon TG, Kaplan A, Osganian S, Masia R, Corey KE. Advanced fibrosis is associated with incident cardiovascular disease in patients with non-alcoholic fatty liver disease. Aliment Pharmacol Ther. 2020;51(7):728-36}}. למרות האמור לעיל, מחקר שבדק שכיחות [[אוטם לבבי|אוטמים לבביים]] ו[[שבץ מוחי|אירועי שבץ מוחי]] בחולי מכ"ש בקרב 18 מיליון מבוטחים בארבע מדינות אירופאיות לא מצא שכיחות מוגברת של אירועים כאלה לאחר תיקנון לגורמי סיכון מרובים. החוקרים מסכמים שהערכת גורמי סיכון למכ"ל בחולי מכ"ש חשובה, אך צריכה להיעשות בדומה לשאר האוכלוסייה. | ||
| + | שכיחות מכ"ש באוכלוסיית המחקר הייתה נמוכה יחסית למחקרים אחרים{{הערה|שם=הערה45|Alexander M, Loomis AK, van der Lei J, Duarte-Salles T, Prieto-Alhambra D, Ansell D, et aL Non-alcoholic fatty liver disease and risk of incident acute myocardial infarction and stroke: findings from matched cohort study of 18 million European adults. BM J. 2019,367:15367}}. | ||
| + | |||
| + | נראה כי פרופיל הליפידים הטרשתי, הנפוץ בחולים עם כבד שומני, הוא אחד הגורמים האחראים לקשר למחלות לב. הסבר אפשרי נוסף לקשר בין כבד שומני לפרופיל ליפידים טרשתי הוא שכבד שומני מוביל ל[[היפרגליקמיה]] ותנגודת לאינסולין. במצב זה קיים ייצור כבדי מוגבר של טריגליצרידים וחלקיקי [[VLDL]]{{כ}} (Very-Low-Density Lipoprotein) שמוביל באופן שניוני לרמות נמוכות של [[ליפופרוטאין בעל צפיפות גבוהה - High density lipoprotein - HDL|HDL{{כ}}]] (High-Density Lipoprotein) ועלייה בצפיפות חלקיקי ה-[[LDL|LDL{{כ}}]] (Low-Density Lipoprotein). בנוסף, הודגם כי חולי כבד שומני מאופיינים ב-Small Dense LDL שנחשב טרשתי במיוחד{{הערה|שם=הערה46|Siddiqui MS, Fuchs M, Idowu MO, Luketic VA, Boyett S, Sargeant C, et al. Severity of nonalcoholic fatty liver disease and progression to cirrhosis are associated with atherogenic lipoprotein profile. Clin Gastroenterol Hepatol. 2015;13(5):1000-8 e3}}, ואף נמצא קשר בין מידת חומרת הכבד השומני ומידת חומרת פרופיל הליפידים הטרשתי{{הערה|שם=הערה47|DeFilippis AP, Blaha MJ, Martin SS, Reed RM, Jones SR, Nasir K, et al. Nonalcoholic fatty liver disease and serum lipoproteins: the Multi-Ethnic Study of Atherosclerosis. Atherosclerosis. 2013;227(2):429-36}}. הסברים נוספים לקשר בין כבד שומני ומחלות לב טמונים בכך שכבד שומני הוא מצב דלקתי תת-קליני. במטא-אנליזה נראה כי כבד שומני מגביר את הסיכון למקרים חדשים של מחלת לב פי 2{{הערה|שם=הערה4}}. | ||
| + | |||
| + | מכ"ש נמצאה קשורה גם ל[[הפרעות קצב לבביות]] כולל [[פרפור עליות]], הפרעות קצב חדריות ו[[הארכת QT]] וכן להפרעות מבניות לבביות כגון הפרעה דיאסטולית והפרעות מסתמיות. ככל שהמכ"ש מתקדמת יותר, ובעיקר ככל שדרגת הפיברוזיס הכבדי חמורה יותר, כך גדל הסיכון למכ"ל ולסיבוכים לבביים והפרעות קצב. לממצאים אלה חשיבות רבה מכיוון שהם יכולים להסביר חלק מהקשר לתמותה עודפת ממכ"ל בחולים עם מכ"ש{{הערה|שם=הערה48|Targher G, Corey KE, Byrne CD. NAFLD, and cardiovascular and cardiac diseases: Factors influencing risk, prediction and treatment. Diabetes Metab. 2021;47(2):101215}}. | ||
| + | |||
| + | == טיפול == | ||
| + | עיקר הטיפול מתמקד במניעה ובטיפול בגורמי הסיכון למחלה הכוללים: השמנה, תנגודת לאינסולין, [[היפרטריגליצרידמיה|היפר-טריגליצרידמיה]], סוכרת ורמות גלוקוז מוגברות בצום (IFG{{כ}} - Impaired Fasting Glucose), וכן טיפול בגורמי הסיכון הנוספים למחלת לב כמו איזון [[כולסטרול - Cholesterol|כולסטרול]] אגרסיבי. | ||
| + | |||
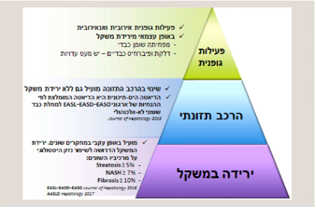
| + | לא נמצא טיפול תרופתי במכ"ש שהודגם במחקרים כיעיל באופן משכנע ושאומץ באופן גורף. מאחר ששינוי אורח חיים הכולל [[ירידה במשקל]] ו[[פעילות גופנית]] נמצא יעיל בהפחתת גורמי הסיכון למכ"ש, הוא הוגדר כקו הראשון של הטיפול במחלה. | ||
| + | |||
| + | === ירידת משקל === | ||
| + | קיימת הסכמה רחבה כי ירידת משקל מתונה של חצי קילו עד קילו בשבוע מסייעת בשיפור ואף נסיגה מוחלטת של השומן בכבד ואף מסייעת בנסיגה של דלקת וצלקת. כמו כן, ירידת משקל משפרת אנזימי כבד ולעיתים קרובות מביאה לחזרתם לתחום התקין. בניסוי קליני בו נעשה שינוי אורחות חיים במשך שנה הודגם יחס מנה תגובה בין מידת ירידת המשקל ומידת הפחתת בשומן בכבד (שנמדד ב-MRS): ירידת 1–5 אחוזים ממשקל הגוף הובילה להפחתה של 33 אחוזים מהשומן הכבדי, ירידת 5–10 אחוזים הובילה להפחתה של 65 אחוזים מהשומן הכבדי וירידת משקל של מעל 10 אחוזים הובילה להפחתה של 80 אחוזים מהשומן הכבדי{{הערה|שם=הערה49|Lazo M, Solga SF, Horska A, Bonekamp S, Diehl AM, Brancati FL, et al. The Effect of a 12-Month Intensive Lifestyle Intervention on Hepatic Steatosis in Adults with type 2 Diabetes. Diabetes Care. 2010}}. | ||
| + | |||
| + | בניסוי אחר שכלל אף הוא שינוי אורחות חיים במשך 12 חודשים, ירידת משקל של לפחות 7 אחוזים מהמשקל ההתחלתי הובילה לשיפור היסטולוגי משמעותי במדדי דלקת הכבדית כפי שנמדדה ב-NAS{{כ}} (NASH histological Activity Score), לגבי צלקת השיפור לא הגיע למובהקות סטטיסטית{{הערה|שם=הערה50|Promrat K, Kleiner DE, Niemeier HM, Jackvony E, Kearns M, Wands JR, et al. Randomized controlled trial testing the effects of weight loss on nonalcoholic steatohepatitis. Hepatology. 2010;51(1):121-9}}. | ||
| + | |||
| + | בניסוי אחר בו הושגה ירידת משקל של 10 אחוזים בממוצע ממשקל הגוף, נצפה גם שיפור מובהק בצלקת לאחר 6 חודשים{{הערה|שם=הערה51|Vilar Gomez E, Rodriguez De Miranda A, Gra Dramas B, Arus Soler E, Llanio Navarro R, Calzadilla Bertot L, et al. Clinical trial: a nutritional supplement Viusid, in combination with diet and exercise, in patients with nonalcoholic fatty liver disease. Aliment Pharmacol Ther. 2009;30(10):999-1009}}. מחקר נוסף גדול תומך באפשרות של שיפור הצלקת. המחקר נערך בקובה על 261 חולי כש"ד שביצעו ביופסיות כבד חוזרות לאחר 52 שבועות של שינוי אורחות חיים וירידת משקל. כל החולים שרזו בלפחות 10 אחוזים ממשקלם ההתחלתי שיפרו את רמת הדלקת שלהם (NAFLD activity score), ל-90 אחוזים הייתה היעלמות של הכש"ד, ול-45 אחוזים הייתה רגרסיה של צלקת{{הערה|שם=הערה52|Vilar-Gomez E, Martinez-Perez Y, Calzadilla-Bertot L, Torres-Gonzalez A, Gra-Oramas B, Gonzalez-Fabian L, et al. Weight Loss Through Lifestyle Modification Significantly Reduces Features of Nonalcoholic Steatohepatitis. Gastroenterology. | ||
| + | |||
| + | 2015;149(2):367-78e5; quiz e14-5}}. | ||
| + | |||
| + | ירידה במשקל מומלצת באמצעות [[דיאטה]] מבוקרת, הבחירה בין דיאטה דלת שומן ודיאטה דלת פחמימות יכולה להיות לפי העדפות המטופל. דיאטה דלת פחמימות במשך חצי שנה (אך גם דלה בשומן רווי ומושתת על עקרונות אכילה בריאה) הובילה לירידת משקל זהה לזו של דיאטה דלת שומן סטנדרטית ולהפחתה זהה בשומן הכבדי וברמות ALT בדם{{הערה|שם=הערה53|Haufe S, Engeli S, Kast P, Bohnke J, Utz W, Haas V, et al. Randomized comparison of reduced fat and reduced carbohydrate hypocaloric diets on intrahepatic fat in overweight and obese human subjects. Hepatology.53(5):1504-14}}. מטא-אנליזה שסיכמה את המחקרים המעטים שהשוו דיאטה סטנדרטית לדיאטה דלת פחמימות הראתה גם היא שאין הבדל ביעילותן בהפחתת שומן כבדי{{הערה|שם=הערה54|Musso G, Cassader M, Rosina F, Gambino R. Impact of current treatments on liver disease, glucose metabolism and cardiovascular risk in non-alcoholic fatty liver disease (NAFLD): a systematic review and meta-analysis of randomised trials. Diabetologia. 2012;55(4):885-904}}. בכל המחקרים המוזכרים נעשתה דיאטה מתונה ומאוזנת לפי ההמלצות התזונתיות המקובלות ובשילוב עם פעילות גופנית מתונה. | ||
| + | |||
| + | בדף עמדה שפורסם על ידי האיגוד האירופאי לחקר הכבד EASL{{כ}} (European Association for the Study of the Liver){{הערה|שם=הערה55|European Association for the Study of the Liver, European Association for the Study of Diabetes, European Association for the Study of Obesity. EASL-EASD-EASO Clinical Practice Guidelines for the Management of Non-Alcoholic Fatty Liver Disease J Hepatol. 2016;64(6):1388-402}}, הומלצה ירידת משקל של 7 אחוזים כטיפול ב-מכ"ש/ כש"ד, כפי שמומלץ על ידי איגודים בינלאומיים אחרים לקבלת תועלת בריאותית{{הערה|שם=הערה17}}. בהנחיות לטיפול בכבד שומני שפורסמו על ידי איגוד הכבד האמריקאי, AASLD{{כ}} (American Association for the Study of Liver Diseases), מושם דגש מיוחד על אורח חיים בריא ומסוכם כי ירידת משקל לבד או בשילוב עם פעילות גופנית מורידה שומן כבדי, כאשר ירידת 3–5 אחוזים לפחות ממשקל התחלתי דרושה לשם כך. עם זאת, ירידת משקל גדולה יותר המתקרבת ל-7–10 אחוזים דרושה לשיפור הדלקת הכבדית ופיברוזיס (NAFLD activity score<u>)</u>{{הערה|שם=הערה12}}. המלצות דומות ניתן למצוא בקווים המנחים שפרסם ה-ESPEN{{כ}} (The European Society for Clinical Nutrition and Metabolism) ב-2019{{הערה|שם=הערה56|Plauth M, Bernal W, Dasarathy S, Merli M, Plank LD, Schutz T, et al. ESPEN guideline on clinical nutrition in liver disease. Clin Nutr. 2019}}. | ||
| + | |||
| + | === הרכב הדיאטה === | ||
| + | על סמך הידע שנצבר ממחקרים הן בבעלי חיים והן בבני אדם נראה כי שינוי הרכב הדיאטה יכול לסייע בטיפול בכבד שומני גם ללא ירידת משקל. | ||
| + | |||
| + | === סוג השומן === | ||
| + | להרכב חומצות השומן בדיאטה השפעה על מטבוליזם שומן בכבד. בניסויי האכלה רנדומליים בהם נעשתה האכלת יתר בשומן רב בלתי רווי או בשומן רווי נראה כי יש להם השפעה שונה על הכבד: רק הדיאטה עם השומן הרווי גרמה לעליית שומן כבדי וויסרלי, למרות עליית משקל דומה{{הערה|שם=הערה57|Rosqvist F, Iggman D, Kullberg J, Cedernaes J, Johansson HE, Larsson A, et al. Overfeeding polyunsaturated and saturated fat causes distinct effects on liver and visceral fat accumulation in humans. Diabetes. 2014;63(7):2356-68}}{{הערה|שם=הערה58|Rosqvist F, Kullberg J, Stahlman M, Cedernaes J, Heurling K, Johansson HE, et al. Overeating Saturated Fat Promotes Fatty Liver and Ceramides Compared With Polyunsaturated Fat: A Randomized Trial. J Clin Endocrinol Metab. 2019;104(12):6207-19}}. באופן דומה, בניסוי קליני אקראי בן 10 שבועות דיאטה איזוקלורית עשירה באומגה 6 הפחיתה שומן כבדי בעוד שדיאטה איזוקלורית עשירה בשומן רווי העלתה שומן כבדי{{הערה|שם=הערה59|Bjermo H, Iggman D, Kullberg J, Dahlman I, Johansson L, Persson L, et al. Effects of n-6 PUFAs compared with SFAs on liver fat, lipoproteins, and inflammation in abdominal obesity: a randomized controlled trial. Am J Clin Nutr. 2012;95(5):1003-12}}. בניסוי קליני אקראי בן 3 שבועות שנערך, שומן רווי העלה את כמות השומן הכבדי אף יותר מכמות איזוקלורית של סוכר{{הערה|שם=הערה60|Luukkonen PK, Sadevirta S, Zhou Y, Kayser B, Ali A, Ahonen L, et al. Saturated Fat Is More Metabolically Harmful for the Human Liver Than Unsaturated Fat or Simple Sugars. Diabetes Care. 2018;41(8):1732-9}}. כמו כן, בעבודה שנערכה בישראל בקרב אוכלוסייה כללית נמצא כי לחולי מכ"ש צריכה מופרזת של בשר לסוגיו ללא קשר ל-BMI ונטייה לצריכה נמוכה של דגים העשירים באומגה 3{{הערה|שם=הערה61|Zelber-Sagi S, Nitzan-Kaluski D, Goldsmith R, Webb M, Blendis L, Halpern Z, et al. Long term nutritional intake and the risk for non-alcoholic fatty liver disease (NAFLD): a population based study. J Hepatol. 2007;47(5):711-7}}. | ||
| + | |||
| + | === פרוקטוז ומשקאות קלים ממותקים בסוכר או פרוקטוז === | ||
| + | סוכר השולחן, הסוכרוז, הוא דו-סוכר המורכב מגלוקוז ופרוקטוז. בעבודה שנערכה בישראל נמצא כי חולי מכ"ש צורכים באופן מובהק כמות גדולה יותר של משקאות קלים הממותקים בסוכר וכי הקשר עצמאי מ-BMI{{הערה|שם=הערה61}}. בהתבסס על הקשר בין צריכה גבוהה של פרוקטוז עם השמנה וסוכרת וכן ההשפעה על הגברת ייצור השומן הכבדי שיש לדיאטות עתירות פרוקטוז נראה כי חולי מכ"ש צריכים להגביל צריכת פרוקטוז או סירופ תירס עתיר פרוקטוז (High fructose corn syrup). לכן כדאי להגביל צריכת משקאות קלים, מיצי פירות גם אם טבעיים ומזון עשיר בסוכרוז (דו סוכר המורכב מגלוקוז ופרוקטוז). במחקר רחב היקף שכלל 341 חולי מכ"ש שעברו ביופסית כבד נראה כי צריכה יומית של משקאות מכילי פרוקטוז קשורה בסיכון מוגבר (פי 2.5) לכש"ד גם לאחר תקנון לגורמי סיכון אחרים כמו BMI, תנגודת לאינסולין, סך צריכה קלורית ורמות ליפידים ו[[חומצה אורית]] בנסיוב. מכאן שלפרוקטוז, מעבר להשפעה הליפוגנית הידועה שלו, עשויה להיות גם השפעה פרו-דלקתית ופרו-פיברוטית{{הערה|שם=הערה62|Abdelmalek MF, Suzuki A, Guy C, Unalp-Arida A, Colvin R, Johnson RJ, et al. Increased fructose consumption is associated with fibrosis severity in patients with nonalcoholic fatty liver disease. Hepatology. 2010;51(6):1961-71}}. מחקר דומה בקרב 271 ילדים הסובלים מהשמנה הראה תוצאות דומות: צריכת פרוקטוז הייתה קשורה באופן עצמאי לכש"ד שנראה בביופסית כבד{{הערה|שם=הערה63|Mosca A, Nobili V, De Vito R, Crudele A, Scorletti E, Villani A, et al. Serum uric acid concentrations and fructose consumption are independently associated with NASH in children and adolescents. J Hepatol. 2017;66(5):1031-6}}. | ||
| + | |||
| + | מספר לא מבוטל של מחקרים אפידמיולוגיים הדגימו קשר בין צריכת משקאות ממותקים ובין כבד שומני לא אלכוהולי{{הערה|שם=הערה61}}{{הערה|שם=הערה64|Ouyang X, Cirillo P, Sautin Y, McCall S, Bruchette JL, Diehl AM, et al. Fructose consumption as a risk factor for non-alcoholic fatty liver disease. J Hepatol. 2008;48(6):993-9}}{{הערה|שם=הערה65| Assy N, Nasser G, Kamayse I, Nseir W, Beniashvili Z, Djibre A, et al. Soft drink consumption linked with fatty liver in the absence of traditional risk factors. Can J Gastroenterol. 2008;22(10):811 -6}}{{הערה|שם=הערה66|Abid A, Taha O, Nseir W, Farah R, Grosovski M, Assy N. Soft drink consumption is associated with fatty liver disease indepen- dent of metabolic syndrome. J Hepatol. 2009;51 (5):918-24}}. קשר כזה הודגם אף במחקר פרמינגהם, שכלל 2,634 איש עם בדיקת CT לאבחון כבד שומני. רמות אנזים הכבד ALT נמדדו אצל 5,908 נבדקים. קשר מנה תגובה ברור הודגם בין צריכת משקאות מכילי סוכר ובין כבד שומני, עם עליית סיכון ב-55 אחוזים בקרב אנשים ששתו משקאות אלו על בסיס יומי לעומת אלו שלא שתו כלל. ממצאים דומים נראו גם לגבי רמות ALT. לעומת זאת, לא נראה קשר בין משקאות דיאט (עם ממתיקים מלאכותיים) ובין כבד שומני או ALT{{הערה|שם=הערה67|Ma J, Fox CS, Jacques PF, Speliotes EK, Hoffmann U, Smith CE, et al. Sugar-sweetened beverage, diet soda, and fatty liver disease in the Framingham Heart Study cohorts. J Hepatol. 2015;63(2):462-9}}. ממצאים אלו נתמכים בתוצאות ניסוי קליני אקראי בו ניתן 1 ליטר של קולה או דיאט קולה או חלב ליום במשך חצי שנה. אף על פי שחלב וקולה מכילים אותה כמות קלוריות, רק בקבוצת הקולה נצפתה עלייה בכמות השומן הכבדי (לפי הדמיה באמצעות מכשיר הדמיה מגנטית MRS), כלומר ההשפעה טמונה בסוכר שיש במשקה הממותק ולא בהכרח בקלוריות עצמן. הקבוצה שטופלה בדיאט קולה לא הראתה עלייה בשומן הכבדי{{הערה|שם=הערה68|Maersk M, Belza A, Stodkilde-Jorgensen H, Ringgaard S, Chabanova E, Thomsen H, et al. Sucrose-sweetened beverag- es increase fat storage in the liver, muscle, and visceral fat depot: a 6-mo randomized intervention study. Am J Clin Nutr. 2012;95(2):283-9}}. מאידך, ישנם ניסויים קליניים שמראים שהפחתת צריכת סוכר מובילה להפחתת שומן כבדי תוך זמן קצר של מספר שבועות{{הערה|שם=הערה69|Schwarz JM, Noworolski SM, Erkin-Cakmak A, Korn NJ, Wen MJ, Tai VW, et al. Effects of Dietary Fructose Restriction on Liver Fat, De Novo Lipogenesis, and Insulin Kinetics in Children With Obesity. Gastroenterology. 2017,T53(3):743-52}}{{הערה|שם=הערה70|Schwimmer JB, Ugalde-Nicalo P, Welsh JA, Angeles J E, Cordero M, Harlow KE, et al. Effect of a Low Free Sugar Diet vs Usual Diet on Nonalcoholic Fatty Liver Disease in Adolescent Boys: A Randomized Clinical Trial. Jama. 2019;321(3):256-65}}. | ||
| − | + | באופן מדאיג, השפעת הפרוקטוז מתחילה כבר מגיל צעיר. פעוטות שבגיל שנה שתו יותר משני משקאות ממותקים ביום היו בסיכון גבוה לפתח מכ"ש בילדות (בגיל 10) בהשוואה לאלה ששתו פחות ממשקה אחד ביום, ללא תלות במדד מסת הגוף{{הערה|שם=הערה71|Geurtsen ML, Santos S, Gaillard R, Felix JF, Jaddoe VWV. Associations Between Intake of Sugar-Containing Beverages in Infancy With Liver Fat Accumulation at School Age. Hepatology. 2020}}. | |
| − | == | + | === מזון מהיר ואולטרא מעובד === |
| + | אין כמעט מחקרים שבחנו את הקשר בין צריכת מזון אולטרא מעובד כקבוצת מזון ובין כבד שומני, אולם זהו מזון (או שתייה מתוקה) שהוא לרוב עתיר סוכר, שומן רווי ודל ב[[סיבים תזונתיים]] ו[[ויטמינים]] ולכן אינו מומלץ לחולים עם כבד שומני. נדגמים בריאים שצרכו במסגרת ניסוי קליני לפחות 2 ארוחות מזון מהיר ביום במשך 4 שבועות, עלו במשקלם ב-5–15 אחוזים וכמות הטריגליצרידים בכבד עלתה אף היא. רמות ALT עלו בממוצע מ-22 ל-97 U/L (יחידות לליטר) ול-11 מתוך 18 הנבדקים היו באופן עקבי רמות ALT מעל הנורמה מהשבוע הראשון ועד לתום ההתערבות{{הערה|שם=הערה72|Kechagias S, Ernersson A, Dahlqvist O, Lundberg P, Lindstrom T, Nystrom FH. Fast-food-based hyper-alimentation can induce rapid and profound elevation of serum alanine aminotransferase in healthy subjects. Gut. 2008;57(5):649-54}}. מחקרים שנעשו הדגימו קשר בין צריכה גבוהה של חלבון מהחי ובאופן ספציפי יותר בשר אדום ומעובד ובין כבד שומני בקרב אוכלוסייה כללית{{הערה|שם=הערה73|Alferink LJ, Kiefte-de Jong JC, Erler NS, Veldt BJ, Schoufour JD, de Knegt RJ, et al. Association of dietary macronutrient composition and non-alcoholic fatty liver disease in an ageing population: the Rotterdam Study. Gut. 2018}}{{הערה|שם=הערה74|Baratta F, Pastori D, Polimeni L, Bucci T, Ceci F, Calabrese C, et al. Adherence to Mediterranean Diet and Non-Alcoholic Fatty Liver Disease: Effect on Insulin Resistance. Am J Gastroenterol. 2017;112(12):1832-9}}{{הערה|שם=הערה75|Zelber-Sagi S, Ivancovsky-Wajcman D, Fliss Isakov N, Webb M, Orenstein D, Shibolet O, et al. High red and processed meat consumption is associated with non-alcoholic fatty liver disease and insulin resistance. J Hepatol. 2018;68(6):1239-46}}. בנוסף, צריכה גבוהה של בשר אדום ומעובד נמצאה קשורה במטא-אנליזות גם לרמות גלוקוז מוגברות, סוכרת ולמחלות לב ולכן אינה מומלצת באופן כללי{{הערה|שם=הערה76|Mozaffarian D. Dietary and Policy Priorities for Cardiovascular Disease, Diabetes, and Obesity: A Comprehensive Review. Circulation. 2016,T33(2):187-225}}. ייתכן ולא מדובר רק במזון מהיר, אלא גם בדפוס אכילה מהיר. מחקר חתך חדש בקרב 149 גברים ו-159 נשים עם סוכרת מסוג 2 מצא כי התנהגות של אכילה בקצב מהיר בקרב גברים הייתה קשורה עם עלייה בסיכוי למכ"ש{{הערה|שם=הערה77|Takahashi F, Hashimoto Y, Kawano R, Kaji A, Sakai R, Kawate Y, et al. Eating Fast Is Associated with Nonalcoholic Fatty Liver Disease in Men But Not in Women with Type 2 Diabetes: A Cross-Sectional Study. Nutrients. 2020,8)12־)}}, ממצאים אלה צריכים להיתמך במחקרים נוספים. | ||
| − | + | === דיאטה ים תיכונית ותבניות אכילה בריאה דומות === | |
| + | מחקרים פרוספקטיביים גדולים תומכים בקשר בין תבניות אכילה בריאות כמו [[דיאטה ים תיכונית]] ודיאטות דומות ומניעת מכ"ש. התמדה לאורך זמן חשובה מאוד לשימור התועלת{{הערה|שם=הערה78|Maskarinec G, Lim U, Jacobs S, Monroe KR, Ernst T, Buchthal SD, et al. Diet Quality in Midadulthood Predicts Visceral Adi- posity and Liver Fatness in Older Ages: The Multiethnic Cohort Study. Obesity (Silver Spring). 2017;25(8):1442-50}}{{הערה|שם=הערה79|Ma J, Hennein R, Liu C, Long MT, Hoffmann U, Jacques PF, et al. Improved Diet Quality Associates With Reduction in Liver Fat, Particularly in Individuals With High Genetic Risk Scores for Nonalcoholic Fatty Liver Disease. Gastroenterology. 2018;155(1 ):107-17}}. בניסוי קליני אקראי שנמשך שנה וחצי בקרב 278 נבדקים, דיאטה ים תיכונית-דלת פחממות הפחיתה שומן כבדי יותר מדיאטה דלת שומן למרות ירידת משקל דומה בשתי הדיאטות{{הערה|שם=הערה80|Gepner Y, Shelef I, Schwarzfuchs D, Zelicha H, Tene L, Yaskolka Meir A, et al. Effect of Distinct Lifestyle Interventions on Mobilization of Fat Storage Pools: CENTRAL Magnetic Resonance Imaging Randomized Controlled Trial. Circulation. 2018;137(11):1143-57}}. | ||
| − | + | שומן חד בלתי רווי (n-9 oleic acid), שנמצא בכמות גדולה בשמן זית והוא אחד ממאפייניה הבולטים של הדיאטה הים תיכונית, מודגם יותר ויותר כבעל תפקיד חשוב בפרופיל המטבולי בבני אדם{{הערה|שם=הערה81|Grosso G, Mistretta A, Frigiola A, Gruttadauria S, Biondi A, Basile F, et al. Mediterranean diet and cardiovascular risk factors: a systematic review. Crit Rev Food Sci Nutr. 2014;54(5):593-610}}. מקורות נוספים לשומן חד בלתי רווי הם אגוזים ואבוקדו. לשומן זה השפעה מיטיבה על פרופיל שומנים. | |
| − | + | במחקרים בבעלי חיים שמן זית הפחית הצטברות טריגליצרידים בכבד{{הערה|שם=הערה82|Hussein O, Grosovski M, Lasri E, Svalb S, Ravid U, Assy N. Monounsaturated fat decreases hepatic lipid content in non-alco- holic fatty liver disease in rats. World journal of gastroenterology: WJG. 2007;13(3):361-8}}. הדיאטה הים תיכונית היא תבנית אכילה המאופיינת באכילה מרובה של שומן חד בלתי רווי, בעיקר שמן זית ואגוזים, אכילה מרובה של ירקות ודגים העשירים באומגה 3 ומיעוט אכילה של בשר אדום ודברי מתיקה. בשני ניסויים קליניים אקראיים נמצא כי אכילה לפי עקרונות הדיאטה הים תיכונית במשך מספר שבועות מובילה לירידה משמעותית בשומן הכבדי בקרב חולים עם כבד שומני, יותר מדיאטה דלת שומן רגילה. ההשפעה הייתה דומה בחולי סוכרת עם כבד שומני, שם הושם דגש על צריכה מרובה של שומן חד בלתי רווי{{הערה|שם=הערה83|Bozzetto L, Prinster A, Annuzzi G, Costagliola L, Mangione A, Vitelli A, et al. Liver fat is reduced by an isoenergetic MUFA diet in a controlled randomized study in type 2 diabetic patients. Diabetes Care. 2012;35(7):1429-35}}{{הערה|שם=הערה84|Trovato FM, Catalano D, Martines GF, Pace P, Trovato GM. Mediterranean diet and non-alcoholic fatty liver disease.: The need of extended and comprehensive interventions. Clin Nutr. 2014}}{{הערה|שם=הערה85|Ryan MC, Itsiopoulos C, Thodis T, Ward G, Trost N, Hofferberth S, et al. The Mediterranean diet improves hepatic steatosis and insulin sensitivity in individuals with non-alcoholic fatty liver disease. J Hepatol. 20l3;59(1):138-43}}. בשני הניסויים הדיאטות היו איזוקלוריות ולא חלה ירידת משקל משמעותית עם אף אחת מהדיאטות, כך שהשינוי בשומן הכבדי היה ללא קשר לירידת משקל. שני המחקרים לא כללו ביופסיית כבד ולכן אין אפשרות להעריך את השפעת הדיאטה הים תיכונית על דלקת וצלקת. כמו כן, ניסויים אלו הם בעלי מדגם קטן וקצרי טווח ולכן דרוש מחקר נוסף בנושא. עם זאת, וגם לאור יתרונותיה הברורים של דיאטה ים תיכונית בירידת משקל, הפחתת הסיכון לסוכרת ומחלות לב, ממליץ האיגוד האירופאי{{הערה|שם=הערה55}} על דיאטה ים תיכונית כאחת הדרכים לטפל בכבד שומני (ראה טבלה מספר 2). גם בהנחיות של ה-ESPEN משנת 2019 ניתנה המלצה לדיאטה ים תיכונית על מנת להפחית שומן כבדי ולשפר רגישות לאינסולין{{הערה|שם=הערה56}}. | |
| − | + | מחקר עוקבה בקרב אוכלוסייה קשישה מצא כי היענות לדפוס האכילה המומלץ של ה-WHO (World Health Organization, שדומה בעקרונותיו לדיאטה הים תיכונית) הייתה קשורה עם רגרסיה של השומן הכבדי. היענות לדפוס אכילה זה נחשבת כעמידה בקריטריונים הבאים: | |
| − | + | # צריכת ירקות ופירות של 400 גרם/יום לפחות | |
| + | # צריכה של פחות מ-10 גרם סוכר מוסף/יום | ||
| + | # אחוז צריכת קק"ל (קילו קלוריות) משומן מסך קק"ל נמוך מ-30 אחוזים | ||
| + | # אחוז צריכת קק"ל משומן רווי מסך הקק"ל נמוך מ-10 אחוזים | ||
| + | # אחוז צריכת קק"ל מ[[שומן טרנס]] מסך קק"ל נמוך מ-1 אחוזים | ||
| + | # צריכת מלח נמוכה מ-5 גרם/יום{{הערה|שם=הערה86|Alferink LJM, Erler NS, de Knegt RJ, Janssen HLA, Metselaar HJ, Darwish Murad S, et al. Adherence to a plant-based, high-fi- bre dietary pattern is related to regression of non-alcoholic fatty liver disease in an elderly population. Eur J Epidemiol. 2020}} | ||
| − | = | + | {| class="wikitable" |
| + | |+טבלה 1. סיכום המלצות הוועדה לטיפול באורחות חיים בכבד שומני לא אלכוהולי לפי רמת הוכחה וחוזק המלצה: A משמעו ניסויים קליניים, B משמעו מחקרים תצפיתיים | ||
| + | |המלצות הוועדה | ||
| + | |חוזק ההמלצה | ||
| + | |רמת ההוכחה | ||
| + | |- | ||
| + | |מומלצת ירידת משקל של לפחות ממשקל התחלתי להפחתת השומן הכבדי ולהורדת אנזימי כבד | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |מומלצת ירידת משקל של לפחות 7–10 אחוזים להפחתת דלקת ופיברוזיס כבדי | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |ניתן לבצע דיאטה דלת פחמימות (בעלת הרכב בריא כולל הגבלת שומן רווי) כחלק מהדיאטות המוצעות לירידת משקל בכבד שומני | ||
| + | |lib | ||
| + | |A | ||
| + | |- | ||
| + | |מומלצת הפחתת צריכת סוכר מוסף והימנעות משתייה ממותקת בסוכר או פרוקטוז לטיפול בכבד שומני | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |מומלצת דיאטה ים תיכונית לטיפול בכבד שומני (גם ללא ירידת משקל וגם במטופלים במשקל תקין) | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |רצוי להפחית שומן רווי לפי ההמלצות לכלל האוכלוסייה על פי עקרונות איגוד הלב האמריקאי, למניעת נזק כבדי ותחלואה לבבית | ||
| + | |Ila | ||
| + | |A | ||
| + | |- | ||
| + | |רצוי להפחית שומן טרנס לפי ההמלצות לכלל האוכלוסייה על פי עקרונות איגוד הלב האמריקאי, למניעת נזק כבדי ותחלואה לבבית | ||
| + | |Ila | ||
| + | |B | ||
| + | |- | ||
| + | |ניתן לצרוך כולסטרול במידה מתונה כמו ההמלצה לכלל האוכלוסייה (קשור לנזק כבדי וסרטן כבד במחקרי חיות ובמחקרים אפידמיולוגיים) | ||
| + | |lib | ||
| + | |B | ||
| + | |- | ||
| + | |מומלצת הגברת פעילות גופנית והפחתת "זמן יושבני" להפחתת שומן כבדי | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |רצוי לבצע פעילות גופנית להפחתת NASH ופיברוזיס | ||
| + | |Ila | ||
| + | |B | ||
| + | |- | ||
| + | |מומלץ לבצע פעילות גופנית אירובית להפחתת שומן כבדי | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |מומלץ לשלב פעילות גופנית מסוג אימון התנגדות כחלק מהאימון הגופני או לבצע אותה בלעדית אם לא ניתן לבצע פעילות אירובית מסיבה כלשהי | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |מומלצות תוכניות מובנות לשינוי אורחות חיים לדיאטה בריאה ופעילות גופנית סדירה לחולים עם כבד שומני | ||
| + | |1 | ||
| + | |A | ||
| + | |- | ||
| + | |ניתן לשקול תוספי אומגה 3 להפחתת טרינליצרידים ושומן כבדי אך לא לטיפול בדלקת או פיברוזיס. בעיקר ניתן לשקול באנשים שאינם אוכלים דגים | ||
| + | |lib | ||
| + | |A | ||
| + | |} | ||
| − | + | === מיקרונוטריינטים, פירות וירקות === | |
| − | + | תזונה עשירה בפירות וירקות קשורה עם סיכון נמוך למחלות לב בחולי מכ"ש{{הערה|שם=הערה87|Godos J, Federico A, Dallio M, Scazzina F. Mediterranean diet and nonalcoholic fatty liver disease: molecular mechanisms of protection. Int J Food Sci Nutr. 2017;68(1 ):18-27}}, וזאת הודות לתכולה גבוהה של סיבים תזונתיים, ויטמינים ונוגדי חמצון שאינם ויטמינים כמו פוליפנולים. במחקרים אפידימיולוגיים ישנן ראיות לקשר בין צריכת פירות וירקות ומכ"ש. במחקר חתך בקרב 977 יפנים נמצא קשר עצמאי בין צריכת פירות וירקות לבין מכ"ש, ללא תלות במדד מסת גוף. צריכת הפירות באוכלוסייה זו היא נמוכה ועומדת על 1–3 מנות פרי ביום. משמעות הדבר היא כי אין צורך בהגבלה נוקשה של כמות הפירות היומית במטרה להקטין את צריכת הפרוקטוז בחולי מכ"ש וכי ניתן לשלבם בתזונה מאוזנת בכמות סבירה כמקור לסיבים וויטמינים. מחקר חתך נוסף נערך בקרב 789 ישראליים שעברו בדיקת [[אולטראסאונד]] לאבחון מכ"ש ובדיקת פיברוטסט (סמנים בסדום) לאיתור חשד לדלקת ופיברוזיס כבדיים, ובחן את הקשר בין צריכת ויטמינים [[ויטמין - Vitamin - E|E]] ו-[[ויטמין Ascorbic acid - C|C]] מהתזונה לבין מכ"ש{{הערה|שם=הערה88| Ivancovsky-Wajcman D, Fliss-lsakov N, Salomone F, Webb M, Shibolet 0, Kariv R, et al. Dietary vitamin E and C intake is inversely associated with the severity of nonalcoholic fatty liver disease. Digestive and Liver Disease. 20l9;51(12):l698-705}}. נמצא כי צריכה גבוהה של ויטמינים אלו נמצאה קשורה עם ירידה בסיכוי להתפתחות דלקת (כש"ד). המקורות התזונתיים הטובים ביותר של הוויטמינים האלו הם אגוזים, גרעינים, שמנים צמחיים, פירות וירקות. מחקרים נוספים הדגישו את חשיבותם של פוליפנולים, נוגדי חמצון חזקים שאינם וויטמינים ומצויים במזונות צמחיים כגון פירות יער, אגוזים, דגנים מלאים, וכן מצויים בקפה ותה. נמצא קשר מגן בין צריכה גבוהה של פוליפנולים ומכ"ש ותנגודת לאינסולין בתקנון לגיל, מגדר, מדד מסת גוף ומשתני תזונה ואורח חיים נוספים{{הערה|שם=הערה89|Salomone F l-WD, Fliss-lsakov N, Webb M, Grosso G, Godos J, Galvano F, Shibolet O, Kariv R, Zelber-Sagi S.. Higher phenolic acid intake independently associates with lower prevalence of insulin resistance and non-alcoholic fatty liver disease. JHEP Reports. 2020}}. | |
| − | |||
| − | + | === סיכום הטיפול התזונתי === | |
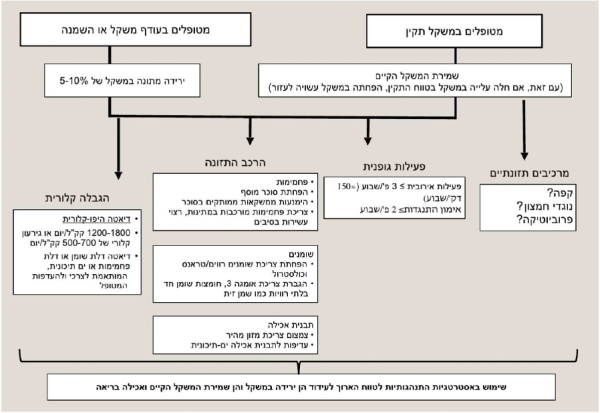
| + | תזונה הודגמה באופן ברור כבעלת קשר הדוק עם מכ"ש וכש"ד הן בחיות מעבדה והן בבני אדם ולכן מהווה אמצעי עיקרי לטיפול. ניסויים קליניים מן השנים האחרונות סייעו רבות בהבנת התועלת הגלומה בדיאטה מאוזנת ומתונה, לירידת משקל ופעילות גופנית כטיפול בכבד שומני. רוב המחקרים מעידים על שיפור בשומן הכבדי ובאנזימי הכבד עם ירידת משקל של כ-5 אחוזים. ירידה של כ-7 אחוזים ממשקל התחלתי דרושה על מנת לשפר דלקת וירידת משקל של כ-10 אחוזים מובילה אולי לירידה בצלקת. יש חשיבות רבה לקביעת יעדים ברי השגה לירידת משקל למניעת תסכול ו"שבירת דיאטה" בקרב המטופלים. לפיכך, הדגשת יעילות ירידת משקל צנועה יחסית של 5–10 אחוזים ממשקל הגוף כמובילה לשיפור משמעותי ולעיתים אף לנסיגה מלאה של הכבד השומני עשויה לעודד היענות והתמדה בשינוי אורחות החיים. כמו כן, חיזוקים חיוביים צריכים להינתן על כל שיפור בהרכב צריכת המזון ותוספת של פעילות גופנית, החשובים בפני עצמם, ולא רק על ירידת משקל. חולי הכבד השומני, בין אם בעודף משקל או במשקל תקין, צריכים להבין את חשיבות הרכב התזונה הנכון עבורם הכולל הפחתת שומן רווי וטרנס, צמצום סוכר מוסף והימנעות משתייה הממותקת בסוכר או בפרוקטוז כולל מיצי פירות. גם פעילות גופנית חשובה לכל החולים ללא קשר למשקלם, וגם תוספת קטנה עשויה להוביל לשיפור קליני. | ||
| − | + | טבלאות 1,2 מתארות את המלצות עמותת עתיד (עמותת הדיאטניות בישראל) שנכתבו על-ידי פורום גסטרו וכבד של עתיד ופורסמו בשנת 2019 ועודכנו בעת כתיבת הפרק. | |
| − | ===כבד | + | == פעילות גופנית == |
| + | במחקר חתך שבוצע בישראל על תת-מדגם של סקר הבריאות והתזונה הלאומי הראשון, מב"ת, (350 איש) נמצא כי נדגמים שאובחנו באולטרסאונד כחולים במכ"ש בצעו פחות פעילות גופנית בשעות הפנאי לעומת כאלו שאובחנו כבעלי כבד תקין. הקשר בין פעילות אימון התנגדות שבונה שריר ומכ"ש נותר מובהק גם בתקנון ל-BMI{{הערה|שם=הערה90|Zelber-Sagi S, Nitzan-Kaluski D, Goldsmith R, Webb M, Zvibel I, Goldiner I, et al. Role of leisure-time physical activity in nonalcoholic fatty liver disease: a population-based study. Hepatology. 2008;48(6):1791-8}}. במחקר רחב טווח שכלל 813 איש שבצעו ביופסיית כבד, פעילות גופנית בעצימות גבוהה בלבד (כמו ריצה או שחייה) נמצאה כגורם מגן מפני כש"ד וצלקת מתקדמת, באופן עצמאי מ-BMI{{הערה|שם=הערה91|Kistler KD, Brunt EM, Clark JM, Diehl AM, Sallis JF, Schwimmer JB. Physical activity recommendations, exercise intensity, and histological severity of nonalcoholic fatty liver disease. Am J Gastroenterol. 2011;106(3):460-8; quiz 9}}. | ||
| − | + | במחקר חתך שכלל 24,588 נחקרים אמריקאים נמצא כי ביצוע של 150 דקות ומעלה של פעילות גופנית בשבוע היה קשור עם ירידה של כ-20 אחוזים למכ"ש ו-30 אחוזים לפיברוזיס. בנוסף, נמצא קשר מנה תגובה בין משך זמן יושבני לבין עלייה בסיכוי למכ"ש. למעשה אנשים היושבים יותר מ-8 שעות בממוצע ביום נמצאים בסיכוי גבוה ב-21 אחוזים לפתח מכ"ש בהשוואה לאנשים היושבים מתחת ל-4 שעות בממוצע, באופן עצמאי מסך ביצוע הפעילות הגופנית{{הערה|שם=הערה92|Kim D, Vazquez-Montesino LM, Li AA, Cholankeril G, Ahmed A. Inadequate Physical Activity and Sedentary Behavior Are Independent Predictors of Nonalcoholic Fatty Liver Disease. Hepatology. 2020;72(5):1556-68}}. במחקר קוהורט גדול בקרב 126 אלף איש, נמצא כי השמנה ורמה נמוכה של פעילות גופנית קשורות בתמותה ממחלות כבד (סיבוכי שחמת או סרטן כבד). אולם, הסיכון המוגבר לתמותה שנבע מהשמנה הופחת משמעותית אצל מי שביצע פעילות גופנית. נמצא כי הליכה בקצב מתון מעל ל-3 שעות בשבוע יכולה להפחית ברבע את מספר מקרי התמותה{{הערה|שם=הערה93|Simon TG, Kim MN, Luo X, Yang W, Ma Y, Chong DQ, et al. Physical activity compared to adiposity and risk of liver-related mortality: Results from two prospective, nationwide cohorts. J Hepatol. 2020,•72(6):1062-9}}. | |
| + | {| class="wikitable" | ||
| + | |+טבלה 3. סיכום מחקרים אפידמיולגיים שבחנו את הקשר בין צריכת אלכוהול בכמות מתונה של עד 1–2 משקאות ביום (לעומת הימנעות משתייה), נזק כבדי, סרטן הכבד ומחלות לב | ||
| + | |Author & Year | ||
| + | |Design & Population | ||
| + | |Steatosis | ||
| + | |NASH | ||
| + | |Fibrosis | ||
| + | |Severe liver event | ||
| + | |HCC/CVD | ||
| + | |- | ||
| + | |Blomdahl J., Metabolism Clinical and Experimental, 2021{{הערה|שם=הערה127|Blomdahl J, Nasr P, Ekstedt M, Kechagias S. Moderate alcohol consumption is associated with advanced fibrosis in non-al- coholic fatty liver disease and shows a synergistic effect with type 2 diabetes mellitus. Metabolism. 2021;! 15:154439}} | ||
| + | |Cross sectional study N=86 patients with biopsy-proven NAFLD | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Increased risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Aberg F., Hepatology 2020{{הערה|שם=הערה122}} | ||
| + | |Cohort study -11y FU N=8,345 subjects with NAFLD | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Increased risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Kashiwagi K., Alcohol, 2020{{הערה|שם=הערה126}} | ||
| + | |Cross sectional study, N=268 subjects with NAFLD | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Increased risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |No association with CVD | ||
| + | |- | ||
| + | |Long M., Clinical Gastroenterology and Hepatology, 2020{{הערה|שם=הערה128|Long MT, Massaro JM, Hoffmann U, Benjamin EJ, Naimi TS. Alcohol Use Is Associated With Hepatic Steatosis Among Per- sons With Presumed Nonalcoholic Fatty Liver Disease. Clin Gastroenterol Hepatol. 2020,18(8):!831-41 e5}} | ||
| + | |Cross-sectional study N=2,475 from Framingham cohort study | ||
| + | |Increased risk (for binge drinking*) | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Chang Y., Hepatology 2020{{הערה|שם=הערה129|Chang Y, Ryu S, Kim Y, Cho YK, Sung E, Kim HN, et al. Low levels of alcohol consumption, obesity, and development of fatty liver with and without evidence of advanced fibrosis. Hepatology. 2020,71 (3):861 -73}} | ||
| + | |Cohort study -4Y FU N=190,048 subjects without NAFLD | ||
| + | |Reduced risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Increased risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Chang Y., Hepatology 2019{{הערה|שם=הערה120}} | ||
| + | |Cohort study -8.3Y FU | ||
| − | == | + | N=58,927 Korean employees |
| + | |<nowiki>-</nowiki> | ||
| + | |''-'' | ||
| + | |Increased risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-■</nowiki> | ||
| + | |- | ||
| + | |Yamada K., PLOS ONE 2018{{הערה|שם=הערה130|Yamada K, Mizukoshi E, Seike T, Horii R, Kitahara M, Sunagozaka H, et al. Light alcohol consumption has the potential to suppress hepatocellular injury and liver fibrosis in non-alcoholic fatty liver disease. PL0S One. 2018;l3(1):e0191026}} | ||
| + | |Cross-sectional study N=178 NAFLD | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Reduced risk | ||
| + | |Reduced risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Aberg F., Hepatology 2018{{הערה|שם=הערה121}} | ||
| + | |Follow-up data from national registers | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Increased risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Hagstrom H., Scand J Gastroenterol 2017{{הערה|שם=הערה131|Hagstrom H, Nasr P, Ekstedt M, Kechagias S, Onnerhag K, Nilsson E, et al. Low to moderate lifetime alcohol consumption is associated with less advanced stages of fibrosis in non-alcoholic fatty liver disease. Scandinavian journal of gastroenterology. 2017;52(2):159-65}} | ||
| + | |Cross-sectional N=120 NAFLD | ||
| + | |<nowiki>-</nowiki> | ||
| + | |No association | ||
| + | |Reduced risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |VanWagner LB., Gastroenterology 2017{{הערה|שם=הערה132|VanWagner LB, Ning H, Allen NB, Ajmera V, Lewis CE, Carr JJ, et al. Alcohol use and cardiovascular disease risk in patients with nonalcoholic fatty liver disease. Gastroenterology. 2017;153(5):1260-72. e3}} | ||
| + | |Cross-sectional N=570 NAFLD | ||
| + | | | ||
| + | | | ||
| + | | | ||
| + | | | ||
| + | |Not protective from subdinical CVD | ||
| + | |- | ||
| + | |Moriya A., J of Hepatology 2015{{הערה|שם=הערה133|Moriya A, Iwasaki Y, Ohguchi S, Kayashima E, MitsumuneT, Taniguchi H, et al. Roles of alcohol consumption in fatty liver: a longitudinal study. Journal of Hepatology. 2015;62(4):921-7}} | ||
| + | |Prospective -2Y FU N=5297 Japanese | ||
| + | |Reduced risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Dunn W., J of Hepatology 2012{{הערה|שם=הערה118}} | ||
| + | |Cross-sectional N=582 NASH | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Reduced risk | ||
| + | |Reduced risk | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Ascha MS., Hepetology 2010{{הערה|שם=הערה123}} | ||
| + | |Prospective -3Y FU N=195 NASH- Cirrhosis | ||
| + | |''-'' | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Increased risk for HCC | ||
| + | |- | ||
| + | | colspan="7" | | ||
| + | * Binge drinking defined as >4 and >5 drinks within 24 hours, for women and men, respectively | ||
| + | |} | ||
| − | + | השמנה בטנית הודגמה באופן עקבי כגורם סיכון משמעותי למכ"ש. מספר מחקרים הראו כי ירידת משקל בעקבות פעילות גופנית באה לידי ביטויי באופן מיוחד ברקמת השומן הבטני וכי למתעמלים יש פחות השמנה בטנית לעומת ביקורות באותו משקל. פעילות גופנית עשויה לסייע בטיפול במכ"ש גם דרך מנגנונים אחרים. פעילות גופנית, ללא ירידת משקל או שינוי הרכב גוף, משרה רגישות לאינסולין ומשפרת מטבוליזם של גלוקוז על ידי העלאת מספר הקולטנים לאינסולין בשריר. בנוסף, פעילות גופנית משפרת מטבוליזם של חומצות שומן. אימון התנגדות נמצא מעלה מסת גוף רזה, מפחית תנגודת לאינסולין והשמנה בטנית ללא קשר לירידת משקל{{הערה|שם=הערה94| Ibanez J, Izquierdo M, Arguelles I, Forga L, Larrion JL, Garcia-Unciti M, et al. Twice-weekly progressive resistance training decreases abdominal fat and improves insulin sensitivity in older men with type 2 diabetes. Diabetes Care. 2005;28(3):662-7}}. ניסויים קליניים, ברובם קטנים וקצרי טווח, הדגימו השפעה חיובית של אימון גופני מובנה (ללא דיאטה וירידת משקל) על כבד שומני ואנזימי כבד. אימוני אופניים 3 פעמים בשבוע במשך חודש הובילו לירידה יחסית בשומן הכבדי ב-21 אחוזים ב-MRS ללא שינוי במשקל או בדיאטה{{הערה|שם=הערה95|Johnson NA, Sachinwalla T, Walton DW, Smith K, Armstrong A, Thompson MW, et al. Aerobic exercise training reduces hepatic and visceral lipids in obese individuals without weight loss. Hepatology. 2009;50(4):1105-12}}. במחקר אחר שכלל פעילות גופנית מתונה יותר - הליכה של כחצי שעה עד שעה, 5-3 ימים בשבוע, במשך 16 שבועות נצפתה ירידה יחסית מתונה יותר של כ-10 אחוזים בתכולת השומן בכבד ללא ירידת משקל{{הערה|שם=הערה96|Sullivan S, Kirk EP, Mittendorfer B, Patterson BW, Klein S. Randomized trial of exercise effect on intrahepatic triglyceride content and lipid kinetics in nonalcoholic fatty liver disease. Hepatology.55(6):1738-45}}. בשני ניסויים קליניים נוספים, האחד במתבגרים הסובלים מהשמנה{{הערה|שם=הערה97|van der Heijden GJ, Wang ZJ, Chu ZD, Sauer PJ, Haymond MW, Rodriguez LM, et al. A 12-week aerobic exercise program reduces hepatic fat accumulation and insulin resistance in obese, Hispanic adolescents. Obesity (Silver Spring).! 8(2)384-90}} והשני בקשישים בריאים{{הערה|שם=הערה98|Finucane FM, Sharp SJ, Purslow LR, Horton K, Horton J, Savage DB, et al. The effects of aerobic exercise on metabolic risk, insulin sensitivity and intrahepatic lipid in healthy older people from the Hertfordshire Cohort Study: a randomised controlled trial. Diabetologia.53(4):624-31}}, נצפה שוב אפקט מיטיב של פעילות גופנית אירובית כאשר שנים עשר שבועות אימון הובילו לירידה יחסית בשומן הכבדי בכ-35 אחוזים. בנוסף, הודגם כי אימון התנגדות בן 8–12 שבועות, שכלל 3 אימונים בשבוע שמשכם 45 דקות, הוביל לירידה יחסית בשומן הכבדי ב-10–13 אחוזים וזאת ללא ירידת משקל משמעותית{{הערה|שם=הערה99|Hallsworth K, Fattakhova G, Hollingsworth KG, Thoma C, Moore S, Taylor R, et al. Resistance exercise reduces liver fat and its mediators in non-alcoholic fatty liver disease independent of weight loss. Gut.60(9):1278-83}}{{הערה|שם=הערה100|Zelber-Sagi S, Buch A, Yeshua H, Vaisman N, Webb M, Harari G, et al. Effect of resistance training on non-alcoholic fatty-liv- er disease a randomized-clinical trial. World journal of gastroenterology: WJG. 2014;20(l5):4382-92}}. בניסוי מבוקר אקראי שהשווה אימץ אירובי לאימון התנגדות שניתן לחולי מכ"ש עם סוכרת 3 פעמים בשבוע במשך 4 חודשים, לא נמצא הבדל מובהק בין שני סוגי האימונים ושניהם נמצאו יעילים בהפחתת השומן הכבדי (כ-30 אחוזים הפחתה){{הערה|שם=הערה101|Bacchi E, Negri C,Targher G, Faccioli N, Lanza M, Zoppini G, etal. Both resistance training and aerobictraining reduce hepatic fat content in type 2 diabetic subjects with nonalcoholic fatty liver disease (the RAED2 Randomized Trial). Hepatology. 2013;58(4):1287-95}}. | |
| − | + | {| class="wikitable" | |
| + | |+טבלה '''4.''' סיכום מחקרים אפידמיולוגיים שבחנו את הקשר בין שתיית קפה או צריכת קפאין וכבד שומני לא אלכוהולי | ||
| + | |Author | ||
| − | + | Publication year | |
| + | |Type of coffee | ||
| + | |N | ||
| + | |Steatosis (protective (association | ||
| + | |Fibrosis (protective (association | ||
| + | |- | ||
| + | |Mikolasevic 1., 2020{{הערה|שם=הערה144|Mikolasevic I, Domislovic V, Filipec Kanizaj T, Radic-Kristo D, Krznaric Z, Milovanovic T, et al. Relationship between coffee consumption, sleep duration and smoking status with elastographic parameters of liver steatosis and fibrosis; controlled attenuation parameter and liver stiffness measurements. Int J Clin Pract. 2020:el3770}} | ||
| + | |All coffee types | ||
| + | |1,998 | ||
| + | |Yes | ||
| + | |Yes | ||
| + | |- | ||
| + | |Zhang Y., 2020{{הערה|שם=הערה145|Zhang Y, Liu Z, Choudhury T, Cornelis MC, Liu W. Habitual coffee intake and risk for nonalcoholic fatty liver disease: a two-sample Mendelian randomization study. Eur J Nutr. 2020}} | ||
| + | |All coffee types | ||
| + | |401,022 | ||
| + | |No | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Soleimani D., 2019{{הערה|שם=הערה146|Soleimani D, Ranjbar G, Rezvani R, Goshayeshi L, Razmpour F, Nematy M. Dietary patterns in relation to hepatic fibrosis among patients with nonalcoholic fatty liver disease. Diabetes Metab Syndr Obes. 2019;12:315-24}} | ||
| + | |Tea and coffee (not separated) | ||
| + | |170 | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Yes | ||
| + | |- | ||
| + | |Veronese N., 2018{{הערה|שם=הערה147|Veronese N, Notarnicola M, Cisternino AM, Reddavide R, Inguaggiato R, Guerra V, et al. Coffee Intake and Liver Steatosis: A Population Study in a Mediterranean Area. Nutrients. 2018;10(1)}} | ||
| + | |All coffee types | ||
| + | |2,819 | ||
| + | |No | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Chen YP., 2019{{הערה|שם=הערה148|Chen YP, Lu FB, Hu YB, Xu LM, Zheng MH, Hu ED. A systematic review and a dose-response meta-analysis of coffee dose and nonalcoholic fatty liver disease. Clin Nutr. 2019;38(6):2552-7}} | ||
| + | |All coffee types | ||
| + | |54,441 | ||
| + | |Yes | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Wijarnpreecha K., 2017{{הערה|שם=הערה149|Wijarnpreecha K, Thongprayoon C, Ungprasert P. Coffee consumption and risk of nonalcoholic fatty liver disease: a sys- tematic reviewand meta-analysis. Eur J Gastroenterol Hepatol. 2017;29(2):e8-e12}} | ||
| + | |Regular coffee | ||
| + | |3,290 | ||
| + | |Yes | ||
| + | |Yes | ||
| + | |- | ||
| + | |Alferink LJM. 2017{{הערה|שם=הערה150|Alferink LJ, Fittipaldi J, Kiefte-de Jong JC, Taimr P, Hansen BE, Metselaar HJ, et al. Coffee and herbal tea consumption is associated with lower liver stiffness in the general population: The Rotterdam study. Journal of hepatology. 2017;67(2):339-48}} | ||
| + | |All coffee types | ||
| + | |2,424 | ||
| + | |No | ||
| + | |Yes | ||
| + | |- | ||
| + | |Setiawan VW. 2017{{הערה|שם=הערה151|Setiawan VW, Parcel J, Wei P, Stram DO, Noureddin N, Lu SC, et al. Coffee drinking and alcoholic and nonalcoholic fatty liver diseases and viral hepatitis in the multiethnic cohort. Clinical Gastroenterology and Hepatology. 2017;15(8):1305-7}} | ||
| + | |All coffee types | ||
| + | |44,576 | ||
| + | |Yes | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Imatoh T. 2015{{הערה|שם=הערה152| Imatoh T, Kamimura S, Miyazaki M. Coffee but not green tea consumption is associated with prevalence and severity of hepatic steatosis: the impacton leptin level. European journal of clinical nutrition. 2015;69(9):1023-7}} | ||
| + | |All coffee types | ||
| + | |1024 | ||
| + | |Yes | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Zelber-Sagi S. 2015{{הערה|שם=הערה134|Zelber-Sagi S, Salomone F, Webb M, Lotan R, Yeshua H, Halpern Z, et al. Coffee consumption and nonalcoholic fatty liver onset: a prospective study in the general population. Translational research : the journal of laboratory and clinical medicine. 2015;165(3):428-36}} | ||
| + | |All caffeinated coffee types | ||
| + | |347 | ||
| + | |No | ||
| + | |Yes | ||
| + | |- | ||
| + | |BambhaK. 2013{{הערה|שם=הערה138|Bambha K, Wilson LA, Unalp A, Loomba R, Neuschwander-Tetri BA, Brunt EM, et al. Coffee consumption in NAFLD patients with lower insulin resistance is associated with lower risk of severe fibrosis. Liver Int. 2013}} | ||
| + | |All coffee types | ||
| + | |782 | ||
| + | |No | ||
| + | |Yes | ||
| + | |- | ||
| + | |AntyR. 2012{{הערה|שם=הערה137|Anty R, Marjoux S, lannelli A, Patouraux S, Schneck AS, Bonnafous S, et al. Regular coffee but not espresso drinking is protective against fibrosis in a cohort mainly composed of morbidly obese European women with NAFLD undergoing bariatric surgery. J Hepatol. 2012;57(5):1090-6}} | ||
| + | |Regular coffee, not espresso | ||
| + | |195 | ||
| + | |<nowiki>-</nowiki> | ||
| + | |Yes | ||
| + | |- | ||
| + | |Birerdinc A. 2012{{הערה|שם=הערה153|Birerdinc A, Stepanova M, Pawloski L, Younossi Z. Caffeine is protective in patients with non-alcoholic fatty liver disease. Alimentary pharmacology & therapeutics. 2012;35(l):76-82}} | ||
| + | |Caffeine intake | ||
| + | |41,658 | ||
| + | |Yes | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Molloy JW. 2012{{הערה|שם=הערה136|Molloy JW, Calcagno CJ, Williams CD, Jones FJ, Torres DM, Harrison SA. Association of coffee and caffeine consumption with fatty liver disease, nonalcoholic steatohepatitis, and degree of hepatic fibrosis. Hepatology. 2012;55(2):429-36}} | ||
| + | |Regular coffee | ||
| + | |306 | ||
| + | |No | ||
| + | |Yes | ||
| + | |- | ||
| + | |Funatsu K.2011{{הערה|שם=הערה154|Funatsu K, Yamashita T, Nakamura H. Coffee consumption is associated with a lower incidence of fatty liver in middle-aged men. Journal of Health Science. 2011;57(5):406-13}} | ||
| + | |All coffee types | ||
| + | |492 | ||
| + | |Yes | ||
| + | |<nowiki>-</nowiki> | ||
| + | |- | ||
| + | |Catalano D. 2010{{הערה|שם=הערה135|Catalano D, Martines GF, Tonzuso A, Pirri C, Trovato FM, Trovato GM. Protective role of coffee in non-alcoholic fatty liver disease (NAFLD). Digestive diseases and sciences. 2010;55(11):3200-6}} | ||
| + | |Espresso coffee | ||
| + | |245 | ||
| + | |Yes | ||
| + | |<nowiki>-</nowiki> | ||
| + | |} | ||
| − | + | בניסוי קליני שבחן איזו עצימות של אימון אירובי ואיזו תדירות הן היעילות ביותר בהפחתת שומן כבדי לא נראה הבדל בין הזרועות ולכן נראה כי כל כמות סבירה של פעילות גופנית, בתדירות ועצימות שנוחות ומתאימות למטופל, טובה יותר מחוסר פעילות{{הערה|שם=הערה102|Keating SE, Hackett DA, Parker HM, O'Connor HT, Gerofi JA, Sainsbury A, et al. Effect of aerobic exercise training dose on liver fat and visceral adiposity. J Hepatol. 2015;63(l):174-82}}, זאת בעיקר לאור העובדה שזמן יושבני ממושך נמצא קשור בפני עצמו בהמצאות גבוהה יותר של כבד שומני{{הערה|שם=הערה103|Ryu S, Chang Y, Jung HS, Yun KE, Kwon MJ, Choi Y, et al. Relationship of sitting time and physical activity with non-alcohol- ic fatty liver disease. J Hepatol. 2015;63(5):122937}}. | |
| − | + | ניסוי קליני שנערך בקרב 45 נשים עם השמנה ומכ"ש מצא כי אימץ כוח של 60–67 דקות בתדירות של 3 פעמים בשבוע למשך שלושה שבועות הוביל לשיפור באניזמי הכבד AST ו-ALT{{הערה|שם=הערה104|Moradi Kelardeh B, Rahmati-Ahmadabad S, Farzanegi P, Helalizadeh M, Azarbayjani MA. Effects of non-linear resistance training and curcumin supplementation on the liver biochemical markers levels and structure in older women with non-alco- holic fatty liver disease. J Body w Mov Ther. 2020;24(3):l54-60}}. בניסוי קליני אחר בקרב 39 מבוגרים עם מכ"ש, השוו את ההשפעה של אימון אירובי או כוח, לעומת קבוצת ביקורת, על [[פרופיל שומנים|פרופיל השומנים בדם]]. נמצא כי ביצוע שלושה אימוני אירובי או כוח בשבוע של 45 דקות יעיל בהפחתת LDL, אך רק אימץ אירובי יעיל להעלאת HDL. בשתי הקבוצות לא היה שינוי ברמות הטריגליצרידים{{הערה|שם=הערה105|Ghamarchehreh ME, Shamsoddini A, Alavian SM. Investigating the impact of eight weeks of aerobic and resistance training on blood lipid profile in elderly with non-alcoholic fatty liver disease: a randomized clinical trial. Gastroenterology and hepatology from bed to bench. 2019;12(3):!90}}. | |
| − | + | ההשפעה המיטיבה של פעילות גופנית נתמכת במטא-אנליזה של ניסויים קליניים שמחבריה הסיקו כי יש ראיות ברורות להשפעה מיטיבה של אימון גופני על שומן כבדי, ללא ירידת משקל או עם ירידת משקל מינימלית{{הערה|שם=הערה106|Keating SE, Hackett DA, George J, Johnson NA. Exercise and non-alcoholic fatty liver disease: a systematic review and meta-analysis. Journal of hepatology. 2012;57(1):157-66}}. | |
| − | == | + | באופן דומה, במטא-אנליזה משנת 2020 שכללה 9 ניסויים קליניים ו-951 נחקרים עם מכ"ש וללא סוכרת נמצא כי הן פעילות אירובית והן פעילות בונה שריר של אימון התנגדות מראות יעילות בשיפור אנזימי הכבד ושומן תוך כבדי{{הערה|שם=הערה107|Wang S-t, Zheng J, Peng H-w, Cai X-l, Pan X-t, Li H-q, et al. Physical activity intervention for non-diabetic patients with non-alcoholic fatty liver disease: a meta-analysis of randomized controlled trials. BMC gastroenterology. 2020;20(1):1-l2}}. אין כמעט מחקר שבדק השפעת אימון גופני על היסטולוגיה כבדית כולל כש"ד ופיברוזיס. אולם, מחקר קטן עם 16 חולי כבד שומני שעברו ביופסיית כבד חוזרת, הדגים כי 12 שבועות של אימון מתון-אינטנסיבי של פעילות גופנית אירובית 2–5 פעמים בשבוע הוביל להפחתת פיברוזיס כבדי{{הערה|שם=הערה108|O'Gorman P, Naimimohasses S, Monaghan A, Kennedy M, Melo AM, Ni Fhloinn D, et al. Improvement in histological end- points of MAFLD following a 12-week aerobic exercise intervention. Aliment Pharmacol Ther. 2020;52(8):l387-98}}. דרוש מחקר נוסף לאשש ממצאים אלו. |
| − | + | == ניתוחים בריאטריים == | |
| − | + | ניתוחים בריאטרים הם השיטה היעילה ביותר לירידה במשקל{{הערה|שם=הערה109|Chang SH, Stoll CR, Song J, Varela JE, Eagon CJ, Colditz GA. The effectiveness and risks of bariatric surgery: an updated systematic review and meta-analysis, 2003-2012. JAMA surgery. 2014;149(3):275-87}} ובנוסף, מובילים לשיפור ניכר בסוכרת ואף לרמיסייה{{הערה|שם=הערה110|Sjostrom L, Peltonen M, Jacobson P, Ahlin S, Andersson-Assarsson J, Anveden A, et al. Association of bariatric surgery with long-term remission of type 2 diabetes and with microvascular and macrovascular complications. JAMA. 2014,311 (22):2297- 304}}. שיפור בשני המדדים הללו אמור לגרום לשיפור ניכר במדדי מכ"ש. אכן, במטא-אנליזה נראה כי בעקבות ניתוח בריאטרי חל שיפור בכל המדדים ההיסטולוגיים של שומן, דלקת וצלקת עד כדי היעלמותם המוחלטת, אך בסקירה (Systematic review) של Cochrane נטען כי מספר הניסויים ואיכותם אינו מספק ואינו מאפשר הערכת תועלת או נזק של [[ניתוחים בריאטריים - Bariatric surgery|ניתוחים בריאטריים]] כטיפול בחולי כש"ד. האיגוד האירופאי לחקר הכבד{{הערה|שם=הערה55}} מסכם כי ניתוח בריאטרי הוא אפשרות טיפולית בחולים שאינם מגיבים לשינוי אורח חיים או לטיפול תרופתי, ושעל-ידי ניתוחים אלה ניתן להגיע לשיפור במדדים מטבוליים לתקופה ממושכת. מחקר עוקבה עם מעקב למשך שנה הראה שיפור בכש"ד ב-85 אחוזים המהחולים ושיפור בצלקת ב-43 אחוזים{{הערה|שם=הערה111|Lassailly G, Caiazzo R, Buob D, Pigeyre M, Verkindt H, Labreuche J, et al. Bariatric Surgery Reduces Features of Nonalcoholic Steatohepatitis in Morbidly Obese Patients. Gastroenterology. 2015;149(2):379-88; quiz e15-6}}. הכותבים מסכמים שצריך לאזן בין התועלת לבין הסיכונים הנובעים מתחלואה בתר-ניתוחית. אותה קבוצה פרסמה תוצאות מעקב לאחר 5 שנים מהניתוח הבריאטרי. ב-84 אחוזים מהמנותחים הייתה העלמות של מכ"ד ללא החמרה בפיברוזיס, ורמת הפיברוזיס השתפרה בכ-70 אחוזים מהמנותחים ונעלמה ב-56 אחוזים מהם. בחולים שהדגימו תוצאות טובות לאחר שנה מהניתוח לא הייתה חזרה של מכ"ד בין 1–5 שנות המעקב{{הערה|שם=הערה112|Lassailly G, Caiazzo R, Ntandja-Wandji LC, Gnemmi V, Baud G, Verkindt H, et al. Bariatric Surgery Provides Long-term Reso- lution of Nonalcoholic Steatohepatitis and Regression of Fibrosis. Gastroenterology. 2020;159(4):l290-301 e5}}. | |
| − | === | ||
| − | + | בחולים עם השמנה מורבידית יש לעודד ניתוחים בריאטריים בעיקר באלה עם כש"ד וצלקת{{הערה|שם=הערה17}}. האיגוד האמריקאי לחקר הכבד מסכם כי אין התווית נגד לניתוח בריאטרי בחולי מכ"ש וכש"ד, אך לגבי חולים שחמתיים אין די ריאיות לגבי בטיחות או יעילות הניתוח וכן, כי מוקדם מדי להגדיר ניתוח בריאטרי כטיפול ספציפי למכ"ש{{הערה|שם=הערה12}}. | |
| − | + | נוספו פרוצדורות בריאטריות אנדוסקופיות לארסנל הטיפולים בהשמנה. טיפולים אלה כוללים [[בלון תוך קיבתי]] ותפירת קיבה אנדוסקופית. במחקר פרוספקטיבי שפורסם נבדקה השפעת בלון תוך קיבתי ב-21 חולים על שיפור במדדי מכ"ד. המטופלים הראו ירידה במדדים מטבוליים כולל משקל (ממוצע 11.7±7.7 אחוזים), ומדדי סוכרת. ניקוד היסטולוגי של מכ"ד השתפר ב-18 מתוך 20 חולים ושיפור בדרגת פיברוזיס של כנקודה אחת ב-15 אחוזים מהמטופלים. החוקרים מסכמים שבלון תוך קיבתי הביא לשיפור מטבולי והיסטולוגי בחולי מכ"ד{{הערה|שם=הערה113|Bazerbachi F, Vargas EJ, Rizk M, Maselli DB, Mounajjed T, Venkatesh SK, et al. Intragastric Balloon Placement Induces Significant Metabolic and Histologic Improvement in Patients With Nonalcoholic Steatohepatitis. Clin Gastroenterol Hepatol. 2021;l9(1):146-54e4}}. ניסוי לא מבוקר נוסף, שכלל 26 משתתפים עם כבד שומני ופיברוזיס כבדי משמעותי, הראה כי בלון תוך קיבתי במשך 6 חודשים הוביל לירידת משקל, שיפור מטבולי וכן הפחתת שומן כבדי ושיפור בפיברוזיס כפי שהודגם בפיברוסקן{{הערה|שם=הערה114|Salomone F, Current! W, Magri G, Boskoski I, Zelber-Sagi S, Galvano F. Effects of intragastric balloon in patients with nonal- coholic fatty liver disease and advanced fibrosis. Liver Int. 2021}} ואנדוסקופית{{הערה|שם=הערה115|Hajifathalian K, Mehta A, Ang B, Skaf D, Shah SL, Saumoy M, etal. Improvement in insulin resistance and estimated hepaticsteatosis and fibrosis after endoscopic sleeve gastroplasty. Gastrointest Endosc. 2021;93(5):11l0-8}}. אולם עקב העלייה בשכיחות השימוש בפרוצדורה זו, אנו צפויים לראות תוצאות מחקרים נוספים בקרוב. | |
| − | + | אלכוהול וכבד שומני (ראו טבלה מספר 3 המסכמת את המחקרים בתחום) | |
| − | + | מחקר בודד הדגים שיפור במדדי השמנה כבדית לאחר תפירת קיבה. | |
| − | + | == אלכוהול וכבד שומני (ראו טבלה מספר 3 המסכמת את המחקרים בתחום) == | |
| + | להגדרת כבד שומני כלא אלכוהולי יש לשלול ראשית צריכת אלכוהול כרונית של מעל 21 משקאות ממוצעים בשבוע לגבר ו-14 לאישה. חולי מכ"ש צריכים להימנע מצריכת אלכוהול כבדה. שתיית אלכוהול מתונה של ככוס משקה ליום נמצאה קשורה בסיכון מופחת לכבד שומני{{הערה|שם=הערה116|Sookoian S, Castano GO, Pirola CJ. Modest alcohol consumption decreases the risk of non-alcoholic fatty liver disease: a meta-analysis of 43 175 individuals. Gut. 2014;63(3):530-2}}, כש"ד ואף צלקת{{הערה|שם=הערה117|Wong VWS, Chu WCW, Wong GLH, Chan RSM, Chim AML, Ong A, et al. Prevalence of non-alcoholic fatty liver disease and advanced fibrosis in Hong Kong Chinese: a population study using proton-magnetic resonance spectroscopy and transient elastography. Gut. 2011;61(3):409-15}}{{הערה|שם=הערה118|Dunn W, Sanyal AJ, Brunt EM, Unalp-Arida A, Donohue M, McCullough AJ, et al. Modest alcohol consumption is associated with decreased prevalence of steatohepatitis in patients with non-alcoholic fatty liver disease (NAFLD). Journal of Hepatology. 2012,•57(2)384-91}}{{הערה|שם=הערה119|Gunji T, Matsuhashi N, Sato H, Fujibayashi K, Okumura M, Sasabe N, et al. Light and moderate alcohol consumption signifi- cantly reduces the prevalence of fatty liver in the Japanese male population. Am J Gastroenterol. 2009;104(9):2189-95}}. אולם, איכות מחקרים אלו מוטלת בספק, בין השאר בשל היותם מחקרי חתך שלא תקננו למשתנים ערפלנים כגון אורחות חיים. לעומת זאת, במחקרים פרוספקטיביים מאוחרים יותר נראה נזק כבדי של שתיית אלכוהול מתונה{{הערה|שם=הערה120|Chang Y, Cho YK, Kim Y, Sung E, Ahn J, Jung HS, et al. Nonheavy Drinking and Worsening of Noninvasive Fibrosis Markers in Nonalcoholic Fatty Liver Disease: A Cohort Study. Hepatology. 2019;69(1):64-75}}{{הערה|שם=הערה121|Aberg F, Helenius-Hietala J, Puukka P, Farkkila M, Jula A. Interaction between alcohol consumption and metabolic syn- drome in predicting severe liver disease in the general population. Hepatology. 2018;67(6):2141-9}}. הודגמה התקדמות פיברוזיס על פי סמנים ביוכימיים לאורך מעקב פרוספקטיבי בקרב מי ששתו כמות מתונה של אלכוהול (עד 20 גרם אלכוהול ליום) לעומת אלו שלא שתו כלל. כמו כן, הודגם כי שתיית אלכוהול מתונה (פחות מ-20 גרם אלכוהול ליום) קשורה בסיכון מוגבר למחלת כבד מתקדמת (כולל: אשפוז, סרטן כבד או תמותה על רקע מחלת כבד){{הערה|שם=הערה122|Aberg F, Puukka P, Salomaa V, Mannisto S, Lundqvist A, Valsta L, et al. Risks of Light and Moderate Alcohol Use in Fatty Liver Disease: Follow-Up of Population Cohorts. Hepatology. 2020;71(3):835-48}}. הראיות חד משמעיות לגבי שחמת על רקע כש"ד{{הערה|שם=הערה123|Ascha MS, Hanouneh IA, Lopez R, Tamimi TA-R, Feldstein AF, Zein NN. The incidence and risk factors of hepatocellular carcinoma in patients with nonalcoholic steatohepatitis. Hepatology. 2010;51(6):1972-8}}, במקרה זה צריכת אלכוהול בכל רמה שהיא נמצאה מגבירה סיכון לסרטן הכבד. צריך לזכור כי כבד שומני והשמנה יכולים להחמיר את הנזק הכבדי בשתיינים{{הערה|שם=הערה124|Pais R, Lebray P, Rousseau G, Charlotte F, Esselma G, Savier E, et al. Nonalcoholic Fatty Liver Disease Increases the Risk of Hepatocellular Carcinoma in Patients With Alcohol-Associated Cirrhosis Awaiting Liver Transplants. Clin Gastroenterol Hepatol. 2014}} ומאידך כי צריכת אלכוהול עודפת עלולה להחמיר נזק כבדי בכבד שומני לא אלכוהולי (למעשה שילוב של כבד שומני אלכוהולי ולא אלכוהולי){{הערה|שם=הערה125|Bellentani S, Saccoccio G, Masutti F, Croce LS, Brandi G, Sasso F, et al. Prevalence of and risk factors for hepatic steatosis in Northern Italy. Ann Intern Med. 2000;132(2):112-7}}. מעניין לציין כי ייתכן וגם לדפוס השתייה יש השפעה. מחקר חתך בקרב 2,475 אנשים מצא כי דפוס בינג׳, Binge drinking (קרי 4 משקאות ומעלה לאישה וחמישה משקאות ומעלה לגבר באותה יממה בפרק זמן קצר) קשורה עם עלייה בסיכוי לסטיאטוזיס כבדי, גם אם הכמות השבועית הכוללת נחשבת כמתונה{{הערה|שם=הערה126|Kashiwagi K, Yamaguchi A, Shiba S, Taniki N, Inoue N, Takaishi H, et al. Moderate alcohol consumption is not associated with subclinical cardiovascular damage but with hepatic fibrosis in non-alcoholic fatty liver disease. Alcohol. 2020;89:1-7}}. בהנחיות האיגוד האמריקאי לחקר הכבד משנת 2017 מסוכם כי אין די נתונים על מנת לתת המלצות לגבי צריכת אלכוהול מתונה בחולי כבד שומני, לאור מחסור במחקרים פרוספקטביים ולאור חשש של השפעה מבלבלת של עודף משקל נמוך יותר בקרב אנשים הצורכים אלכוהול באופן מתון{{הערה|שם=הערה12}}. לגבי החולים עם שחמת על רקע כבד שומני דלקתי{{הערה|שם=הערה123}}, במקרה זה צריכת אלכוהול בכל רמה שהיא נמצאה מגבירה סיכון לסרטן הכבד ולכן מומלץ להימנע לחלוטין מאלכוהול{{הערה|שם=הערה55}}. בהנחיות מ-2019 של ה-ESPEN מומלץ שחולי כבד שומני ימנעו משתיית אלכוהול לחלוטין{{הערה|שם=הערה56}}. לגבי הטיעון שכמות מתונה של אלכוהול מסייעת במניעת מחלות לב וכלי דם, הרי שהדבר לא הודגם ספציפית בחולי כבד שומני. בפועל, נראה כי ההחלטה נתונה בידי הרופא המטפל ולפי מצב המטופל, בחולים ללא עדות לפיברוזיס משמעותית שרוצים לשתות אלכוהול יש להקפיד על כמות מתונה מאוד ורצוי לבחור ביין. בחולים עם עדות לפיברוזיס רצוי להימנע במידת האפשר ובחולים עם שחמת יש להימנע לחלוטין. | ||
| − | + | == קפה וכבד שומני (ראו טבלה מספר 4 המסכמת את המחקרים בתחום) == | |
| + | פורסמו מספר מחקרי חתך שמצאו השפעה מגינה של קפה מפני צלקת בכבד שומני{{הערה|שם=הערה134}}{{הערה|שם=הערה135}}{{הערה|שם=הערה136}}{{הערה|שם=הערה137}}{{הערה|שם=הערה138}}. בנוסף, יש גם ראיות ממחקר פרוספקטיבי כי קפה קשור בהפחתת הסיכון לסרטן הכבד{{הערה|שם=הערה139|Setiawan VW, Wilkens LR, Lu SC, Hernandez BY, Le Marchand L, Henderson BE. Association of coffee intake with reduced incidence of liver cancer and death from chronic liver disease in the US multiethnic cohort. Gastroenterology. 2015;148(1):118- 25; quize15}} אולם, לגבי השומן הכבדי הראיות סותרות וברוב המחקרים לא נמצא קשר מגן, כולל מחקר שבחן קשר בין צריכת קפה והיארעות כבד שומני באופן פרוספקטיבי{{הערה|שם=הערה134}}. | ||
| − | + | נמצא במחקר אפידמיולוגי גדול עם קרוב ל-500,000 משתתפים כי צריכת כל סוגי הקפה מגינה מפני מחלת כבד כרונית וכבד שומני, תמותה ממחלת כבד וסרטן כבד (בהשוואה למי שלא שותה קפה כלל){{הערה|שם=הערה140|Kennedy OJ, Fallowfield JA, Poole R, Hayes PC, Parkes J, Roderick PJ. All coffee types decrease the risk of adverse clinical outcomes in chronic liver disease: a UK Biobank study. BMC Public Health. 2021 ;21 (l):970}}. | |
| − | == | + | המרכיבים בקפה שמגינים מפני צלקת או סרטן הכבד אינם ידועים{{הערה|שם=הערה141|Godos J, Pluchinotta FR, Marventano S, Buscemi S, Li Volti G, Galvano F, et al. Coffee components and cardiovascular risk: beneficial and detrimental effects. Int J Food Sci Nutr. 2014;65(8):925-36}} אבל ייתכן שאין מדובר בקפאין עצמו אלא בפוליפנולים שיש בקפה או בתרכובות אחרות שמצויות בו{{הערה|שם=הערה142|Vitaglione P, Morisco F, Mazzone G, Amoruso DC, Ribecco MT, Romano A, et al. Coffee reduces liver damage in a rat model of steatohepatitis: the underlying mechanisms and the role of polyphenols and melanoidins. Hepatology. 2010;52(5):1652-61}}{{הערה|שם=הערה143|Salomone F, Li Volti G, Vitaglione P, Morisco F, Fogliano V, Zappala A, et al. Coffee enhances the expression of chaperones and antioxidant proteins in rats with nonalcoholic fatty liver disease. Translational research : the journal of laboratory and clinical medicine. 2013}}. אין המלצה לשתיית קפה בחולים עם כבד שומני{{הערה|שם=הערה55}}, אבל גם אין מניעה לשתייה במידה סבירה בקרב מי שרגיל לשתות (משקאות ללא סוכר). |
| − | + | == תרופות אנטי סוכרתיות לטיפול בכבד שומני == | |
| + | לאור הקשר המטבולי בין סוכרת לכבד שומני, ניתן לשער שהתערבויות המשפרות את הלקויות המטבוליות בחולי סוכרת כמו שנוי אורחות חיים וטיפול תרופתי בהיפרגליקמיה ו[[דיסליפדמיה]] יועיל גם במכ"ש. מירב המחקרים בנושא מתמקדים ב[[מטפורמין]], ב[[תיאזולידינדיונים - Thiazolidinediones|תיאזולידינדיונים]] ובדור החדש של תרופות לטיפול בסוכרת. | ||
| − | == | + | === ביגואנידים-מטפורמין === |
| + | התרופה מטפורמין, משמשת היום בתרופת הבחירה הראשונה לטיפול בסוכרת. היא שייכת למשפחת הביגואנידים ועיקר פעילותה היא דרך שיפור התנגודת הכבדית לאינסולין. מבחינת בטיחות השימוש, מדובר בתרופה בטוחה מבחינה כבדית, כאשר עד היום דווח על מקרים בודדים של [[דלקת כבד חריפה]] בהקשר לטיפול במטפורמין בחולים עם סוכרת. התרופה לא ניתנת ב[[אי ספיקת כבד]] קשה, [[אי ספיקת לב - Congestive heart failure|אי ספיקת לב]] קשה ובחולים עם [[הפרעה בתפקוד הכלייתי|הפרעה קשה בתפקודי כליה]]. | ||
| − | + | הטיפול במטפורמין במטופלים עם כבד שומני הניב תוצאות סותרות, בחלקם נראתה ירידה באנזימים ושיפור היסטולוגי ובחלקם לא{{הערה|שם=הערה155|Loomba R, Lutchman G, Kleiner DE, Ricks M, Feld JJ, Borg BB, et al. Clinical trial: pilot study of metformin for the treatment of non-alcoholic steatohepatitis. Aliment Pharmacol Ther. 2009;29(2):172-82}}{{הערה|שם=הערה156|Lavine JE, Schwimmer JB, Van Natta ML, Molleston JP, Murray KF, Rosenthal P, et al. Effect of vitamin E or metformin for treatment of nonalcoholic fatty liver disease in children and adolescents: the TONIC randomized controlled trial. Jama. 2011;305(16):1659-68}}{{הערה|שם=הערה157|Bugianesi E, Gentilcore E, Manini R, Natale S, Vanni E, Villanova N, et al. A randomized controlled trial of metformin versus vitamin E or prescriptive diet in nonalcoholic fatty liver disease. Am J Gastroenterol. 2005;100(5):1082-90}}{{הערה|שם=הערה158|Haukeland JW, Konopski Z, Eggesbo HB, von Volkmann HL, Raschpichler G, Bjoro K, et al. Metformin in patients with non-alcoholic fatty liver disease: a randomized, controlled trial. Scand J Gastroenterol. 2009;44(7):853-60}}. עצם השימוש במטפורמין במחלת כבד קשה נותר שנוי במחלוקת. במחקר רטרוספקטיבי שבדק האם המשך טיפול במטפורמין לאחר אבחון שחמת בחולים סוכרתיים משפר תוחלת חיים נמצאה ירידה בתמותה במטופלים סוכרתיים עם שחמת ובעיקר במטופלים שסבלו משחמת על רקע כבד שומני שהמשיכו להיות מטופלים במטפורמין לעומת כאלו שלא טופלו. במחקר זה אף מטופל לא פיתח [[חמצת לקטית|Lactic acidosis]]{{הערה|שם=הערה159|Zhang X, Harmsen WS, Mettler TA, Kim WR, Roberts RO, Therneau TM, et al. Continuation of metformin use after a diagnosis of cirrhosis significantly improves survival of patients with diabetes. Hepatology. 2014;60(6):2008-16}}. יתרה מכך, קיימים מספר מחקרים פרה-קליניים הרומזים על פעילות אנטי גידולית של מטפורמין בסרטן כבד. הנתונים בבני אדם מוגבלים למחקרים רטרוספקטיבים{{הערה|שם=הערה160|Bhalla K, Hwang BJ, Dewi RE,Twaddel W, Goloubeva OG, Wong KK, et al. Metformin prevents liver tumorigenesis by inhibiting pathways driving hepatic lipogenesis. Cancer Prev Res (Phila). 2012;5(4):544-52}}{{הערה|שם=הערה161|Zhang ZJ, Zheng ZJ, Shi R, Su Q, Jiang Q, Kip KE. Metformin for liver cancer prevention in patients with type 2 diabetes: a systematic review and meta-analysis. J Clin Endocrinol Metab. 2012;97(7):2347-53}}. נכון להיום, אין המלצה להשתמש באופן שגרתי במטפורמין במטופלים עם כבד שומני ללא סוכרת{{הערה|שם=הערה55}}. | |
| − | == | + | === גליטזונים-תיאזולידנידיונים - Thiazolidinediones === |
| + | הגליטזונים הם קבוצת תרופות המעלות רגישות לאינסולין בתאי שומן פריפריים. התרופות במשפחה זו פועלות כאגוניסטים של Peroxisome Proliferator Activated Receptor Gamma{{כ}} (PPAR-Gamma). התרופות הנמצאות היום בשוק הן [[Rosiglitazone]] ו-[[Pioglitazone]]. | ||
| − | + | מטא-אנליזה של מספר ניסויים קליניים אקראיים כפולי סמיות שבוצעו, הראתה כי מתן תרופה ממשפחת הגליטזונים משפר משמעותית היסטולוגיה כבדית מבחינת מדדי דלקת ורמת שומן במטופלים עם כש"ד לעומת פלצבו{{הערה|שם=הערה162|Boettcher E, Csako G, Pucino F, Wesley R, Loomba R. Meta-analysis: pioglitazone improves liver histology and fibrosis in patients with non-alcoholic steatohepatitis. Aliment Pharmacol Ther. 2012;35(1 ):66-75}}. לגבי פיברוזיס התוצאות אינן עקביות. בעוד שמתן Rosiglitazone גרם לשיפור ברגישות לאינסולין וירידה של אנזימי כבד, ירידה בכמות שומן בכבד ומדדי דלקת כבדית, לא נצפה שיפור בדרגת הצלקת בכבד בחולים עם כבד שומני עם או ללא סוכרת. הארכת משך הטיפול משנה לשנתיים לא שיפרה את התוצאות וסוכם כי ללא שינוי באורחות חיים הטיפול התרופתי ב-Rosiglitazone לא יוביל לשינוי משמעותי{{הערה|שם=הערה163|Ratziu V, Giral P, Jacqueminet S, Charlotte F, Hartemann-Heurtier A, Serfaty L, et al. Rosiglitazone for nonalcoholic steato- hepatitis: one-year results of the randomized placebo-controlled Fatty Liver Improvement with Rosiglitazone Therapy (FLIRT) Trial. Gastroenterology. 2008;135(1):100-10}}. עובדה זו רומזת שטיפול בעמידות לאינסולין אינו מספיק בחולים עם כבד שומני. השימוש ברוזיגליטזון פוחת מאוד עקב ספקות שעלו בקשר לבטיחות הקרדיוואסקולרית של תרופה זו. | |
| − | |||
| − | |||
| − | + | להבדיל מ-Rosiglitazone{{כ}}, Aithai וחבריו הראו שמתן Pioglitazone לתקופה של שנה בחולים עם NASH (ללא סוכרת) שיפר גם מדדים מטבולים וגם מדדים היסטולוגיים כולל דרגת צלקת{{הערה|שם=הערה164|Aithal GP, Thomas JA, Kaye PV, Lawson A, Ryder SD, Spendlove I, et al. Randomized, placebo-controlled trial of pioglita- zone in nondiabetic subjects with nonalcoholic steatohepatitis. Gastroenterology. 2008;135(4):1176-84}}. תוצאות דומות מבחינת שיפור במדדי הפיברוזיס הודגם גם על ידי Cusi ועמיתיו במחקר שכלל 101 חולים עם סוכרת או מצב טרום סוכרת וכבד שומני{{הערה|שם=הערה165|Cusi K, Orsak B, Bril F, Lomonaco R, Hecht J, Ortiz-Lopez C, et al. Long-Term Pioglitazone Treatment for Patients With Nonal- coholic Steatohepatitis and Prediabetes or Type 2 Diabetes Mellitus: A Randomized Trial. Ann Intern Med. 2016;165(5):305-15}}. | |
| − | + | בשני ניסויים קליניים נוספים ואחד מהם לתקופה של 96 שבועות, עם זרוע שבדקה גם יעילות של מתן [[ויטמין - Vitamin - E|ויטמין E]]{{כ}} (PIVENS trial), מתן Pioglitazone היה כרוך בשיפור רמות אנזימי כבד, רמת שומן בכבד ושיפור היסטולוגי בחלק ממרכיבי הדלקת, ללא שיפור ברמת הצלקת{{הערה|שם=הערה166|Belfort R, Harrison SA, Brown K, Darland C, Finch J, Hardies J, et al. A placebo-controlled trial of pioglitazone in subjects with nonalcoholic steatohepatitis. N Engl J Med. 2006;355(22):2297-307}}{{הערה|שם=הערה167|Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et al. Pioglitazone, vitamin E, or placebo for nonal- coholic steatohepatitis. N Engl J Med. 2010;362(18):1675-85}}. ההנחיה של איגוד הכבד האירופאי{{הערה|שם=הערה55}} היא לתת Pioglitazone לחולים עם כש"ד שהוכח בביופסיה עם עדיפות למטופלים עם סוכרת שבה לתרופה יש שימוש רשום. יש להדגיש, שרב המחקרים שחקרו מתן Pioglitazone בחולים עם כש"ד, היו בחולים ללא סוכרת ולמשך טווחי זמן קצרים. מקובל להיזהר במתן גליטזונים במטופלים סוכרתיים עם עלייה באנזימי כבד ואף קיימת התווית-נגד לטיפול במטופלים עם טרנסאמינאזות מעל פי 3 מהערך העליון של הנורמה{{הערה|שם=הערה168|Chalasani N, Teal E, Hall SD. Effect of rosiglitazone on serum liver biochemistries in diabetic patients with normal and elevated baseline liver enzymes. Am J Gastroenterol. 2005;100(6):1317-21}}. | |
| − | === | + | === נוגדי 4-DPP === |
| + | תרופות מסוג [[מעכבי DPP-4 inhibitors - DPP-4|נוגדי 4-DPP]] מונעות את פירוק האינקרטינים ועל ידי כך מעלות הפרשת אינסולין ומורידות הפרשת [[גלוקגון - Glucagon|גלוקגון]]. מספר המחקרים שבדקו יעילות קבוצה זו כטיפול בכבד שומני הוא מצומצם. בניסוי קליני קטן בלתי אקראי נמצא קשר בין מתן התרופה לירידה ברמת אנזימי כבד{{הערה|שם=הערה169|Iwasaki T, Yoneda M, Inamori M, Shirakawa J, Higurashi T, Maeda S, et al. Sitagliptin as a novel treatment agent for non-al- coholic Fatty liver disease patients with type 2 diabetes mellitus. Hepato-gastroenterology. 2011;58(112):2103-5}}. ובניסוי נוסף אקראי כפול סמויות שנמשך חצי שנה נמצאה ירידה ברמות טריגליצרידים כבדיים{{הערה|שם=הערה170|Macauley M, Hollingsworth KG, Smith FE, Thelwall PE, Al-Mrabeh A, Schweizer A, et al. Effect of vildagliptin on hepatic steatosis. The Journal of Clinical Endocrinology & Metabolism. 2015;100(4):1578-85}}. במחקר נוסף שפורסם ב-2016 וכלל 50 מטופלים עם כבד שומני שחלקם קיבלו [[Sitagliptin|סיטגליפטין]] וחלקם פלצבו למשך 24 שבועות, לא נמצא הבדל משמעותי בין 2 הקבוצות מבחינת אנזימי כבד או דרגת הפיברוזיס הכבדית שנבדקה באמצעים לא פולשניים{{הערה|שם=הערה171|Cui J, Philo L, Nguyen P, Hofflich H, Hernandez C, Bettencourt R, et al. Sitagliptin vs. placebo for non-alcoholic fatty liver disease: a randomized controlled trial. Journal of hepatology. 2016;65(2):369-76}}. | ||
| − | + | במחקר קטן נוסף שכלל ביופסיות, שוב לא נמצא הבדל בין קבוצת הפלצבו לקבוצה שטופלה בסיטגליפטין מבחינת מדדי פיברוזיס{{הערה|שם=הערה172| Joy TR, McKenzie CA, Tirona RG, Summers K, Seney S, Chakrabarti S, et al. Sitagliptin in patients with non-alcoholic steato- hepatitis: a randomized, placebo-controlled trial. World journal of gastroenterology. 2017;23(1):141}}. הפרופיל הבטיחותי של תרופות מסוג נוגדי 4-DPP מצוין. | |
| − | + | לסיכום: מספר המחקרים שבדקו את הנושא קטן, ההמלצות לא חד משמעיות ונכון להיום יעילות נוגדי 4-DPP בכבד שומני איננה ברורה והם אינם מומלצים כטיפול ייעודי. | |
| − | |||
| − | + | === התרופות החדשות לטיפול בסוכרת === | |
| + | אחת מפריצות הדרך המשמעותיות ביותר בתחום הטיפול בסוכרת אירעה עם הכנסת הדור החדש של טיפולים תרופתיים בסוכרת מסוג [[GLP-1|GLP-1 agonist]] ו[[SGLT2 inhibitor|מעכבי SGLT2]]. | ||
| − | + | מדובר ב-2 קבוצות של תרופות שבמספר לא מבוטל של מחקרים שכלל מעל 75,000 מטופלים הוכיחו הפחתה של הסיכון לסיבוכים קרדיו-ווסקולריים משמעותיים ([[אוטם לבבי]], [[אוטם מוחי]] ומוות ממחלה קרדיווסקולרית) בחולי סוכרת עם מחלת לב טרשתית ידועה{{הערה|שם=הערה173|Marso SP, Daniels GH, Brown-Frandsen K, Kristensen P, Mann JF, Nauck MA, et al. Liraglutide and cardiovascular outcomes in type 2 diabetes. New England Journal of Medicine. 2016;375(4):311-22}}{{הערה|שם=הערה174|Marso SP, Bain SC, Consoli A, Eliaschewitz FG, Jodar E, Leiter LA, et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med. 2016;375:1834-44}}{{הערה|שם=הערה175| Hernandez AF, Green JB, Janmohamed S, D'Agostino Sr RB, Granger CB, Jones NP, et al. Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double-blind, randomised place- bo-controlled trial. The Lancet. 2018,392(10157):! 519-29}}. בנוסף, הטיפול בתרופות אלו הפחית את הסיכון להתקדמות מחלת כליות בחולים סוכרתיים{{הערה|שם=הערה176|Neal B, Perkovic V, Mahaffey KW, De Zeeuw D, Fulcher G, Erondu N, et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes. New England Journal of Medicine. 2017;377(7):644-57}}{{הערה|שם=הערה177|Mann JF, 0rsted DD, Brown-Frandsen K, Marso SP, Poulter NR, Rasmussen S, et al. Liraglutide and renal outcomes in type 2 diabetes. New England Journal of Medicine. 2017;377(9):839-48}}{{הערה|שם=הערה178|McGuire DK, Shih WJ, Cosentino F, Charbonnel B, Cherney DZ, Dagogo-Jack S, et al. Association of SGLT2 inhibitors with cardiovascular and kidney outcomes in patients with type 2 diabetes: a meta-analysis. JAMA cardiology. 2021;6(2):148-58}}. | |
| − | |||
| − | + | [[קובץ:Fatty diabetes 2.png|מרכז|ממוזער|600 פיקסלים|'''תרשים 2. סיכום ממצאים לפי "פירמידת ההוכחה" של הטיפול בשינוי אורחות חיים בכבד שומני לא אלכוהולי'''.]] | |
| + | [[קובץ:Fatty diabetes 3.png|מרכז|ממוזער|600 פיקסלים|'''תרשים 3. סיכום ההמלצות לאורחות חיים כטיפול בכבד שומני'''.]] | ||
| − | + | === GLP-1 Agonists === | |
| + | פעולתם העיקרית של האגוניסטים של קולטני 1-GLP הוא שחרור אינסולין מתאי בתא בלבלב ועיכוב שחרור גלוקגון. בנוסף להשפעה ישירה על רמות הגלוקוז, נמצא שתרופות אלו משפיעות על תחושת השובע וגורמות לירידה במשקל וכאמור מפחיתות את הסיכון לאירועים קרדיווסקולריים משמעותיים והתקדמות מחלת כליות בחולים הסוכרתיים. במספר מחקרים נמצא שקיימים קולטנים ל-1-GLP בתאי בכבד ושקולטנים אלו חשובים בהורדת דרגת סטאטוזיס In vitro{{הערה|שם=הערה179|Gupta NA, Mells J, Dunham RM, Grakoui A, Handy J, Saxena NK, et al. Glucagon-like peptide-1 receptor is present on hu-man hepatocytes and has a direct role in decreasing hepatic steatosis in vitro by modulating elements of the insulin signaling pathway. Hepatology. 2010;51(5):1584-92}}, השילוב של תרופה שמורידה תיאבון, מפחיתה במשקל ומשפיעה על המטבוליזם של גלוקוז יחד עם קיום קולטנים על תאי הכבד, הוביל לבדיקת ההשפעה של קבוצת תרופות זו על כבד שומני. מספר המחקרים שבדק את השפעת האגוניסטים לקולטני 1-GLP על כבד שומני מוגבל - חלקם לא כפולי סמיות, חלקם ללא פלצבו, רובם מערב מספר קטן של מטופלים. במטא-אנליזה של 11 מחקרים שכללו כ-950 מטופלים שטופלו למחלת הכבד השומני עם אגוניסטים לקולטני 1-GLP שונים בממוצע ל-26 שבועות נמצאה ירידה בכמות השומן הכבדי כפי שנבדק ב-[[MRI|MRI{{כ}}]] (Magnetic Resonance Imaging) או ביופסיה, ירידה ברמת אנזימי כבד ושיפור היסטולוגי ללא החמרת פיברוזיס במחקרים שכללו ביופסיה{{הערה|שם=הערה180|Mantovani A, Petracca G, Beatrice G, Csermely A, Lonardo A, Targher G. Glucagon-Like Peptide-1 receptor agonists for treatment of nonalcoholic fatty liver disease and nonalcoholic steatohepatitis: an Updated Meta-Analysis of randomized controlled trials. Metabolites. 2021;11(2):73}}. נרחיב על 3 מהמחקרים הגדולים יותר בתחום. בראשון, נבדקה השפעת [[Liraglutide]] על הכבד. | ||
| − | == | + | Liraglutide הוא אגוניסט לקולטני 1-GLP, הניתן פעם ביום, ונרשם בארצות הברית, אירופה וישראל כתרופה כנגד השמנה. במטא-אנליזה גדולה שכללה כ-4,000 מטופלים עם סוכרת מסוג 2, נמצא שטיפול במשך 26 שבועות בLiraglutide שיפר באופן משמעותי אנזימי כבד ונסבל בצורה טובה{{הערה|שם=הערה181|Armstrong MJ, Houlihan DD, Rowe IA, Clausen WH, Elbrond B, Gough SC, et al. Safety and efficacy of liraglutide in patients with type 2 diabetes and elevated liver enzymes: individual patient data meta-analysis of the LEAD program. Aliment Pharma- col Then 2013;37(2):234-42}}. ההשפעה הישירה של Liraglutide על ההיסטולוגיה הכבדית נבדקה במחקר ה-LEAN. במחקר זה ניתן Liraglutide במינון יומי של 1.8 מיליגרם בחולים עם מכ"ש. הניסוי היה מבוקר, אקראי, כפול סמיות וכלל 52 מטופלים עם מכ"ד, חלקם עם סוכרת. במחקר נמצא שהטיפול בלירגלוריד הוביל לירידה בכמות השומן הכבדי ושיפור במרקרים היסטולוגיים כמו Hepatocyte ballooning, אבל ללא שינוי משמעותי בדלקת. אף שלא נצפתה נסיגה משמעותית בדרגת הפיברוזיס, דווח על האטה בהתקדמות הפיברוזיס במספר גדול יותר של מטופלים שטופלו לעומת כאלו שלא קבלו טיפול{{הערה|שם=הערה182|Armstrong MJ, Gaunt P, Aithal GP, Barton D, Hull D, Parker R, et al. Liraglutide safety and efficacy in patients with non-alcoholic steatohepatitis (LEAN): a multicentre, double-blind, randomised, placebo-controlled phase 2 study. Lancet. 2016;387(10019):679-90}}. במחקר קטן אחר נמצא שטיפול ב-[[Exenatide]], אגוניסט 1-GLP קצר טווח הניתן פעמיים ביום, שיפר רמות טרנסאמינזות וגרם לירידה במשקל בחולים עם כבד שומני{{הערה|שם=הערה183| Klonoff DC, Buse JB, Nielsen LL, Guan X, Bowlus CL, Holcombe JH, et al. Exenatide effects on diabetes, obesity, cardiovas- cular risk factors and hepatic biomarkers in patients with type 2 diabetes treated for at least 3 years. Current medical research and opinion. 2008;24(1):275-86}}. במחקר כפול סמויות נוסף שפורסם בספטמבר 2020 ב-NEJM{{כ}} (New England Journal of Medicine) נבדק האם הטיפול ב[[Semaglutide]] משפר היסטולוגיה כבדית בחולים עם מכ"ד. מדובר באגוניסט לקולטני 1-GLP ארוך טווח הניתן אחת לשבוע. המחקר, כפול סמויות נמשך 72 שבועות, כלל 320 מטופלים עם ובלי סוכרת, עם כבד שומני-מכ"ד ופיברוזיס כבדי בדרגה אחת עד שלוש (מוכח בביופסיה) כשחלקם קיבלו Semaglutide במינונים שונים-0.1, 0.2 ו-0.4 מיליגרם או קבלו פלצבו. המטרה הראשונית של המחקר הייתה לבדוק שיפור בסמנים ההיסטולוגים מבחינת המכ"ד ללא החמרה של פיברוזיס. במחקר נמצא ש-59 אחוזים מהמטופלים שקבלו Semaglutide במינון של 0.4 מיליגרם תת-עורי הראו נסיגה של מכ"ד ללא החמרה במצב הפיברוזיס (0.001 >p). המחקר לא הצליח להוכיח שיפור משמעותי סטטיסטי בדרגת הפיברוזיס בקבוצה שקיבלה Semaglutide{{הערה|שם=הערה184|Newsome PN, Buchholtz K, Cusi K, Linder M, Okanoue T, Ratziu V, et al. A placebo-controlled trial of subcutaneous sema- glutide in nonalcoholic steatohepatitis. New England Journal of Medicine. 2021;384(12):1113-24}}. בניסוי אחר שהשווה מתן שילוב של Exenatide ואינסולין למתן אינסולין בלבד בחולים עם כבד שומני, השמנת יתר וסוכרת נמצא שבקבוצה שטופלה ב-Exenatide ואינסולין הייתה ירידה משמעותית במשקל גוף, היקף מותן ורמות אנזימי כבד לעומת הקבוצה שטופלה באינסולין בלבד{{הערה|שם=הערה185|Shao N, Kuang HY, Hao M, Gao XY, Lin WJ, Zou W. Effects of exenatide on obesity and NAFLD with elevated liver enzymes in patients with type 2 diabetes. Diabetes/metabolism research and reviews. 2014}}. |
| − | == | + | בניסוי נוסף, השוו מתן מטפורמין ל-Exenatide בחולים סכרתיים עם כבד שומני ונמצא יתרון למתן אקסנטייד מבחינת נרמול אנזימי כבד, ירידה במשקל וירידה במדדי דלקת{{הערה|שם=הערה186| Fan H, Pan Q, Xu Y, Yang X. Exenatide improves type 2 diabetes concomitant with non-alcoholic fatty liver disease. Arquiv- os brasileiros de endocrinologia e metabologia. 2013;57(9):702-8}}. בניסוי קטן שכלל 21 מטופלים נמצא יתרון לשילוב של Pioglitazone ו-Exenatide לעומת Pioglitazone לבד מבחינת הורדת כמות שומן בכבד{{הערה|שם=הערה187|Sathyanarayana P, Jogi M, Muthupillai R, Krishnamurthy R, Samson SL, Bajaj M. Effects of combined exenatide and pioglita- zone therapy on hepatic fat content in type 2 diabetes. Obesity (Silver Spring). 2011;19(12):2310-5}}. נכון להיום, קיים מידע מוגבל לגבי יעילות הטיפול באגוניסטים לקולטני 1-GLP בחולים עם כבד שומני וסוכרת. יש מקום לביצוע ניסויים מבוקרים אקראיים גדולים לפני מתן המלצה גורפת. |
| − | + | מעניין לציין שבמספר מחקרים שבדקו את היעילות של Liraglutide לעומת מטפורמין או גליקלזיד ל-24 שבועות, נמצא שבכל הקבוצות הייתה ירידה בשומן התוך כבדי אבל הירידה הגדולה ביותר הייתה בקבוצה של ה-Liraglutide. אין המלצה של שום איגוד מקצועי להשתמש באגוניסטים לקולטני 1-GLP כתרופת הבחירה הראשונה בחולים עם כבד שומני וסוכרת. | |
| − | |||
| − | |||
| − | + | === מעכבי SGLT2 === | |
| + | תרופות ממשפחת מעכבי SGLT2 מפחיתות את רמות הסוכר בדם באמצעות מניעת ספיגתו בכליות והפרשתו בשתן. נמצא שמטופלים שנטלו תרופות ממשפחה זו הפחיתו ממשקל גופם ומהיקף המותניים. כמו כן תרופות אלו מסייעות בהפחתת [[לחץ דם|לחץ הדם]] במידה מתונה. ההשפעה המשמעותית ביותר של תרופות מהקבוצה הזו היא, כאמור, בהפחתה הדרמטית בסיכון לאירועים קרדיווסקולריים משמעותיים כולל הפחתה באשפחים עקב אי ספיקת לב ובסיכון להתקדמות מחלת כליות בחולים הסוכרתיים. במספר מחקרי מעבדה נמצא קשר בין מתן תרופות אלו לבד או בשילוב עם תרופות מסוג מעכבי 4-DPP לירידה בכמות השומן בכבד ושיפור בדרגת הצלקת הכבדית{{הערה|שם=הערה188|Nishimura N, Kitade M, Noguchi R, Namisaki T, Moriya K, Takeda K, et al. IpragIiflozin, a sodium-glucose cotransporter 2 inhibitor, ameliorates the development of liver fibrosis in diabetic Otsuka Long-Evans Tokushima fatty rats. J Gastroenterol. 2016;51(12):1141-9}}{{הערה|שם=הערה189|Jojima T, Tomotsune T, Iijima T, Akimoto K, Suzuki K, Aso Y. Empagliflozin (an SGLT2 inhibitor), alone or in combination with linagliptin (a DPP-4 inhibitor), prevents steatohepatitis in a novel mouse model of non-alcoholic steatohepatitis and diabetes. Diabetol Metab Syndr. 2016;8:45}}. | ||
| − | + | מספר מחקרים שפורסמו בדקו את ההשפעה של תרופות ממשפחה זו על כבד שומני במספר מצומצם של חולים עם סכרת. נדון בחלק מהם - במחקר הראשון, שכלל 66 חולים עם סוכרת וכבד שומני, נמצא שבמטופלים שקיבלו תרופה ממשפחת מעכבי SGLT2 נראה שיפור בכמות השומן הויסרלי ובמשקל ללא שינוי באנזימי כבד{{הערה|שם=הערה190| Ito D, Shimizu S, Inoue K, Saito D, Yanagisawa M, Inukai K, et al. Comparison of Ipragliflozin and Pioglitazone Effects on Nonalcoholic Fatty Liver Disease in Patients With Type 2 Diabetes: A Randomized, 24-Week, Open-Label, Active-Controlled Trial. Diabetes Care. 2017;40(10):1364-72}}. | |
| − | == | + | במחקר השני, שכלל 50 מטופלים עם סוכרת וכבד שומני, נמצאה ירידה משמעותית בכמות השומן הכבדי בקבוצת המטופלים שקיבלה [[Empagliflozin]] לצד ירידה ברמת ה-ALT{{הערה|שם=הערה191|Kuchay MS, Krishan S, Mishra SK, Farooqui KJ, Singh MK, Wasir JS, et al. Effect of Empagliflozin on Liver Fat in Patients With Type 2 Diabetes and Nonalcoholic Fatty Liver Disease: A Randomized Controlled Trial (E-LIFTTrial). Diabetes Care. 2018;41(8):1801-8}}. מחקר נוסף כפול סמויות שפורסם בשנת 2020 וכלל 84 חולים עם סוכרת חדשה מאוזנת הדגים גם הוא ירידה בכמות השומן הכבדי (נבדק ב-MRI) במטופלים שקיבלו ב-Empagliflozin במשך 24 שבועות באופן משמעותי יחסית לקבוצת הפלצבו{{הערה|שם=הערה192|Kahl S, Gancheva S, StraBburger K, Herder C, Machann J, Katsuyama H, et al. Empagliflozin effectively lowers liver fat content in well-controlled type 2 diabetes: a randomized, double-blind, phase 4, placebo-controlled trial. Diabetes Care. 2020;43(2):298-305}}. |
| − | אין | + | אחת מתופעות הלוואי החשובות והשכיחות של קבוצה זו של תרופות היא העלייה בשכיחות [[דלקות בדרכי השתן]], הנרתיק ואזור הפין. תופעות לוואי נוספות הם קטואצידוזיס עם רמת סוכר תקינה, התייבשות ועליה ברמת הכולסטרול. נכון להיום אין הנחיה לתת מעכבי SGLT2 כתרופת קו ראשון לחולים עם כבד שומני וסוכרת. |
| − | == | + | === טיפולים תרופתיים אחרים === |
| + | אין טיפול תרופתי המאושר על ידי גופים רגולטוריים לטיפול במחלת הכבד השומני. מעבר לתרופות לטיפול בסוכרת והשמנה שתוארו לעיל, קיימות מספר תרופות נוספות הנמצאות במחקרים מתקדמים ומיועדות ספציפית לטיפול במכ"ש. | ||
| − | + | '''אגוניסטים ל-FXR -''' האגוניסט ל-FXR חומצה אבטכולית מאושר לטיפול ב[[דלקת מרתית ראשונית]] (PBC{{כ}} - Primary Biliary Cholangitis). תרופה זו נוסתה גם כתרופה למכ"ש ותוצאות מחקר ה-FLINT הראו שיפור במדדי דלקת ללא החמרה בפיברוזיס{{הערה|שם=הערה193|Neuschwander-Tetri BA, Loomba R, Sanyal AJ, Lavine JE, Van Natta ML, Abdelmalek MF, et al. Farnesoid X nuclear receptor ligand obeticholic acid for non-cirrhotic, non-alcoholic steatohepatitis (FLINT): a multicentre, randomised, placebo-controlled trial. Lancet. 2015;385(9972):956-65}}. | |
| − | + | במחקר פאזה שלישית נוסף בתרופה נבדק השימוש במינונים עולים של חומצה אבטיכולית לעומת פלצבו בכ-2000 חולים עם פיברוזיס בדרגות F1-3, (מתוכם 931 עם פיברוזיס בדרגות F2-3). תוצאות ביניים של מחקר זה פורסמו. היה שיפור משמעותי תלוי מינון ברמת הפיברוזיס בקבוצות הטיפול מול הפלצבו. לא היה הבדל בהעלמות המכ"ד (NASH resolution) בין הקבוצות. החוקרים סיכמו שחומצה אובטיכולית במינון 25 מיליגרם גרם לשיפור משמעותי בפיברוזיס ומדדי מכ"ד. למרות התוצאות המבטיחות, התרופה לא אושרה בינתיים על ידי ה-FDA{{כ}} (Food and Drug Administration){{הערה|שם=הערה194|Younossi ZM, Ratziu V, Loomba R, Rinella M, Anstee QM, Goodman Z, et al. Obeticholic acid for the treatment of non-alcoholic steatohepatitis: interim analysis from a multicentre, randomised, placebo-controlled phase 3 trial. Lancet. 2019;394(10215):2184-96}}. | |
| − | = | + | אנלוגים ל-FGF19 מחקרים שונים הראו שהרמות של פקטור השיעתוק 19 Fibroblast Growth Factor נמוכות בחולי מכ"ש ועולות לאחר ניתוחים בריאטריים. זהו סקטור המושפע מ-FXR ומשפיע על יצור [[מלחי מרה]]. התרופה אלדפאמין ([[Aldafamin]]) נבדקה במחקר פאזה שנייה ב-82 חולי מכ"ש שהוכח בביופסיה. התרופה ניתנה בזריקה תת-עורית במינונים שונים והראתה שיפור בתכולת השומן בכבד כפי שנמדד בהדמיה{{הערה|שם=הערה195|Harrison SA, Rinella ME, Abdelmalek MF, Trotter JF, Paredes AH, Arnold HL, et al. NGM282 for treatment of non-alcoholic steatohepatitis: a multicentre, randomised, double-blind, placebo-controlled, phase 2 trial. Lancet. 2018;391(10126):1174-85}}. |
| − | + | במחקר פתוח וללא קבוצת בקורת הדגימה התרופה שיפור במדדים היסטולוגיים של מכ"ד ללא השפעה על ממדים מטבוליים. בנוסף החולים קיבלו סטטין על מנת לסתור את תופעת הלוואי הידועה של תרופה זו הגורמת לעליית כלוסטרול{{הערה|שם=הערה196|Harrison SA, Rossi SJ, Paredes AH, Trotter JF, Bashir MR, Guy CD, et al. NGM282 Improves Liver Fibrosis and Histology in 12 Weeks in Patients With Nonalcoholic Steatohepatitis. Hepatology. 2020,71 (4):1198-212}}. תרופות נוספות הכוללות אנלוג ל-FGF21 הפטוקין המבקר את משק הסוכר, מעכבי (Acetyl COA Carboxylase (ACC ואגוניסטים של Stearoyl CoA desaturase המבקרים את משק הליפידים ואגוניסטים של Thyroid hormone receptor beta המבקרים את פעולת [[הורמוני התריס]] נמצאים במחקר מתקדם. בנוסף מתמקדות חברות התרופות בתרופות להיכולות להביא לנסיגת פיברוזיס, מבין המובילות נמצא מעכב ל-2 CC chemokine receptor שהראה תוצאות מבטיחות במחקרים ראשוניים. | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | == | + | '''סטטינים -''' מחקרים עדכניים מרמזים שלטיפול עם [[סטטינים]] במטופלים עם כבד שומני יש השפעה מיטבית על דרגת השומן והצלקת הכבדית ואף עשוי לנרמל אנזימי כבד{{הערה|שם=הערה197|Athyros VG, Tziomalos K, Gossios TD, Griva T, Anagnostis P, Kargiotis K, et al. Safety and efficacy of long-term statin treat- ment for cardiovascular events in patients with coronary heart disease and abnormal liver tests in the Greek Atorvastatin and Coronary Heart Disease Evaluation (GREACE) Study: a post-hoc analysis. Lancet. 2010;376(9756):1916-22}}{{הערה|שם=הערה198|Dongiovanni P, Petta S, Mannisto V, Mancina RM, Pipitone R, Karja V, et al. Statin use and non-alcoholic steatohepatitis in at risk individuals. J Hepatol. 2015;63(3):705-12}}. בסקירת ספרות של Cochrane שפורסמה ב-2013 נמצאו 2 מחקרים בלבד עם מספר קטן של משתתפים שבדקו באופן ישיר את השימוש בסטטינים כטיפול בכבד שומני. הרושם הוא שסטטינים יכולים לשפר רמת טרנסאמינזות{{הערה|שם=הערה199| Eslami L, Merat S, Malekzadeh R, Nasseri-Moghaddam S, Aramin H. Statins for non-alcoholic fatty liver disease and non-al- coholic steatohepatitis. The Cochrane database of systematic reviews. 2013;12:CD008623}}. גם בהצהרת מומחים שפורסמה ב-2017 צוין כי אץ התווית נגד למתן סטטינים במטופלים עם כבד שומני, וייתכן אף שלסטטינים יש פוטנציאל להאט את חומרת המחלה הכבדית במטופלים עם כבד שומני ודיסליפידמיה במקביל להורדת הסיכון הלבבי{{הערה|שם=הערה200|Athyros VG, Alexandrides TK, Bilianou H, Cholongitas E, Doumas M, Ganotakis ES, et al. The use of statins alone, or in com- bination with pioglitazone and other drugs, for the treatment of non-alcoholic fatty liver disease/non-alcoholic steatohepati- tis and related cardiovascular risk. An Expert Panel Statement. Metabolism. 2017;71:17-32}}. יש לציץ שההמלצות המשותפות של האיגודים האירופאים לחקר מחלות כבד, סוכרת והשמנה הן שאמנם סטטינים לא נבדקו בצורה מספקת כטיפול לכש"ד, אבל השימוש שלהם במחלת הכבד השומני הוא בטוח, לא מעלה את הסיכון לנזק כבדי וייתכן אף שמוריד רמת אנזימי כבד{{הערה|שם=הערה55}}. |
| − | + | ||
| − | + | בהתבסס על הממצאים מהספרות, אין התוויית נגד למתן סטטינים במטופלים עם כבד שומני. חלק גדול ממטופלים עם כבד שומני סובלים מתסמונת מטבולית, סוכרת ומחלת לב כלילית וזקוקים לסטטינים כחלק מהטיפול הכולל בגורמי סיכון לבביים. | |
| − | {{ | + | |
| − | + | == תוספי מזון == | |
| − | + | === ויטמין E === | |
| + | מספר ניסויים קליניים אקראיים בדקו את השפעת ויטמין E במינונים גבוהים בחולים עם כבד שומני ללא סוכרת. הגדול מביניהם הוא מחקר שפורסם ב-2010 ב-NEJM{{כ}} (PIVENS trail) וכלל 247 מטופלים עם כבד שומני ללא סוכרת וללא שחמת, ובו הושוו 3 זרועות: מטופלים שקבלו Pioglitazone או ויטמין E (במינון של 800 מיליגרם ליום) או פלצבו לתקופה של 96 שבועות. נמצא שהמטופלים שקיבלו ויטמין E הראו שיפור ברמת אנזימי הכבד עם שיפור במדדי הדלקת וירידה בכמות השומן הכבדי אך ללא שיפור ברמת הצלקת{{הערה|שם=הערה167}}. בניסוי קליני אקראי נוסף, השתתפו 105 חולים עם סברת שחולקו ל-3 קבוצות - קבוצה ראשונה קבלה ויטמין E במינון של 400 מיליגרם פעמיים ביום, קבוצה שנייה קיבלה ויטמין E במינון של 400 מיליגרם פעמיים ביום ו-Pioglitazone{{כ}} 45 מיליגרם ליום וקבוצה שלישית קיבלה פלצבו. משך המחקר היה 18 חודשים, ומטרתו הייתה לבדוק שיפור היסטולוגי כבדי משמעותי ללא החמרה בדרגת הפיברוזיס הכבדי. בקבוצה שקיבלה טיפול משולב נמצא שיפור היסטולוגי משמעותי עם שיפור בדרגת הסטאטוזיס, שיפור בדרגת הדלקת ושיפור בדרגת ה-Ballooning, לעומת הקבוצה שקיבלה ויטמין E בלבד ובה נמצא שיפור בדרגת הסטאטוזיס בלבד. ב-2 הקבוצות לא נצפה שיפור בדרגת הפיברוזיס{{הערה|שם=הערה201|Bril F, Biernacki DM, Kalavalapalli S, Lomonaco R, Subbarayan SK, Lai J, et al. Role of Vitamin Efor Nonalcoholic Steatohep- atitis in Patients With Type 2 Diabetes: A Randomized Controlled Trial. Diabetes Care. 2019;42(8):1481-8}}. | ||
| + | |||
| + | אולם, עצם השימוש בוויטמין E במינונים גבוהים שנוי במחלוקת עקב עדויות לגבי קשר בין צריכתו לעלייה בתמותה{{הערה|שם=הערה202|Bjelakovic G, Nikolova D, Gluud LL, Simonetti RG, Gluud C. Mortality in randomized trials of antioxidant supplements for primary and secondary prevention: systematic review and meta-analysis. Jama. 2007;297(8):842-57}}, עלייה בהיארעות אוטם מוחי המורגי{{הערה|שם=הערה203|Schurks M, Glynn RJ, Rist PM, Tzourio C, Kurth T. Effects of vitamin E on stroke subtypes: meta-analysis of randomised controlled trials. BMJ. 2010;341:c5702}} ועלייה בהיארעות [[סרטן הערמונית|שאת ממאירה של ערמונית]]{{הערה|שם=הערה204|Klein EA, Thompson IM, Jr., Tangen CM, Crowley JJ, Lucia MS, Goodman PJ, et al. Vitamin E and the risk of prostate cancer: the Selenium and Vitamin E Cancer Prevention Trial (SELECT). Jama. 2011 ;306(14):1549-56}}. נכון להיום אין המלצה של EASL למתן ויטמין E בחולים עם סוכרת וכבד שומני{{הערה|שם=הערה55}}. בהנחיות של ה-AASLD{{הערה|שם=הערה12}} וכן בהנחיות מ-2019 של ה-ESPEN יש המלצה למתן ויטמין E, אך רק בחולים לא סוכרתיים ועם כש"ד שהודגם היסטולוגיה{{הערה|שם=הערה56}}. | ||
| + | |||
| + | === אומגה 3 === | ||
| + | נערכו מספר ניסויים קליניים אקראיים באיכות גבוהה מבחינת גודל המדגם, משך המעקב וביצוע ביופסיית כבד עוקבת בחלקם, שבחנו השפעת תוסף אומגה 3 בכבד שומני. המחקרים לא הראו תוצאות עקביות, אולי עקב שימוש בתוספים במינונים שונים והרכב שונה של חומצות שומן אומגה 3. אולם, נראה כי תיתכן השפעה מיטיבה על השומן הכבדי אך לא על דלקת, צלקת ואף לא על תנגודת לאינסולין{{הערה|שם=הערה205| Scorletti E, Bhatia L, McCormick KG, Clough GF, Nash K, Hodson L, et al. Effects of purified eicosapentaenoic and docosa- hexaenoic acids in non-alcoholic fatty liver disease: Results from the *WELCOME study. Hepatology. 2014}}{{הערה|שם=הערה206|Sanyal AJ, Abdelmalek MF, Suzuki A, Cummings OW, Chojkier M, Group E-AS. No significant effects of ethyl-eicosapenta- noic acid on histologic features of nonalcoholic steatohepatitis in a phase 2 trial. Gastroenterology. 2014;147(2):377-84 e1}}{{הערה|שם=הערה207|Argo CK, Patrie JT, Lackner C, Henry TD, de Lange EE, Weltman AL, et al. Effects of n-3 fish oil on metabolic and histological parameters in NASH: a double-blind, randomized, placebo-controlled trial. Journal of hepatology. 2015;62(1 ):190-7}}. בהנחיות של האיגוד האירופאי לחקר הכבד (EASL) משנת 2016 אין המלצה לתת אומגה 3 כטיפול ספציפי בכבד שומני{{הערה|שם=הערה55}} וכך גם בהנחיות החדשות משנת 2018 של האיגוד האמריקאי לחקר הכבד - AASLD{{כ}} (American Association for the Study of Liver Diseases){{הערה|שם=הערה12}}, ובהנחיות של ה-ESPEN משנת 2019{{הערה|שם=הערה56}}. | ||
| + | {| class="wikitable" | ||
| + | |+טבלה 5. ניסויים קליניים אקראיים כפולי סמיות שבחנו השפעת תוסף אומנה 3 (שמן דנים) על כבד שומני לא אלכוהולי | ||
| + | |Author | ||
| + | |Supplement mg/day | ||
| + | |Duration | ||
| + | |||
| + | (M) | ||
| + | |Sample | ||
| + | |Improved Steatosis | ||
| + | |Improved NASH | ||
| + | |Improved Fibrosis | ||
| + | |- | ||
| + | |Argo CK, J of Hepatology 2015 | ||
| + | |EPA & DHA 3000 | ||
| + | |12 | ||
| + | |34 NASH | ||
| + | |Yes | ||
| + | |No | ||
| + | |No | ||
| + | |- | ||
| + | |Sanyal AJ, Gastroenterology 2014 | ||
| + | |EPA 2700 | ||
| + | |12 | ||
| + | |243 NASH | ||
| + | |No | ||
| + | |No | ||
| + | |No | ||
| + | |- | ||
| + | |Scorletti E, Hepatology 2014 | ||
| + | |EPA & DHA 4000 | ||
| + | |15-18 | ||
| + | |91 NAFLD | ||
| + | |Yes | ||
| + | |NE | ||
| + | |No | ||
| + | |||
| + | (by fibrosis score) | ||
| + | |- | ||
| + | |Nobili V, Arch DisChild 2011 | ||
| + | |DHA 500 or 250 | ||
| + | |6 | ||
| + | |60 children NAFLD | ||
| + | |Yes | ||
| + | |NE | ||
| + | |NE | ||
| + | |- | ||
| + | | colspan="7" |הערה: NE מציין כי המדד לא נבדק | ||
| + | |} | ||
| + | |||
| + | === סיכום === | ||
| + | הגישה הטיפולית בחולה הסוכרתי עם כבד שומני מתבססת על איתור וטיפול מיטבי במרכיבים נוספים של התסמונת המטבולית, איתור וטיפול בגורמי סיכון לבביים נוספים, הערכת חומרת המחלה הכבדית מבחינת נוכחות צלקת, שחמת או [[הפטומה]] על ידי מעקב קבוע הכולל סונר, טיפול בשומן כבדי עצמו על ידי שינוי אורחות חיים ואיזון הסוכרת. | ||
| − | + | ההמלצות מבוססות הראיות לתזונה ופעילות גופנית בחולי מכ"ש מסוכמות בגרף מספר 1. | |
| + | == חשוב לזכור - הכבד השומני - הקשר לסוכרת מסוג 2 ודרכי טיפול == | ||
| + | # המצאות מחלת הכבד השומני שאינה בגין צריכת אלכוהול מגיעה עד 75 אחוזים בחולים הסוכרתיים | ||
| + | # היארעות סוכרת באנשים עם כבד שומני גבוהה יותר מאשר באוכלוסייה דומה מבחינת גיל וגורמי סיכון מקובלים אחרים | ||
| + | # סוכרת נחשבת כגורם סיכון להופעת דלקת וצלקת כבדית בחולים עם כבד שומני. השכיחות של שחמת בחולים עם כבד שומני וסוכרת היא 25 אחוזים לעומת 10 אחוזים בחולים עם כבד שומני ללא סוכרת | ||
| + | # הסיכון של חולה סוכרת עם כבד שומני למות מכל סיבה שהיא הוא פי 2.2 מאשר חולה סוכרתי ללא כבד שומני | ||
| + | # עצם הנוכחות של כבד שומני בחולה סוכרת חושף אותו לסיכון מוגבר למחלת לב כלילית, ללא קשר למרכיבי הסינדרום המטבולי | ||
| + | # לסוכרת ביטוי קשה יותר בחולים המשלבים סוכרת וכבד שומני, הן מבחינת הכבד והן מבחינת סיבוכים מאקרו ומיקרווסקולריים | ||
| + | # כל הערכה של מטופל עם סוכרת וכבד שומני צריכה לכלול הערכה של הפגיעה הכבדית והערכה כללית של מצב קרדיומטבולי | ||
| + | # בחולי סוכרת עם כבד שומני רצוי במיוחד לבצע הערכה של צלקת מתקדמת (פיברוזיס דרגה 3–4) באמצעים בלתי פולשניים מתוקפים שקיימים היום ואינם כרוכים בעלות נוספת, דונמת 4-FIB או באמצעות פיברוסקן | ||
| + | # שינוי באורחות חיים הוא אבן היסוד לטיפול בכבד שומני | ||
| − | {{ | + | ==ביבליוגרפיה== |
| − | + | {{הערות שוליים|יישור=שמאל}} | |
| − | |||
| − | }} | ||
| − | + | {{ייחוס|פרופסור שירה זלבר-שגיא, דיאטנית קלינית ואפידמיולוגית, ראש בית הספר לבריאות הציבור, אוניברסיטת חיפה והמכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי{{ש}}ד"ר חני ישועה, המכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי ושירותי בריאות כללית, מחוז תל-אביב יפו{{ש}}דנה איבנקובסקי-וכקמן, דוקטורנטית, בית הספר לבריאות הציבור, אוניברסיטת חיפה, והמכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי{{ש}}ד"ר מאיה מרגלית, המכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי{{ש}}פרופ׳ אורן שבולת, מנהל המכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי ואוניברסיטת תל-אביב}} | |
[[קטגוריה:אנדוקרינולוגיה וסוכרת]] | [[קטגוריה:אנדוקרינולוגיה וסוכרת]] | ||
[[קטגוריה:גסטרואנטרולוגיה]] | [[קטגוריה:גסטרואנטרולוגיה]] | ||
[[קטגוריה:פנימית]] | [[קטגוריה:פנימית]] | ||
| + | [[קטגוריה:משפחה]] | ||
גרסה אחרונה מ־10:12, 30 ביוני 2023
המדריך לטיפול בסוכרת
מאת המועצה הלאומית לסוכרת, משרד הבריאות. עורכים מדעיים: ד"ר עופרי מוסנזון, פרופ׳ איתמר רז
| המדריך לטיפול בסוכרת | ||
|---|---|---|

| ||
| שם המחבר | פרופסור שירה זלבר-שגיא, ד"ר חני ישועה, דנה איבנקובסקי-וכקמן, ד"ר מאיה מרגלית, פרופסור אורן שבולת | |
| שם הפרק | כבד השומני - הקשר לסוכרת מסוג 2 ודרכי טיפול | |
| מאת | המועצה הלאומית לסוכרת, משרד הבריאות |
|
| מועד הוצאה | 2022 | |
| מספר עמודים | 614 | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – כבד שומני וסוכרת
הצטברות שומן בתוך תאי הכבד נקראת Hepatic steatosis וכאשר היא עולה על 5 אחוזים מוגדרת התופעה ככבד שומני (Hepatic steatosis, Fatty liver) נובע מצירוף של עודף יצור שומן (ליפוגנזה), הגעה מוגברת של טריגליצרידים מרקמת שומן פריפרי לכבד ותזונה עתירת שומן. גורמים אלה מובילים ל"הצפת" הכבד בשומן, בכמות העולה על יכולת הוצאתו.
NAFLD) Nonalcoholic Fatty Liver Disease) (מחלת הכבד השומני - מכ"ש), הוכרה כמחלה המהווה נטל רפואי רב משקל בשל הימצאותה הגבוהה באוכלוסייה הכללית, בשל היותה גורם סיכון משמעותי להתפתחות נזק כבדי ובשל הקשר לתחלואה נלווית. מכ"ש מוכרת כמחלת הכבד השכיחה ביותר בעולם[1], הימצאותה המוערכת באוכלוסייה הבוגרת היא 20–30 אחוזים ברוב המחקרים[2] ודווח אף על 46 אחוזים בארצות הברית[3] המצאות מכ"ש בקרב הסובלים מהשמנה מגיעה ל-70–80 אחוזים[2] ול-50–74 אחוזים בחולי סוכרת מסוג 2[3].
בעבר הקרוב נחשב כבד שומני לממצא מקרי ללא משמעות קלינית. אולם נכון ל-2022 ברור שכ-10–20 אחוזים מהסובלים מכבד שומני עלולים לפתח NASH) Non-Alcoholic Steato-Hepatitis) (כבד שומני דלקתי - כש"ד), שעשוי להוביל להצטלקות (פיברוזיס) ועד לשחמת על סיבוכיה, כולל סרטן כבד ראשוני.
בנוסף, כבד שומני נחשב למרכיב הכבדי של הסינדרום המטבולי וכגורם סיכון מוקדם לסוכרת ולמחלת לב איסכמית. במטא-אנליזה נמצא כי מכ"ש מגביר את הסיכון למחלת לב פי 2 (95% רווח בר סמך 2.3-1.8)[4]. בנוסף, הודגם כי מכ"ש מגביר את הסיכון לסוכרת פי 3.5 (95% רווח בר סמך 5.4-2.3) באופן בלתי תלוי בגורמי סיכון ידועים אחרים[4]. מחקרים נוספים הדגימו קשר בין כבד שומני לבין גידולים מחוץ לכבד, בעיקר במערכת העיכול[5][6].
גורמי סיכון עיקריים לכבד שומני
כבד שומני הוא מחלה מולטיפקטוריאלית שגורמיה ידועים רק בחלקם. בין גורמי הסיכון החשובים ביותר נכללים תנגודת לאינסולין ועלייה בשומן בטני עם עלייה ברמת לפטין וירידה ברמת האדיפונקטין. הקשר החזק של מכ"ש עם תנגודת לאינסולין ועם הסינדרום המטבולי תועד בהרחבה בספרות ויש ראיות לכך כי תנגודת לאינסולין קיימת גם בחולי מכ"ש רזים ולא סוכרתיים[7]. כמות גבוהה של שומן בטני מהווה גם היא גורם סיכון למכ"ש עקב השפעתה על ויסות השומן בכבד והתגלתה כגורם סיכון חשוב גם בבעלי משקל תקין[8]. גורם סיכון נוסף, ידוע פחות הוא עליית משקל. במחקר מעקב בן 7 שנים נמצא כי עליית משקל של 3–5 קילוגרם היא גורם קובע בהיארעות של כבד שומני חדש או ברמיסיה של כבד שומני קיים, ללא קשר למשקל התחלתי[9].
קיימת הסכמה רחבה כי גורמים התנהגותיים מעורבים בפתופזיולוגיה של כבד שומני כשההיבטים החשובים ביותר הם צריכת אנרגיה מופרזת, הרכב תזונה לקוי ואורח חיים יושבני המהווה גורם סיכון בפני עצמו לכבד שומני.
מאפיינים קליניים ואבחון של כבד שומני
מרבית המטופלים הם א-תסמיניים, ורוב המקרים של כבד שומני מתגלים באקראי בעת ביצוע בדיקת אולטרסאונד (סונר) או כשמודגמת הפרעה באנזימי הכבד בבדיקות דם שגרתיות. הפרעה באנזימי כבד תופיע בכ-10 אחוזים מהמטופלים עם כבד שומני ומתאפיינת לרוב בעלייה קלה עד בינונית בטרנסאמינזות עם יחס AST/ALT (Aspartate Transaminase/Alanine Transaminase) של פחות מ-1. תיתכן גם עלייה ב-GGT (Gamma Glutamyl Transferase) ובשכיחות נמוכה יותר גם בפוספטזה הבסיסית (ALK). לא נמצא קשר בין רמת האנזימים לחומרת המחלה ההיסטולוגית[10]. ירידה בספירת שורות הדם (בעיקר תרומבוציטופניה), היפואלבומינמיה או הארכת זמן פרותרומבין (PT, Prothrombin Time) עשויים לרמז על נוכחות שחמת כבד.
במטופלים ללא הפרעה באנזימי כבד בהם התגלה כבד שומני באקראי בסונר והם א-תסמינים מבחינת מחלות כבד וללא אנמנזה של צריכת אלכוהול מופרזת או נטילת תרופות היכולות לגרום לכבד שומני, ניתן להסיק שמדובר במכ"ש.
הסבירות למכ"ש עולה בנוכחות הסינדרום המטבולי הכולל השמנת יתר, רמת סוכר גבוהה בצום, סוכרת או דיסליפידמיה. אם קיימת הפרעה באנזימי כבד, האבחנה של כבד שומני תתבצע רק לאחר שלילת סיבות משניות אחרות להפרעה באנזימים, כמקובל בספרות, ובעיקר שלילת זיהום בנגיף דלקת הכבד מסוג B או C[11].
ביופסית כבד ואמצעי אבחון לא פולשניים
על אף חסרונות הבדיקה (ביניהם עלות, שונות דגימה, תחלואה ואף תמותה הקשורות בפרוצדורה)[12], ביופסיית כבד היא עדיין הדרך האמינה ביותר לאבחון של כש"ד ופיברוזיס במטופלים עם מכ"ש. יש לשקול ביופסיה בחולים עם מכ"ש ב-3 מצבים עיקריים:
- במטופלים בהם נותרה שאלה אבחנתית אם מדובר בכש"ד או בכש"ד בלבד (לאור ההיארעות הגבוהה של מכ"ש, לא נדיר למצוא מכ"ש במטופלים עם מחלות כבד אחרות) - לדוגמה מטופלים עם הפרעה ניכרת באנזימי הכבד, עם כייל גבוה של נוגדנים אוטואימוניים, ללא תסמונת מטבולית וכיוצא בזה;
- לאישוש חומרת הפגיעה ההיסטולוגית בכבד;
- בגיוס לניסויים קליניים
קיימים גם אמצעים לא חודרניים להעריך את חומרת ההצטלקות הכבדית, שהיא המדד היחיד שנקשר לתחלואה ותמותה כבדית ולהשתלת כבד במטופלים עם מכ"ש[13][14]. אמצעים אלו משמשים לסיווג חולים לכאלו המצויים בסיכון גבוה לפיברוזיס משמעותי (F3 - פיברוזיס מתקדם, או F4 - שחמת), שיש להפנות לבירור כבדי שיכלול בחלק לא מבוטל מהמקרים גם ביופסיית כבד, ולכאלו המצויים בסיכון נמוך לפיברוזיס משמעותי (F0 או F1), שאינם זקוקים לבירור כזה. האמצעים הבלתי פולשניים הנהוגים כוללים אלגוריתמים מנבאים המבוססים על בדיקות מעבדה (כגון NAFLD Fibrosis Score - NFS, Fibrosis 4 - FIB4 ו-Enhanced Liver Fibrosis (ELF) score) ובדיקות הדמיה המעריכות את אלסטיות הכבד, שמהן בדיקת הפיברוסקן - Vibration Controlled Transient Elastography) VCTE), היא הנפוצה והנחקרת ביותר. חשוב להדגיש, שבדיקות אלה תוקפו בהשוואה לביופסיית כבד; מכיוון שקיימות מגבלות לביופסיית כבר כסטנדרט להשוואה (כגון שונות דגימה, מהימנות בתוך הבודק ובין בודקים), ישנו ערך מקסימום אינהרנטי למידת הדיוק של בדיקות אלה.
אלגוריתמים מעבדתיים: מבין האלגוריתמים המעבדתיים המנבאים, FIB4 וה-NAFLD Fibrosis Score (NFS) נחקרו באופן נרחב באוכלוסיות מגוונות, והם מומלצים להערכה מוקדמת של מטופלים עם גורמי סיכון מטבוליים ומכ"ש[12][15][16][17]. אלגוריתמים אלו, המבוססים על פרמטרים קליניים ומעבדתיים פשוטים וניתנים לחישוב בקלות, בסיוע מחשבונים אינטרנטיים, ב-Point of care, הודגמו כמנבאים תמותה (Overall), תמותה קרדיווסקולרית ותמותה הקשורה בכבד (Liver-related mortality) בחולים עם מכ"ש.
FIB4 מבוסס על גיל, AST ,ALT ורמת טסיות, ומתאפיין ב-0.8< (Area under the receiver Operating characteristic (AUROC (שטח מתחת לעקומה, כמה שהוא יותר גבוה וקרוב ל-1 כך הרגישות והסגוליות, כלומר תוקף הבדיקה טוב יותר). לאבחנה של פיברוזיס בדרגה של F3 או F4.
ה-NFS מתבסס על גיל, BMI (Body Mass Index) ,ALT ,AST, נוכחות/העדר Impaired fasting glucose או סוכרת, ורמת אלבומין. במטא-אנליזה של 13 מחקרים לגבי NFS, שכללה 3,064 חולים עם מכ"ש, דווח על 0.85 AUROC לניבוי פיברוזיס מתקדם[4]. אלגוריתם מעבדתי נוסף שקיים באופן מסחרי, כרוך בעלות, ומבוסס על בדיקות שאינן מבוצעות באופן רוטיני (Procollagen III amino terminal peptide, חומצה היאלורונית ו-Tissue inhibitor of matrix metalloproteinase) הוא ה-(panel ELF (Enhanced Liver Fibrosis, שדווחו לגביו במטופלים עם מכ"ש AUROC, רגישות וסגוליות 0.90, 0.80 ו-0.90, בהתאמה, לאיתור פיברוזיס מתקדם[18]. בדיקת ה-ELF אושרה לשימוש מסחרי באירופה ונכנסה להמלצות ה-NICE לשלילת פיברוזיס מתקדם במטופלים עם מכ"ש; נכון לתחילת 2021, היא אינה בשימוש נרחב בישראל.
ב-FIB4 וב-NFS מוגדרים שני ערכי סף (cut-off); מטופלים בעלי ציון נמוך מערך הסף הנמוך 1.3> ל-FIB4 ו-1.455-> בבדיקת ה-NFS[4][19] הם בסיכון נמוך לפיברוזיס מתקדם, אינם זקוקים להערכה הפטולוגית באותה נקודת זמן, ומומלץ לחזור בהם על ההערכה כעבור שנתיים לפי המלצות האיגוד האירופי. במטופלים בעלי ציון גבוה מערך הסף הגבוה (2.67< בבדיקת ה-FIB4 ו-0.676< בבדיקת ה-NFS[4][19]) קיים חשד לפיברוזיס מתקדם או שחמת, ויש להפנותם להערכה הפטולוגית (הערך הספציפי לחולים עם מכ"ש הוא מעל 2.67 לחשד לפיברוזיס מתקדם). בכ-30–50 אחוזים מהמטופלים מתקבל ערך שהוא בין ערך הסף הנמוך לערך הסף הגבוה; במקרים אלו נדרשת הערכה נוספת כדי לקבוע את דרגת הסיכון, ומומלץ להפנות את המטופל להערכה הפטולוגית. ב-ELF panel קיימים ערכי סף בדומה ל-FIB4 וה-NFS, אך בהנחיות ה-NICE נקבע ערך סף אחד (10.51) לניבוי פיברוזיס מתקדם; במטופלים מבוגרים שבהם תוצאת הבדיקה נמוכה מ-10.51 קיימת המלצה למעקב על ידי בדיקת ELF חוזרת לאחר 3 שנים[20].
(Vibration Controlled Transient Elastography (VCTE - פיברוסקן: קיימים מספר סוגים של בדיקות מבוססות פרמטרים פיזיקליים להערכת אלסטיות הכבד, כגון Vibration Controlled Transient Elastography (VCTE), (Acoustic Radiation Force Impulse (ARFI ו-Magnetic Resonance Elastography (MRE). מביניהן, בדיקת VCTE היא הבדיקה הזמינה והנפוצה ביותר[21][22][23][24]. ה-VCTE מבוסס על עקרונות של אלסטוגרפיה על קולית, ומבוצע על ידי מכשיר פיברוסקן (חברת Echosens). תוצאת הבדיקה, LSM (Liver Stiffness Measure), נמדדת בקילו-פסקל (KPa). בדיקת ה-VCTE תוקפה על פני ספקטרום רחב של מחלות כבד כרוניות ונמצאה עם רמת דיוק גבוהה. יתרונות הבדיקה כוללים: בדיקה קצרה וקלה לביצוע, נסבלת היטב על ידי הנבדקים, ומעריכה נפח כבד גדול פי 100–200 לעומת ביופסיית כבד. במטא-אנליזה של 9 מחקרים על TE שכללו 1,047 חולים עם מכ"ש, רמת הדיוק הייתה בינונית עבור 2 ≤ F (רגישות וספציפיות 79 אחוזים ו-75 אחוזים בהתאמה), וטובה מאוד עבור F3 ו-F4 (רגישות וספציפיות של 85 אחוזים ו-85 אחוזים, בהתאמה, עבור F3; רגישות וספציפיות 92 אחוזים ו-92 אחוזים, בהתאמה, עבור F4[24]). יתרון נוסף של בדיקת הפיברוסקן הוא שברוב המכשירים מתאפשרת מדידה בו זמנית של ערך ה-CAP (Controlled Attenuation Parameter), שנותן הערכה כמותית של השומן בכבד[22].
הגישה לשימוש באמצעי אבחון לא פולשניים
מרבית האמצעים הלא פולשניים שתוארו מתאפיינים בערך מנבא שלילי (NPV - Negative Predictive Value) גבוה להיעדר פיברוזיס מתקדם, ובערך מנבא חיובי (PPV - Positive Predictive Value) טוב במידה פחותה לניבוי פיברוזיס מתקדם; לאור זאת, מדובר בכלים המאפשרים לסווג באופן אמין מטופלים לקבוצת סיכון נמוך ולהתריע אודות מטופלים עם סיכון גבוה למחלה מתקדמת, שבהם נדרש בירור נוסף. היכולת להבחין באמצעות אמצעים אלו בדרגות פיברוזיס שאינן בקצוות, לדוגמה - בין פיברוזיס בדרגה F2 (פיברוזיס משמעותי), F1, או F0 (העדר פיברוזיס) מוגבלת.
חישוב ה-FIB4 או ה-NFS יכול להתבצע במסגרת הרפואית שבה מתקיים המעקב הרגיל אחר המטופל עם סוכרת או סינדרום מטבולי (רפואה ראשונית, מרפאת סוכרת). לפי הנחיות האיגוד האירופי, במטופלים ללא הפרעה באנזימי הכבד עם תוצאת FIB4 או NFS המעידה על סיכון נמוך מומלץ לחזור על בדיקת אנזימי הכבד ועל FIB4 או NFS כעבור שנתיים. מטופלים עם הפרעה באנזימי הכבד או עם תוצאת FIB4 או NFS שהיא מעל לערך הסף התחתון יש להפנות לבירור במרפאת כבד. מטופלים עם תוצאת FIB4 או NFS שהיא Indeterminate יופנו על פי רוב לבדיקה לא פולשנית נוספת, כגון VCTE; גישה זו נתמכת על ידי מחקרים שהדגימו ששילוב של גישות לא פולשניות מעלה את דיוק הניבוי[25][26]. במטופלים שבהם הבדיקה השנייה מעידה על סיכון נמוך לפיברוזיס מתקדם הגישה דומה למטופלים שבהם נמצא סיכון נמוך בבדיקת ה-FIB4 או ה-NFS. הגישה למטופלים עם עדות בבדיקה בלתי פולשנית לפיברוזיס מתקדם היא אינדיבידואלית ומותאמת לנתונים הקליניים של המטופל. כשהבדיקה המעידה על פיברוזיס מתקדם היא FIB4 או NFS, בחלק מן המקרים תבוצע בנוסף בדיקה לא פולשנית מקו שני (VCTE); עם זאת, לאור ספציפיות ו-PPV תת-אופטימלי של כל האמצעים הלא פולשניים, בהתחשב במשמעות של אבחנה של שחמת כבד למטופל ובמשאבים הנדרשים למעקב אחר מטופל עם שחמת ובהינתן המידע הנוסף שניתן לקבל מביופסיה, מקובל לנקוט בגישה מתירנית בהפניית מטופלים אלו לביופסיית כבד.
מצטברות עדויות שאמצעי אבחון לא פולשניים יכולים גם לנבא תוצאים קליניים (Clinical outcomes) במטופלים עם מכ"ש. בהקשר זה, השכיחות המצטברת (Cumulative probability) של תמותה או השתלת כבד נמצאה קשורה בציון ה-FIB4 ו-NFS[27] עם ערך ניבויי דומה לשל ביופסיית כבד[28]; ערכי סף של ELF נמצאו מנבאים התקדמות לשחמת כבד ולאירוע דקומפנסציה של שחמת[29] ו-VCTE נמצא מנבא שרידות כוללת (Overall survival) ושרידות ללא תמותה מסיבוכי מחלת כבד[30]. בעבודה נוספת הראו Sanyal וחבריו שערכי ELF ,NFS ,FIB4 ו-VCTE ב-baseline ושינוי בערכי NFS ו-VCTE לאורך תקופת המעקב קשורים לתוצאים קליניים הקשורים בשחמת: מיימת, דמם משני ליתר לחץ דם פורטלי, אנצפלופתיה כבדית, ציון 15 ≤ MELD או השתלת כבד או מוות[31].
יחסי הגומלין בין כבד שומני וסוכרת
מכ"ש וסכרת הן שתי מחלות מטבוליות שכיחות היכולות ללגרום באופן סינרגיסטי להגברת הסיכון לסיבוכים מטבוליים. גורמים המנבאים מעבר מהשמנה כבדית פשוטה (סטאטוזיס) למצב דלקתי-צלקתי בחולי מכ"ש הינם: גיל מבוגר, השמנת יתר, יחס ALT/AST גבוה מ-1 ונוכחות סוכרת[32]. Younossi וחבריו העריכו על סמך מטא-אנליזה שמכ"ש מתקיימת בכ-55 אחוזים מחולי סוכרת[33]. הם גם מצאו שכיחות גבוהה יותר של דלקת וצלקת כבדית בחולים סוכרתיים עם כבד שומני, לעומת חולים ללא סוכרת עם כבד שומני. השכיחות של שחמת בחולים עם סוכרת וכבד שומני, הייתה 25 אחוזים לעומת 10 אחוזים בחולים עם כבד שומני ללא סוכרת. בנוסף, שיעורי התמותה מסיבות כבדיות היו גבוהים באופן משמעותי בחולי הסוכרת, לעומת חולים ללא סוכרת[34]. מקובל לחשוב שהקשר בין שתי המחלות הוא דו-כיווני כאשר מכ"ש היא גורם סיכון לסיבוכים מטבוליים וסוכרת מסוג 2, באופן עצמאי מגורמי סיכון ידועים אחרים[35].
מחקרים פרוספקטיביים מהשנים האחרונות תומכים בכך שכבד שומני מקדים סוכרת, אפילו באנשים ללא עודף משקל[36] ואף הועלתה הצעה כי נסיגה של כבד שומני מפחיתה סיכון להיארעות סוכרת[37]. לעומת זאת, נוכחות סוכרת בחולי מכ"ש נקשרה להתקדמות מהירה של פיברוזיס ותחלואה חוץ כבדית קשה יותר[38].
הסיבה לממצאים הקליניים וההיסטולוגים הקשים יותר בחולים סוכרתיים אינה ברורה, אך קשורה כנראה למצב דלקתי כרוני, עקה חמצונית ושחרור יתר של ציטוקינים הרעילים לכבד. ההסבר לכך הוא שהצטברות שומן בכבד מעכבת את העברת האותות הקשורים לאינסולין בתאי הכבד וגורמת לתנגודת כבדית לאינסולין עם פגיעה בדיכוי ייצור גלוקוז אנדוגני (גלוקונאוגנזה). חולים עם סוכרת ומחלת כבד נמצאים גם בסיכון גבוה יותר להתפתחות סרטן כבד ראשוני[39].
כבד שומני כגורם סיכון למחלות לב
מרבית החולים עם מכ"ש לא ימותו ממחלות כבד אלא ממחלות כלי דם ולב (מכ"ל) (Cardio-Vascular Diseases - CVD). מקובל לקבוע שכ-40 אחוזים ממקרי המוות בחולי מכ"ש הם תוצאה של מכ"ל (אחריהן: סרטן במקום השני, ומחלות כבד במקום שלישי)[38].
מספר מחקרים אפידמיולוגים הראו כי כבד שומני הוא גורם סיכון עצמאי למחלה טרשתית. בסקר שכלל 3,166 מטופלים הסובלים מסוכרת, נמצאה שכיחות גבוהה יותר למחלת לב כלילית (27 אחוזים לעומת 18 אחוזים), מחלת כלי דם מוחיים (20 אחוזים לעומת 13 אחוזים) ומחלת כלי דם היקפית (15 אחוזים לעומת 10 אחוזים) בחולים הסובלים מסוכרת וכבד שומני לעומת חולים עם סוכרת בלבד[40]. במחקרים נוספים נמצאה עלייה בשכיחות פגיעה כלייתית ופגיעה עינית בחולי סוכרת עם כבד שומני לעומת חולי סוכרת ללא כבד שומני[41]. מחקרים נוספים תמכו בקשר בין כבד שומני להתפתחות מחלת לב, כולל מחקר פרמינגהם (Framingham) שהראה קשר לסמנים תת-קליניים של מחלת לב בקרב אנשים עם כבד שומני[42]. מחקר מטא-אנליזה שכלל 16 מחקרים עם 34,000 משתתפים הראה שמכ"ש קשור לאירועים קרדיווסקולריים קטלניים ולא קטלניים ושעוצמת הקשר התגברה עם עלייה בחומרת מכ"ש גם לאחר תקנון גורמי סיכון קלאסיים למכ"ל[43].
מחקר דומה, שבדק התפתחות מכ"ל בחולי מכ"ש שהוכחה בביופסיה, מצא אף הוא קשר מובהק בין חומרת הפיברוזיס הכבדי לבין התפתחות אירועים קרדיו-ווסקולרים[44]. למרות האמור לעיל, מחקר שבדק שכיחות אוטמים לבביים ואירועי שבץ מוחי בחולי מכ"ש בקרב 18 מיליון מבוטחים בארבע מדינות אירופאיות לא מצא שכיחות מוגברת של אירועים כאלה לאחר תיקנון לגורמי סיכון מרובים. החוקרים מסכמים שהערכת גורמי סיכון למכ"ל בחולי מכ"ש חשובה, אך צריכה להיעשות בדומה לשאר האוכלוסייה. שכיחות מכ"ש באוכלוסיית המחקר הייתה נמוכה יחסית למחקרים אחרים[45].
נראה כי פרופיל הליפידים הטרשתי, הנפוץ בחולים עם כבד שומני, הוא אחד הגורמים האחראים לקשר למחלות לב. הסבר אפשרי נוסף לקשר בין כבד שומני לפרופיל ליפידים טרשתי הוא שכבד שומני מוביל להיפרגליקמיה ותנגודת לאינסולין. במצב זה קיים ייצור כבדי מוגבר של טריגליצרידים וחלקיקי VLDL (Very-Low-Density Lipoprotein) שמוביל באופן שניוני לרמות נמוכות של HDL (High-Density Lipoprotein) ועלייה בצפיפות חלקיקי ה-LDL (Low-Density Lipoprotein). בנוסף, הודגם כי חולי כבד שומני מאופיינים ב-Small Dense LDL שנחשב טרשתי במיוחד[46], ואף נמצא קשר בין מידת חומרת הכבד השומני ומידת חומרת פרופיל הליפידים הטרשתי[47]. הסברים נוספים לקשר בין כבד שומני ומחלות לב טמונים בכך שכבד שומני הוא מצב דלקתי תת-קליני. במטא-אנליזה נראה כי כבד שומני מגביר את הסיכון למקרים חדשים של מחלת לב פי 2[4].
מכ"ש נמצאה קשורה גם להפרעות קצב לבביות כולל פרפור עליות, הפרעות קצב חדריות והארכת QT וכן להפרעות מבניות לבביות כגון הפרעה דיאסטולית והפרעות מסתמיות. ככל שהמכ"ש מתקדמת יותר, ובעיקר ככל שדרגת הפיברוזיס הכבדי חמורה יותר, כך גדל הסיכון למכ"ל ולסיבוכים לבביים והפרעות קצב. לממצאים אלה חשיבות רבה מכיוון שהם יכולים להסביר חלק מהקשר לתמותה עודפת ממכ"ל בחולים עם מכ"ש[48].
טיפול
עיקר הטיפול מתמקד במניעה ובטיפול בגורמי הסיכון למחלה הכוללים: השמנה, תנגודת לאינסולין, היפר-טריגליצרידמיה, סוכרת ורמות גלוקוז מוגברות בצום (IFG - Impaired Fasting Glucose), וכן טיפול בגורמי הסיכון הנוספים למחלת לב כמו איזון כולסטרול אגרסיבי.
לא נמצא טיפול תרופתי במכ"ש שהודגם במחקרים כיעיל באופן משכנע ושאומץ באופן גורף. מאחר ששינוי אורח חיים הכולל ירידה במשקל ופעילות גופנית נמצא יעיל בהפחתת גורמי הסיכון למכ"ש, הוא הוגדר כקו הראשון של הטיפול במחלה.
ירידת משקל
קיימת הסכמה רחבה כי ירידת משקל מתונה של חצי קילו עד קילו בשבוע מסייעת בשיפור ואף נסיגה מוחלטת של השומן בכבד ואף מסייעת בנסיגה של דלקת וצלקת. כמו כן, ירידת משקל משפרת אנזימי כבד ולעיתים קרובות מביאה לחזרתם לתחום התקין. בניסוי קליני בו נעשה שינוי אורחות חיים במשך שנה הודגם יחס מנה תגובה בין מידת ירידת המשקל ומידת הפחתת בשומן בכבד (שנמדד ב-MRS): ירידת 1–5 אחוזים ממשקל הגוף הובילה להפחתה של 33 אחוזים מהשומן הכבדי, ירידת 5–10 אחוזים הובילה להפחתה של 65 אחוזים מהשומן הכבדי וירידת משקל של מעל 10 אחוזים הובילה להפחתה של 80 אחוזים מהשומן הכבדי[49].
בניסוי אחר שכלל אף הוא שינוי אורחות חיים במשך 12 חודשים, ירידת משקל של לפחות 7 אחוזים מהמשקל ההתחלתי הובילה לשיפור היסטולוגי משמעותי במדדי דלקת הכבדית כפי שנמדדה ב-NAS (NASH histological Activity Score), לגבי צלקת השיפור לא הגיע למובהקות סטטיסטית[50].
בניסוי אחר בו הושגה ירידת משקל של 10 אחוזים בממוצע ממשקל הגוף, נצפה גם שיפור מובהק בצלקת לאחר 6 חודשים[51]. מחקר נוסף גדול תומך באפשרות של שיפור הצלקת. המחקר נערך בקובה על 261 חולי כש"ד שביצעו ביופסיות כבד חוזרות לאחר 52 שבועות של שינוי אורחות חיים וירידת משקל. כל החולים שרזו בלפחות 10 אחוזים ממשקלם ההתחלתי שיפרו את רמת הדלקת שלהם (NAFLD activity score), ל-90 אחוזים הייתה היעלמות של הכש"ד, ול-45 אחוזים הייתה רגרסיה של צלקת[52].
ירידה במשקל מומלצת באמצעות דיאטה מבוקרת, הבחירה בין דיאטה דלת שומן ודיאטה דלת פחמימות יכולה להיות לפי העדפות המטופל. דיאטה דלת פחמימות במשך חצי שנה (אך גם דלה בשומן רווי ומושתת על עקרונות אכילה בריאה) הובילה לירידת משקל זהה לזו של דיאטה דלת שומן סטנדרטית ולהפחתה זהה בשומן הכבדי וברמות ALT בדם[53]. מטא-אנליזה שסיכמה את המחקרים המעטים שהשוו דיאטה סטנדרטית לדיאטה דלת פחמימות הראתה גם היא שאין הבדל ביעילותן בהפחתת שומן כבדי[54]. בכל המחקרים המוזכרים נעשתה דיאטה מתונה ומאוזנת לפי ההמלצות התזונתיות המקובלות ובשילוב עם פעילות גופנית מתונה.
בדף עמדה שפורסם על ידי האיגוד האירופאי לחקר הכבד EASL (European Association for the Study of the Liver)[55], הומלצה ירידת משקל של 7 אחוזים כטיפול ב-מכ"ש/ כש"ד, כפי שמומלץ על ידי איגודים בינלאומיים אחרים לקבלת תועלת בריאותית[17]. בהנחיות לטיפול בכבד שומני שפורסמו על ידי איגוד הכבד האמריקאי, AASLD (American Association for the Study of Liver Diseases), מושם דגש מיוחד על אורח חיים בריא ומסוכם כי ירידת משקל לבד או בשילוב עם פעילות גופנית מורידה שומן כבדי, כאשר ירידת 3–5 אחוזים לפחות ממשקל התחלתי דרושה לשם כך. עם זאת, ירידת משקל גדולה יותר המתקרבת ל-7–10 אחוזים דרושה לשיפור הדלקת הכבדית ופיברוזיס (NAFLD activity score)[12]. המלצות דומות ניתן למצוא בקווים המנחים שפרסם ה-ESPEN (The European Society for Clinical Nutrition and Metabolism) ב-2019[56].
הרכב הדיאטה
על סמך הידע שנצבר ממחקרים הן בבעלי חיים והן בבני אדם נראה כי שינוי הרכב הדיאטה יכול לסייע בטיפול בכבד שומני גם ללא ירידת משקל.
סוג השומן
להרכב חומצות השומן בדיאטה השפעה על מטבוליזם שומן בכבד. בניסויי האכלה רנדומליים בהם נעשתה האכלת יתר בשומן רב בלתי רווי או בשומן רווי נראה כי יש להם השפעה שונה על הכבד: רק הדיאטה עם השומן הרווי גרמה לעליית שומן כבדי וויסרלי, למרות עליית משקל דומה[57][58]. באופן דומה, בניסוי קליני אקראי בן 10 שבועות דיאטה איזוקלורית עשירה באומגה 6 הפחיתה שומן כבדי בעוד שדיאטה איזוקלורית עשירה בשומן רווי העלתה שומן כבדי[59]. בניסוי קליני אקראי בן 3 שבועות שנערך, שומן רווי העלה את כמות השומן הכבדי אף יותר מכמות איזוקלורית של סוכר[60]. כמו כן, בעבודה שנערכה בישראל בקרב אוכלוסייה כללית נמצא כי לחולי מכ"ש צריכה מופרזת של בשר לסוגיו ללא קשר ל-BMI ונטייה לצריכה נמוכה של דגים העשירים באומגה 3[61].
פרוקטוז ומשקאות קלים ממותקים בסוכר או פרוקטוז
סוכר השולחן, הסוכרוז, הוא דו-סוכר המורכב מגלוקוז ופרוקטוז. בעבודה שנערכה בישראל נמצא כי חולי מכ"ש צורכים באופן מובהק כמות גדולה יותר של משקאות קלים הממותקים בסוכר וכי הקשר עצמאי מ-BMI[61]. בהתבסס על הקשר בין צריכה גבוהה של פרוקטוז עם השמנה וסוכרת וכן ההשפעה על הגברת ייצור השומן הכבדי שיש לדיאטות עתירות פרוקטוז נראה כי חולי מכ"ש צריכים להגביל צריכת פרוקטוז או סירופ תירס עתיר פרוקטוז (High fructose corn syrup). לכן כדאי להגביל צריכת משקאות קלים, מיצי פירות גם אם טבעיים ומזון עשיר בסוכרוז (דו סוכר המורכב מגלוקוז ופרוקטוז). במחקר רחב היקף שכלל 341 חולי מכ"ש שעברו ביופסית כבד נראה כי צריכה יומית של משקאות מכילי פרוקטוז קשורה בסיכון מוגבר (פי 2.5) לכש"ד גם לאחר תקנון לגורמי סיכון אחרים כמו BMI, תנגודת לאינסולין, סך צריכה קלורית ורמות ליפידים וחומצה אורית בנסיוב. מכאן שלפרוקטוז, מעבר להשפעה הליפוגנית הידועה שלו, עשויה להיות גם השפעה פרו-דלקתית ופרו-פיברוטית[62]. מחקר דומה בקרב 271 ילדים הסובלים מהשמנה הראה תוצאות דומות: צריכת פרוקטוז הייתה קשורה באופן עצמאי לכש"ד שנראה בביופסית כבד[63].
מספר לא מבוטל של מחקרים אפידמיולוגיים הדגימו קשר בין צריכת משקאות ממותקים ובין כבד שומני לא אלכוהולי[61][64][65][66]. קשר כזה הודגם אף במחקר פרמינגהם, שכלל 2,634 איש עם בדיקת CT לאבחון כבד שומני. רמות אנזים הכבד ALT נמדדו אצל 5,908 נבדקים. קשר מנה תגובה ברור הודגם בין צריכת משקאות מכילי סוכר ובין כבד שומני, עם עליית סיכון ב-55 אחוזים בקרב אנשים ששתו משקאות אלו על בסיס יומי לעומת אלו שלא שתו כלל. ממצאים דומים נראו גם לגבי רמות ALT. לעומת זאת, לא נראה קשר בין משקאות דיאט (עם ממתיקים מלאכותיים) ובין כבד שומני או ALT[67]. ממצאים אלו נתמכים בתוצאות ניסוי קליני אקראי בו ניתן 1 ליטר של קולה או דיאט קולה או חלב ליום במשך חצי שנה. אף על פי שחלב וקולה מכילים אותה כמות קלוריות, רק בקבוצת הקולה נצפתה עלייה בכמות השומן הכבדי (לפי הדמיה באמצעות מכשיר הדמיה מגנטית MRS), כלומר ההשפעה טמונה בסוכר שיש במשקה הממותק ולא בהכרח בקלוריות עצמן. הקבוצה שטופלה בדיאט קולה לא הראתה עלייה בשומן הכבדי[68]. מאידך, ישנם ניסויים קליניים שמראים שהפחתת צריכת סוכר מובילה להפחתת שומן כבדי תוך זמן קצר של מספר שבועות[69][70].
באופן מדאיג, השפעת הפרוקטוז מתחילה כבר מגיל צעיר. פעוטות שבגיל שנה שתו יותר משני משקאות ממותקים ביום היו בסיכון גבוה לפתח מכ"ש בילדות (בגיל 10) בהשוואה לאלה ששתו פחות ממשקה אחד ביום, ללא תלות במדד מסת הגוף[71].
מזון מהיר ואולטרא מעובד
אין כמעט מחקרים שבחנו את הקשר בין צריכת מזון אולטרא מעובד כקבוצת מזון ובין כבד שומני, אולם זהו מזון (או שתייה מתוקה) שהוא לרוב עתיר סוכר, שומן רווי ודל בסיבים תזונתיים וויטמינים ולכן אינו מומלץ לחולים עם כבד שומני. נדגמים בריאים שצרכו במסגרת ניסוי קליני לפחות 2 ארוחות מזון מהיר ביום במשך 4 שבועות, עלו במשקלם ב-5–15 אחוזים וכמות הטריגליצרידים בכבד עלתה אף היא. רמות ALT עלו בממוצע מ-22 ל-97 U/L (יחידות לליטר) ול-11 מתוך 18 הנבדקים היו באופן עקבי רמות ALT מעל הנורמה מהשבוע הראשון ועד לתום ההתערבות[72]. מחקרים שנעשו הדגימו קשר בין צריכה גבוהה של חלבון מהחי ובאופן ספציפי יותר בשר אדום ומעובד ובין כבד שומני בקרב אוכלוסייה כללית[73][74][75]. בנוסף, צריכה גבוהה של בשר אדום ומעובד נמצאה קשורה במטא-אנליזות גם לרמות גלוקוז מוגברות, סוכרת ולמחלות לב ולכן אינה מומלצת באופן כללי[76]. ייתכן ולא מדובר רק במזון מהיר, אלא גם בדפוס אכילה מהיר. מחקר חתך חדש בקרב 149 גברים ו-159 נשים עם סוכרת מסוג 2 מצא כי התנהגות של אכילה בקצב מהיר בקרב גברים הייתה קשורה עם עלייה בסיכוי למכ"ש[77], ממצאים אלה צריכים להיתמך במחקרים נוספים.
דיאטה ים תיכונית ותבניות אכילה בריאה דומות
מחקרים פרוספקטיביים גדולים תומכים בקשר בין תבניות אכילה בריאות כמו דיאטה ים תיכונית ודיאטות דומות ומניעת מכ"ש. התמדה לאורך זמן חשובה מאוד לשימור התועלת[78][79]. בניסוי קליני אקראי שנמשך שנה וחצי בקרב 278 נבדקים, דיאטה ים תיכונית-דלת פחממות הפחיתה שומן כבדי יותר מדיאטה דלת שומן למרות ירידת משקל דומה בשתי הדיאטות[80].
שומן חד בלתי רווי (n-9 oleic acid), שנמצא בכמות גדולה בשמן זית והוא אחד ממאפייניה הבולטים של הדיאטה הים תיכונית, מודגם יותר ויותר כבעל תפקיד חשוב בפרופיל המטבולי בבני אדם[81]. מקורות נוספים לשומן חד בלתי רווי הם אגוזים ואבוקדו. לשומן זה השפעה מיטיבה על פרופיל שומנים.
במחקרים בבעלי חיים שמן זית הפחית הצטברות טריגליצרידים בכבד[82]. הדיאטה הים תיכונית היא תבנית אכילה המאופיינת באכילה מרובה של שומן חד בלתי רווי, בעיקר שמן זית ואגוזים, אכילה מרובה של ירקות ודגים העשירים באומגה 3 ומיעוט אכילה של בשר אדום ודברי מתיקה. בשני ניסויים קליניים אקראיים נמצא כי אכילה לפי עקרונות הדיאטה הים תיכונית במשך מספר שבועות מובילה לירידה משמעותית בשומן הכבדי בקרב חולים עם כבד שומני, יותר מדיאטה דלת שומן רגילה. ההשפעה הייתה דומה בחולי סוכרת עם כבד שומני, שם הושם דגש על צריכה מרובה של שומן חד בלתי רווי[83][84][85]. בשני הניסויים הדיאטות היו איזוקלוריות ולא חלה ירידת משקל משמעותית עם אף אחת מהדיאטות, כך שהשינוי בשומן הכבדי היה ללא קשר לירידת משקל. שני המחקרים לא כללו ביופסיית כבד ולכן אין אפשרות להעריך את השפעת הדיאטה הים תיכונית על דלקת וצלקת. כמו כן, ניסויים אלו הם בעלי מדגם קטן וקצרי טווח ולכן דרוש מחקר נוסף בנושא. עם זאת, וגם לאור יתרונותיה הברורים של דיאטה ים תיכונית בירידת משקל, הפחתת הסיכון לסוכרת ומחלות לב, ממליץ האיגוד האירופאי[55] על דיאטה ים תיכונית כאחת הדרכים לטפל בכבד שומני (ראה טבלה מספר 2). גם בהנחיות של ה-ESPEN משנת 2019 ניתנה המלצה לדיאטה ים תיכונית על מנת להפחית שומן כבדי ולשפר רגישות לאינסולין[56].
מחקר עוקבה בקרב אוכלוסייה קשישה מצא כי היענות לדפוס האכילה המומלץ של ה-WHO (World Health Organization, שדומה בעקרונותיו לדיאטה הים תיכונית) הייתה קשורה עם רגרסיה של השומן הכבדי. היענות לדפוס אכילה זה נחשבת כעמידה בקריטריונים הבאים:
- צריכת ירקות ופירות של 400 גרם/יום לפחות
- צריכה של פחות מ-10 גרם סוכר מוסף/יום
- אחוז צריכת קק"ל (קילו קלוריות) משומן מסך קק"ל נמוך מ-30 אחוזים
- אחוז צריכת קק"ל משומן רווי מסך הקק"ל נמוך מ-10 אחוזים
- אחוז צריכת קק"ל משומן טרנס מסך קק"ל נמוך מ-1 אחוזים
- צריכת מלח נמוכה מ-5 גרם/יום[86]
| המלצות הוועדה | חוזק ההמלצה | רמת ההוכחה |
| מומלצת ירידת משקל של לפחות ממשקל התחלתי להפחתת השומן הכבדי ולהורדת אנזימי כבד | 1 | A |
| מומלצת ירידת משקל של לפחות 7–10 אחוזים להפחתת דלקת ופיברוזיס כבדי | 1 | A |
| ניתן לבצע דיאטה דלת פחמימות (בעלת הרכב בריא כולל הגבלת שומן רווי) כחלק מהדיאטות המוצעות לירידת משקל בכבד שומני | lib | A |
| מומלצת הפחתת צריכת סוכר מוסף והימנעות משתייה ממותקת בסוכר או פרוקטוז לטיפול בכבד שומני | 1 | A |
| מומלצת דיאטה ים תיכונית לטיפול בכבד שומני (גם ללא ירידת משקל וגם במטופלים במשקל תקין) | 1 | A |
| רצוי להפחית שומן רווי לפי ההמלצות לכלל האוכלוסייה על פי עקרונות איגוד הלב האמריקאי, למניעת נזק כבדי ותחלואה לבבית | Ila | A |
| רצוי להפחית שומן טרנס לפי ההמלצות לכלל האוכלוסייה על פי עקרונות איגוד הלב האמריקאי, למניעת נזק כבדי ותחלואה לבבית | Ila | B |
| ניתן לצרוך כולסטרול במידה מתונה כמו ההמלצה לכלל האוכלוסייה (קשור לנזק כבדי וסרטן כבד במחקרי חיות ובמחקרים אפידמיולוגיים) | lib | B |
| מומלצת הגברת פעילות גופנית והפחתת "זמן יושבני" להפחתת שומן כבדי | 1 | A |
| רצוי לבצע פעילות גופנית להפחתת NASH ופיברוזיס | Ila | B |
| מומלץ לבצע פעילות גופנית אירובית להפחתת שומן כבדי | 1 | A |
| מומלץ לשלב פעילות גופנית מסוג אימון התנגדות כחלק מהאימון הגופני או לבצע אותה בלעדית אם לא ניתן לבצע פעילות אירובית מסיבה כלשהי | 1 | A |
| מומלצות תוכניות מובנות לשינוי אורחות חיים לדיאטה בריאה ופעילות גופנית סדירה לחולים עם כבד שומני | 1 | A |
| ניתן לשקול תוספי אומגה 3 להפחתת טרינליצרידים ושומן כבדי אך לא לטיפול בדלקת או פיברוזיס. בעיקר ניתן לשקול באנשים שאינם אוכלים דגים | lib | A |
מיקרונוטריינטים, פירות וירקות
תזונה עשירה בפירות וירקות קשורה עם סיכון נמוך למחלות לב בחולי מכ"ש[87], וזאת הודות לתכולה גבוהה של סיבים תזונתיים, ויטמינים ונוגדי חמצון שאינם ויטמינים כמו פוליפנולים. במחקרים אפידימיולוגיים ישנן ראיות לקשר בין צריכת פירות וירקות ומכ"ש. במחקר חתך בקרב 977 יפנים נמצא קשר עצמאי בין צריכת פירות וירקות לבין מכ"ש, ללא תלות במדד מסת גוף. צריכת הפירות באוכלוסייה זו היא נמוכה ועומדת על 1–3 מנות פרי ביום. משמעות הדבר היא כי אין צורך בהגבלה נוקשה של כמות הפירות היומית במטרה להקטין את צריכת הפרוקטוז בחולי מכ"ש וכי ניתן לשלבם בתזונה מאוזנת בכמות סבירה כמקור לסיבים וויטמינים. מחקר חתך נוסף נערך בקרב 789 ישראליים שעברו בדיקת אולטראסאונד לאבחון מכ"ש ובדיקת פיברוטסט (סמנים בסדום) לאיתור חשד לדלקת ופיברוזיס כבדיים, ובחן את הקשר בין צריכת ויטמינים E ו-C מהתזונה לבין מכ"ש[88]. נמצא כי צריכה גבוהה של ויטמינים אלו נמצאה קשורה עם ירידה בסיכוי להתפתחות דלקת (כש"ד). המקורות התזונתיים הטובים ביותר של הוויטמינים האלו הם אגוזים, גרעינים, שמנים צמחיים, פירות וירקות. מחקרים נוספים הדגישו את חשיבותם של פוליפנולים, נוגדי חמצון חזקים שאינם וויטמינים ומצויים במזונות צמחיים כגון פירות יער, אגוזים, דגנים מלאים, וכן מצויים בקפה ותה. נמצא קשר מגן בין צריכה גבוהה של פוליפנולים ומכ"ש ותנגודת לאינסולין בתקנון לגיל, מגדר, מדד מסת גוף ומשתני תזונה ואורח חיים נוספים[89].
סיכום הטיפול התזונתי
תזונה הודגמה באופן ברור כבעלת קשר הדוק עם מכ"ש וכש"ד הן בחיות מעבדה והן בבני אדם ולכן מהווה אמצעי עיקרי לטיפול. ניסויים קליניים מן השנים האחרונות סייעו רבות בהבנת התועלת הגלומה בדיאטה מאוזנת ומתונה, לירידת משקל ופעילות גופנית כטיפול בכבד שומני. רוב המחקרים מעידים על שיפור בשומן הכבדי ובאנזימי הכבד עם ירידת משקל של כ-5 אחוזים. ירידה של כ-7 אחוזים ממשקל התחלתי דרושה על מנת לשפר דלקת וירידת משקל של כ-10 אחוזים מובילה אולי לירידה בצלקת. יש חשיבות רבה לקביעת יעדים ברי השגה לירידת משקל למניעת תסכול ו"שבירת דיאטה" בקרב המטופלים. לפיכך, הדגשת יעילות ירידת משקל צנועה יחסית של 5–10 אחוזים ממשקל הגוף כמובילה לשיפור משמעותי ולעיתים אף לנסיגה מלאה של הכבד השומני עשויה לעודד היענות והתמדה בשינוי אורחות החיים. כמו כן, חיזוקים חיוביים צריכים להינתן על כל שיפור בהרכב צריכת המזון ותוספת של פעילות גופנית, החשובים בפני עצמם, ולא רק על ירידת משקל. חולי הכבד השומני, בין אם בעודף משקל או במשקל תקין, צריכים להבין את חשיבות הרכב התזונה הנכון עבורם הכולל הפחתת שומן רווי וטרנס, צמצום סוכר מוסף והימנעות משתייה הממותקת בסוכר או בפרוקטוז כולל מיצי פירות. גם פעילות גופנית חשובה לכל החולים ללא קשר למשקלם, וגם תוספת קטנה עשויה להוביל לשיפור קליני.
טבלאות 1,2 מתארות את המלצות עמותת עתיד (עמותת הדיאטניות בישראל) שנכתבו על-ידי פורום גסטרו וכבד של עתיד ופורסמו בשנת 2019 ועודכנו בעת כתיבת הפרק.
פעילות גופנית
במחקר חתך שבוצע בישראל על תת-מדגם של סקר הבריאות והתזונה הלאומי הראשון, מב"ת, (350 איש) נמצא כי נדגמים שאובחנו באולטרסאונד כחולים במכ"ש בצעו פחות פעילות גופנית בשעות הפנאי לעומת כאלו שאובחנו כבעלי כבד תקין. הקשר בין פעילות אימון התנגדות שבונה שריר ומכ"ש נותר מובהק גם בתקנון ל-BMI[90]. במחקר רחב טווח שכלל 813 איש שבצעו ביופסיית כבד, פעילות גופנית בעצימות גבוהה בלבד (כמו ריצה או שחייה) נמצאה כגורם מגן מפני כש"ד וצלקת מתקדמת, באופן עצמאי מ-BMI[91].
במחקר חתך שכלל 24,588 נחקרים אמריקאים נמצא כי ביצוע של 150 דקות ומעלה של פעילות גופנית בשבוע היה קשור עם ירידה של כ-20 אחוזים למכ"ש ו-30 אחוזים לפיברוזיס. בנוסף, נמצא קשר מנה תגובה בין משך זמן יושבני לבין עלייה בסיכוי למכ"ש. למעשה אנשים היושבים יותר מ-8 שעות בממוצע ביום נמצאים בסיכוי גבוה ב-21 אחוזים לפתח מכ"ש בהשוואה לאנשים היושבים מתחת ל-4 שעות בממוצע, באופן עצמאי מסך ביצוע הפעילות הגופנית[92]. במחקר קוהורט גדול בקרב 126 אלף איש, נמצא כי השמנה ורמה נמוכה של פעילות גופנית קשורות בתמותה ממחלות כבד (סיבוכי שחמת או סרטן כבד). אולם, הסיכון המוגבר לתמותה שנבע מהשמנה הופחת משמעותית אצל מי שביצע פעילות גופנית. נמצא כי הליכה בקצב מתון מעל ל-3 שעות בשבוע יכולה להפחית ברבע את מספר מקרי התמותה[93].
| Author & Year | Design & Population | Steatosis | NASH | Fibrosis | Severe liver event | HCC/CVD |
| Blomdahl J., Metabolism Clinical and Experimental, 2021[94] | Cross sectional study N=86 patients with biopsy-proven NAFLD | - | - | Increased risk | - | - |
| Aberg F., Hepatology 2020[95] | Cohort study -11y FU N=8,345 subjects with NAFLD | - | - | - | Increased risk | - |
| Kashiwagi K., Alcohol, 2020[96] | Cross sectional study, N=268 subjects with NAFLD | - | - | Increased risk | - | No association with CVD |
| Long M., Clinical Gastroenterology and Hepatology, 2020[97] | Cross-sectional study N=2,475 from Framingham cohort study | Increased risk (for binge drinking*) | - | - | - | - |
| Chang Y., Hepatology 2020[98] | Cohort study -4Y FU N=190,048 subjects without NAFLD | Reduced risk | - | Increased risk | - | - |
| Chang Y., Hepatology 2019[99] | Cohort study -8.3Y FU
N=58,927 Korean employees |
- | - | Increased risk | - | -■ |
| Yamada K., PLOS ONE 2018[100] | Cross-sectional study N=178 NAFLD | - | Reduced risk | Reduced risk | - | - |
| Aberg F., Hepatology 2018[101] | Follow-up data from national registers | - | - | - | Increased risk | - |
| Hagstrom H., Scand J Gastroenterol 2017[102] | Cross-sectional N=120 NAFLD | - | No association | Reduced risk | - | - |
| VanWagner LB., Gastroenterology 2017[103] | Cross-sectional N=570 NAFLD | Not protective from subdinical CVD | ||||
| Moriya A., J of Hepatology 2015[104] | Prospective -2Y FU N=5297 Japanese | Reduced risk | - | - | - | - |
| Dunn W., J of Hepatology 2012[105] | Cross-sectional N=582 NASH | - | Reduced risk | Reduced risk | - | - |
| Ascha MS., Hepetology 2010[106] | Prospective -3Y FU N=195 NASH- Cirrhosis | - | - | - | - | Increased risk for HCC |
| ||||||
השמנה בטנית הודגמה באופן עקבי כגורם סיכון משמעותי למכ"ש. מספר מחקרים הראו כי ירידת משקל בעקבות פעילות גופנית באה לידי ביטויי באופן מיוחד ברקמת השומן הבטני וכי למתעמלים יש פחות השמנה בטנית לעומת ביקורות באותו משקל. פעילות גופנית עשויה לסייע בטיפול במכ"ש גם דרך מנגנונים אחרים. פעילות גופנית, ללא ירידת משקל או שינוי הרכב גוף, משרה רגישות לאינסולין ומשפרת מטבוליזם של גלוקוז על ידי העלאת מספר הקולטנים לאינסולין בשריר. בנוסף, פעילות גופנית משפרת מטבוליזם של חומצות שומן. אימון התנגדות נמצא מעלה מסת גוף רזה, מפחית תנגודת לאינסולין והשמנה בטנית ללא קשר לירידת משקל[107]. ניסויים קליניים, ברובם קטנים וקצרי טווח, הדגימו השפעה חיובית של אימון גופני מובנה (ללא דיאטה וירידת משקל) על כבד שומני ואנזימי כבד. אימוני אופניים 3 פעמים בשבוע במשך חודש הובילו לירידה יחסית בשומן הכבדי ב-21 אחוזים ב-MRS ללא שינוי במשקל או בדיאטה[108]. במחקר אחר שכלל פעילות גופנית מתונה יותר - הליכה של כחצי שעה עד שעה, 5-3 ימים בשבוע, במשך 16 שבועות נצפתה ירידה יחסית מתונה יותר של כ-10 אחוזים בתכולת השומן בכבד ללא ירידת משקל[109]. בשני ניסויים קליניים נוספים, האחד במתבגרים הסובלים מהשמנה[110] והשני בקשישים בריאים[111], נצפה שוב אפקט מיטיב של פעילות גופנית אירובית כאשר שנים עשר שבועות אימון הובילו לירידה יחסית בשומן הכבדי בכ-35 אחוזים. בנוסף, הודגם כי אימון התנגדות בן 8–12 שבועות, שכלל 3 אימונים בשבוע שמשכם 45 דקות, הוביל לירידה יחסית בשומן הכבדי ב-10–13 אחוזים וזאת ללא ירידת משקל משמעותית[112][113]. בניסוי מבוקר אקראי שהשווה אימץ אירובי לאימון התנגדות שניתן לחולי מכ"ש עם סוכרת 3 פעמים בשבוע במשך 4 חודשים, לא נמצא הבדל מובהק בין שני סוגי האימונים ושניהם נמצאו יעילים בהפחתת השומן הכבדי (כ-30 אחוזים הפחתה)[114].
| Author
Publication year |
Type of coffee | N | Steatosis (protective (association | Fibrosis (protective (association |
| Mikolasevic 1., 2020[115] | All coffee types | 1,998 | Yes | Yes |
| Zhang Y., 2020[116] | All coffee types | 401,022 | No | - |
| Soleimani D., 2019[117] | Tea and coffee (not separated) | 170 | - | Yes |
| Veronese N., 2018[118] | All coffee types | 2,819 | No | - |
| Chen YP., 2019[119] | All coffee types | 54,441 | Yes | - |
| Wijarnpreecha K., 2017[120] | Regular coffee | 3,290 | Yes | Yes |
| Alferink LJM. 2017[121] | All coffee types | 2,424 | No | Yes |
| Setiawan VW. 2017[122] | All coffee types | 44,576 | Yes | - |
| Imatoh T. 2015[123] | All coffee types | 1024 | Yes | - |
| Zelber-Sagi S. 2015[124] | All caffeinated coffee types | 347 | No | Yes |
| BambhaK. 2013[125] | All coffee types | 782 | No | Yes |
| AntyR. 2012[126] | Regular coffee, not espresso | 195 | - | Yes |
| Birerdinc A. 2012[127] | Caffeine intake | 41,658 | Yes | - |
| Molloy JW. 2012[128] | Regular coffee | 306 | No | Yes |
| Funatsu K.2011[129] | All coffee types | 492 | Yes | - |
| Catalano D. 2010[130] | Espresso coffee | 245 | Yes | - |
בניסוי קליני שבחן איזו עצימות של אימון אירובי ואיזו תדירות הן היעילות ביותר בהפחתת שומן כבדי לא נראה הבדל בין הזרועות ולכן נראה כי כל כמות סבירה של פעילות גופנית, בתדירות ועצימות שנוחות ומתאימות למטופל, טובה יותר מחוסר פעילות[131], זאת בעיקר לאור העובדה שזמן יושבני ממושך נמצא קשור בפני עצמו בהמצאות גבוהה יותר של כבד שומני[132].
ניסוי קליני שנערך בקרב 45 נשים עם השמנה ומכ"ש מצא כי אימץ כוח של 60–67 דקות בתדירות של 3 פעמים בשבוע למשך שלושה שבועות הוביל לשיפור באניזמי הכבד AST ו-ALT[133]. בניסוי קליני אחר בקרב 39 מבוגרים עם מכ"ש, השוו את ההשפעה של אימון אירובי או כוח, לעומת קבוצת ביקורת, על פרופיל השומנים בדם. נמצא כי ביצוע שלושה אימוני אירובי או כוח בשבוע של 45 דקות יעיל בהפחתת LDL, אך רק אימץ אירובי יעיל להעלאת HDL. בשתי הקבוצות לא היה שינוי ברמות הטריגליצרידים[134].
ההשפעה המיטיבה של פעילות גופנית נתמכת במטא-אנליזה של ניסויים קליניים שמחבריה הסיקו כי יש ראיות ברורות להשפעה מיטיבה של אימון גופני על שומן כבדי, ללא ירידת משקל או עם ירידת משקל מינימלית[135].
באופן דומה, במטא-אנליזה משנת 2020 שכללה 9 ניסויים קליניים ו-951 נחקרים עם מכ"ש וללא סוכרת נמצא כי הן פעילות אירובית והן פעילות בונה שריר של אימון התנגדות מראות יעילות בשיפור אנזימי הכבד ושומן תוך כבדי[136]. אין כמעט מחקר שבדק השפעת אימון גופני על היסטולוגיה כבדית כולל כש"ד ופיברוזיס. אולם, מחקר קטן עם 16 חולי כבד שומני שעברו ביופסיית כבד חוזרת, הדגים כי 12 שבועות של אימון מתון-אינטנסיבי של פעילות גופנית אירובית 2–5 פעמים בשבוע הוביל להפחתת פיברוזיס כבדי[137]. דרוש מחקר נוסף לאשש ממצאים אלו.
ניתוחים בריאטריים
ניתוחים בריאטרים הם השיטה היעילה ביותר לירידה במשקל[138] ובנוסף, מובילים לשיפור ניכר בסוכרת ואף לרמיסייה[139]. שיפור בשני המדדים הללו אמור לגרום לשיפור ניכר במדדי מכ"ש. אכן, במטא-אנליזה נראה כי בעקבות ניתוח בריאטרי חל שיפור בכל המדדים ההיסטולוגיים של שומן, דלקת וצלקת עד כדי היעלמותם המוחלטת, אך בסקירה (Systematic review) של Cochrane נטען כי מספר הניסויים ואיכותם אינו מספק ואינו מאפשר הערכת תועלת או נזק של ניתוחים בריאטריים כטיפול בחולי כש"ד. האיגוד האירופאי לחקר הכבד[55] מסכם כי ניתוח בריאטרי הוא אפשרות טיפולית בחולים שאינם מגיבים לשינוי אורח חיים או לטיפול תרופתי, ושעל-ידי ניתוחים אלה ניתן להגיע לשיפור במדדים מטבוליים לתקופה ממושכת. מחקר עוקבה עם מעקב למשך שנה הראה שיפור בכש"ד ב-85 אחוזים המהחולים ושיפור בצלקת ב-43 אחוזים[140]. הכותבים מסכמים שצריך לאזן בין התועלת לבין הסיכונים הנובעים מתחלואה בתר-ניתוחית. אותה קבוצה פרסמה תוצאות מעקב לאחר 5 שנים מהניתוח הבריאטרי. ב-84 אחוזים מהמנותחים הייתה העלמות של מכ"ד ללא החמרה בפיברוזיס, ורמת הפיברוזיס השתפרה בכ-70 אחוזים מהמנותחים ונעלמה ב-56 אחוזים מהם. בחולים שהדגימו תוצאות טובות לאחר שנה מהניתוח לא הייתה חזרה של מכ"ד בין 1–5 שנות המעקב[141].
בחולים עם השמנה מורבידית יש לעודד ניתוחים בריאטריים בעיקר באלה עם כש"ד וצלקת[17]. האיגוד האמריקאי לחקר הכבד מסכם כי אין התווית נגד לניתוח בריאטרי בחולי מכ"ש וכש"ד, אך לגבי חולים שחמתיים אין די ריאיות לגבי בטיחות או יעילות הניתוח וכן, כי מוקדם מדי להגדיר ניתוח בריאטרי כטיפול ספציפי למכ"ש[12].
נוספו פרוצדורות בריאטריות אנדוסקופיות לארסנל הטיפולים בהשמנה. טיפולים אלה כוללים בלון תוך קיבתי ותפירת קיבה אנדוסקופית. במחקר פרוספקטיבי שפורסם נבדקה השפעת בלון תוך קיבתי ב-21 חולים על שיפור במדדי מכ"ד. המטופלים הראו ירידה במדדים מטבוליים כולל משקל (ממוצע 11.7±7.7 אחוזים), ומדדי סוכרת. ניקוד היסטולוגי של מכ"ד השתפר ב-18 מתוך 20 חולים ושיפור בדרגת פיברוזיס של כנקודה אחת ב-15 אחוזים מהמטופלים. החוקרים מסכמים שבלון תוך קיבתי הביא לשיפור מטבולי והיסטולוגי בחולי מכ"ד[142]. ניסוי לא מבוקר נוסף, שכלל 26 משתתפים עם כבד שומני ופיברוזיס כבדי משמעותי, הראה כי בלון תוך קיבתי במשך 6 חודשים הוביל לירידת משקל, שיפור מטבולי וכן הפחתת שומן כבדי ושיפור בפיברוזיס כפי שהודגם בפיברוסקן[143] ואנדוסקופית[144]. אולם עקב העלייה בשכיחות השימוש בפרוצדורה זו, אנו צפויים לראות תוצאות מחקרים נוספים בקרוב.
אלכוהול וכבד שומני (ראו טבלה מספר 3 המסכמת את המחקרים בתחום)
מחקר בודד הדגים שיפור במדדי השמנה כבדית לאחר תפירת קיבה.
אלכוהול וכבד שומני (ראו טבלה מספר 3 המסכמת את המחקרים בתחום)
להגדרת כבד שומני כלא אלכוהולי יש לשלול ראשית צריכת אלכוהול כרונית של מעל 21 משקאות ממוצעים בשבוע לגבר ו-14 לאישה. חולי מכ"ש צריכים להימנע מצריכת אלכוהול כבדה. שתיית אלכוהול מתונה של ככוס משקה ליום נמצאה קשורה בסיכון מופחת לכבד שומני[145], כש"ד ואף צלקת[146][105][147]. אולם, איכות מחקרים אלו מוטלת בספק, בין השאר בשל היותם מחקרי חתך שלא תקננו למשתנים ערפלנים כגון אורחות חיים. לעומת זאת, במחקרים פרוספקטיביים מאוחרים יותר נראה נזק כבדי של שתיית אלכוהול מתונה[99][101]. הודגמה התקדמות פיברוזיס על פי סמנים ביוכימיים לאורך מעקב פרוספקטיבי בקרב מי ששתו כמות מתונה של אלכוהול (עד 20 גרם אלכוהול ליום) לעומת אלו שלא שתו כלל. כמו כן, הודגם כי שתיית אלכוהול מתונה (פחות מ-20 גרם אלכוהול ליום) קשורה בסיכון מוגבר למחלת כבד מתקדמת (כולל: אשפוז, סרטן כבד או תמותה על רקע מחלת כבד)[95]. הראיות חד משמעיות לגבי שחמת על רקע כש"ד[106], במקרה זה צריכת אלכוהול בכל רמה שהיא נמצאה מגבירה סיכון לסרטן הכבד. צריך לזכור כי כבד שומני והשמנה יכולים להחמיר את הנזק הכבדי בשתיינים[148] ומאידך כי צריכת אלכוהול עודפת עלולה להחמיר נזק כבדי בכבד שומני לא אלכוהולי (למעשה שילוב של כבד שומני אלכוהולי ולא אלכוהולי)[149]. מעניין לציין כי ייתכן וגם לדפוס השתייה יש השפעה. מחקר חתך בקרב 2,475 אנשים מצא כי דפוס בינג׳, Binge drinking (קרי 4 משקאות ומעלה לאישה וחמישה משקאות ומעלה לגבר באותה יממה בפרק זמן קצר) קשורה עם עלייה בסיכוי לסטיאטוזיס כבדי, גם אם הכמות השבועית הכוללת נחשבת כמתונה[96]. בהנחיות האיגוד האמריקאי לחקר הכבד משנת 2017 מסוכם כי אין די נתונים על מנת לתת המלצות לגבי צריכת אלכוהול מתונה בחולי כבד שומני, לאור מחסור במחקרים פרוספקטביים ולאור חשש של השפעה מבלבלת של עודף משקל נמוך יותר בקרב אנשים הצורכים אלכוהול באופן מתון[12]. לגבי החולים עם שחמת על רקע כבד שומני דלקתי[106], במקרה זה צריכת אלכוהול בכל רמה שהיא נמצאה מגבירה סיכון לסרטן הכבד ולכן מומלץ להימנע לחלוטין מאלכוהול[55]. בהנחיות מ-2019 של ה-ESPEN מומלץ שחולי כבד שומני ימנעו משתיית אלכוהול לחלוטין[56]. לגבי הטיעון שכמות מתונה של אלכוהול מסייעת במניעת מחלות לב וכלי דם, הרי שהדבר לא הודגם ספציפית בחולי כבד שומני. בפועל, נראה כי ההחלטה נתונה בידי הרופא המטפל ולפי מצב המטופל, בחולים ללא עדות לפיברוזיס משמעותית שרוצים לשתות אלכוהול יש להקפיד על כמות מתונה מאוד ורצוי לבחור ביין. בחולים עם עדות לפיברוזיס רצוי להימנע במידת האפשר ובחולים עם שחמת יש להימנע לחלוטין.
קפה וכבד שומני (ראו טבלה מספר 4 המסכמת את המחקרים בתחום)
פורסמו מספר מחקרי חתך שמצאו השפעה מגינה של קפה מפני צלקת בכבד שומני[124][130][128][126][125]. בנוסף, יש גם ראיות ממחקר פרוספקטיבי כי קפה קשור בהפחתת הסיכון לסרטן הכבד[150] אולם, לגבי השומן הכבדי הראיות סותרות וברוב המחקרים לא נמצא קשר מגן, כולל מחקר שבחן קשר בין צריכת קפה והיארעות כבד שומני באופן פרוספקטיבי[124].
נמצא במחקר אפידמיולוגי גדול עם קרוב ל-500,000 משתתפים כי צריכת כל סוגי הקפה מגינה מפני מחלת כבד כרונית וכבד שומני, תמותה ממחלת כבד וסרטן כבד (בהשוואה למי שלא שותה קפה כלל)[151].
המרכיבים בקפה שמגינים מפני צלקת או סרטן הכבד אינם ידועים[152] אבל ייתכן שאין מדובר בקפאין עצמו אלא בפוליפנולים שיש בקפה או בתרכובות אחרות שמצויות בו[153][154]. אין המלצה לשתיית קפה בחולים עם כבד שומני[55], אבל גם אין מניעה לשתייה במידה סבירה בקרב מי שרגיל לשתות (משקאות ללא סוכר).
תרופות אנטי סוכרתיות לטיפול בכבד שומני
לאור הקשר המטבולי בין סוכרת לכבד שומני, ניתן לשער שהתערבויות המשפרות את הלקויות המטבוליות בחולי סוכרת כמו שנוי אורחות חיים וטיפול תרופתי בהיפרגליקמיה ודיסליפדמיה יועיל גם במכ"ש. מירב המחקרים בנושא מתמקדים במטפורמין, בתיאזולידינדיונים ובדור החדש של תרופות לטיפול בסוכרת.
ביגואנידים-מטפורמין
התרופה מטפורמין, משמשת היום בתרופת הבחירה הראשונה לטיפול בסוכרת. היא שייכת למשפחת הביגואנידים ועיקר פעילותה היא דרך שיפור התנגודת הכבדית לאינסולין. מבחינת בטיחות השימוש, מדובר בתרופה בטוחה מבחינה כבדית, כאשר עד היום דווח על מקרים בודדים של דלקת כבד חריפה בהקשר לטיפול במטפורמין בחולים עם סוכרת. התרופה לא ניתנת באי ספיקת כבד קשה, אי ספיקת לב קשה ובחולים עם הפרעה קשה בתפקודי כליה.
הטיפול במטפורמין במטופלים עם כבד שומני הניב תוצאות סותרות, בחלקם נראתה ירידה באנזימים ושיפור היסטולוגי ובחלקם לא[155][156][157][158]. עצם השימוש במטפורמין במחלת כבד קשה נותר שנוי במחלוקת. במחקר רטרוספקטיבי שבדק האם המשך טיפול במטפורמין לאחר אבחון שחמת בחולים סוכרתיים משפר תוחלת חיים נמצאה ירידה בתמותה במטופלים סוכרתיים עם שחמת ובעיקר במטופלים שסבלו משחמת על רקע כבד שומני שהמשיכו להיות מטופלים במטפורמין לעומת כאלו שלא טופלו. במחקר זה אף מטופל לא פיתח Lactic acidosis[159]. יתרה מכך, קיימים מספר מחקרים פרה-קליניים הרומזים על פעילות אנטי גידולית של מטפורמין בסרטן כבד. הנתונים בבני אדם מוגבלים למחקרים רטרוספקטיבים[160][161]. נכון להיום, אין המלצה להשתמש באופן שגרתי במטפורמין במטופלים עם כבד שומני ללא סוכרת[55].
גליטזונים-תיאזולידנידיונים - Thiazolidinediones
הגליטזונים הם קבוצת תרופות המעלות רגישות לאינסולין בתאי שומן פריפריים. התרופות במשפחה זו פועלות כאגוניסטים של Peroxisome Proliferator Activated Receptor Gamma (PPAR-Gamma). התרופות הנמצאות היום בשוק הן Rosiglitazone ו-Pioglitazone.
מטא-אנליזה של מספר ניסויים קליניים אקראיים כפולי סמיות שבוצעו, הראתה כי מתן תרופה ממשפחת הגליטזונים משפר משמעותית היסטולוגיה כבדית מבחינת מדדי דלקת ורמת שומן במטופלים עם כש"ד לעומת פלצבו[162]. לגבי פיברוזיס התוצאות אינן עקביות. בעוד שמתן Rosiglitazone גרם לשיפור ברגישות לאינסולין וירידה של אנזימי כבד, ירידה בכמות שומן בכבד ומדדי דלקת כבדית, לא נצפה שיפור בדרגת הצלקת בכבד בחולים עם כבד שומני עם או ללא סוכרת. הארכת משך הטיפול משנה לשנתיים לא שיפרה את התוצאות וסוכם כי ללא שינוי באורחות חיים הטיפול התרופתי ב-Rosiglitazone לא יוביל לשינוי משמעותי[163]. עובדה זו רומזת שטיפול בעמידות לאינסולין אינו מספיק בחולים עם כבד שומני. השימוש ברוזיגליטזון פוחת מאוד עקב ספקות שעלו בקשר לבטיחות הקרדיוואסקולרית של תרופה זו.
להבדיל מ-Rosiglitazone, Aithai וחבריו הראו שמתן Pioglitazone לתקופה של שנה בחולים עם NASH (ללא סוכרת) שיפר גם מדדים מטבולים וגם מדדים היסטולוגיים כולל דרגת צלקת[164]. תוצאות דומות מבחינת שיפור במדדי הפיברוזיס הודגם גם על ידי Cusi ועמיתיו במחקר שכלל 101 חולים עם סוכרת או מצב טרום סוכרת וכבד שומני[165].
בשני ניסויים קליניים נוספים ואחד מהם לתקופה של 96 שבועות, עם זרוע שבדקה גם יעילות של מתן ויטמין E (PIVENS trial), מתן Pioglitazone היה כרוך בשיפור רמות אנזימי כבד, רמת שומן בכבד ושיפור היסטולוגי בחלק ממרכיבי הדלקת, ללא שיפור ברמת הצלקת[166][167]. ההנחיה של איגוד הכבד האירופאי[55] היא לתת Pioglitazone לחולים עם כש"ד שהוכח בביופסיה עם עדיפות למטופלים עם סוכרת שבה לתרופה יש שימוש רשום. יש להדגיש, שרב המחקרים שחקרו מתן Pioglitazone בחולים עם כש"ד, היו בחולים ללא סוכרת ולמשך טווחי זמן קצרים. מקובל להיזהר במתן גליטזונים במטופלים סוכרתיים עם עלייה באנזימי כבד ואף קיימת התווית-נגד לטיפול במטופלים עם טרנסאמינאזות מעל פי 3 מהערך העליון של הנורמה[168].
נוגדי 4-DPP
תרופות מסוג נוגדי 4-DPP מונעות את פירוק האינקרטינים ועל ידי כך מעלות הפרשת אינסולין ומורידות הפרשת גלוקגון. מספר המחקרים שבדקו יעילות קבוצה זו כטיפול בכבד שומני הוא מצומצם. בניסוי קליני קטן בלתי אקראי נמצא קשר בין מתן התרופה לירידה ברמת אנזימי כבד[169]. ובניסוי נוסף אקראי כפול סמויות שנמשך חצי שנה נמצאה ירידה ברמות טריגליצרידים כבדיים[170]. במחקר נוסף שפורסם ב-2016 וכלל 50 מטופלים עם כבד שומני שחלקם קיבלו סיטגליפטין וחלקם פלצבו למשך 24 שבועות, לא נמצא הבדל משמעותי בין 2 הקבוצות מבחינת אנזימי כבד או דרגת הפיברוזיס הכבדית שנבדקה באמצעים לא פולשניים[171].
במחקר קטן נוסף שכלל ביופסיות, שוב לא נמצא הבדל בין קבוצת הפלצבו לקבוצה שטופלה בסיטגליפטין מבחינת מדדי פיברוזיס[172]. הפרופיל הבטיחותי של תרופות מסוג נוגדי 4-DPP מצוין.
לסיכום: מספר המחקרים שבדקו את הנושא קטן, ההמלצות לא חד משמעיות ונכון להיום יעילות נוגדי 4-DPP בכבד שומני איננה ברורה והם אינם מומלצים כטיפול ייעודי.
התרופות החדשות לטיפול בסוכרת
אחת מפריצות הדרך המשמעותיות ביותר בתחום הטיפול בסוכרת אירעה עם הכנסת הדור החדש של טיפולים תרופתיים בסוכרת מסוג GLP-1 agonist ומעכבי SGLT2.
מדובר ב-2 קבוצות של תרופות שבמספר לא מבוטל של מחקרים שכלל מעל 75,000 מטופלים הוכיחו הפחתה של הסיכון לסיבוכים קרדיו-ווסקולריים משמעותיים (אוטם לבבי, אוטם מוחי ומוות ממחלה קרדיווסקולרית) בחולי סוכרת עם מחלת לב טרשתית ידועה[173][174][175]. בנוסף, הטיפול בתרופות אלו הפחית את הסיכון להתקדמות מחלת כליות בחולים סוכרתיים[176][177][178].
GLP-1 Agonists
פעולתם העיקרית של האגוניסטים של קולטני 1-GLP הוא שחרור אינסולין מתאי בתא בלבלב ועיכוב שחרור גלוקגון. בנוסף להשפעה ישירה על רמות הגלוקוז, נמצא שתרופות אלו משפיעות על תחושת השובע וגורמות לירידה במשקל וכאמור מפחיתות את הסיכון לאירועים קרדיווסקולריים משמעותיים והתקדמות מחלת כליות בחולים הסוכרתיים. במספר מחקרים נמצא שקיימים קולטנים ל-1-GLP בתאי בכבד ושקולטנים אלו חשובים בהורדת דרגת סטאטוזיס In vitro[179], השילוב של תרופה שמורידה תיאבון, מפחיתה במשקל ומשפיעה על המטבוליזם של גלוקוז יחד עם קיום קולטנים על תאי הכבד, הוביל לבדיקת ההשפעה של קבוצת תרופות זו על כבד שומני. מספר המחקרים שבדק את השפעת האגוניסטים לקולטני 1-GLP על כבד שומני מוגבל - חלקם לא כפולי סמיות, חלקם ללא פלצבו, רובם מערב מספר קטן של מטופלים. במטא-אנליזה של 11 מחקרים שכללו כ-950 מטופלים שטופלו למחלת הכבד השומני עם אגוניסטים לקולטני 1-GLP שונים בממוצע ל-26 שבועות נמצאה ירידה בכמות השומן הכבדי כפי שנבדק ב-MRI (Magnetic Resonance Imaging) או ביופסיה, ירידה ברמת אנזימי כבד ושיפור היסטולוגי ללא החמרת פיברוזיס במחקרים שכללו ביופסיה[180]. נרחיב על 3 מהמחקרים הגדולים יותר בתחום. בראשון, נבדקה השפעת Liraglutide על הכבד.
Liraglutide הוא אגוניסט לקולטני 1-GLP, הניתן פעם ביום, ונרשם בארצות הברית, אירופה וישראל כתרופה כנגד השמנה. במטא-אנליזה גדולה שכללה כ-4,000 מטופלים עם סוכרת מסוג 2, נמצא שטיפול במשך 26 שבועות בLiraglutide שיפר באופן משמעותי אנזימי כבד ונסבל בצורה טובה[181]. ההשפעה הישירה של Liraglutide על ההיסטולוגיה הכבדית נבדקה במחקר ה-LEAN. במחקר זה ניתן Liraglutide במינון יומי של 1.8 מיליגרם בחולים עם מכ"ש. הניסוי היה מבוקר, אקראי, כפול סמיות וכלל 52 מטופלים עם מכ"ד, חלקם עם סוכרת. במחקר נמצא שהטיפול בלירגלוריד הוביל לירידה בכמות השומן הכבדי ושיפור במרקרים היסטולוגיים כמו Hepatocyte ballooning, אבל ללא שינוי משמעותי בדלקת. אף שלא נצפתה נסיגה משמעותית בדרגת הפיברוזיס, דווח על האטה בהתקדמות הפיברוזיס במספר גדול יותר של מטופלים שטופלו לעומת כאלו שלא קבלו טיפול[182]. במחקר קטן אחר נמצא שטיפול ב-Exenatide, אגוניסט 1-GLP קצר טווח הניתן פעמיים ביום, שיפר רמות טרנסאמינזות וגרם לירידה במשקל בחולים עם כבד שומני[183]. במחקר כפול סמויות נוסף שפורסם בספטמבר 2020 ב-NEJM (New England Journal of Medicine) נבדק האם הטיפול בSemaglutide משפר היסטולוגיה כבדית בחולים עם מכ"ד. מדובר באגוניסט לקולטני 1-GLP ארוך טווח הניתן אחת לשבוע. המחקר, כפול סמויות נמשך 72 שבועות, כלל 320 מטופלים עם ובלי סוכרת, עם כבד שומני-מכ"ד ופיברוזיס כבדי בדרגה אחת עד שלוש (מוכח בביופסיה) כשחלקם קיבלו Semaglutide במינונים שונים-0.1, 0.2 ו-0.4 מיליגרם או קבלו פלצבו. המטרה הראשונית של המחקר הייתה לבדוק שיפור בסמנים ההיסטולוגים מבחינת המכ"ד ללא החמרה של פיברוזיס. במחקר נמצא ש-59 אחוזים מהמטופלים שקבלו Semaglutide במינון של 0.4 מיליגרם תת-עורי הראו נסיגה של מכ"ד ללא החמרה במצב הפיברוזיס (0.001 >p). המחקר לא הצליח להוכיח שיפור משמעותי סטטיסטי בדרגת הפיברוזיס בקבוצה שקיבלה Semaglutide[184]. בניסוי אחר שהשווה מתן שילוב של Exenatide ואינסולין למתן אינסולין בלבד בחולים עם כבד שומני, השמנת יתר וסוכרת נמצא שבקבוצה שטופלה ב-Exenatide ואינסולין הייתה ירידה משמעותית במשקל גוף, היקף מותן ורמות אנזימי כבד לעומת הקבוצה שטופלה באינסולין בלבד[185].
בניסוי נוסף, השוו מתן מטפורמין ל-Exenatide בחולים סכרתיים עם כבד שומני ונמצא יתרון למתן אקסנטייד מבחינת נרמול אנזימי כבד, ירידה במשקל וירידה במדדי דלקת[186]. בניסוי קטן שכלל 21 מטופלים נמצא יתרון לשילוב של Pioglitazone ו-Exenatide לעומת Pioglitazone לבד מבחינת הורדת כמות שומן בכבד[187]. נכון להיום, קיים מידע מוגבל לגבי יעילות הטיפול באגוניסטים לקולטני 1-GLP בחולים עם כבד שומני וסוכרת. יש מקום לביצוע ניסויים מבוקרים אקראיים גדולים לפני מתן המלצה גורפת.
מעניין לציין שבמספר מחקרים שבדקו את היעילות של Liraglutide לעומת מטפורמין או גליקלזיד ל-24 שבועות, נמצא שבכל הקבוצות הייתה ירידה בשומן התוך כבדי אבל הירידה הגדולה ביותר הייתה בקבוצה של ה-Liraglutide. אין המלצה של שום איגוד מקצועי להשתמש באגוניסטים לקולטני 1-GLP כתרופת הבחירה הראשונה בחולים עם כבד שומני וסוכרת.
מעכבי SGLT2
תרופות ממשפחת מעכבי SGLT2 מפחיתות את רמות הסוכר בדם באמצעות מניעת ספיגתו בכליות והפרשתו בשתן. נמצא שמטופלים שנטלו תרופות ממשפחה זו הפחיתו ממשקל גופם ומהיקף המותניים. כמו כן תרופות אלו מסייעות בהפחתת לחץ הדם במידה מתונה. ההשפעה המשמעותית ביותר של תרופות מהקבוצה הזו היא, כאמור, בהפחתה הדרמטית בסיכון לאירועים קרדיווסקולריים משמעותיים כולל הפחתה באשפחים עקב אי ספיקת לב ובסיכון להתקדמות מחלת כליות בחולים הסוכרתיים. במספר מחקרי מעבדה נמצא קשר בין מתן תרופות אלו לבד או בשילוב עם תרופות מסוג מעכבי 4-DPP לירידה בכמות השומן בכבד ושיפור בדרגת הצלקת הכבדית[188][189].
מספר מחקרים שפורסמו בדקו את ההשפעה של תרופות ממשפחה זו על כבד שומני במספר מצומצם של חולים עם סכרת. נדון בחלק מהם - במחקר הראשון, שכלל 66 חולים עם סוכרת וכבד שומני, נמצא שבמטופלים שקיבלו תרופה ממשפחת מעכבי SGLT2 נראה שיפור בכמות השומן הויסרלי ובמשקל ללא שינוי באנזימי כבד[190].
במחקר השני, שכלל 50 מטופלים עם סוכרת וכבד שומני, נמצאה ירידה משמעותית בכמות השומן הכבדי בקבוצת המטופלים שקיבלה Empagliflozin לצד ירידה ברמת ה-ALT[191]. מחקר נוסף כפול סמויות שפורסם בשנת 2020 וכלל 84 חולים עם סוכרת חדשה מאוזנת הדגים גם הוא ירידה בכמות השומן הכבדי (נבדק ב-MRI) במטופלים שקיבלו ב-Empagliflozin במשך 24 שבועות באופן משמעותי יחסית לקבוצת הפלצבו[192].
אחת מתופעות הלוואי החשובות והשכיחות של קבוצה זו של תרופות היא העלייה בשכיחות דלקות בדרכי השתן, הנרתיק ואזור הפין. תופעות לוואי נוספות הם קטואצידוזיס עם רמת סוכר תקינה, התייבשות ועליה ברמת הכולסטרול. נכון להיום אין הנחיה לתת מעכבי SGLT2 כתרופת קו ראשון לחולים עם כבד שומני וסוכרת.
טיפולים תרופתיים אחרים
אין טיפול תרופתי המאושר על ידי גופים רגולטוריים לטיפול במחלת הכבד השומני. מעבר לתרופות לטיפול בסוכרת והשמנה שתוארו לעיל, קיימות מספר תרופות נוספות הנמצאות במחקרים מתקדמים ומיועדות ספציפית לטיפול במכ"ש.
אגוניסטים ל-FXR - האגוניסט ל-FXR חומצה אבטכולית מאושר לטיפול בדלקת מרתית ראשונית (PBC - Primary Biliary Cholangitis). תרופה זו נוסתה גם כתרופה למכ"ש ותוצאות מחקר ה-FLINT הראו שיפור במדדי דלקת ללא החמרה בפיברוזיס[193].
במחקר פאזה שלישית נוסף בתרופה נבדק השימוש במינונים עולים של חומצה אבטיכולית לעומת פלצבו בכ-2000 חולים עם פיברוזיס בדרגות F1-3, (מתוכם 931 עם פיברוזיס בדרגות F2-3). תוצאות ביניים של מחקר זה פורסמו. היה שיפור משמעותי תלוי מינון ברמת הפיברוזיס בקבוצות הטיפול מול הפלצבו. לא היה הבדל בהעלמות המכ"ד (NASH resolution) בין הקבוצות. החוקרים סיכמו שחומצה אובטיכולית במינון 25 מיליגרם גרם לשיפור משמעותי בפיברוזיס ומדדי מכ"ד. למרות התוצאות המבטיחות, התרופה לא אושרה בינתיים על ידי ה-FDA (Food and Drug Administration)[194].
אנלוגים ל-FGF19 מחקרים שונים הראו שהרמות של פקטור השיעתוק 19 Fibroblast Growth Factor נמוכות בחולי מכ"ש ועולות לאחר ניתוחים בריאטריים. זהו סקטור המושפע מ-FXR ומשפיע על יצור מלחי מרה. התרופה אלדפאמין (Aldafamin) נבדקה במחקר פאזה שנייה ב-82 חולי מכ"ש שהוכח בביופסיה. התרופה ניתנה בזריקה תת-עורית במינונים שונים והראתה שיפור בתכולת השומן בכבד כפי שנמדד בהדמיה[195].
במחקר פתוח וללא קבוצת בקורת הדגימה התרופה שיפור במדדים היסטולוגיים של מכ"ד ללא השפעה על ממדים מטבוליים. בנוסף החולים קיבלו סטטין על מנת לסתור את תופעת הלוואי הידועה של תרופה זו הגורמת לעליית כלוסטרול[196]. תרופות נוספות הכוללות אנלוג ל-FGF21 הפטוקין המבקר את משק הסוכר, מעכבי (Acetyl COA Carboxylase (ACC ואגוניסטים של Stearoyl CoA desaturase המבקרים את משק הליפידים ואגוניסטים של Thyroid hormone receptor beta המבקרים את פעולת הורמוני התריס נמצאים במחקר מתקדם. בנוסף מתמקדות חברות התרופות בתרופות להיכולות להביא לנסיגת פיברוזיס, מבין המובילות נמצא מעכב ל-2 CC chemokine receptor שהראה תוצאות מבטיחות במחקרים ראשוניים.
סטטינים - מחקרים עדכניים מרמזים שלטיפול עם סטטינים במטופלים עם כבד שומני יש השפעה מיטבית על דרגת השומן והצלקת הכבדית ואף עשוי לנרמל אנזימי כבד[197][198]. בסקירת ספרות של Cochrane שפורסמה ב-2013 נמצאו 2 מחקרים בלבד עם מספר קטן של משתתפים שבדקו באופן ישיר את השימוש בסטטינים כטיפול בכבד שומני. הרושם הוא שסטטינים יכולים לשפר רמת טרנסאמינזות[199]. גם בהצהרת מומחים שפורסמה ב-2017 צוין כי אץ התווית נגד למתן סטטינים במטופלים עם כבד שומני, וייתכן אף שלסטטינים יש פוטנציאל להאט את חומרת המחלה הכבדית במטופלים עם כבד שומני ודיסליפידמיה במקביל להורדת הסיכון הלבבי[200]. יש לציץ שההמלצות המשותפות של האיגודים האירופאים לחקר מחלות כבד, סוכרת והשמנה הן שאמנם סטטינים לא נבדקו בצורה מספקת כטיפול לכש"ד, אבל השימוש שלהם במחלת הכבד השומני הוא בטוח, לא מעלה את הסיכון לנזק כבדי וייתכן אף שמוריד רמת אנזימי כבד[55].
בהתבסס על הממצאים מהספרות, אין התוויית נגד למתן סטטינים במטופלים עם כבד שומני. חלק גדול ממטופלים עם כבד שומני סובלים מתסמונת מטבולית, סוכרת ומחלת לב כלילית וזקוקים לסטטינים כחלק מהטיפול הכולל בגורמי סיכון לבביים.
תוספי מזון
ויטמין E
מספר ניסויים קליניים אקראיים בדקו את השפעת ויטמין E במינונים גבוהים בחולים עם כבד שומני ללא סוכרת. הגדול מביניהם הוא מחקר שפורסם ב-2010 ב-NEJM (PIVENS trail) וכלל 247 מטופלים עם כבד שומני ללא סוכרת וללא שחמת, ובו הושוו 3 זרועות: מטופלים שקבלו Pioglitazone או ויטמין E (במינון של 800 מיליגרם ליום) או פלצבו לתקופה של 96 שבועות. נמצא שהמטופלים שקיבלו ויטמין E הראו שיפור ברמת אנזימי הכבד עם שיפור במדדי הדלקת וירידה בכמות השומן הכבדי אך ללא שיפור ברמת הצלקת[167]. בניסוי קליני אקראי נוסף, השתתפו 105 חולים עם סברת שחולקו ל-3 קבוצות - קבוצה ראשונה קבלה ויטמין E במינון של 400 מיליגרם פעמיים ביום, קבוצה שנייה קיבלה ויטמין E במינון של 400 מיליגרם פעמיים ביום ו-Pioglitazone 45 מיליגרם ליום וקבוצה שלישית קיבלה פלצבו. משך המחקר היה 18 חודשים, ומטרתו הייתה לבדוק שיפור היסטולוגי כבדי משמעותי ללא החמרה בדרגת הפיברוזיס הכבדי. בקבוצה שקיבלה טיפול משולב נמצא שיפור היסטולוגי משמעותי עם שיפור בדרגת הסטאטוזיס, שיפור בדרגת הדלקת ושיפור בדרגת ה-Ballooning, לעומת הקבוצה שקיבלה ויטמין E בלבד ובה נמצא שיפור בדרגת הסטאטוזיס בלבד. ב-2 הקבוצות לא נצפה שיפור בדרגת הפיברוזיס[201].
אולם, עצם השימוש בוויטמין E במינונים גבוהים שנוי במחלוקת עקב עדויות לגבי קשר בין צריכתו לעלייה בתמותה[202], עלייה בהיארעות אוטם מוחי המורגי[203] ועלייה בהיארעות שאת ממאירה של ערמונית[204]. נכון להיום אין המלצה של EASL למתן ויטמין E בחולים עם סוכרת וכבד שומני[55]. בהנחיות של ה-AASLD[12] וכן בהנחיות מ-2019 של ה-ESPEN יש המלצה למתן ויטמין E, אך רק בחולים לא סוכרתיים ועם כש"ד שהודגם היסטולוגיה[56].
אומגה 3
נערכו מספר ניסויים קליניים אקראיים באיכות גבוהה מבחינת גודל המדגם, משך המעקב וביצוע ביופסיית כבד עוקבת בחלקם, שבחנו השפעת תוסף אומגה 3 בכבד שומני. המחקרים לא הראו תוצאות עקביות, אולי עקב שימוש בתוספים במינונים שונים והרכב שונה של חומצות שומן אומגה 3. אולם, נראה כי תיתכן השפעה מיטיבה על השומן הכבדי אך לא על דלקת, צלקת ואף לא על תנגודת לאינסולין[205][206][207]. בהנחיות של האיגוד האירופאי לחקר הכבד (EASL) משנת 2016 אין המלצה לתת אומגה 3 כטיפול ספציפי בכבד שומני[55] וכך גם בהנחיות החדשות משנת 2018 של האיגוד האמריקאי לחקר הכבד - AASLD (American Association for the Study of Liver Diseases)[12], ובהנחיות של ה-ESPEN משנת 2019[56].
| Author | Supplement mg/day | Duration
(M) |
Sample | Improved Steatosis | Improved NASH | Improved Fibrosis |
| Argo CK, J of Hepatology 2015 | EPA & DHA 3000 | 12 | 34 NASH | Yes | No | No |
| Sanyal AJ, Gastroenterology 2014 | EPA 2700 | 12 | 243 NASH | No | No | No |
| Scorletti E, Hepatology 2014 | EPA & DHA 4000 | 15-18 | 91 NAFLD | Yes | NE | No
(by fibrosis score) |
| Nobili V, Arch DisChild 2011 | DHA 500 or 250 | 6 | 60 children NAFLD | Yes | NE | NE |
| הערה: NE מציין כי המדד לא נבדק | ||||||
סיכום
הגישה הטיפולית בחולה הסוכרתי עם כבד שומני מתבססת על איתור וטיפול מיטבי במרכיבים נוספים של התסמונת המטבולית, איתור וטיפול בגורמי סיכון לבביים נוספים, הערכת חומרת המחלה הכבדית מבחינת נוכחות צלקת, שחמת או הפטומה על ידי מעקב קבוע הכולל סונר, טיפול בשומן כבדי עצמו על ידי שינוי אורחות חיים ואיזון הסוכרת.
ההמלצות מבוססות הראיות לתזונה ופעילות גופנית בחולי מכ"ש מסוכמות בגרף מספר 1.
חשוב לזכור - הכבד השומני - הקשר לסוכרת מסוג 2 ודרכי טיפול
- המצאות מחלת הכבד השומני שאינה בגין צריכת אלכוהול מגיעה עד 75 אחוזים בחולים הסוכרתיים
- היארעות סוכרת באנשים עם כבד שומני גבוהה יותר מאשר באוכלוסייה דומה מבחינת גיל וגורמי סיכון מקובלים אחרים
- סוכרת נחשבת כגורם סיכון להופעת דלקת וצלקת כבדית בחולים עם כבד שומני. השכיחות של שחמת בחולים עם כבד שומני וסוכרת היא 25 אחוזים לעומת 10 אחוזים בחולים עם כבד שומני ללא סוכרת
- הסיכון של חולה סוכרת עם כבד שומני למות מכל סיבה שהיא הוא פי 2.2 מאשר חולה סוכרתי ללא כבד שומני
- עצם הנוכחות של כבד שומני בחולה סוכרת חושף אותו לסיכון מוגבר למחלת לב כלילית, ללא קשר למרכיבי הסינדרום המטבולי
- לסוכרת ביטוי קשה יותר בחולים המשלבים סוכרת וכבד שומני, הן מבחינת הכבד והן מבחינת סיבוכים מאקרו ומיקרווסקולריים
- כל הערכה של מטופל עם סוכרת וכבד שומני צריכה לכלול הערכה של הפגיעה הכבדית והערכה כללית של מצב קרדיומטבולי
- בחולי סוכרת עם כבד שומני רצוי במיוחד לבצע הערכה של צלקת מתקדמת (פיברוזיס דרגה 3–4) באמצעים בלתי פולשניים מתוקפים שקיימים היום ואינם כרוכים בעלות נוספת, דונמת 4-FIB או באמצעות פיברוסקן
- שינוי באורחות חיים הוא אבן היסוד לטיפול בכבד שומני
ביבליוגרפיה
- ↑ Loomba R, Sanyal AJ. The global NAFLD epidemic. Nature reviews Gastroenterology & hepatology. 2013;10(11):686-90
- ↑ 2.0 2.1 Zelber-Sagi S, Nitzan-Kaluski D, Halpern Z, Oren R. Prevalence of primary non-alcoholic fatty liver disease in a population-based study and its association with biochemical and anthropometric measures. Liver Int. 2006;26(7):856-63
- ↑ 3.0 3.1 Williams CD, Stengel J, A sike MI, Torres DM, Shaw J, Contreras M, et al. Prevalence of nonalcoholic fatty liver disease and nonalcoholic steatohepatitis among a largely middle-aged population utilizing ultrasound and liver biopsy: a prospective study. Gastroenterology. 2011;140(1):124-31
- ↑ 4.0 4.1 4.2 4.3 4.4 4.5 Musso G, Gambino R, Cassader M, Pagano G. Meta-analysis: natural history of non-alcoholic fatty liver disease (NAFLD) and diagnostic accuracy of non-invasive tests for liver disease severity. Ann Med. 2011;43(8):617-49
- ↑ Hudng KW, Leu HB, Wang YJ, Luo JC, Lin HC, Lee FY, et al. Patients with nonalcoholic fatty liver disease have higher risk of colorectal adenoma after negative baseline colonoscopy. Colorectal Disease. 2013;15(7):830-5
- ↑ Allen AM, Hicks SB, Mar a KC, Larson JJ, Therneau TM. The risk of incident extrahepatic cancers is higher in non-alcoholic fatty liver disease than obesity—A longitudinal cohort study. Journal of hepatology. 2019;71(6):1229-36
- ↑ Kim CH, Younossi ZM. Nonalcoholic fatty liver disease: a manifestation of the metabolic syndrome. Cleve Clin J Med. 2008;75(10):721-8
- ↑ Stefan N, Kantartzis K, Haring HU. Causes and metabolic consequences of Fatty liver. Endocr Rev. 2008;29(7):939-60
- ↑ Zelber-Sagi S, Lotan R, Shlomai A, Webb M, Harrari G, Buch A, et al. Predictors for incidence and remission of NAFLD in the general population during a seven-year prospective follow-up. J Hepatol. 2012;S6(5):1 l45-51
- ↑ Vernon G, Baranova A, Younossi ZM. Systematic review: the epidemiology and natural history of non-alcoholic fatty liver disease and non-alcoholic steatohepatitis in adults. Aliment Pharmacol Ther.34(3):274-85
- ↑ Pratt DS, Kaplan MM. Evaluation of abnormal liver-enzyme results in asymptomatic patients. N Engl J Med. 2000;342(17):1266-71
- ↑ 12.0 12.1 12.2 12.3 12.4 12.5 12.6 Chalasani N, Younossi Z, Lavine JE, Charlton M, Cusi K, Rinella M, et al. The diagnosis and management of nonalcoholic fatty liver disease: Practice guidance from the American Association for the Study of Liver Diseases. Hepatology. 2018;67(1):328-57
- ↑ Angulo P, Kleiner DE, Dam-Larsen S, Adams LA, Bjornsson ES, Charatcharoenwitthaya P, et al. Liver Fibrosis, but No Other Histologic Features, 1s Associated With Long-term Outcomes of Patients With Nonalcoholic Fatty Liver Disease. Gastroenterol- ogy. 2015;149(2):389-97 e10
- ↑ Ekstedt M, Hagstrom H, Nasr P, Fredrikson M, Stal P, Kechagias S, et al. Fibrosis stage is the strongest predictor for dis- ease-specific mortality in NAFLD after up to 33 years of follow-up. Hepatology. 201S;61(5):1547-54
- ↑ McPherson S, Anstee QM, Henderson E, Day CP, Burt AD. Are simple noninvasive scoring systems for fibrosis reliable in patients with NAFLD and normal ALT levels? Eur J Gastroenterol Hepatol. 2013;2S(6):652-8
- ↑ lmajo K, Kessoku T, Honda Y, Tome no W, Ogawa Y, Mawatari H, et al. Magnetic Resonance Imaging More Accurately Clas- sifies Steatosis and Fibrosis in Patients With Nonalcoholic Fatty Liver Disease Than Transient Elastog raphy. Gastroenterology. 2016;150(3):626-37 e7
- ↑ 17.0 17.1 17.2 Ratziu V, Bellentani S, Cortez-Pinto H, Day C, Marchesini G. A position statement on NAFLD/NASH based on the EASL 2009 special conference. J Hepatol. 2010;53(2):372-84
- ↑ Guha IN, Parkes J, Roderick P, Chattopadhyay D, Cross R, Harris S, et al. Noninvasive markers of fibrosis in nonalcoholic fatty liver disease: Validating the European Liver Fibrosis Panel and exploring simple markers. Hepatology. 2008;47(2):455-60
- ↑ 19.0 19.1 Kaswala DH, Lai M, Afdhal NH. Fibrosis Assessment in Nonalcoholic Fatty Liver Disease (NAFLD) in 2016. Dig Dis Sci. 2016;61(5):1356-64
- ↑ NACE guideline ”Non-alcoholic fatty liver disease (NAFLD): assessment and management.“ Published b July 2016
- ↑ Vuppalanchi R, Siddiqui MS, Van Natta ML, Hallinan E, Brandman D, Kowdley K, et al. Performance characteristics of vibra- tion־controlled transient elastography for evaluation of nonalcoholic fatty liver disease. Hepatology. 2018;67(1):134-44
- ↑ 22.0 22.1 Kwok R, Choi KC, Wong GL, Zhang Y, Chan HL, Luk AO, et aL Screening diabetic patients for non-alcoholic fatty liver disease with controlled attenuation parameter and liver stiffness measurements: a prospective cohort study. Gut. 2016;65(8):1359-68
- ↑ Tapper EB, Castera L, Afdhal NH. FibroScan (vibration-controlled transient elastography): where does it stand in the United States practice. Clin Gastroenterol Hepatol. 2015;13(1):27-36
- ↑ 24.0 24.1 Kwok R, Tse YK, Wong GL, Ha Y, Lee AU, Ngu MC, et al. Systematic review with meta-analysis: non-invasive assessment of non-alcoholic fatty liver disease-the role of transient elastography and plasma cytokeratin-18 fragments. Aliment Pharmacol Ther. 2014;39(3):254-69
- ↑ Tsochatzis EA, Newsome PN. Non-alcoholic fatty liver disease and the interface between primary and secondary care. Lancet Gastroenterol Hepatol. 2018;3(7):509-17
- ↑ Petta S, Vanni E, Bugianesi E, Di Marco V, Camma C, Cabibi D, et al. The combination of liver stiffness measurement and NAFLD fibrosis score improves the noninvasive diagnostic accuracy for severe liver fibrosis in patients with nonalcoholic fatty liver disease. Liver Int. 2015;35(5):1566-73
- ↑ Angulo P, Bugianesi E, Bjornsson ES, Charatcharoenwitthaya P, Mills PR, Barrera F, et al. Simple noninvasive systems predict long-term outcomes of patients with nonalcoholic fatty liver disease. Gastroenterology. 2013;145(4):782-9. e4
- ↑ Hagstrom H, Nasr P. Ekstedt M, Hammar U, St3l P, Hultcrantz R, et al. Fibrosis stage but not NASH predicts mortality and time to development of severe liver disease in biopsyproven NAFLD. J Hepatol. 2017;67:1265-73
- ↑ Sanyal AJ, Harrison SA, Ratziu V, Abdelmalek MF, Diehl AM, Caldwell S, et al. The natural history of advanced fibrosis due to nonalcoholic steatohepatitis: data from the simtuzumab trials. Hepatology. 2019;70(6):1913-27
- ↑ Boursier J, Vergniol J, Guillet A, Hiriart J-B, Lannes A, Le Bail B, et al. Diagnostic accuracy and prognostic significance of blood fibrosis tests and liver stiffness measurement by FibroScan in non-alcoholic fatty liver disease. Journal of hepatology. 2016;65(3):570-8
- ↑ Sanyal AJ, Anstee QM, Trauner MH, Lawitz EJ, Abdelmalek MF, Ding D, et al., editors. CIRRHOSIS REGRESSION IS ASSOCIATED WITH IMPROVED CLINICAL OUTCOMES IN PATIENTS WITH NONALCOHOLIC STEATOHEPATITIS (NASH). HEPATOLOGY; 2020: WILEY 111 RIVER ST, HOBOKEN 07030-5774, NJ USA
- ↑ Angulo P, Keach JC, Batts KP, Lindor KD. Independent predictors of liver fibrosis in patients with nonalcoholic steatohepati- tis. Hepatology. 1999,30(6):! 356-62
- ↑ Younossi ZM, Golabi P, de Avila L, Paik JM, Srishord M, Fukui N, et al. The global epidemiology of NAFLD and NASH in pa- tients with type 2 diabetes: A systematic review and meta-analysis. J Hepatol. 2019;71(4):793-801
- ↑ Younossi ZM, Gramlich T, Matteoni CA, Boparai N, McCullough AJ. Nonalcoholic fatty liver disease in patients with type 2 diabetes. Clin Gastroenterol Hepatol. 2004;2(3):262-5
- ↑ Targher G, Corey KE, Byrne CD, Roden M. The complex link between NAFLD and type 2 diabetes mellitus - mechanisms and treatments. Nat Rev Gastroenterol Hepatol. 2021
- ↑ Fukuda T, Hamaguchi M, Kojima T, Hashimoto Y, Ohbora A, Kato T, et al. The impact of non-alcoholic fatty liver disease on incident type 2 diabetes mellitus in non-overweight individuals. Liver international: official journal of the International Associ- ation for the Study of the Liver. 2016;36(2):275-83
- ↑ Yamazaki H, Tsuboya T, Tsuji K, Dohke M, Maguchi H. Independent Association Between Improvement of Nonalcoholic Fatty Liver Disease and Reduced Incidence of Type 2 Diabetes. Diabetes Care. 2015;38(9):1673-9
- ↑ 38.0 38.1 Mantovani A, Scorletti E, Mosca A, Alisi A, Byrne CD, Targher G. Complications, morbidity and mortality of nonalcoholic fatty liver disease. Metabolism. 2020;111 S:154170
- ↑ Bugianesi E, Vanni E, Marchesini G. NASH and the risk of cirrhosis and hepatocellular carcinoma in type 2 diabetes. Curr Diab Rep. 2007;7(3):175-80
- ↑ Targher G, Bertolini L, Padovani R, Rodella S, Tessari R, Zenari L, et al. Prevalence of nonalcoholic fatty liver disease and its association with cardiovascular disease among type 2 diabetic patients. Diabetes Care. 2007;30(5):1212-8
- ↑ Targher G, Bertolini L, Rodella S, Zoppini G, Lippi G, Day C, et al. Non-alcoholic fatty liver disease is independently associated with an increased prevalence of chronic kidney disease and proliferative/laser-treated retinopathy in type 2 diabetic patients. Diabetologia. 2008;51(3):444-50
- ↑ Mellinger JL, Pencina KM, Massaro JM, Hoffmann U, Seshadri S, Fox CS, et al. Hepatic steatosis and cardiovascular disease outcomes: An analysis of the Framingham Heart Study. Journal of hepatology. 2015;63(2):470-6
- ↑ Targher G, Byrne CD, Lonardo A, Zoppini G, Barbui C. Non-alcoholic fatty liver disease and risk of incident cardiovascular disease: A meta-analysis. J Hepatol. 2016;65(3):589-600
- ↑ Henson JB, Simon TG, Kaplan A, Osganian S, Masia R, Corey KE. Advanced fibrosis is associated with incident cardiovascular disease in patients with non-alcoholic fatty liver disease. Aliment Pharmacol Ther. 2020;51(7):728-36
- ↑ Alexander M, Loomis AK, van der Lei J, Duarte-Salles T, Prieto-Alhambra D, Ansell D, et aL Non-alcoholic fatty liver disease and risk of incident acute myocardial infarction and stroke: findings from matched cohort study of 18 million European adults. BM J. 2019,367:15367
- ↑ Siddiqui MS, Fuchs M, Idowu MO, Luketic VA, Boyett S, Sargeant C, et al. Severity of nonalcoholic fatty liver disease and progression to cirrhosis are associated with atherogenic lipoprotein profile. Clin Gastroenterol Hepatol. 2015;13(5):1000-8 e3
- ↑ DeFilippis AP, Blaha MJ, Martin SS, Reed RM, Jones SR, Nasir K, et al. Nonalcoholic fatty liver disease and serum lipoproteins: the Multi-Ethnic Study of Atherosclerosis. Atherosclerosis. 2013;227(2):429-36
- ↑ Targher G, Corey KE, Byrne CD. NAFLD, and cardiovascular and cardiac diseases: Factors influencing risk, prediction and treatment. Diabetes Metab. 2021;47(2):101215
- ↑ Lazo M, Solga SF, Horska A, Bonekamp S, Diehl AM, Brancati FL, et al. The Effect of a 12-Month Intensive Lifestyle Intervention on Hepatic Steatosis in Adults with type 2 Diabetes. Diabetes Care. 2010
- ↑ Promrat K, Kleiner DE, Niemeier HM, Jackvony E, Kearns M, Wands JR, et al. Randomized controlled trial testing the effects of weight loss on nonalcoholic steatohepatitis. Hepatology. 2010;51(1):121-9
- ↑ Vilar Gomez E, Rodriguez De Miranda A, Gra Dramas B, Arus Soler E, Llanio Navarro R, Calzadilla Bertot L, et al. Clinical trial: a nutritional supplement Viusid, in combination with diet and exercise, in patients with nonalcoholic fatty liver disease. Aliment Pharmacol Ther. 2009;30(10):999-1009
- ↑ Vilar-Gomez E, Martinez-Perez Y, Calzadilla-Bertot L, Torres-Gonzalez A, Gra-Oramas B, Gonzalez-Fabian L, et al. Weight Loss Through Lifestyle Modification Significantly Reduces Features of Nonalcoholic Steatohepatitis. Gastroenterology. 2015;149(2):367-78e5; quiz e14-5
- ↑ Haufe S, Engeli S, Kast P, Bohnke J, Utz W, Haas V, et al. Randomized comparison of reduced fat and reduced carbohydrate hypocaloric diets on intrahepatic fat in overweight and obese human subjects. Hepatology.53(5):1504-14
- ↑ Musso G, Cassader M, Rosina F, Gambino R. Impact of current treatments on liver disease, glucose metabolism and cardiovascular risk in non-alcoholic fatty liver disease (NAFLD): a systematic review and meta-analysis of randomised trials. Diabetologia. 2012;55(4):885-904
- ↑ 55.0 55.1 55.2 55.3 55.4 55.5 55.6 55.7 55.8 55.9 European Association for the Study of the Liver, European Association for the Study of Diabetes, European Association for the Study of Obesity. EASL-EASD-EASO Clinical Practice Guidelines for the Management of Non-Alcoholic Fatty Liver Disease J Hepatol. 2016;64(6):1388-402
- ↑ 56.0 56.1 56.2 56.3 56.4 Plauth M, Bernal W, Dasarathy S, Merli M, Plank LD, Schutz T, et al. ESPEN guideline on clinical nutrition in liver disease. Clin Nutr. 2019
- ↑ Rosqvist F, Iggman D, Kullberg J, Cedernaes J, Johansson HE, Larsson A, et al. Overfeeding polyunsaturated and saturated fat causes distinct effects on liver and visceral fat accumulation in humans. Diabetes. 2014;63(7):2356-68
- ↑ Rosqvist F, Kullberg J, Stahlman M, Cedernaes J, Heurling K, Johansson HE, et al. Overeating Saturated Fat Promotes Fatty Liver and Ceramides Compared With Polyunsaturated Fat: A Randomized Trial. J Clin Endocrinol Metab. 2019;104(12):6207-19
- ↑ Bjermo H, Iggman D, Kullberg J, Dahlman I, Johansson L, Persson L, et al. Effects of n-6 PUFAs compared with SFAs on liver fat, lipoproteins, and inflammation in abdominal obesity: a randomized controlled trial. Am J Clin Nutr. 2012;95(5):1003-12
- ↑ Luukkonen PK, Sadevirta S, Zhou Y, Kayser B, Ali A, Ahonen L, et al. Saturated Fat Is More Metabolically Harmful for the Human Liver Than Unsaturated Fat or Simple Sugars. Diabetes Care. 2018;41(8):1732-9
- ↑ 61.0 61.1 61.2 Zelber-Sagi S, Nitzan-Kaluski D, Goldsmith R, Webb M, Blendis L, Halpern Z, et al. Long term nutritional intake and the risk for non-alcoholic fatty liver disease (NAFLD): a population based study. J Hepatol. 2007;47(5):711-7
- ↑ Abdelmalek MF, Suzuki A, Guy C, Unalp-Arida A, Colvin R, Johnson RJ, et al. Increased fructose consumption is associated with fibrosis severity in patients with nonalcoholic fatty liver disease. Hepatology. 2010;51(6):1961-71
- ↑ Mosca A, Nobili V, De Vito R, Crudele A, Scorletti E, Villani A, et al. Serum uric acid concentrations and fructose consumption are independently associated with NASH in children and adolescents. J Hepatol. 2017;66(5):1031-6
- ↑ Ouyang X, Cirillo P, Sautin Y, McCall S, Bruchette JL, Diehl AM, et al. Fructose consumption as a risk factor for non-alcoholic fatty liver disease. J Hepatol. 2008;48(6):993-9
- ↑ Assy N, Nasser G, Kamayse I, Nseir W, Beniashvili Z, Djibre A, et al. Soft drink consumption linked with fatty liver in the absence of traditional risk factors. Can J Gastroenterol. 2008;22(10):811 -6
- ↑ Abid A, Taha O, Nseir W, Farah R, Grosovski M, Assy N. Soft drink consumption is associated with fatty liver disease indepen- dent of metabolic syndrome. J Hepatol. 2009;51 (5):918-24
- ↑ Ma J, Fox CS, Jacques PF, Speliotes EK, Hoffmann U, Smith CE, et al. Sugar-sweetened beverage, diet soda, and fatty liver disease in the Framingham Heart Study cohorts. J Hepatol. 2015;63(2):462-9
- ↑ Maersk M, Belza A, Stodkilde-Jorgensen H, Ringgaard S, Chabanova E, Thomsen H, et al. Sucrose-sweetened beverag- es increase fat storage in the liver, muscle, and visceral fat depot: a 6-mo randomized intervention study. Am J Clin Nutr. 2012;95(2):283-9
- ↑ Schwarz JM, Noworolski SM, Erkin-Cakmak A, Korn NJ, Wen MJ, Tai VW, et al. Effects of Dietary Fructose Restriction on Liver Fat, De Novo Lipogenesis, and Insulin Kinetics in Children With Obesity. Gastroenterology. 2017,T53(3):743-52
- ↑ Schwimmer JB, Ugalde-Nicalo P, Welsh JA, Angeles J E, Cordero M, Harlow KE, et al. Effect of a Low Free Sugar Diet vs Usual Diet on Nonalcoholic Fatty Liver Disease in Adolescent Boys: A Randomized Clinical Trial. Jama. 2019;321(3):256-65
- ↑ Geurtsen ML, Santos S, Gaillard R, Felix JF, Jaddoe VWV. Associations Between Intake of Sugar-Containing Beverages in Infancy With Liver Fat Accumulation at School Age. Hepatology. 2020
- ↑ Kechagias S, Ernersson A, Dahlqvist O, Lundberg P, Lindstrom T, Nystrom FH. Fast-food-based hyper-alimentation can induce rapid and profound elevation of serum alanine aminotransferase in healthy subjects. Gut. 2008;57(5):649-54
- ↑ Alferink LJ, Kiefte-de Jong JC, Erler NS, Veldt BJ, Schoufour JD, de Knegt RJ, et al. Association of dietary macronutrient composition and non-alcoholic fatty liver disease in an ageing population: the Rotterdam Study. Gut. 2018
- ↑ Baratta F, Pastori D, Polimeni L, Bucci T, Ceci F, Calabrese C, et al. Adherence to Mediterranean Diet and Non-Alcoholic Fatty Liver Disease: Effect on Insulin Resistance. Am J Gastroenterol. 2017;112(12):1832-9
- ↑ Zelber-Sagi S, Ivancovsky-Wajcman D, Fliss Isakov N, Webb M, Orenstein D, Shibolet O, et al. High red and processed meat consumption is associated with non-alcoholic fatty liver disease and insulin resistance. J Hepatol. 2018;68(6):1239-46
- ↑ Mozaffarian D. Dietary and Policy Priorities for Cardiovascular Disease, Diabetes, and Obesity: A Comprehensive Review. Circulation. 2016,T33(2):187-225
- ↑ Takahashi F, Hashimoto Y, Kawano R, Kaji A, Sakai R, Kawate Y, et al. Eating Fast Is Associated with Nonalcoholic Fatty Liver Disease in Men But Not in Women with Type 2 Diabetes: A Cross-Sectional Study. Nutrients. 2020,8)12־)
- ↑ Maskarinec G, Lim U, Jacobs S, Monroe KR, Ernst T, Buchthal SD, et al. Diet Quality in Midadulthood Predicts Visceral Adi- posity and Liver Fatness in Older Ages: The Multiethnic Cohort Study. Obesity (Silver Spring). 2017;25(8):1442-50
- ↑ Ma J, Hennein R, Liu C, Long MT, Hoffmann U, Jacques PF, et al. Improved Diet Quality Associates With Reduction in Liver Fat, Particularly in Individuals With High Genetic Risk Scores for Nonalcoholic Fatty Liver Disease. Gastroenterology. 2018;155(1 ):107-17
- ↑ Gepner Y, Shelef I, Schwarzfuchs D, Zelicha H, Tene L, Yaskolka Meir A, et al. Effect of Distinct Lifestyle Interventions on Mobilization of Fat Storage Pools: CENTRAL Magnetic Resonance Imaging Randomized Controlled Trial. Circulation. 2018;137(11):1143-57
- ↑ Grosso G, Mistretta A, Frigiola A, Gruttadauria S, Biondi A, Basile F, et al. Mediterranean diet and cardiovascular risk factors: a systematic review. Crit Rev Food Sci Nutr. 2014;54(5):593-610
- ↑ Hussein O, Grosovski M, Lasri E, Svalb S, Ravid U, Assy N. Monounsaturated fat decreases hepatic lipid content in non-alco- holic fatty liver disease in rats. World journal of gastroenterology: WJG. 2007;13(3):361-8
- ↑ Bozzetto L, Prinster A, Annuzzi G, Costagliola L, Mangione A, Vitelli A, et al. Liver fat is reduced by an isoenergetic MUFA diet in a controlled randomized study in type 2 diabetic patients. Diabetes Care. 2012;35(7):1429-35
- ↑ Trovato FM, Catalano D, Martines GF, Pace P, Trovato GM. Mediterranean diet and non-alcoholic fatty liver disease.: The need of extended and comprehensive interventions. Clin Nutr. 2014
- ↑ Ryan MC, Itsiopoulos C, Thodis T, Ward G, Trost N, Hofferberth S, et al. The Mediterranean diet improves hepatic steatosis and insulin sensitivity in individuals with non-alcoholic fatty liver disease. J Hepatol. 20l3;59(1):138-43
- ↑ Alferink LJM, Erler NS, de Knegt RJ, Janssen HLA, Metselaar HJ, Darwish Murad S, et al. Adherence to a plant-based, high-fi- bre dietary pattern is related to regression of non-alcoholic fatty liver disease in an elderly population. Eur J Epidemiol. 2020
- ↑ Godos J, Federico A, Dallio M, Scazzina F. Mediterranean diet and nonalcoholic fatty liver disease: molecular mechanisms of protection. Int J Food Sci Nutr. 2017;68(1 ):18-27
- ↑ Ivancovsky-Wajcman D, Fliss-lsakov N, Salomone F, Webb M, Shibolet 0, Kariv R, et al. Dietary vitamin E and C intake is inversely associated with the severity of nonalcoholic fatty liver disease. Digestive and Liver Disease. 20l9;51(12):l698-705
- ↑ Salomone F l-WD, Fliss-lsakov N, Webb M, Grosso G, Godos J, Galvano F, Shibolet O, Kariv R, Zelber-Sagi S.. Higher phenolic acid intake independently associates with lower prevalence of insulin resistance and non-alcoholic fatty liver disease. JHEP Reports. 2020
- ↑ Zelber-Sagi S, Nitzan-Kaluski D, Goldsmith R, Webb M, Zvibel I, Goldiner I, et al. Role of leisure-time physical activity in nonalcoholic fatty liver disease: a population-based study. Hepatology. 2008;48(6):1791-8
- ↑ Kistler KD, Brunt EM, Clark JM, Diehl AM, Sallis JF, Schwimmer JB. Physical activity recommendations, exercise intensity, and histological severity of nonalcoholic fatty liver disease. Am J Gastroenterol. 2011;106(3):460-8; quiz 9
- ↑ Kim D, Vazquez-Montesino LM, Li AA, Cholankeril G, Ahmed A. Inadequate Physical Activity and Sedentary Behavior Are Independent Predictors of Nonalcoholic Fatty Liver Disease. Hepatology. 2020;72(5):1556-68
- ↑ Simon TG, Kim MN, Luo X, Yang W, Ma Y, Chong DQ, et al. Physical activity compared to adiposity and risk of liver-related mortality: Results from two prospective, nationwide cohorts. J Hepatol. 2020,•72(6):1062-9
- ↑ Blomdahl J, Nasr P, Ekstedt M, Kechagias S. Moderate alcohol consumption is associated with advanced fibrosis in non-al- coholic fatty liver disease and shows a synergistic effect with type 2 diabetes mellitus. Metabolism. 2021;! 15:154439
- ↑ 95.0 95.1 Aberg F, Puukka P, Salomaa V, Mannisto S, Lundqvist A, Valsta L, et al. Risks of Light and Moderate Alcohol Use in Fatty Liver Disease: Follow-Up of Population Cohorts. Hepatology. 2020;71(3):835-48
- ↑ 96.0 96.1 Kashiwagi K, Yamaguchi A, Shiba S, Taniki N, Inoue N, Takaishi H, et al. Moderate alcohol consumption is not associated with subclinical cardiovascular damage but with hepatic fibrosis in non-alcoholic fatty liver disease. Alcohol. 2020;89:1-7
- ↑ Long MT, Massaro JM, Hoffmann U, Benjamin EJ, Naimi TS. Alcohol Use Is Associated With Hepatic Steatosis Among Per- sons With Presumed Nonalcoholic Fatty Liver Disease. Clin Gastroenterol Hepatol. 2020,18(8):!831-41 e5
- ↑ Chang Y, Ryu S, Kim Y, Cho YK, Sung E, Kim HN, et al. Low levels of alcohol consumption, obesity, and development of fatty liver with and without evidence of advanced fibrosis. Hepatology. 2020,71 (3):861 -73
- ↑ 99.0 99.1 Chang Y, Cho YK, Kim Y, Sung E, Ahn J, Jung HS, et al. Nonheavy Drinking and Worsening of Noninvasive Fibrosis Markers in Nonalcoholic Fatty Liver Disease: A Cohort Study. Hepatology. 2019;69(1):64-75
- ↑ Yamada K, Mizukoshi E, Seike T, Horii R, Kitahara M, Sunagozaka H, et al. Light alcohol consumption has the potential to suppress hepatocellular injury and liver fibrosis in non-alcoholic fatty liver disease. PL0S One. 2018;l3(1):e0191026
- ↑ 101.0 101.1 Aberg F, Helenius-Hietala J, Puukka P, Farkkila M, Jula A. Interaction between alcohol consumption and metabolic syn- drome in predicting severe liver disease in the general population. Hepatology. 2018;67(6):2141-9
- ↑ Hagstrom H, Nasr P, Ekstedt M, Kechagias S, Onnerhag K, Nilsson E, et al. Low to moderate lifetime alcohol consumption is associated with less advanced stages of fibrosis in non-alcoholic fatty liver disease. Scandinavian journal of gastroenterology. 2017;52(2):159-65
- ↑ VanWagner LB, Ning H, Allen NB, Ajmera V, Lewis CE, Carr JJ, et al. Alcohol use and cardiovascular disease risk in patients with nonalcoholic fatty liver disease. Gastroenterology. 2017;153(5):1260-72. e3
- ↑ Moriya A, Iwasaki Y, Ohguchi S, Kayashima E, MitsumuneT, Taniguchi H, et al. Roles of alcohol consumption in fatty liver: a longitudinal study. Journal of Hepatology. 2015;62(4):921-7
- ↑ 105.0 105.1 Dunn W, Sanyal AJ, Brunt EM, Unalp-Arida A, Donohue M, McCullough AJ, et al. Modest alcohol consumption is associated with decreased prevalence of steatohepatitis in patients with non-alcoholic fatty liver disease (NAFLD). Journal of Hepatology. 2012,•57(2)384-91
- ↑ 106.0 106.1 106.2 Ascha MS, Hanouneh IA, Lopez R, Tamimi TA-R, Feldstein AF, Zein NN. The incidence and risk factors of hepatocellular carcinoma in patients with nonalcoholic steatohepatitis. Hepatology. 2010;51(6):1972-8
- ↑ Ibanez J, Izquierdo M, Arguelles I, Forga L, Larrion JL, Garcia-Unciti M, et al. Twice-weekly progressive resistance training decreases abdominal fat and improves insulin sensitivity in older men with type 2 diabetes. Diabetes Care. 2005;28(3):662-7
- ↑ Johnson NA, Sachinwalla T, Walton DW, Smith K, Armstrong A, Thompson MW, et al. Aerobic exercise training reduces hepatic and visceral lipids in obese individuals without weight loss. Hepatology. 2009;50(4):1105-12
- ↑ Sullivan S, Kirk EP, Mittendorfer B, Patterson BW, Klein S. Randomized trial of exercise effect on intrahepatic triglyceride content and lipid kinetics in nonalcoholic fatty liver disease. Hepatology.55(6):1738-45
- ↑ van der Heijden GJ, Wang ZJ, Chu ZD, Sauer PJ, Haymond MW, Rodriguez LM, et al. A 12-week aerobic exercise program reduces hepatic fat accumulation and insulin resistance in obese, Hispanic adolescents. Obesity (Silver Spring).! 8(2)384-90
- ↑ Finucane FM, Sharp SJ, Purslow LR, Horton K, Horton J, Savage DB, et al. The effects of aerobic exercise on metabolic risk, insulin sensitivity and intrahepatic lipid in healthy older people from the Hertfordshire Cohort Study: a randomised controlled trial. Diabetologia.53(4):624-31
- ↑ Hallsworth K, Fattakhova G, Hollingsworth KG, Thoma C, Moore S, Taylor R, et al. Resistance exercise reduces liver fat and its mediators in non-alcoholic fatty liver disease independent of weight loss. Gut.60(9):1278-83
- ↑ Zelber-Sagi S, Buch A, Yeshua H, Vaisman N, Webb M, Harari G, et al. Effect of resistance training on non-alcoholic fatty-liv- er disease a randomized-clinical trial. World journal of gastroenterology: WJG. 2014;20(l5):4382-92
- ↑ Bacchi E, Negri C,Targher G, Faccioli N, Lanza M, Zoppini G, etal. Both resistance training and aerobictraining reduce hepatic fat content in type 2 diabetic subjects with nonalcoholic fatty liver disease (the RAED2 Randomized Trial). Hepatology. 2013;58(4):1287-95
- ↑ Mikolasevic I, Domislovic V, Filipec Kanizaj T, Radic-Kristo D, Krznaric Z, Milovanovic T, et al. Relationship between coffee consumption, sleep duration and smoking status with elastographic parameters of liver steatosis and fibrosis; controlled attenuation parameter and liver stiffness measurements. Int J Clin Pract. 2020:el3770
- ↑ Zhang Y, Liu Z, Choudhury T, Cornelis MC, Liu W. Habitual coffee intake and risk for nonalcoholic fatty liver disease: a two-sample Mendelian randomization study. Eur J Nutr. 2020
- ↑ Soleimani D, Ranjbar G, Rezvani R, Goshayeshi L, Razmpour F, Nematy M. Dietary patterns in relation to hepatic fibrosis among patients with nonalcoholic fatty liver disease. Diabetes Metab Syndr Obes. 2019;12:315-24
- ↑ Veronese N, Notarnicola M, Cisternino AM, Reddavide R, Inguaggiato R, Guerra V, et al. Coffee Intake and Liver Steatosis: A Population Study in a Mediterranean Area. Nutrients. 2018;10(1)
- ↑ Chen YP, Lu FB, Hu YB, Xu LM, Zheng MH, Hu ED. A systematic review and a dose-response meta-analysis of coffee dose and nonalcoholic fatty liver disease. Clin Nutr. 2019;38(6):2552-7
- ↑ Wijarnpreecha K, Thongprayoon C, Ungprasert P. Coffee consumption and risk of nonalcoholic fatty liver disease: a sys- tematic reviewand meta-analysis. Eur J Gastroenterol Hepatol. 2017;29(2):e8-e12
- ↑ Alferink LJ, Fittipaldi J, Kiefte-de Jong JC, Taimr P, Hansen BE, Metselaar HJ, et al. Coffee and herbal tea consumption is associated with lower liver stiffness in the general population: The Rotterdam study. Journal of hepatology. 2017;67(2):339-48
- ↑ Setiawan VW, Parcel J, Wei P, Stram DO, Noureddin N, Lu SC, et al. Coffee drinking and alcoholic and nonalcoholic fatty liver diseases and viral hepatitis in the multiethnic cohort. Clinical Gastroenterology and Hepatology. 2017;15(8):1305-7
- ↑ Imatoh T, Kamimura S, Miyazaki M. Coffee but not green tea consumption is associated with prevalence and severity of hepatic steatosis: the impacton leptin level. European journal of clinical nutrition. 2015;69(9):1023-7
- ↑ 124.0 124.1 124.2 Zelber-Sagi S, Salomone F, Webb M, Lotan R, Yeshua H, Halpern Z, et al. Coffee consumption and nonalcoholic fatty liver onset: a prospective study in the general population. Translational research : the journal of laboratory and clinical medicine. 2015;165(3):428-36
- ↑ 125.0 125.1 Bambha K, Wilson LA, Unalp A, Loomba R, Neuschwander-Tetri BA, Brunt EM, et al. Coffee consumption in NAFLD patients with lower insulin resistance is associated with lower risk of severe fibrosis. Liver Int. 2013
- ↑ 126.0 126.1 Anty R, Marjoux S, lannelli A, Patouraux S, Schneck AS, Bonnafous S, et al. Regular coffee but not espresso drinking is protective against fibrosis in a cohort mainly composed of morbidly obese European women with NAFLD undergoing bariatric surgery. J Hepatol. 2012;57(5):1090-6
- ↑ Birerdinc A, Stepanova M, Pawloski L, Younossi Z. Caffeine is protective in patients with non-alcoholic fatty liver disease. Alimentary pharmacology & therapeutics. 2012;35(l):76-82
- ↑ 128.0 128.1 Molloy JW, Calcagno CJ, Williams CD, Jones FJ, Torres DM, Harrison SA. Association of coffee and caffeine consumption with fatty liver disease, nonalcoholic steatohepatitis, and degree of hepatic fibrosis. Hepatology. 2012;55(2):429-36
- ↑ Funatsu K, Yamashita T, Nakamura H. Coffee consumption is associated with a lower incidence of fatty liver in middle-aged men. Journal of Health Science. 2011;57(5):406-13
- ↑ 130.0 130.1 Catalano D, Martines GF, Tonzuso A, Pirri C, Trovato FM, Trovato GM. Protective role of coffee in non-alcoholic fatty liver disease (NAFLD). Digestive diseases and sciences. 2010;55(11):3200-6
- ↑ Keating SE, Hackett DA, Parker HM, O'Connor HT, Gerofi JA, Sainsbury A, et al. Effect of aerobic exercise training dose on liver fat and visceral adiposity. J Hepatol. 2015;63(l):174-82
- ↑ Ryu S, Chang Y, Jung HS, Yun KE, Kwon MJ, Choi Y, et al. Relationship of sitting time and physical activity with non-alcohol- ic fatty liver disease. J Hepatol. 2015;63(5):122937
- ↑ Moradi Kelardeh B, Rahmati-Ahmadabad S, Farzanegi P, Helalizadeh M, Azarbayjani MA. Effects of non-linear resistance training and curcumin supplementation on the liver biochemical markers levels and structure in older women with non-alco- holic fatty liver disease. J Body w Mov Ther. 2020;24(3):l54-60
- ↑ Ghamarchehreh ME, Shamsoddini A, Alavian SM. Investigating the impact of eight weeks of aerobic and resistance training on blood lipid profile in elderly with non-alcoholic fatty liver disease: a randomized clinical trial. Gastroenterology and hepatology from bed to bench. 2019;12(3):!90
- ↑ Keating SE, Hackett DA, George J, Johnson NA. Exercise and non-alcoholic fatty liver disease: a systematic review and meta-analysis. Journal of hepatology. 2012;57(1):157-66
- ↑ Wang S-t, Zheng J, Peng H-w, Cai X-l, Pan X-t, Li H-q, et al. Physical activity intervention for non-diabetic patients with non-alcoholic fatty liver disease: a meta-analysis of randomized controlled trials. BMC gastroenterology. 2020;20(1):1-l2
- ↑ O'Gorman P, Naimimohasses S, Monaghan A, Kennedy M, Melo AM, Ni Fhloinn D, et al. Improvement in histological end- points of MAFLD following a 12-week aerobic exercise intervention. Aliment Pharmacol Ther. 2020;52(8):l387-98
- ↑ Chang SH, Stoll CR, Song J, Varela JE, Eagon CJ, Colditz GA. The effectiveness and risks of bariatric surgery: an updated systematic review and meta-analysis, 2003-2012. JAMA surgery. 2014;149(3):275-87
- ↑ Sjostrom L, Peltonen M, Jacobson P, Ahlin S, Andersson-Assarsson J, Anveden A, et al. Association of bariatric surgery with long-term remission of type 2 diabetes and with microvascular and macrovascular complications. JAMA. 2014,311 (22):2297- 304
- ↑ Lassailly G, Caiazzo R, Buob D, Pigeyre M, Verkindt H, Labreuche J, et al. Bariatric Surgery Reduces Features of Nonalcoholic Steatohepatitis in Morbidly Obese Patients. Gastroenterology. 2015;149(2):379-88; quiz e15-6
- ↑ Lassailly G, Caiazzo R, Ntandja-Wandji LC, Gnemmi V, Baud G, Verkindt H, et al. Bariatric Surgery Provides Long-term Reso- lution of Nonalcoholic Steatohepatitis and Regression of Fibrosis. Gastroenterology. 2020;159(4):l290-301 e5
- ↑ Bazerbachi F, Vargas EJ, Rizk M, Maselli DB, Mounajjed T, Venkatesh SK, et al. Intragastric Balloon Placement Induces Significant Metabolic and Histologic Improvement in Patients With Nonalcoholic Steatohepatitis. Clin Gastroenterol Hepatol. 2021;l9(1):146-54e4
- ↑ Salomone F, Current! W, Magri G, Boskoski I, Zelber-Sagi S, Galvano F. Effects of intragastric balloon in patients with nonal- coholic fatty liver disease and advanced fibrosis. Liver Int. 2021
- ↑ Hajifathalian K, Mehta A, Ang B, Skaf D, Shah SL, Saumoy M, etal. Improvement in insulin resistance and estimated hepaticsteatosis and fibrosis after endoscopic sleeve gastroplasty. Gastrointest Endosc. 2021;93(5):11l0-8
- ↑ Sookoian S, Castano GO, Pirola CJ. Modest alcohol consumption decreases the risk of non-alcoholic fatty liver disease: a meta-analysis of 43 175 individuals. Gut. 2014;63(3):530-2
- ↑ Wong VWS, Chu WCW, Wong GLH, Chan RSM, Chim AML, Ong A, et al. Prevalence of non-alcoholic fatty liver disease and advanced fibrosis in Hong Kong Chinese: a population study using proton-magnetic resonance spectroscopy and transient elastography. Gut. 2011;61(3):409-15
- ↑ Gunji T, Matsuhashi N, Sato H, Fujibayashi K, Okumura M, Sasabe N, et al. Light and moderate alcohol consumption signifi- cantly reduces the prevalence of fatty liver in the Japanese male population. Am J Gastroenterol. 2009;104(9):2189-95
- ↑ Pais R, Lebray P, Rousseau G, Charlotte F, Esselma G, Savier E, et al. Nonalcoholic Fatty Liver Disease Increases the Risk of Hepatocellular Carcinoma in Patients With Alcohol-Associated Cirrhosis Awaiting Liver Transplants. Clin Gastroenterol Hepatol. 2014
- ↑ Bellentani S, Saccoccio G, Masutti F, Croce LS, Brandi G, Sasso F, et al. Prevalence of and risk factors for hepatic steatosis in Northern Italy. Ann Intern Med. 2000;132(2):112-7
- ↑ Setiawan VW, Wilkens LR, Lu SC, Hernandez BY, Le Marchand L, Henderson BE. Association of coffee intake with reduced incidence of liver cancer and death from chronic liver disease in the US multiethnic cohort. Gastroenterology. 2015;148(1):118- 25; quize15
- ↑ Kennedy OJ, Fallowfield JA, Poole R, Hayes PC, Parkes J, Roderick PJ. All coffee types decrease the risk of adverse clinical outcomes in chronic liver disease: a UK Biobank study. BMC Public Health. 2021 ;21 (l):970
- ↑ Godos J, Pluchinotta FR, Marventano S, Buscemi S, Li Volti G, Galvano F, et al. Coffee components and cardiovascular risk: beneficial and detrimental effects. Int J Food Sci Nutr. 2014;65(8):925-36
- ↑ Vitaglione P, Morisco F, Mazzone G, Amoruso DC, Ribecco MT, Romano A, et al. Coffee reduces liver damage in a rat model of steatohepatitis: the underlying mechanisms and the role of polyphenols and melanoidins. Hepatology. 2010;52(5):1652-61
- ↑ Salomone F, Li Volti G, Vitaglione P, Morisco F, Fogliano V, Zappala A, et al. Coffee enhances the expression of chaperones and antioxidant proteins in rats with nonalcoholic fatty liver disease. Translational research : the journal of laboratory and clinical medicine. 2013
- ↑ Loomba R, Lutchman G, Kleiner DE, Ricks M, Feld JJ, Borg BB, et al. Clinical trial: pilot study of metformin for the treatment of non-alcoholic steatohepatitis. Aliment Pharmacol Ther. 2009;29(2):172-82
- ↑ Lavine JE, Schwimmer JB, Van Natta ML, Molleston JP, Murray KF, Rosenthal P, et al. Effect of vitamin E or metformin for treatment of nonalcoholic fatty liver disease in children and adolescents: the TONIC randomized controlled trial. Jama. 2011;305(16):1659-68
- ↑ Bugianesi E, Gentilcore E, Manini R, Natale S, Vanni E, Villanova N, et al. A randomized controlled trial of metformin versus vitamin E or prescriptive diet in nonalcoholic fatty liver disease. Am J Gastroenterol. 2005;100(5):1082-90
- ↑ Haukeland JW, Konopski Z, Eggesbo HB, von Volkmann HL, Raschpichler G, Bjoro K, et al. Metformin in patients with non-alcoholic fatty liver disease: a randomized, controlled trial. Scand J Gastroenterol. 2009;44(7):853-60
- ↑ Zhang X, Harmsen WS, Mettler TA, Kim WR, Roberts RO, Therneau TM, et al. Continuation of metformin use after a diagnosis of cirrhosis significantly improves survival of patients with diabetes. Hepatology. 2014;60(6):2008-16
- ↑ Bhalla K, Hwang BJ, Dewi RE,Twaddel W, Goloubeva OG, Wong KK, et al. Metformin prevents liver tumorigenesis by inhibiting pathways driving hepatic lipogenesis. Cancer Prev Res (Phila). 2012;5(4):544-52
- ↑ Zhang ZJ, Zheng ZJ, Shi R, Su Q, Jiang Q, Kip KE. Metformin for liver cancer prevention in patients with type 2 diabetes: a systematic review and meta-analysis. J Clin Endocrinol Metab. 2012;97(7):2347-53
- ↑ Boettcher E, Csako G, Pucino F, Wesley R, Loomba R. Meta-analysis: pioglitazone improves liver histology and fibrosis in patients with non-alcoholic steatohepatitis. Aliment Pharmacol Ther. 2012;35(1 ):66-75
- ↑ Ratziu V, Giral P, Jacqueminet S, Charlotte F, Hartemann-Heurtier A, Serfaty L, et al. Rosiglitazone for nonalcoholic steato- hepatitis: one-year results of the randomized placebo-controlled Fatty Liver Improvement with Rosiglitazone Therapy (FLIRT) Trial. Gastroenterology. 2008;135(1):100-10
- ↑ Aithal GP, Thomas JA, Kaye PV, Lawson A, Ryder SD, Spendlove I, et al. Randomized, placebo-controlled trial of pioglita- zone in nondiabetic subjects with nonalcoholic steatohepatitis. Gastroenterology. 2008;135(4):1176-84
- ↑ Cusi K, Orsak B, Bril F, Lomonaco R, Hecht J, Ortiz-Lopez C, et al. Long-Term Pioglitazone Treatment for Patients With Nonal- coholic Steatohepatitis and Prediabetes or Type 2 Diabetes Mellitus: A Randomized Trial. Ann Intern Med. 2016;165(5):305-15
- ↑ Belfort R, Harrison SA, Brown K, Darland C, Finch J, Hardies J, et al. A placebo-controlled trial of pioglitazone in subjects with nonalcoholic steatohepatitis. N Engl J Med. 2006;355(22):2297-307
- ↑ 167.0 167.1 Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et al. Pioglitazone, vitamin E, or placebo for nonal- coholic steatohepatitis. N Engl J Med. 2010;362(18):1675-85
- ↑ Chalasani N, Teal E, Hall SD. Effect of rosiglitazone on serum liver biochemistries in diabetic patients with normal and elevated baseline liver enzymes. Am J Gastroenterol. 2005;100(6):1317-21
- ↑ Iwasaki T, Yoneda M, Inamori M, Shirakawa J, Higurashi T, Maeda S, et al. Sitagliptin as a novel treatment agent for non-al- coholic Fatty liver disease patients with type 2 diabetes mellitus. Hepato-gastroenterology. 2011;58(112):2103-5
- ↑ Macauley M, Hollingsworth KG, Smith FE, Thelwall PE, Al-Mrabeh A, Schweizer A, et al. Effect of vildagliptin on hepatic steatosis. The Journal of Clinical Endocrinology & Metabolism. 2015;100(4):1578-85
- ↑ Cui J, Philo L, Nguyen P, Hofflich H, Hernandez C, Bettencourt R, et al. Sitagliptin vs. placebo for non-alcoholic fatty liver disease: a randomized controlled trial. Journal of hepatology. 2016;65(2):369-76
- ↑ Joy TR, McKenzie CA, Tirona RG, Summers K, Seney S, Chakrabarti S, et al. Sitagliptin in patients with non-alcoholic steato- hepatitis: a randomized, placebo-controlled trial. World journal of gastroenterology. 2017;23(1):141
- ↑ Marso SP, Daniels GH, Brown-Frandsen K, Kristensen P, Mann JF, Nauck MA, et al. Liraglutide and cardiovascular outcomes in type 2 diabetes. New England Journal of Medicine. 2016;375(4):311-22
- ↑ Marso SP, Bain SC, Consoli A, Eliaschewitz FG, Jodar E, Leiter LA, et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med. 2016;375:1834-44
- ↑ Hernandez AF, Green JB, Janmohamed S, D'Agostino Sr RB, Granger CB, Jones NP, et al. Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double-blind, randomised place- bo-controlled trial. The Lancet. 2018,392(10157):! 519-29
- ↑ Neal B, Perkovic V, Mahaffey KW, De Zeeuw D, Fulcher G, Erondu N, et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes. New England Journal of Medicine. 2017;377(7):644-57
- ↑ Mann JF, 0rsted DD, Brown-Frandsen K, Marso SP, Poulter NR, Rasmussen S, et al. Liraglutide and renal outcomes in type 2 diabetes. New England Journal of Medicine. 2017;377(9):839-48
- ↑ McGuire DK, Shih WJ, Cosentino F, Charbonnel B, Cherney DZ, Dagogo-Jack S, et al. Association of SGLT2 inhibitors with cardiovascular and kidney outcomes in patients with type 2 diabetes: a meta-analysis. JAMA cardiology. 2021;6(2):148-58
- ↑ Gupta NA, Mells J, Dunham RM, Grakoui A, Handy J, Saxena NK, et al. Glucagon-like peptide-1 receptor is present on hu-man hepatocytes and has a direct role in decreasing hepatic steatosis in vitro by modulating elements of the insulin signaling pathway. Hepatology. 2010;51(5):1584-92
- ↑ Mantovani A, Petracca G, Beatrice G, Csermely A, Lonardo A, Targher G. Glucagon-Like Peptide-1 receptor agonists for treatment of nonalcoholic fatty liver disease and nonalcoholic steatohepatitis: an Updated Meta-Analysis of randomized controlled trials. Metabolites. 2021;11(2):73
- ↑ Armstrong MJ, Houlihan DD, Rowe IA, Clausen WH, Elbrond B, Gough SC, et al. Safety and efficacy of liraglutide in patients with type 2 diabetes and elevated liver enzymes: individual patient data meta-analysis of the LEAD program. Aliment Pharma- col Then 2013;37(2):234-42
- ↑ Armstrong MJ, Gaunt P, Aithal GP, Barton D, Hull D, Parker R, et al. Liraglutide safety and efficacy in patients with non-alcoholic steatohepatitis (LEAN): a multicentre, double-blind, randomised, placebo-controlled phase 2 study. Lancet. 2016;387(10019):679-90
- ↑ Klonoff DC, Buse JB, Nielsen LL, Guan X, Bowlus CL, Holcombe JH, et al. Exenatide effects on diabetes, obesity, cardiovas- cular risk factors and hepatic biomarkers in patients with type 2 diabetes treated for at least 3 years. Current medical research and opinion. 2008;24(1):275-86
- ↑ Newsome PN, Buchholtz K, Cusi K, Linder M, Okanoue T, Ratziu V, et al. A placebo-controlled trial of subcutaneous sema- glutide in nonalcoholic steatohepatitis. New England Journal of Medicine. 2021;384(12):1113-24
- ↑ Shao N, Kuang HY, Hao M, Gao XY, Lin WJ, Zou W. Effects of exenatide on obesity and NAFLD with elevated liver enzymes in patients with type 2 diabetes. Diabetes/metabolism research and reviews. 2014
- ↑ Fan H, Pan Q, Xu Y, Yang X. Exenatide improves type 2 diabetes concomitant with non-alcoholic fatty liver disease. Arquiv- os brasileiros de endocrinologia e metabologia. 2013;57(9):702-8
- ↑ Sathyanarayana P, Jogi M, Muthupillai R, Krishnamurthy R, Samson SL, Bajaj M. Effects of combined exenatide and pioglita- zone therapy on hepatic fat content in type 2 diabetes. Obesity (Silver Spring). 2011;19(12):2310-5
- ↑ Nishimura N, Kitade M, Noguchi R, Namisaki T, Moriya K, Takeda K, et al. IpragIiflozin, a sodium-glucose cotransporter 2 inhibitor, ameliorates the development of liver fibrosis in diabetic Otsuka Long-Evans Tokushima fatty rats. J Gastroenterol. 2016;51(12):1141-9
- ↑ Jojima T, Tomotsune T, Iijima T, Akimoto K, Suzuki K, Aso Y. Empagliflozin (an SGLT2 inhibitor), alone or in combination with linagliptin (a DPP-4 inhibitor), prevents steatohepatitis in a novel mouse model of non-alcoholic steatohepatitis and diabetes. Diabetol Metab Syndr. 2016;8:45
- ↑ Ito D, Shimizu S, Inoue K, Saito D, Yanagisawa M, Inukai K, et al. Comparison of Ipragliflozin and Pioglitazone Effects on Nonalcoholic Fatty Liver Disease in Patients With Type 2 Diabetes: A Randomized, 24-Week, Open-Label, Active-Controlled Trial. Diabetes Care. 2017;40(10):1364-72
- ↑ Kuchay MS, Krishan S, Mishra SK, Farooqui KJ, Singh MK, Wasir JS, et al. Effect of Empagliflozin on Liver Fat in Patients With Type 2 Diabetes and Nonalcoholic Fatty Liver Disease: A Randomized Controlled Trial (E-LIFTTrial). Diabetes Care. 2018;41(8):1801-8
- ↑ Kahl S, Gancheva S, StraBburger K, Herder C, Machann J, Katsuyama H, et al. Empagliflozin effectively lowers liver fat content in well-controlled type 2 diabetes: a randomized, double-blind, phase 4, placebo-controlled trial. Diabetes Care. 2020;43(2):298-305
- ↑ Neuschwander-Tetri BA, Loomba R, Sanyal AJ, Lavine JE, Van Natta ML, Abdelmalek MF, et al. Farnesoid X nuclear receptor ligand obeticholic acid for non-cirrhotic, non-alcoholic steatohepatitis (FLINT): a multicentre, randomised, placebo-controlled trial. Lancet. 2015;385(9972):956-65
- ↑ Younossi ZM, Ratziu V, Loomba R, Rinella M, Anstee QM, Goodman Z, et al. Obeticholic acid for the treatment of non-alcoholic steatohepatitis: interim analysis from a multicentre, randomised, placebo-controlled phase 3 trial. Lancet. 2019;394(10215):2184-96
- ↑ Harrison SA, Rinella ME, Abdelmalek MF, Trotter JF, Paredes AH, Arnold HL, et al. NGM282 for treatment of non-alcoholic steatohepatitis: a multicentre, randomised, double-blind, placebo-controlled, phase 2 trial. Lancet. 2018;391(10126):1174-85
- ↑ Harrison SA, Rossi SJ, Paredes AH, Trotter JF, Bashir MR, Guy CD, et al. NGM282 Improves Liver Fibrosis and Histology in 12 Weeks in Patients With Nonalcoholic Steatohepatitis. Hepatology. 2020,71 (4):1198-212
- ↑ Athyros VG, Tziomalos K, Gossios TD, Griva T, Anagnostis P, Kargiotis K, et al. Safety and efficacy of long-term statin treat- ment for cardiovascular events in patients with coronary heart disease and abnormal liver tests in the Greek Atorvastatin and Coronary Heart Disease Evaluation (GREACE) Study: a post-hoc analysis. Lancet. 2010;376(9756):1916-22
- ↑ Dongiovanni P, Petta S, Mannisto V, Mancina RM, Pipitone R, Karja V, et al. Statin use and non-alcoholic steatohepatitis in at risk individuals. J Hepatol. 2015;63(3):705-12
- ↑ Eslami L, Merat S, Malekzadeh R, Nasseri-Moghaddam S, Aramin H. Statins for non-alcoholic fatty liver disease and non-al- coholic steatohepatitis. The Cochrane database of systematic reviews. 2013;12:CD008623
- ↑ Athyros VG, Alexandrides TK, Bilianou H, Cholongitas E, Doumas M, Ganotakis ES, et al. The use of statins alone, or in com- bination with pioglitazone and other drugs, for the treatment of non-alcoholic fatty liver disease/non-alcoholic steatohepati- tis and related cardiovascular risk. An Expert Panel Statement. Metabolism. 2017;71:17-32
- ↑ Bril F, Biernacki DM, Kalavalapalli S, Lomonaco R, Subbarayan SK, Lai J, et al. Role of Vitamin Efor Nonalcoholic Steatohep- atitis in Patients With Type 2 Diabetes: A Randomized Controlled Trial. Diabetes Care. 2019;42(8):1481-8
- ↑ Bjelakovic G, Nikolova D, Gluud LL, Simonetti RG, Gluud C. Mortality in randomized trials of antioxidant supplements for primary and secondary prevention: systematic review and meta-analysis. Jama. 2007;297(8):842-57
- ↑ Schurks M, Glynn RJ, Rist PM, Tzourio C, Kurth T. Effects of vitamin E on stroke subtypes: meta-analysis of randomised controlled trials. BMJ. 2010;341:c5702
- ↑ Klein EA, Thompson IM, Jr., Tangen CM, Crowley JJ, Lucia MS, Goodman PJ, et al. Vitamin E and the risk of prostate cancer: the Selenium and Vitamin E Cancer Prevention Trial (SELECT). Jama. 2011 ;306(14):1549-56
- ↑ Scorletti E, Bhatia L, McCormick KG, Clough GF, Nash K, Hodson L, et al. Effects of purified eicosapentaenoic and docosa- hexaenoic acids in non-alcoholic fatty liver disease: Results from the *WELCOME study. Hepatology. 2014
- ↑ Sanyal AJ, Abdelmalek MF, Suzuki A, Cummings OW, Chojkier M, Group E-AS. No significant effects of ethyl-eicosapenta- noic acid on histologic features of nonalcoholic steatohepatitis in a phase 2 trial. Gastroenterology. 2014;147(2):377-84 e1
- ↑ Argo CK, Patrie JT, Lackner C, Henry TD, de Lange EE, Weltman AL, et al. Effects of n-3 fish oil on metabolic and histological parameters in NASH: a double-blind, randomized, placebo-controlled trial. Journal of hepatology. 2015;62(1 ):190-7
המידע שבדף זה נכתב על ידי פרופסור שירה זלבר-שגיא, דיאטנית קלינית ואפידמיולוגית, ראש בית הספר לבריאות הציבור, אוניברסיטת חיפה והמכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי
ד"ר חני ישועה, המכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי ושירותי בריאות כללית, מחוז תל-אביב יפו
דנה איבנקובסקי-וכקמן, דוקטורנטית, בית הספר לבריאות הציבור, אוניברסיטת חיפה, והמכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי
ד"ר מאיה מרגלית, המכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי
פרופ׳ אורן שבולת, מנהל המכון למחלות דרכי העיכול והכבד, המרכז הרפואי ת"א ע"ש סוראסקי ואוניברסיטת תל-אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק