יתר לחץ דם אנדוקריני - Endocrine hypertension
הופניתם מהדף יתר לחץ דם אנדוקריני לדף הנוכחי.
יתר לחץ דם - הנחיה קלינית - Hypertension
מאת פרופסור עדי לייבה, ד"ר שוקי לשם, ד"ר סוהיר אסדי, פרופסור אהוד גרוסמן
|
| ||
|---|---|---|
| יתר לחץ דם – אבחנה, טיפול ואיזון פרק 14: יתר לחץ דם אנדוקריני | ||
| ||
| הוועדה המקצועית | האיגוד הישראלי לנפרולוגיה ויתר לחץ דם; החברה ליתר לחץ דם בישראל; האיגוד הישראלי לרפואה פנימית; האיגוד הקרדיולוגי בישראל; האיגוד הישראלי למחלות ילדים; איגוד רופאי המשפחה בישראל; האגודה הישראלית לאנדוקרינולוגיה | |
| עריכה | ד"ר יונית מרקוס ופרופסור נפתלי שטרן | |
| תחום | נפרולוגיה ויתר לחץ דם | |
| תאריך פרסום | ינואר 2019 | |
| הנחיות קליניות מתפרסמות ככלי עזר לרופא/ה ואינן באות במקום שיקול דעתו/ה בכל מצב נתון | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – יתר לחץ דם מערכתי
יתר לחץ דם ראשוני, בו איננו מצליחים לזהות גורם ברור, אחראי על כ-85 אחוזים מכלל מקרי יתר לחץ דם. יתר לחץ דם אנדוקריני, הכולל היפראלדוסטרוניזם ראשוני, פאוכרומוציטומה, תסמונת קושינג, אקרומגליה, הפרעות בתפקודי תריס, היפרפאראתירואידיזם והפרעות מינרלוקורטיקואידיות אחרות (כגון, apparent mineralocorticoid excess, Liddle syndrome), גידול מפריש רנין, מהווה גורם עיקרי ביתר לחץ דם שניוני. מעבר לכך, השמנה וסוכרת, תסמונות אנדוקריניות/ מטבוליות המוניות, הנוכחות בכמחצית האוכלוסייה הבוגרת תורמות אף הן להתפתחות לחץ דם באוכלוסייה הכללית. אבחון נכון של יתר לחץ דם אנדוקריני יאפשר לרופא להציע טיפול ניתוחי שיכול להביא לריפוי, הקלה או בחירה מושכלת בטיפול תרופתי ספציפי שיביא לתגובה מיטבית. בפרק זה לא נדון בגידולים מפרישי רנין או ב-congenital adrenal hyperplasia.
פאוכרומוציטומה ופאראגנגליומה - Pheochromocytoma and paragangliomas - PPGLs
PPGLs הם גידולים נוירואנדוקריניים של תאים כרומפיניים מהמדולה של האדרנל, בדרך כלל מפרישים קטכולאמינים ואז נקראים פאוכרומוציטומה או גנגליונים paravertebral של המערכת הסימפתטית, ואז הם קרויים בשם הכללי פארארגנגליומות. מכיוון שמקור התאים דומה, ומוטציות מסוימות עלולות להביא להתפתחות פאוכרומוציטומות או פאראגנגליומות באותו הפרט או בבני אותה משפחה, תסמונות אלה נכרכות עתה יחד תחת הכותרת תסמונות הפאוכרומוציטומה-פאראגנגליומה או PPGLs. פאראגנגליומות המתפתחות בבסיס הגולגולת והצוואר בדרך כלל אינן מפרישות הורמונים, אם כי חלקן מפרישות דופאמין.
שכיחות PPGLs היא 1.5 מקרים ל-10,000 איש (בניתוחים לאחר מוות השכיחות היא 5 ל-10,000 איש).
הפרשה של אפינפרין, נוראפינפרין והמטבוליטים שלהם וצורות ההסתמנות הקלינית - יתר לחץ דם התקפי או קבוע יכולות לרמז על מקור ההפרשה. ההבדלה ביניהן עשויה לכוון למוטציות גנטיות ספציפיות ולכן יש להסתמנות קלינית זו משמעות בעת בירור החולה, משפחתו וצורת המעקב.
הסתמנות קלינית: נעה בין העדר תסמינים להופעה מסכנת חיים. הטריאדה הקלאסית של כאב ראש הולם, הזעה, ודפיקות לב מתרחשת בהתקפים האורכים בין דקה לשעה. תדירות ההתקפים נעה מיומית לאחת לחודש ויותר, חלק מההתקפים ספונטאניים וחלקם משניים לגירוי כגון הרדמה, השתנה, שימוש בתרופות כגון חוסמי ביתא, נוגדי דיכאון טריציקלים, וסטרואידים. הופעת הטריאדה היא בעלת רגישות וספציפיות גבוהות לאבחנה של פאוכרומוציטומה. גידולים המפרישים אפינפרין בלבד יסתמנו כתת-לחץ דם התקפי. באופן כללי, יתר לחץ דם יופיע בהתקפים אצל 48 אחוזים מהמקרים, כתמידי ב-29 אחוזים וב-13 אחוזים לא נמצא יתר לחץ דם.
- את מי נסקור ל-PPGLs:
- סימפטומים התקפיים או מכוונים להפרשת יתר של קטכולאמינים
- תגובה מוגזמת של עליית לד כתגובה לתרופות, ניתוח או הרדמה
- יתר לחץ דם עמיד
- מסה אדרנאלית שנתגלתה במקרה. PPGLs ידוע כחלק ממעקב שנתי
- נטייה גנטית ידועה לפתח PPGLs (אנו יודעים כי עד 40 אחוזים מהמקרים נובעים ממוטציה גנטית)
- מאפיין חשוד לפתח פאוכרומוציטומה תורשתית
בירור ביוכימי
האבחנה הביוכימית של פאוכרומוציטומה מבוססת על מציאת רמות גבוהות של תוצרי מסלול מטבוליזם של קטכולאמינים. פרקציונציה של מטנפרינים בפלזמה או בשתן (הכוללים מטנפרינים, נורמטנפרינים ומטוקסיטיראמין - מטבוליטים של אפינפרין, נוראפינפרין ודופמין בהתאמה) היא הבדיקה הרגישה ביותר לגילוי פאוכרומוציטומה (רגישות של 98 אחוזים וסגוליות של 92 אחוזים כאשר הבדיקה בפלזמה רגישה יותר אך ספציפית פחות). תגובות חיוביות כוזבות (false positive) תתקבלנה במקרים של פעילות יתר סימפתטית כגון אי ספיקת לב, אי ספיקה כלייתית, היפוגליקמיה, נטילת הדם בישיבה ללא מנוחה מוקדמת. יש לוודא כי דגימות הדם והשתן נלקחו כראוי וכי הוספה חומצה לכלי המשמש לאיסוף השתן, לצורך השגת pH חומצי. ישנן מספר תרופות שיתנו תשובות חיוביות כוזבות ומומלץ להכירן (ראו טבלה). רמות נורמטנפרינים בפלזמה עולות עם הגיל, כתוצאה מהעלייה תלוית הגיל של נוראפינפרין בפלזמה.
רמות מטנפרינים בדם הגבוהות פי שלושה מהנורמה או מטנפרינים באסוף שתן ברמה פי 2 מהנורמה מחשידים מאד לקיום PPGLs וניתן להמשיך לבדיקות הדמיה CT (Computed Tomography)/MRI (Magnetic Resonance Imaging). בגלל האופי הציקלי של המחלה ומגבלות שמקורן באיסוף השתן ובפעילות ההפרשתית של הגידולים, רמות פחות גבוהות אינן שוללות, בהכרח, את אפשרות קיומה של פאוכרומוציטומה. אם הרמות אינן מובהקות ניתן לחזור עליהן, למדוד רמות כרומוגרנין A או לבצע מבחן קלונידין. בדיקת MIBG רגישה פחות למציאות PPGLs אבל FDG-PET) Fludeoxyglucose-positron emission tomography) טובה יותר בעיקר בנוכחות מחלה ממאירה של PPGLs.
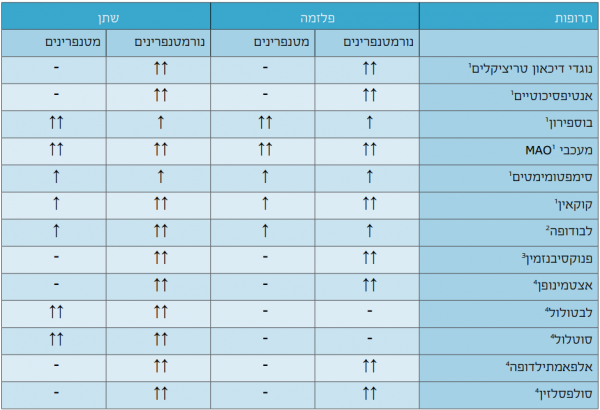
1. פרמקודינמיקה משפיעה על כל השיטות האנליטיות
2. ישנה הפרעה אנליטית עם חלק מ LIQUID CHROMATOGRAPHY עם אבחנה אלקטרוכימית והפרעה פרמקודינמית מעלה רמות דופמין ומטוקסיטיראמין.
3. ישנה הפרעה פרמקודינמית בימים הראשונים לשימוש בתרופה.
4. ישנה הפרעה אנליטית בחלק מהשיטות של LIQUID CHROMATOGRAPHY עם אבחנה אלקטרוכימית, תרופות אילו אינן גורמות לתשובת כזב חיובית בTANDEM MASS SPECTROSCOPY ASSAYS.
מקור: Lenders JWM et al; Pheochromocytoma and Paraganglioma: An Endocrine Society Clinical Practice .Guideline, J Clin Endocrinol Metab 99: 1915-1942, 2014
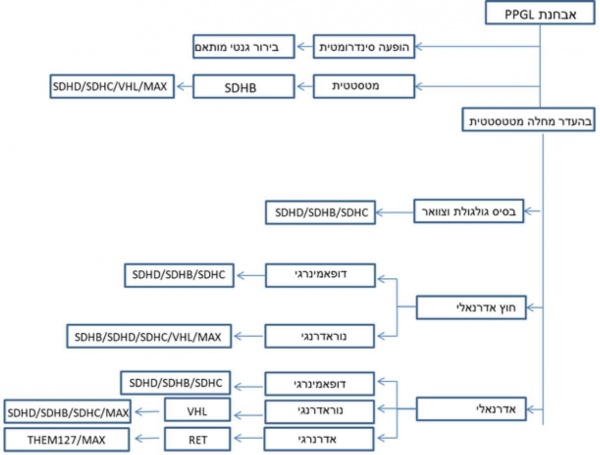
לברור גנטי, ישנה חשיבות רבה מאחר:
- לכשליש מחולי PPGLs אנו מוצאים germline mutation
- מוטציה ב SDHB מביאה לממאירות ב-40 אחוזים מהנשאים
- מציאות מוטציה בחולה תאפשר גילוי מוקדם בבני משפחתו
בדרך כלל חולים עם רקע גנטי יתאפיינו בגיל צעיר של הופעת המחלה, סיפור משפחתי חיובי, ביטוי סינדרומטי, מיקום אופייני לגידול, מולטיפוקאליות, מחלה דו צדדית, מטסטטית. נבדוק בעיקר (לפי השכיחות) את המוטציות ב: SDHB, SDHD, VHL, RET ו-NF1.
הטיפול המומלץ הוא ניתוחי במרכז רב תחומי המשלב כירורגים, אנדוקרינולוגים ומומחי יתר לחץ דם והדמיה. הניתוח מחייב הכנה מתאימה (מתן חוסמי אלפא כגון phenoxybenzamine ולאחר מכן חוסמי ביתא) וישנו צורך במעקב ארוך טווח אחר חולים אלו.
היפראלדוסטרוניזם ראשוני - (Primary hyperaldosteronism (PA
הפרשה עודפת ולא מבוקרת של אלדוסטרון מביאה לספיגה מוגברת של נתרן דרך תעלות נתרן בנפרון הדיסטאלי, דבר המביא לעלית לחץ דם ודיכוי מערכת הרנין-אנגיוטנסין. איבוד בשתן של אשלגן ויוני מימן המוחלפים בנתרן, עשויים להביא להיפוקלמיה ובססת מטבולית. אלדוסטרון עצמו, לבד מעליית לחץ דם, הוא הורמון המשרה דלקת ופיברוזיס ומגביר עקה חמצונית במערכת הקרדיווסקולרית וגורם עקב כך לתהליכים דלקתיים ופיברוטיים בשריר הלב, בכלי הדם ובכליות באופן שאיננו תלוי לחלוטין בלחץ דם. כמו כן ישנה עליה בשכיחות תסמונת מטבולית, סכרת, אוסטאופורוזיס ודיכאון בחולי PA.
ישנם שני סוגים עיקריים של PA: הראשון הוא אדנומה מפרישת אלדוסטרון - APA (Aldosterone producing adenoma, מהווה 35-40 אחוזים מהמקרים). השני הוא היפרפלזיה דו צדדית - בה שני האדרנלים מייצרים כמות עודפת של אלדוסטרון - BAH (60 אחוזים מהמקרים bilateral adrenal hyperplasia). סוגים נוספים הם GRA (glucocorticoid remediable aldosteronism, קטן מ-1 אחוזים-2 אחוזים), Unilateral primary adrenal hyperplasia (2 אחוזים), וקרצינומה אדרנלית (פחות מ-1 אחוזים).
PA נחשב לצורה השכיחה ביותר של יתר לחץ דם אנדוקריני ושיעורה בקרב הלוקים ביתר לחץ דם מגיע לכדי 5-10 אחוזים. יש הטוענים כי השימוש הגובר בבדיקת יחס אלדוסטרון לרנין מעלה את שכיחות האבחנה עד ל-20 אחוזים, במיוחד במקרי יתר לחץ דם עמיד. ל-PA טיפול ספציפי עם פוטנציאל סביר לריפוי או להקלה משמעותית. מרבית החולים הם נורמוקלמיים ובעשורים 3–6 לחייהם. יתר לחץ דם בחולי PA נע בין קל לקשה ביותר. ב-PA שכיחות יתר של דום נשימה בשינה והוא נטה להשתפר עם טיפול ספציפי.
את מי נסקור למציאות PA
- לחץ דם גבוה מ-150 מילימטר כספית סיסטולי ואו 100 מילימטר כספית דיאסטולי
- יתר לחץ דם עמיד
- לחץ דם מתחת ל-140/90 מילימטר כספית אבל בטיפול של ארבע או יותר תרופות
- לחץ דם והיפוקלמיה ספונטאנית או משנית לטיפול במשתנים
- יתר לחץ דם ואינסידנטלומה אדרנלית
- יתר לחץ דם ודום נשימה בשינה
- יתר לחץ דם וסיפור משפחתי של יתר לחץ דם בגיל צעיר או אירוע מוחי בגיל צעיר (מתחת לגיל 40)
- מומלץ לסקור את קרובי המשפחה מדרגה ראשונה של חולה PA
הערכה גנטית מומלצת לחולי PA מתחת לגיל 20, או לקרובי משפחה של חולה PA אשר אובחן בטרם מלאו לו 40 שנה או עבר אירוע מוחי מתחת לגיל זה (גן היברידי /GLUCOCORTICOID-REMEDIABLE ALDOSTERONISM-CYP11B1 CYP11 B2 - בו אפשר לטפל בדקסמטזון, או במקרה של גיל צעיר בלבד לנוכחות היפראלדוסטרוניזם משפחתי - TYPE III מוטציה בגן KCNJ5 המקודד לתעלת אשלגן. לצורה השנייה יותאם ככל הנראה בעתיד טיפול תרופתי ספציפי).
אבחנת PA
בדיקת הסקר הראשונה היא מדידת ARR (Aldosterone/renin ratio), אך יש להיות ערנים למספר רב של מגבלות:
- תוצאת כזב חיובית של מדידת ריכוז רנין (ולא אם מודדים פעילות רנין) תיתכן בשלב הלוטאלי של המחזור, או בשימוש בגלולות המכילות אסטרוגן, המורידות רמות רנין
- תשובת כזב חיובית של ARR תיתכן באי ספיקה כליתית (יצור רנין מופחת והיפרקלמיה מגרה הפרשת אלדוסטרון), בגיל מבוגר (הפרשת רנין יורדת הרבה יותר מאשר הפרשת אלדוסטרון עם הגיל), בחולי תסמונת גורדון (יתר לחץ דם בנוכחות היפרקלמיה- פסאודוהיפראלדוסטרוניזם TYPE II)
- חוסמי בטא, אלפא מתיל דופא, קלונידין ו-NSAIDS יכולים לדכא רמות רנין ולגרום ליחס ARR שהוא כוזב חיובית
- מציאות היפוקלמיה גורם לתוצאת כזב שלילית של ARR עקב דיכוי הפרשת אלדוסטרון
- תשובת כזב שלילית של ARR תיתכן במצבים מגרי הפרשת רנין כגון: הגבלת מלח בדיאטה, היצרות בעורקי הכליה ולחץ דם קיצוני, היריון (הפרוגסטרון נוגד את פעילות האלדוסטרון ברמת הרצפטור), טיפול במשתנים (כולל אלדקטון), חוסמי תעלות סידן מסוג דיהידרופירידינים, חוסמי האנזים המהפך וחוסמי הקולטן לאנגיוטנסין ACE/ARB
- לא ברור האם שימוש ב-SSRI (Serotonin Selective Reuptake Inhibitor) יגרמו לירידה כוזבת של ARR
כאשר מודדים פעילות רנין וערכי אלדוסטרון בנ"ג לד"ל הערך הסף המקובל של ARR הוא מעל ל-30. במחקרים, כאשר מודדים רמת רנין ישירה - DRC ב-mU/l ו-PAC בננוגרם לדציליטר הטענה היא שהסף לאבחנה צריך להיות נמוך יותר באזור 1.12-3.7. שימוש בערכי החציון התחתון בטווח זה, מביא ללא ספק לאבחנת יתר.
- טבלה מספר 2 - ערכי סף של ARR, בתלות בשיטת הבדיקה ובמדידת PAC, PRA -DRC ביחידות קונבנציונליות ויחידות בינלאומיות (SI)
| PRA בננוגרם/מיליליטר/לשעה | PRA בפיקומול/ליטר/דקה | DRC מילי-יחידה/ליטר (*) | DRC ננוגרם/לליטר (*) | |
|---|---|---|---|---|
| אלדוסטרון בפלזמה נ"ג/ד"ל | 20 | 1.6 | 2.4 | 3.8 |
| 30 (**) | 2.5 | 3.7 | 5.7 | |
| 40 | 3.1 | 4.9 | 7.7 | |
| אלדוסטרון בפלזמה פיקומול/לליטר | 750 (**) | 60 | 91 | 144 |
| 1000 | 80 | 122 | 192 |
(*) DRC – direct renin concentration - בדיקה בה הקורלציה בין DRC ל- PRA גרועה בתחום מתחת ל-1 ננוגרם למיליליטר לשעה שזה תחום העניין להגדרת PA.
(**) ערך הסף המקובל ל ARR הוא 30, והוא 750 אם מבטאים אלדוסטרון ב-SI UNITS
להגברת הרגישות לפני בצוע בדיקת ARR מומלץ להפסיק טיפול במשתנים לפחות 4 שבועות ותרופות אחרות לפחות בין 2–4 שבועות. על מנת לאזן לחץ דם ניתן להיעזר בורפאמיל, הידראלזין או פרזוצין. אם לא ניתן להחליף לתרופות אילו יש לזכור כי ARR גבוה בנוכחות טיפול במשתנים, ACE/ARB/CCB - dihydropyridine מאוששים את האבחנה בעוד שחוסמי ביתא כנראה מגבירים את תשובת הכזב השלילית.
יש לבצע את הבדיקה כשהחולה נורמוקלמי. רצוי לעודד צריכת מלח חופשית במידת האפשר לפני הבדיקה. בדיקה בשעות המאוחרות של הבוקר, בישיבה, לאחר שעתיים עד 4 שעות של הליכה או עמידה יגבירו את רגישות הבדיקה.
יש להתייחס לבדיקת ה-ARR כבדיקת סקר בלבד. יש לחזור עליה פעם נוספת לפני החלטה על המשך ברור על ידי מבחני דיכוי אשר יאששו או ידחו את האבחנה (מומלץ העמסת מלח פומי או מתן סליין תוך ורידי או דיכוי על ידי Fludrocortisone או קפטופריל). רמת אלדוסטרון גבוהה מ-10 ננוגרם/דציליטר ורמת פעילות של רנין בפלזמה הנמוכה מ-1 ננוגרם/מיליליטר/לשעה דורשות המשך ברור.
באם מבחן הדיכוי הוא חיובי מומלץ להמשיך בבדיקות הדמיה CT או MRI. בדיקות אלו נכשלות לעיתים קרובות בזיהוי APA ומזהות גם אדנומות שאינן מפרישות, ולכן (Adrenal venous sampling (AVS נחשב ל-gold standard על פיו יוחלט על ניתוח ממצא אדרנלי (באבחנה בין APA ל-BAH). בדיקה זו מבוצעת במרכזים המומחים בכך והיא בדיקה פולשנית ומסובכת הדורשת מיומנות גבוהה מצד המצנתר. אין לבצע בדיקת AVS בחולים צעירים מגיל 35, אדנומה חד צדדית ברורה בהדמיה מעל לסנטימטר אחד, התנהגות קלאסית, רמות אלדוסטרון גבוהות מעל 30 נ"ג לד"ל והיפוקלמיה בהם ניתן להמשיך ישרות לניתוח. כמו כן, אין לבצע את הבדיקה במטופלים עם תחלואה גבוהה והוריות נגד לניתוח.
אם נמצאה APA טיפול הבחירה הוא ניתוחי. ניתוח משיג ריפוי יתר לחץ דם ב-50-60 אחוזים או יותר, בעיקר שלא בגיל המבוגר, ולהפחתה בטיפול התרופתי הנצרך באחרים. בשאר המקרים הטיפול הוא על ידי טיפול נוגד פעילות אלדוסטרון: אלדקטון, אפלרנון ואמילוריד. תופעות הלוואי של אלדקטון הם גניקומסטיה, erectile dysfunction, וירידה בליבידו עקב חסימה לא ספציפית של הרצפטור לאנדרוגנים בגברים, ובנשים עקב הפעילות האסטרוגנית והפרוגסטטיבית נראה הפרעות מחזור והגדלת חזה. אפלרנון הוא ספציפי יותר ולכן שיעור תופעות הלוואי שלו קטן יותר. ברם, הוא פוטנטי פחות ודורש מינון של פעמיים ביום. בעתיד יהיה מקום ל-Aldosterone synthase inhibitors הנמצאים בפיתוח.
AME - Apparent mineralocorticoid excess syndrome
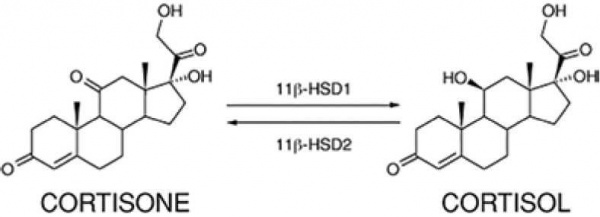
קורטיזול נקשר לרצפטור המינרולקורטיקואידי ביעילות דומה לזו של אלדוסטרון, ורק נוכחותו של האנזים 11β-HSD2, הצמוד לרצפטור ואשר גורם לאינאקטיבציה של קורטיזול על ידי היפוך שלו לקורטיזון, מגנה עליו מהפעלת יתר על ידי קורטיזול שריכוזו בדם גבוה פי 100 מזה של אלדוסטרון. פגיעה בפעילות האנזים 11β-HSD2 גורמת להפעלה מינרלוקורטיקואידית עודפת על ידי קורטיזול שלא "נוטרל".
ירידה בפעילות 11β-HSD2 יכולה להיות תורשתית או משנית לעיכוב על ידי glycyrrhizic acid (נגזרת של ליקוריץ). התסמונת המולדת מועברת בצורה אוטוזומלית רצססיבית.
התסמונת המולדת תתבטא ביתר לחץ דם בילדות, היפוקלמיה, משקל לידה נמוך, קושי בעליה במשקל ובגדילה, פוליאוריה ופולדיפסיה. בחולים אלה נראה בססת מטבולית, ערכי רנין ואלדוסטרון נמוכים וערכי קורטיזול תקינים.
לעיתים נראה הסתמנות של AME במקרים של קושינג אקטופי בו כמויות הקורטיזול גבוהות מכפי יכולת ה"נטרול" של האנזים 11β-HSD2.
אבחנה תתקבל על ידי הדגמה של יחס גבוה של מטבוליטים של קורטיזול לקורטיזון באיסוף שתן של 24 שעות (בדרך כלל מעל לפי 10 מהנורמה).
תסמונת קושינג - Cushing Syndrome
הצורה הנפוצה ביותר של תסמונת קושינג היא יאטרוגנית (מתן סטרואידים). קושינג אנדוגני הוא יחסית נדיר ומוערך כ 1–3 מקרים חדשים למיליון איש לשנה. הפרשת יתר של ACTH על ידי גידול היפופיזארי אחראית ל-85 אחוזים ממקרי תסמונת קושינג אנדוגני ונקראת "Cushing disease". קושינג היפופיזארי נפוץ יותר בנשים ובדרך כלל מסתמן בין גילאים 20–50 שנה. הפרשה אקטופית של ACTH וצורות שהן בלתי תלויות בהפרשת ACTH (כגון אדנומות אדרנאלית, קרצינומות אדרנאליות, והיפרפלסיה נודולארית של האדרנלים) מהוות יחדיו כ־15 אחוזים מהמקרים. יתר לחץ דם מופיע ב-75-80 אחוזים מהמקרים. המנגנונים בהם נוצר יתר לחץ דם בתסמונת זו הם: יצור יתר של DOC) deoxycortisol), השפעות גלוקוקורטיקואידיות ישירות כגון רגישות יתר לחומרים מכווצי כלי דם (כגון אפינפרין, אנגיוטנסין II), עליה בתפוקת הלב, אקטיבצית מערכת רנין אנגיוטנסין על ידי עליה ביצור אניגיוטנסינוגן בכבד, וכן הפעלת הרצפטור למינרלקורטקואידים על ידי קורטיזול.
הסתמנות קלינית: הסמנים והתסמינים הטיפוסיים הם עליה במשקל והשמנה בטנית, פנים עגולות ואדומות, צבירת שומן מעל עצמות הבריח ובעורף, easy bruising, עור דק, סטריאות סגולות בדרך כלל בעובי מעל 1 סנטימטר, ריפוי פצע איטי, חולשת שרירים, שינויים התנהגותיים (כגון חוסר שקט, דיכאון), שיעור יתר, היפראנדרוגניזם, יתר לחץ דם, אוסטאופניה ואוסטאופורוזיס, אי סבילות לסוכר עד לסוכרת, דיסליפידמיה, זיהומים אופורטוניסטיים ופטרייתיים, אי סדירות מחזור ואבני כליה.
מומלץ לסקור לתסמונת קושינג בחולי יתר לחץ דם אשר מופיעים עם מקבץ מהסמנים והתסמינים המצוינים למעלה.
בבדיקות המעבדה נוכל למצוא ערכי סוכר גבוהים בצום, דיסליפידמיה, היפוקלמיה, ספירת דם לבנה גבוהה עם לימפופניה יחסית, רמות אלדוסטרון ורנין הן בדרך כלל תקינות או נמוכות (ערכי DOC תקינים עד גבוהים). ערכים גבוהים של אנדרוגנים, אלדוסטרון - DOC יכולים לרמז על קרצינומה אדרנלית.
מומלץ לבצע מבחן דיכוי לילי של 1 מיליגרם דקסמטזון (רמת קורטיזול מעל 50 ננומול לליטר דורשת המשך בירור), מדידת רמות קורטיזול חופשי לילי ברוק ואיסוף שתן של 24 שעות לקורטיזול חופשי. יש להמשיך בירור אם הממצאים חיוביים בשניים מהמבחנים המתוארים למעלה. בדיקת הרוק ואיסוף השתן בודקים קורטיזול חופשי ולכן אינם תלויים בנסיבות המעלות cortisol binding globulin (כגון היריון או שימוש בגלולות המכילות אסטרוגן אשר יכולות לתת תשובת כזב חיובית בבדיקת דיכוי דקסמטזון) כמו גם שימוש בתרופות הגורמות לפינוי מהיר של דקסמטזון מהפלזמה (כגון תרופות אנטיאפילפיטיות). לאחר בצוע בדיקות הסקר מומלץ להפנות את החולה לאנדוקרינולוג לבצוע מבחנים נוספים לאישור האבחנה ולבחינת מקור הפרשת היתר (היפופיזארית מול אדרנאלית או אקטופית).
אקרומגליה Acromegaly
הפרשת יתר של הורמון גדילה מגידול היפופיזארי גורמת לתסמינים הקליניים של אקרומגליה. התסמונת נדירה ושכיחותה כ-70 מקרים למיליון איש.
ההתבטאות הקלינית היא acral and soft tissue overgrowth, dental malocclusion, ארתריטיס דגנרטיבית, הזעה מרובה, עור שמנוני, הצרות תעלה קרפאלית, הפרעות לבביות, סוכרת ויתר לחץ דם. יתר לחץ דם נמצא ב-20-40 אחוזים מכלל החולים וקשור באצירת נתרן והרחבת הנפח החוץ תאי.
מומלץ לסקור חולי יתר לחץ דם שאצלם נמצא גידול היפופיזארי ו/או תסמיני אקרומגליה כמתואר לעיל.
האבחנה הראשונית נעשית על ידי מדידת רמות 1 Insulin-like growth factor בסרום. לאחר בירור ביוכימי, יש לבצע בדיקת הדמיה של ההיפופיזה בעזרת MRI.
ניתוח היפופיזארי הוא טיפול הבחירה ובמידת הצורך תוספת של טיפול תרופתי וקרינה. יתר לחץ דם מגיב בדרך כלל לטיפול בתסמונת אך אם אי אפשר להשיג ריפוי ניתוחי אזי ישנה תגובה קלינית טובה לשימוש במשתנים.
הפרעות בתפקוד בלוטת התריס
פעילות יתר/ היפרתירואידיזם
שכיחות: כ-0.5-1 אחוזים מהאוכלוסייה, נפוץ יותר בנשים. הגורמים לכך הם מחלת גרייבס, זפק רב קשרי טוקסי, אדנומה טוקסית ותירואידיטיס.
השפעת פעילות יתר של הורמוני בלוטת התריס על הרקמות ועליה ברגישות לקטכולאמינים מביאה לדופק גבוה, עליה בתפוקת הלב, עליה בנפח הפעימה, ירידה בתנגודת הסיסטמית והעלייה בלחץ דם הסיסטולי. כמו כן החולים ירדו במשקל, יספרו על אי סבילות לחום, הזעה וחולשת שרירים.
בחולי יתר לחץ דם אשר יבטאו תסמינים אלה יש לבדוק רמות Free T4-TSH. הטיפול הראשוני בהם יכלול חוסמי ביתא לטיפול בלחץ דם, דופק מהיר ורעד. הטיפול המכוון ישתנה בהתאם לאטיולוגיה של פעילות היתר.
תת פעילות/היפותירואידיזם
שכיחות: תת-פעילות מוערכת ב-3.8 אחוזים מהאוכלוסייה כאשר שיעור תת-פעילות תת-קלינית מגיעה בין 4.3-8.5 אחוזים מהאוכלוסייה. יתר לחץ דם בעיקר דיאסטולי נפוץ פי 3 בקרב חולים אילו מאשר באוכלוסייה הכללית ואחראי על 1 אחוזים ממקרי יתר לחץ דם דיאסטולי. הסיבות לכך קשורות בעליה בתנגודת הסיסטמית והרחבה בנפח החוץ תאי.
ההסתמנות הקלינית תלויה ברמת ההורמונים הפריפריים ובקצב התפתחות תת-הפעילות. חולים יסתמנו כעייפים, בעלי קצב דיבור וחשיבה איטיים, בעלי אי סבילות לקור, סובלים מעצירות, בעלי דופק איטי, בעלי עור יבש, פנים ובעיקר עפעפיים תפוחות, לשון נפוחה וקול נמוך וצרוד. תפוקת הלב נמוכה ולחץ דמם הדיאסטולי יהיה גבוה. הם יתלוננו על קוצר נשימה בבצוע מאמצים.
בנוכחות סימנים ותסמינים אלו בחולים עם יתר לחץ דם, יש לקחת רמות בדם של TSH ו-Free T4 על מנת להבדיל בין תת-פעילות ראשונית שהיא כשל של הבלוטה מתת פעילות שניונית הנובעת מכשל היפופיזארי/היפותלמי. טיפול בהורמוני בלוטת התריס (מתן תכשיר T4) יביא לירידה בלחץ דם בשני שלישים מהמקרים ולנרמול לחץ דם ביתר.
היפרקלצמיה והיפרפאראתירואידיזם ראשוני (PHPT = primary hyperparathyroidism)
הגורם השכיח ביותר להיפרקלצמיה הוא היפרפאראתירואידיזם ראשוני ששכיחותו 0.2 אחוזים בנשים ו-0.09 אחוזים בגברים. שכיחות המחלה עולה עם הגיל. בחולי PHPT שכיחות יתר לחץ דם נעה בין 10-60 אחוזים. ברוב המקרים PHPT עשויה להיות אסימפטומטית, אך עלולה להביא גם למגוון סימפטומים הקשורים בהיפרקלצמיה כרונית כגון פוליאוריה, פולידפסיה, עצירות, אוסטאופורוזיס, אבני כליה, כיב פפטי ויתר לחץ דם. לא נמצאה קורלציה ישירה בין רמות הורמון הפאראתירואיד או רמות הקלציום ליתר לחץ דם. חלק ממקרי יתר לחץ דם יכולים לנבוע מסיבוך כלייתי של PHPT.
מומלץ לסקור חולי יתר לחץ דם היפרקלצמיים לנוכחות PHPT על ידי מדידת רמות פאראתירואיד הורמון בדם ואיסוף שתן של 24 שעות להפרשת סידן (בכדי לשלול מקרי familial hypocalciuric hypercalcemia).
הטיפול ההמומלץ ב-PHPT הוא ניתוחי, אך לניתוח אין השפעה ברורה או עקבית על לחץ הדם. בחולים שאינם כשירים לניתוח, ניתן להציע טיפול בקלציממטים כגון cinacalcet.
ביבליוגרפיה
- Lenders JWM et al; Pheochromocytoma and Paraganglioma: An Endocrine Society Clinical Practice Guideline, J Clin Endocrinol Metab 99: 1915-1942, 2014.
- Young WF et al ; Screening for Endocrine Hypertension: An Endocrine Society Scientific Statement, Endocrine Reviews 38: 103-122, 2017.
- Williams TA et al; Diagnosis and management of primary aldosteronism: the Endocrine Society guideline 2016 revisited, European Journal of Endocrinology 179, R19-R29, 2018.
- Funder JW et al; The Management of Primary Aldosteronism: Case Detection, Diagnosis, and Treatment: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 101: 1889¬1916, 2016.
- Manolopoulou J et al .Clinical validation for the aldosterone-to-renin ratio and aldosterone suppression testing using simultaneous fully automated chemiluminescence immunoassays. J. Hypertens. 33 (12): 2500-2511, 2015.
- Yang J et al. Diagnosing endocrine hypertension: a practical approach Nephrology; 22: 663-677, 2017.
- Young WF et al. Endocrine HTN: then and now. ENDOCRINE PRACTICE 16; 5; 888-902, 2010.
- Guignat L et al. The diagnosis of Cushing's syndrome: an Endocrine Society Clinical Practice Guideline: commentary from a European Perspective. European Journal of Endocrinology 163; 9-13;2010.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק