שאתות אחור-צפקיות והרקמות הרכות - Retroperitoneal and soft tissue tumors
הופניתם מהדף ליפוסרקומה לדף הנוכחי.
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הצפק | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מחלות של הצפק
שאתות שמקורן באחורי הצפק (רטרופריטונאום) הן: פיברוסרקומות, ליומיוסרקומות, ליפוסרקומות ולימפומות.
התסמינים הקליניים האופייניים לשאתות אלה הם:
בצילום בטן סקירה המתבצע עקב תפיחות הבטן נראה דחיקה של המעי או הכליות על-ידי המסה. האבחנה מתבצעת על ידי CT בטן בו ניתן לראות את המסה האחור צפקית.
רק לעתים נדירות השאתות הן שפירות או בעלות ממאירות מדרגה נמוכה. בשאתות ממאירות, חוץ מהליפוסרקומה, הטיפולים הכירורגיים אינם משיגים תוצאות טובות, ולרוב הניתוחים הם מקלים (פלאטיביים) בלבד. פתיחת בטן חוקרת, ביופסיה, והקטנת המסה השאתית, הם הטיפולים הכירורגיים המקובלים. לאחר הניתוח ניתן להקל על החולים באמצעות טיפולים כימיים והקרנות, המשפרים את ההיוותרות בחיים.
ליפוסרקומה
התיאור הראשון של ליפוסרקומה מיוחס ל-Virchow. זו אחת השאתות השכיחות ביותר מקרב הסרקומות של הרקמות הרכות, ומשקפת 11%-28% מכלל השאתות המשתייכות לקבוצה זו. סרקומה עלולה להתפתח בכל אזור בגוף, אך האזורים השכיחים ביותר להתפתחותה הם הגפיים התחתונים והחלל האחור-צפקי. בסקירה של 3,400 חולים הלוקים בסרקומות של הרקמות הרכות נמצאו 24.1% בעלי פיברוסרקומה ואילו 18.7% היו בעלי שאתות מסוג ליפוסרקומה. סוג זה עלול להופיע בכל גיל, אך שיא שכיחותה בין העשור החמישי לעשור השביעי לחיים, בגברים יותר מאשר בנשים. שאתות אלה ממאירות מעצם התהוותן. מקובל כיום, שליפומות שפירות אינן עוברות תהליך של התמרה ממארת לליפוסרקומה. כשאר הסרקומות של הרקמות הרכות, רוב הליפוסרקומות מופיעות בגפיים התחתונים ובחלל האחור-צפקי. ליפוסרקומה היא שאת שכיחה ביותר ברטרופריטונאום.
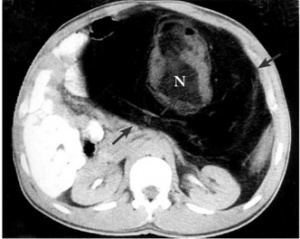
בטומוגרפיה ממוחשבת של הבטן ניתן לראות שאת ענקית, המאופיינת לעתים בנמק מרכזי הדוחק את איברי הבטן (תצלום 4.2).
התפשטות גרורתית לקשריות הלימפה האזוריות נדירה בחולים עם ליפוסרקומה ואכן רק בכ-5% מהחולים הלוקים בליפוסרקומה יתגלו קשריות נגועות על-ידי השאת. הגרורות נשלחות בעיקר דרך הדם, לריאות, לכבד ולעצמות.
פתולוגיה
הליפוסרקומות מסווגות ל-3 דרגות התמיינות: ליפוסרקומות בעלות התמיינות גבוהה (Myxoid well differentiated) נחשבות כפחות ממאירות או בעלות דירוג נמוך, ולכן מסווגות כ- Grade 1) G1), ואילו הליפוסרקומות מסוג תאים עגולים-רב צורתיים (פלאומורפיים) הן ממאירות יותר וההיוותרות בחיים לאחר 5 שנים נמוכה יותר, ולכן הן מסווגות כבעלות דירוג גבוה או Grade 2-3) G2-3) (טבלה 2.5).
| דרגת ההתמיינות | סוג |
|---|---|
| G1 | ליפומה דמוית ליפוסרקומה |
| G1 | מיקסואיד ליפוסרקומה |
| G2-3 | ליפוסרקומה מסוג תאים עגולים |
| G2-3 | פלאומורפיק ליפוסרקומה |
דרגת ההתמיינות של הסרקומות היא אחד המאפיינים הפרוגנוסטיים, וככל שהדירוג נמוך, כך הפרוגנוזה טובה יותר. הדירוג ההיסטולוגי ומאפיינים נוספים, כגון גודל השאת, התפשטות מקומית, מעורבות קשריות לימפה אזוריות, וכמובן נוכחות גרורות מרוחקות כל אלה יחד קובעים את שלב המחלה. מבחינה היסטולוגית יש שאתות המוגדרות מראש כבעלות דירוג גבוה, לדוגמה רבדומיוסרקומה, ואילו אחרות בעלות דירוג נמוך, לדוגמה Dermatofibrosarcoma protuberance.
טיפול
בגישה הטיפולית-ניתוחית בשאתות של הרקמות הרכות חלו כמה שלבי התפתחות, מהגישה הרדיקלית שכללה קטיעות גפיים נגועים בסרקומות לגישה השמרנית יותר הנוקטת כריתה נרחבת של השאת וטיפול בתר-ניתוחי משלים בקרינה ובטיפול כימי. בכמה סדרות, רובן בשנים האחרונות, הוכח שהגישה השמרנית יותר - כריתה נרחבת של השאת, המלווה בטיפול בתר-ניתוחי משלים - השיגה תוצאות מצוינות עם שיעור היוותרות בחיים של יותר מ-80% לאחר 5 שנים. בסדרה מבוקרת היטב של Rosenberg וחבריו לא הוכח, שקטיעה מקנה שיעור גבוה יותר של היוותרות בחיים מאשר בקבוצה שטופלה בגישה שמרנית. יתרה מזו, הוכח שניתן לדחות את מועד הקטיעה לשלב שני לאחר הישנות מקומית של השאת כאשר הטיפול הראשוני נכשל, ואין גישה זו מסכנת או מחמירה את הפרוגנוזה של החולה.
הניסיון המצטבר בטיפול בחולים אלה וניסויים מבוקרים לימדו שהגישה לחולה עם ליפוסרקומה חייבת להתבסס על כריתה בשילוב טיפול משלים בתר-ניתוחי. גישה זו הניבה תוצאות מצוינות בחולים הלוקים בסרקומה בדירוג גבוה שהפרוגנוזה שלהם לפני יישום גישה טיפולית זו היתה גרועה.
גישה חדשנית לטיפול בסרקומות של הרקמות הרכות היא זילוח (פרפוזיה) רקמתי מבודד של האזור הנגוע לאחר הכריתה הכירורגית של השאת.
אחת הבעיות הקשות ביותר בטיפול הכימי במחלות ממאירות היא תופעות הלוואי הנגרמות עקב פגיעות ברקמות בריאות, אם התכשיר הכימותרפי ניתן במינונים הורגי גידול (טומוריצידיים). זילוח (פרפוזיה) רקמתי מבודד יספק תשובה לבעיה זו.
עקרונות השיטה כוללים בידוד מחזור הדם של האיבר המטופל ממחזור הדם הכללי וחיבורו למחזור דם חוץ-גופני מטיפוס משאבת לב-ריאה (Extra corporcal pump oxygenator). כך יושגו זילוח וחימום האיבר. כאשר מושגת הטמפרטורה הדרושה, מוחדר התכשיר הכימותרפי למערכת, והזילוח נמשך פרק זמן נוסף. בדרך זו אפשר להגיע לריכוזים הורגי גידול (טומוריצידיים) באזור השאת במיעוט תופעות לוואי כלליות של התרופה. כמו-כן אפשר לחמם את האיבר לטמפרטורות גבוהות יחסית, בלא חשש לנזק רב-מערכתי בגלל חימום-יתר.
האזור האנטומי הנוח ביותר לזילוח בדרך זו הוא הגפיים, בשל האפשרות האנטומית לבידוד מוחלט של מחזור הדם המקומי. ואכן שיטת טיפול זו נמצאת בשימוש נרחב במקרים של שאתות של הרקמות הרכות בגפיים, בעיקר מלנומה ממארת וסרקומות של הרקמות הרכות. בגפיים התחתונים מבוצע הזילוח דרך כלי הדם הכיסליים (Iliac vessels)(לטיפול בשאתות הממוקמות בברכיים) או כלי הדם המפשעתיים (בשאתות הממוקמות נמוך יותר). צנתרים מוחדרים לעורק ולווריד ובעזרת מערכת צינורות מתחברים למחזור החוץ-גופני. בידוד כלי הדם של הגף מבוצע על-ידי מלחציים חוסמים קריבנית למקום כניסת הצנתרים וחסם הממוקם על שורש הגף. החימום נעשה בעזרת מזרן חימום, העוטף את הגף, וחימום הדם העובר דרך משאבת המחזור החוץ-גופני. כאשר הטמפרטורה מגיעה לרמה הדרושה (39-41 מ"צ), מוחדר התכשיר הכימי ואז מתרחש זילוח למשך כ-60 - 90 דקות. בתום הטיפול מבוצעת שטיפת מחזור הדם של הגף, שנועדה להקטין את כמות התכשיר הכימותרפי שחדר למחזור הדם הכללי עם הסרת בידוד כלי הדם של הגף.
עקרונות טיפוליים אלה יפים לביצוע זילוח באיברים נוספים, כגון הגפיים העליונים, שם מבוצע הזילוח דרך כלי הדם התת-בריחיים (Subclavian). באגן מבוצע הזילוח דרך כלי הדם הכיסליים והוא כרוך בחסימה זמנית של הוותין (האאורטה) הבטני, הווריד החלול התחתון וכלי הדם המפשעתיים.
כמויות התכשיר הכימי המגיעות לאזור השאת גבוהות פי 6-5 מהכמות שהיתה מגיעה לו ניתן טיפול מערכתי. המגבלה הכמותית היא גבול הנזק הרעלני הישיר של התכשיר הכימותרפי ברקמות. הנזק נגרם לכלי הדם (Vasculitis), לעצבים היקפיים (Peripheral neuropathy) ולעור (Dermatitis, bullous changes).
תופעות אלו הן זמניות ברובן וחולפות בתוך כמה ימים מתום הטיפול. תופעות הלוואי הכלליות הן מועטות ונמצאות ביחס ישר לדרגת בידוד האיבר. שמירה על לחצי זילוח נמוכים ב-1.5 מ"מ כספית מלחץ הדם במחזור הכללי, מונעת אף היא דליפת התכשיר הכימי ומאפשרת זילוח רקמתי יעיל. דרגת הדלף למחזור הדם הכללי ניתנת למדידה על-ידי החדרת תכשיר רדיואקטיבי למחזור החוץ-גופני ומדידת הרדיואקטיביות בדגימות ממחזור הדם הכללי.
ריכוזי חמצן גבוהים באזור הזילוח הם כנראה בעלי השפעה הורגת גידול (טומוריצידית) ישירה. חימום-יתר (Hyperthermia) ידוע כבעל השפעה הורגת גידול (טומוריצידית) ישירה.
דרגת החום הנחשבת יעילה בזילוח רקמתי מבודד היא 39 - 41 מ"צ. דרגת חום החורגת כלפי מעלה ביותר מ-2 מ"צ גורמת נזק רקמתי ישיר לאיבר המטופל, ולעתים נגרם דיכוי של פעילות התכשירים הכימותרפיים המוחדרים למערכת הזילוח הרקמתי המבודד. בידוד האיבר מונע את פגיעת החום באיברים חיוניים.
הגורם העיקרי המשפיע על ריכוז התרופה הוא קצב פירוקה הטבעי. כמו-כן, על התכשיר להיות יציב בדרגות חום גבוהות יחסית. נוסף על כך, התרופה צריכה לפעול מהר בשל משך הזמן הקצר, שבו מתקיים מגע בין התרופה לרקמות. לפיכך, סוגי התרופות המתאימים ביותר לשימוש בזילוח רקמתי מבודד הם תכשירי אלקילציה (Alkylating agents) ותכשירים אנטיביוטיים. התרופה השכיחה ביותר לשימוש בזילוח רקמתי מבודד בלוקים במלנומה היא Alkeran (Melphalan - Phenylanin mustard). באחרונה, בשל ריבוי יחסי של תופעות לוואי, נערכת בחינה מחודשת של תרופה זו. תרופות אחרות הן Actinomycin D, Dacarbazine וה-Cisplatin.
המינון הניתן בזילוח רקמתי מבודד מחושב ביחס לשטח הגוף. במקרי זילוח של גף מחשבים את המינון לפי נפח הגף. הכמות הניתנת היא בדרך כלל 20-10 מ"ג לכל ליטר נפח הגוף.
סיבוכים
סיבוכי זילוח רקמתי מבודד אינם שכיחים. רוב הסיבוכים הם מקומיים וקשורים בפגיעה בכלי הדם המספקים דם לאיבר או בטיפול התרופתי המקומי. הוריות הנגד לביצוע זילוח רקמתי מבודד, בעיקר בגפיים, מתקיימות בכל החולים הלוקים במחלות כלי דם היקפיים (Peripheral vascular disease) או בנוכחות סוכרת קשה.
בקבוצה של 60 חולים שטופלו בזילוח רקמתי מבודד של הגפיים התחתונים דיווח Bulman על שני חולים שלקו בפקקת ורידים עמוקה (DVT) וארבעה אחרים שלקו בחסימת עורק המפשעה בקריש (נדרש טיפול ניתוחי). Stehlin דיווח בסדרה של 175 חולים שטופלו בזילוח רקמתי מבודד על 3 חולים שבוצעה בהם כריתת גף בשל נמק רקמתי נרחב עקב מינון תרופתי מקומי גבוה.
תופעות לוואי כלליות של הטיפול התרופתי יופיעו אם אין בידוד רקמתי יעיל. Krementz דיווח על שכיחות גבוהה, יחסית, של תופעות מקומיות הקשורות בטיפול תרופתי: בצקות והפרעה בתפקוד הגף עקב פגיעה עצבית או שרירית, בקבוצה של 275 חולים שטופלו בזילוח רקמתי מבודד.
פיברוסרקומה
שאת השכיחה ברטרופריטונאום, הפוגעת בשני המינים באופן שווה. היא בעלת קופסית מדומה (Pseudo capsule), כאשר תאי השאת חודרים דרכה. שאת זו שכיחה יותר בגפיים התחתונים מאשר ברטרופריטונאום. האבחנה מתבצעת על-ידי ביופסיה פתוחה. בהיסטולוגיה ניתן למצוא בחלקים שונים של השאת תבניות היסטולוגיות שונות.
ליומיוסרקומה
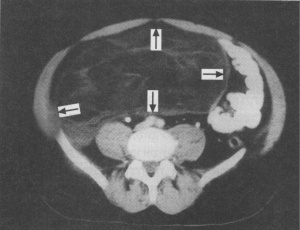
שאת בעלת פוטנציאל ממאיר, השכיחה בעיקר ברטרופריטונאום, בייחוד בגילאי 40 - 80 שנה, וגדלה לממדים גדולים מאוד. לשאת זו אין קופסית מגבילה. בטומוגרפיה ממוחשבת אפשר לראות את ממדי השאת הדוחקת את איברי הבטן (תצלום 5.2).
ראבדומיוסרקומה
שאת זו נחלקת לכמה קבוצות:
- Rhabdomyosarcoma botryoid, השכיחה בילדים עד גיל 15, ומופיעה בעיקר בגפיים ומאחורי העין. שאתות אלה הן פוליפואידיות ושולחות גרורות לקשריות הלימפה. השאת נראית כאשכול ענבים.
שיעור ההיוותרות בחיים למשך 5 שנים הוא 42%. שיעור החזרות המקומיות הוא 14%-18%. - Alveolor and pleomorphic rabdomysarcoma, שאתות ממאירות ביותר השולחות גרורות מקומיות, שכיחות יותר בכתף ובעצם השכם (Scapula). בהיסטולוגיה יתגלו מיובלסטים עם שריר משורטט ותאי ענק.
סרקומה סינובית
שאת היוצאת מהסינוביה, ומכילה שני מרכיבים: (1) סינוביאל בלסט, (2) פיברובלסט. השאת היא ביפזית. בהיסטולוגיה ניתן לראות מבנה פסיפס (מוזאיקה), עם אזורים קשים וביניהם מבנים ציסטיים נמקיים. שאת זו גדלה מהר, ושכיחה יותר בנשים.
שאתות נוירוגניות
שוואנומה שפירה או ממאירה, גנגליוניורומה, כרומופינומה ממאירה ואחרות, מדווחות ברטרופריטונאום. השאתות מופיעות לאורך שורשי העצבים, וייתכן שיופיעו כגוש יחיד או כגושים מרובים. הנוירונומות שכיחות יותר בראש ובצוואר, ונדירות יותר ברטרופריטונאום. השאתות נראות כבצל, ואפשר לקלפן בלי לפגוע בעצב.
אנגיומה
מצויה בצורה הקפילרית והקורנוזית, ובצורה הממאירה המאנגיוסרקומה ואנגיופריציטומה. שאת ממאירה ביותר ממקור לימפתי היא הלימפאנגיוסרקומה. רוב שאתות אלה מופיעות לאחר דיסקציה של בלוטות הלימפה, גורמות לבצקת לימפטית (לימפאדמה), ואף נוטות לשלוח גרורות לריאות.
שאתות דסמואידיות
לפני כ-150 שנה תיאר Macfarlane בראשונה שאת מסוג דסמואיד. שם השאת נגזר מהמילה היוונית "Desmos", שפירושה רצועה או דמוי גיד. השאת נמנית עם השאתות הלייפתיות, ומקורה בשגשוג פיברובלסטי מהשכבות השריריות-אפונוירוטיות, והיא עלולה להופיע בכל גיל. מבחינה היסטולוגית מורכבת השאת מתאי כישור ארוגים במצע קולגן, בלא רכיבים אפיתליאליים, מאופיינת בחלוקת תאים תקינה ובהעדר גרורות מרוחקות. גורמים אטיולוגיים אפשריים כוללים חבלה, בעיקר ניתוחית, השפעות הורמונליות, בעיקר במהלך היריון וליקויים תורשתיים בוויסות רקמת החיבור.
בעבר נחשבה השאת שפירה וניתנת לטיפול פשוט, והוא - כריתה. כיום ברור, שהשאת צומחת במהירות ונוטה לחדירה מקומית ולהישנות מקומית לאחר כריתה. נטייתה לחדירה מקומית מבדילה אותה משאתות שפירות.
השאת יכולה להופיע כחלק מתסמונת גרדנר (Gardner), ויש הסבורים, כי שאת זו בקיר הבטן או בחלל הצפק היא התבטאות חוץ-כרכשתית של פוליפוזיס משפחתית (Familial adenomatous polyposis).
דסמואיד משקף כ-0.03% מכלל הסרקומות וכ-3.6% מהשאתות ממקור לייפתי. ההיארעות השנתית של שאת זו היא 3.7 למיליון בני אדם.
המיקום השכיח ביותר של הדסמואיד הוא באזור דופן הבטן (49%). כאן השאת מערבת בעיקר את השריר הישר-בטני (Rectus abdominis). בשכיחות נמוכה יותר (43%) מעורבים אזורים חוץ-בטניים בלא עירוב בולט של שריר כלשהו, ואילו המזנטריום מעורב בשכיחות הנמוכה ביותר - 8%. הדסמואיד שכיח יותר באזורי גוף שנחבלו או הצטלקו בניתוח, וכן בעצם הספנואידית וסביב צנרור עוקף של נוזל השדרה (CSF shunt tubing).
תסמינים קליניים
הדסמואיד מתבטא במעט תסמינים קליניים. התסמין השכיח ביותר הוא הופעת גוש. כאב מופיע בכשליש מהחולים, בעיקר באלה שבהם השאת קרובה לפרקים או מפריעה לתנועת השרירים. חסימת מעיים תיתכן בחולים שבהם השאתות מתפתחות בפדר (אומנטום).
מבחינה קלינית יש 4 קבוצות גיל, לכל קבוצה מאפייני שאת שונים. בקבוצת הילדות (4.5+3.5 שנים), לדוגמה, יש יחס של 3:1 בין מספר הילדות למספר הילדים, והיא מתאפיינת בשכיחות גבוהה יותר של שאתות חוץ-בטניות. בקבוצת הגיל 27+4.4 שנים יש יחס של 1: 1.8 בין בנות לבנים, ושכיחות השאת בדופן הבטן גבוהה פי 11 מאשר באזורי גוף אחרים. בקבוצת הגיל 44+7 שנים קיימות יותר שאתות בדופן הבטן (פי 2.6 יותר מאשר באיברים אחרים), בלא הבדלי מין, ואילו בקבוצת הגיל 68+4.4 שנים השאת ממוקמת בכל חלקי הגוף ובשני המינים באותו יחס.
בחולות רבות (59%-30%) התפתחה שאת הדסמואיד בדופן הבטן אחרי היריונן השני ובמיעוטן אובחנה השאת במהלך השליש האחרון של ההיריון. נמצאו יותר נשים פוריות הלוקות בדסמואיד, ומאופיינות ברמת אסטרוגנים גבוהה ומיעוטן בעלות רמת פרוגסטרון גבוהה. מכאן שגורמים הורמונליים יש בהם כדי לתרום לוויסות הגדילה של דסמואיד. השערה זו נתמכת בתצפיות, שבהן קצב גדילת השאת בבנים היה קבוע בכל קבוצות הגיל, בניגוד לנצפה בבנות. כמות הקולטנים לאסטרדיול גבוהה באורח ניכר מכמות הקולטנים לפרוגסטרון, אך קטנה בהשוואה לקולטני אסטרדיול שבסרטן השד.
במקצת החולים שלקו בדסמואיד אובחנו ליקויים קטנים ורבים במבנה העצם, שכללו עיבוי קליפתי, Exostosis, אזורים כיסתיים (ציסטיים), איים קומפקטיים בעצם הירך ועוד. בדיקה גנטית העלתה את האפשרות, כי הנטייה לליקויים אלה היא מורשת באופן אוטוזומלי שולטני (דומיננטי).
פתולוגיה
מבחינה היסטופתולוגית שאתות אלה הן גושים המאופיינים ברצועות ארוגות של תאי כישור. אלה מכילים כמויות משתנות של קולגן ולעתים תאי ענק סרקולמיים. ממצאים אלה דומים לממצאים בפיברוסרקומה מדרגה נמוכה (Low grade fibrosarcoma). בדסמואיד יש חלוקות תאים מעטות ותקינות, דבר שיכול להסביר תיאורטית את התגובה הדלה של השאתות לטיפול המבוסס על קינטיקת מעגל התא (Cell-cycle kinetics).
אבחנה מבדלת
האבחנה המבדלת של דסמואיד כוללת שאתות של הרקמות הרכות (פיברוסרקומות, ליפוסרקומות, ליפומות ועוד). בקעים, בעיקר מסוג Spigelian hernia, ובקע לאחר ניתוח (Incisional hernia), עלולים לעוות את התמונה.
שאתות דסמואידיות תוך-בטניות או מזנטריות עלולות להיות מאובחנות בטעות כליפומות או כלייפת אחור-צפקית.
טיפול
הטיפול העיקרי הוא כריתה נרחבת. קרינה כטיפול משלים אפשרית, אם כי יעילותה מוטלת בספק. נוסו בלא הצלחה תרופות אנטינאופלסטיות, סטרואידים, נוגדי דלקת לא-סטרואידיים (NSAID) וטיפולים הורמונליים. לגבי מידת היקף הכריתה עדיין אין נתונים, אך יש עדויות, שהישנות מקומית שכיחה יותר לאחר כריתה לא-מלאה.
ראו גם
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הוושט
- לפרק הבא: כירורגיה של הקיבה והתריסריון
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק