פיזיולוגיה של הקיבה והתריסריון - Gastric and duodenal physiology
הופניתם מהדף פיזיולוגיה של הקיבה והתריסריון לדף הנוכחי.
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הקיבה והתריסריון | |
המזון הנבלע מתערבב בנוזל הקיבה, אבל אינו מתעכל בה, מלבד תהליך מפרק חלבון (פרוטאוליטי) קל. משם עובר הנוזל לתריסריון ומתערבב במיצי הלבלב והמרה. החומצה מנוטרלת על-ידי מיצים אלה. מכיוון שפפסינוגן הופך לפפסין פעיל רק בסביבה חומצית, הרי שלא ייתכן כיב עיכולי (פפטי) בלא חומצה.
הפרשת החומצה בקיבה
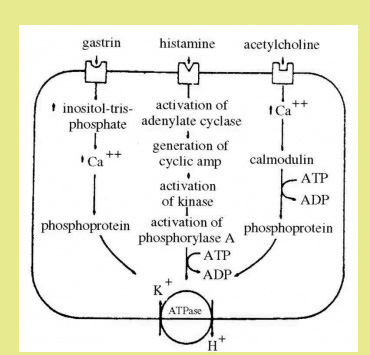
התאים הפריאטליים מפרישים חומצה, והם מסוגלים לרכז יוני מימן פי מיליון מריכוזם בדם. הגורמים המשפיעים על הפרשת החומצה בקיבה הם אצטילכולין, המשוחרר מקצות עצב התועה (הואגוס), גסטרין, אנטרואוקסין, היסטמין וחלבון. התאים הפריאטליים מייצרים ומפרישים כ-170 מא"ק/ל' של יוני מימן, כמות דומה של כלור וכ-7 מא"ק/ל' אשלגן. הנתרן אינו מופרש כלל על-ידי התאים הללו. תאי האפיתל מפרישים נוזל הדומה לנוזל החוץ-תאי, והוא מכיל 150 מא"ק/ל' נתרן בלא יוני מימן. ריכוז המימן בקיבה נקבע על סמך היחס שבין כמות ההפרשה מהתאים הפריאטליים לבין התאים האפיתליאליים. הפרשה זו מושפעת מזרימת הדם בקיבה, בייחוד ברירית. יש שתי דרכי הפרשה: עצמונית ותגובתית. ההפרשה העצמונית נובעת מפעילות רקע של הוואגוס והגסטרין, הגורמים להפרשת חומצה. פעילות זו היא סינרגיסטית. ההפרשה התגובתית נובעת מגירויים שונים של רירית הקיבה על-ידי מזון או גורמים אחרים.
השלב המוחי (צפלי) של הפרשת החומצה
בשלב זה הגירוי עובר דרך גרעיני עצב התועה (הואגוס) במוח המאורך (מדולה - Medulla), המגורים על-ידי ריח, טעם וכו'. בעקבות גירוי הגרעינים, מפריש הוואגוס אצטילכולין, המגרה את רירית כיפת הקיבה (הפונדוס) ואת גוף הקיבה ואלה מפרישים חומצה מהתאים הפריאטליים ופפסינוגן מתאי צ'יף. בתגובה לגירוי הואגוס, מפרישה הרירית של מערת השוער (האנטרום) גסטרין, המגרה אף הוא להפרשת חומצה. התרחבות הקיבה בתגובה לכניסת המזון אליה, מגרה אף היא את הואגוס, דרך הרפלקס הואגו-וגלי, להפרשת חומצה.
השלב הקיבתי של הפרשת החומצה
שלב זה מושפע ממגע ישיר של רירית הקיבה עם מזון, או ממתיחת דופן הקיבה. אלה גורמים להפרשת גסטרין ואצטילכולין. קיים מנגנון של משוב שלילי — כשחומצה שוטפת את האנטרום, הדבר גורם להפסקה בהפרשת הגסטרין. הגסטרין מופרש בהתאם לרמת החומצה בקיבה, כאשר ה-pH יורד לפחות מ-3.5, פוחתת הפרשת הגסטרין. כאשר ערך ה-pH נמוך מ-1.5 אין כלל הפרשת גסטרין.
הגסטרין והשפעתו על הפרשת החומצה
התקדמות רבה חלה בהבנת הפיזיולוגיה והפתופיזיולוגיה של מנגנון הפרשת החומצה על-ידי התאים הפריאטליים. הדעה המקובלת בספרי הלימוד - כאילו הפרשת החומצה מווסתת על-ידי שני מנגנונים נפרדים: בהשפעת הואגוס (עצב התועה) מחד גיסא, ובהשפעה ישירה של גסטרין (G) או היסטמין מאידך גיסא - אינה מדויקת וטעונה הבהרה.
ב-1905 העלה Edkin את ההשערה בדבר קיום הגסטרין. Gregory וחבריו זיהו את הגסטרין ב-1964 והחלו בהפקתו. הוא הורמון המופרש לדם על-ידי תאי G. הגסטרין משפיע על מערכת העיכול בצורות הבאות:
- מגרה את הקיבה להפרשת יתר של פפסין, חומצה, מים ואלקטרוליטים.
- מגרה את הקיבה והמעי לתנועתיות יתר.
- מגרה את הלבלב להפרשת יתר.
- מגביר את טונוס הסוגר התחתון של הוושט.
- גורם להרפית שוער הקיבה.
בכל התופעות שנזכרו, במידה שונה, אפשר לצפות בתסמונת על-שם זולינגר-אליסון, שבה רמת ה-G גבוהה מהרגיל.
בשנים האחרונות נמצא שיש 4 מבנים שונים של G:
- המבנה המובהק, שזיהו Gregory וחבריו, אשר כיום משווקת צורתו הסינתטית. הוא בעל 17 חומצות אמינו (17-G) ונקרא גם הקטן (Little gastrin). הוא משקף כ-90% מסך כל המצוי בדם, ומופרש בעיקר מהאנטרום של הקיבה.
- מבנה ה-G השני זוהה בידי Yellow. הוא מצוי בתריסריון וברירית המעי הדק בכמויות קטנות. בחולים הלוקים בתסמונת זולינגר-אליסון ובלוקים בחסר דם ממאיר (Pernicious anemia) זיהו את העיקרי המצוי בדם Go המורכב מ-34 חומצות אמינו ונקרא Big gastrin. הוא שונה מה-17-G בכך שהתחלת פעולתו מאוחרת, והשפעתו על התאים הפריאטליים ממושכת יותר.
- מבנה ה-G השלישי, ה- Mini gastrin, הוא בעל 13 חומצות אמינו ומשקלו המולקולרי נמוך (13-G). הוא בודד מרקמת גסטרינומה בידי Gregory & Tracy והוא בעל השפעה חלשה יחסית על הפרשת החומצה.
- מבנה ה-G הרביעי, הנקרא Big-big gastrin, עדיין לא בודד ואף לא פוענח, אך ידוע שהוא בעל משקל מולקולרי גבוה ומופרש בתריסריון. הוא מתפרק על-ידי טריפסין ל-13-G.
ה-G הרגיל (17-G) הוא ה-G הפעיל ביותר בנסיוב. כל סוגי האחרים הם למעשה מטבוליטים של אותה תרכובת, כלומר: הגדול הוא פרואנזים, שעל-ידי פירוקו נוצרות התרכובות הפעילות. סוגי ה-G השונים נמצאים בשתי צורות: עם קשר גופריתני ובלעדיו. רמת ה-G בלא הקשר הגופריתני גבוהה יותר בנסיוב ביחס של 1:2.
כ-80% מה-G בדם נוצר באנטרום, וכאמור, כ-90% ממנו 17-G, ואילו בתריסריון נוצרים כ-10% מסך ה-G והוא מסוג 34-G.
ה-G מופרש על-ידי 4 מנגנונים:
- בהשפעת גירוי ישיר על-ידי תוכן הקיבה או המעי, ובהשפעת הרכבו הכימי. לדוגמה, חלבונים, אלכוהול וחומצות אמינו מגרים את מערכת העיכול להפרשת G, בעוד ששומנים וסוכרים יוצרים גירוי חלש.
- בהשפעת התרחבות מכנית של מערת השוער (האנטרום) או קרקעית הקיבה (הפונדוס).
- בהשפעת גירוי עצב התועה (ואגאלי) ישיר על תאי ה-G
- בהשפעה ישירה של חומרים כימיים ופרמקולוגיים המגיעים דרך הדם, או משתחררים בסינפסות. אצטילכולין לדוגמה, משפיע ישירות על תאי ה-G. Epinephrine ו- Norepinephrine הם בעלי השפעה דרך הדם על תאי ה-G השפעה הניתנת לביטול על-ידי חוסמי קולטנים (רצפטורים) α ו-β. סידן משפיע אף הוא דרך הדם על תאי ה-G ולכן רמת ה-G גבוהה בחולים הלוקים בהיפרפאראתירואידיזם.
השפעת על התאים הפריאטליים להפרשת חומצה מורכבת אף היא. לתאים אלה יש קולטנים לגסטרין, לאצטילכולין ולהיסטמין, ואם כי באדם בריא יכולה להיות הפעלה של התאים הפריאטליים על-ידי כל אחד משלושת החומרים האלה, הרי שיש תלות ביניהם, וחסימת הקולטנים לאצטילכולין על-ידי Atropine תביא בעקבותיה גם לחסימת הקולטנים לגסטרין. ממצאים אלה מעידים על הקשר בין הגירויים השונים להפרשת החומצה בקיבה, ועל ויסות עדין, בד בבד עם פעולת גומלין הדדית בין הגירויים הואגאליים לבין הגסטרין.
באחרונה מכירים יותר ויותר בחשיבות ההיסטמין כחומר מוביל גירויים, וכמפעיל העיקרי והאחרון של התאים הפריאטליים להפרשת החומצה. בהעדר היסטמין, או בחסימת הקולטנים להיסטמין על-ידי חומרים כגון חסמי H2, יש נטרול של הגירויים הואגאליים, וגם של השפעת על הפרשת החומצה. חסימה כזו יש בה כדי לשתק את כל צורות הגירויים המופעלים על התאים הפריאטליים. קביעה זו הביאה לפיתוח תרופות לטיפול שמרני יעיל בכיב עיכולי, על-ידי מציאת חוסמים יעילים לקולטנים H2.
לאחר חיתוך הואגוסים רמת החומצה בקיבה יורדת, ובד בבד עולה רמת החומצה בדם פי 3-2. במתן גירוי ישיר מרבי על-ידי היסטמין או Pentagastrin יורדת יכולת הפרשת החומצה בכ-65% לעומת הרמה ששררה לפני הניתוח. פירוש הדבר, אין השפעה של ממש על התאים הפריאטליים להפרשת חומצה לאחר חיתוך העצבים, אף שרמתו בדם גבוהה. לעומת זאת, בניתוחי כריתת קיבה, כשנכרת האנטרום, יש ירידה מקבילה ברמת הגסטרין והחומציות גם יחד, אך ירידת חומציות זו אפשר לבטל על-ידי מתן Pentagastrin. בהעדר G, לאחר כריתת קיבה חלקית, מופחתת באורח ניכר התגובה החומצית לגירויים ואגאליים, אף כי הן הואגוסים והן התאים הפריאטליים לא נפגעו. עובדות אלו מוכיחות שוב את המנגנון המשולב של גירויים ואגאליים בנוכחות G והיסטמין.
לאחר ניתוחי כריתת קיבה לפי בילרות' 2 נצפתה רמת G נמוכה מאשר לאחר בילרות' 1, גם כאשר הייתה ירידה זהה ברמת החומציות. הבדל זה נובע מנוכחות תאי G המפרישים גסטרין בתריסריון. לאחר ניתוחי בילרות' 1 הגירוי רב יותר, עקב מעבר מזון מהקיבה לתריסריון, להפרשת גסטרין חוץ-קיבתי, בעוד שבניתוח בילרות' 2 התריסריון נעקף. עלייה ברמת הגסטרין הוכחה בשלוש הצורות של הואגוטומיה (כריתת עצב התועה), ולכן הועלתה ההשערה בדבר קיומם של סיבי עצב בעלי השפעה בולמת על תאי ה-G שחיתוכם בזמן חיתוך הואגוס משחרר את תאי ה-G להפרשת יתר. השערה זו עדיין לא הוכחה, אך עם זאת ידוע כי רמת הגסטרין נמוכה יותר לאחר ואגוטומיה על-ברירנית מאשר אחרי ואגוטומיה שלמה. הסבר אחר לעליית לאחר ניתוחי חיתוך הואגוס, קשור בעלייה של רמת ה-pH, הגורמת לגירוי האנטרום ולהפרשת גסטרין. כמו-כן מופיע לאחר הניתוחים רפיון הקיבה, שאף הוא מגרה את תאי ה-G להפרשה. תופעות אלה בולטות ביחס הפוך לאיכות ניקוז הקיבה.
גסטרין, כולציסטוקינין, סקרטין, גלוקוגן, GIP ו-VIP פועלים על אותו איבר מטרה, ולכן חוסמים זה את פעולתו של זה. הגסטרין מתפרק בקורטקס של הכליה, ואולם תוצרי הפירוק אינם מופיעים בשתן. בחולים הלוקים באי-ספיקה כלייתית ניתן למצוא רמות גבוהות של גסטרין עקב הירידה בכושר פירוק הכליות את הגסטרין.
ריכוז הגסטרין התקין הוא 100-50 פיקוגרם למ"ל. חולי כיב מפרישים לרוב כמויות תקינות של גסטרין, אך בתגובה למזון מתרחשת אצלם הפרשת יתר של גסטרין, הגורמת להפרשת יתר של חומצה. מצב זה נובע מהפרעה במנגנון המשוב (פידבק) המעכב הפרשת גסטרין.
היסטמין
ההיסטמין (Histamine) מגרה להפרשת חומצה בקיבה. הוא מגרה חלש יותר מאשר הגסטרין. הסברה היא, שההיסטמין הנוצר בתאי מאסט של רירית הקיבה הוא המתווך של הגירויים על-ידי עצב התועה (הואגוס) והגסטרין, ופעולתם מתבצעת דרכו. ההוכחה העקיפה היא העובדה, שאפשר לחסום את פעולת הגסטרין והאצטילכולין, על-ידי מתן חוסמי H2, כגון Cimetidine. מתברר שלאחר חיתוך הואגוסים קטנה השפעת ההיסטמין, ולכן המסקנה הנוספת היא שלואגוס השפעה על התא הפריאטלי והופך אותו רגיש יותר להיסטמין (איור 4.3).
לאחר כריתת הואגוסים מצאו Troidel וחבריו עלייה ברמת ההיסטמין בתוך רירית הקיבה של המנותחים בהשוואה לבני אדם בריאים. נמצא שרמת ההיסטמין התוך-תאי בחולי כיב התריסריון היא נמוכה מאוד. ההסבר לכך הוא, שההיסטמין בחולי כיב התריסריון משתחרר בכמות רבה יותר וגורם להפרשת יתר של חומצה, ולכן כמות ההיסטמין הנותרת בתאי המאסט קטנה. שחרור ההיסטמין מבוקר על-ידי הואגוסים. כשטונוס הואגוס מוגבר, כמות ההיסטמין המשתחררת עולה, ואולם אם מנתקים את הואגוסים, כמות ההיסטמין המשתחררת יורדת והוא מצטבר בתאים.
בכריתה לא שלמה של הואגוסים ניתן למצוא ירידה ברמת ההיסטמין בתאים, בעוד שבחולים שבוצעה בהם ואגוטומיה על-בררנית רמת ההיסטמין נותרה כפי שהיא בבני אדם בריאים.
ריר
הריר מופרש על-ידי תאי הצ'יף של צוואר בלוטות הקיבה. עיקר הפרשת הריר היא באנטרום, ולו מייחסים חלק נכבד במנגנון ההגנה של הרירית מפני החומצה והפפסין.
הריר מורכב מ-3 מרכיבים עיקריים:
- מוקואיד - המורכב ממולקולות של גליקופרוטאין אשר עבר עליהם תהליך פולימריזציה והן בעלות משקל מולקולרי הגדול מ- 3x106
- חלבונים הזהים בהרכבם לאלה של הפלזמה, ומכילים אלבומין ואימונוגלובולינים שלא ברור אם מקורם מהתאים או מהפלזמה, והם מסוגלים לפעול מבחינה אימונולוגית בעיקר פעילות בולמת חיידקים (בקטריוסטטית).
- פוליפפטידים שתפקידם עדיין אינו ברור.
הריר בנוי מפולימר רשתי של גליקופרוטאין המוחזק בקשרים כימיים, ובין המולקולות יש מעברים המאפשרים מעבר חומצה ושאר הפרשות של הבלוטות. החלבונים נמצאים בתוך רשת הגליקופרוטאינים, ולכן מוגנים מפני עיכול של פפסין ומיצי העיכול האחרים. הקשרים הסבוכים של הריר יוצרים כיסוי סמיך שלו על רירית שלא מתפרקת בקיבה. תנועות הקיבה והמזון בתוכה מקלפות באיטיות את הריר, ומתחתיו נוצר כל העת ריר חדש. האלמנטים החופשיים הבסיסיים של הריר מקנים לו pH בסיסי, המאפשר נטרול החומצה הבאה במגע אתו.
הפרשת הריר מושפעת מכמה גורמים:
- הגורם המדרבן ביותר ליצירת הריר הוא ה-pH של הקיבה, במיוחד באנטרום. ככל שה-pH נמוך יותר, נוצר יותר ריר. תהליך זה נבלם על-ידי כריתת הואגוסים. הכריתה גורמת לשינוי בהרכב הריר, כך שיש בו יותר חומצה סיאלית והקסוזות.
- הואגוס והמערכת הסימפתטית משפיעים על כמות הריר הנוצר.
- סרוטונין מגביר את הפרשת הריר, וכן משנה את המבנה שלו. החומצה משפיעה על יצירת הריר דרך הסרוטונין ולא דרך מערכת העצבים.
- חומרים כגון Heparin וסקרטין מגבירים את הפרשת הריר.
- הורמון הפאראתירואיד מגביר את הפרשת הריר, וייתכן שזו הסיבה להיווצרות כיבים בתריסריון ולא בקיבה בחולים הלוקים בפעילות יתר של בלוטות הפאראתירואיד.
- מזון מדכא את יצירת הריר.
- ברעב, יש ירידה ביצירת הריר.
- תרופות שונות משפיעות על ירידה ביצירת הריר. Acetylsalicylic acid מעכבת את ההידרוגינציה של החומצה הגלוקורונית, שהיא מרכיב חשוב ביותר במבנה הריר, ובעקבות זאת נפגמת איכות הריר וכמותו פוחתת. כמו-כן, החומצה הסלצילית מעכבת יצירת ATP בתוך תאי הקיבה, על-ידי הפרעה בתהליכי חמצון קרום התא. בכך, לדעת חוקרים, משמשת החומצה הסלצילית הדק ביצירת הגליקוליזה התוך-תאית וביצירת ה-ATP. ההפרעה בחמצון נובעת מכך, שהחומצה הסלצילית נושאת קבוצה הידרוקסילית ארומטית המתחמצנת בקלות ומפריעה בחמצון קרום התא. ה-Epinephrine וה-Norepinephrine מפחיתים אף הם את יצירת הריר, ולכן חושפים את הקיבה, במצבי דחק, לפעילות הרסנית של החומצה והפפסין.
כל מנגנון המפר את האיזון שבין הפרשת הריר לבין כמות החומצה והפפסין חושף את הקיבה להופעת כיבים.
מנגנון ההגנה הנקרא גם Cytoprotection מושפע על-ידי הפרוסטגלנדינים, בייחוד מהקבוצה של ה-PGE2 (Dinoprostone), ומגדיל את כמות הריר ואת כמות הביקרבונט המופרש. הפרוסטגלנדינים האחרים מגבירים את זרימת הדם ברירית, את פעולת משאבת הנתרן-כלור ואת ייצור ה-AMP.
שלב המעי
חלבונים והתרחבות המעי הדק האמצעי מגרים להפרשת חומצה. גירוי זה מועבר על-ידי הורמון אנטרואוקסיטין. השפעת השלב האינטסטינלי היא בעיקרה השפעה מעכבת. נוכחות מזון חומצי במעי גורמת לעיכוב בהפרשת החומצה בקיבה.
מדידות של הפרשות הקיבה
באופן ניסיוני ניתן למדוד את הפרשת החומצה בקיבה בבעלי חיים, על-ידי יצירת כיס מקטע הקיבה וניתוק העצבוב (Heidenhain poach), או כיס בעל עצבוב, כגון כיס Pavlov. בבני אדם מבצעים את המדידות על-ידי שאיבה דרך הזונדה, שמיקומה נקבע בעזרת שיקוף רנטגן. מיצי הקיבה נאספים אחת ל-15 -30 דקות. דגימה ראשונה אינה נחשבת, ואילו דגימה שנייה מהווה את ההפרשה הבסיסית, והיא נמדדת כריכוז חומצה ב- mEq/L או כ- BAO (Basal acid output) ב- mEq/H. לאחר קביעת הרמה הבסיסית מזריקים חומר המגרה להפרשת חומצה, כמו Pentagastrin או היסטולוג, מודדים את הפרשת החומצה, ועל-ידי כך קובעים את ה-MAO (Maximal acid output). במדידות יש לציין כמה משתנים:
- זכרים מפרישים יותר מנקבות.
- לאחר גיל 50 מפרישים פחות.
- הכמות המופרשת, בממוצע, בחולים הסובלים מכיב עיכולי (פפטי) היא כפולה מזו שבאוכלוסייה רגילה. אמנם 60% מהחולים מפרישים חומצה בתחום התקין, כ-27% מהחולים הסובלים מכיב מפרישים חומצה בעלת רמת בסיס תקינה, ואילו 35% מפרישים חומצה בעלת רמה תקינה בתגובה למגרים.
- בחולים הסובלים מכיב קיבה רמות החומצה נמוכות מהרמות התקניות.
חולים בעלי רמות גבוהות יותר של חומצה סובלים מתסמינים בולטים יותר, וכן מסת התאים הפריאטליים בהם גדולה יותר, באופן ראשוני או משני. יותר חולים בקבוצה זו יזדקקו לטיפול ניתוחי. חולים בלא חומצה בקיבה לא יפתחו כיב עיכולי, ולכן הכיבים בחולים אלה הם ממאירים.
מה מעכב את הפרשת החומצה?
כאשר ה-pH יורד, הפרשת החומצה קטנה, עקב ירידה בגסטרין. חומצה, שומנים ונוזלים היפרטוניים מעכבים את הפרשת הקיבה. הורמונים המופרשים מהתריסריון כגון סקרטין או GIP, מדכאים את הפרשת הקיבה, בין השאר דרך עיכוב הגסטרין.
תנועתיות הקיבה
בשונה משאר המעי, הקיבה מורכבת מ-3 שכבות שרירים. השכבה החיצונית ביותר בנויה משרירים אורכיים, השכבה מתחתיה בנויה משרירים מעגליים, והשכבה הפנימית בנויה משרירים אלכסוניים. באזור האנטרום השכבה המעגלית מתעבה והופכת לשוער הקיבה.
קיבה ריקה מכילה כ-50 סמ"ק נוזל, היא יכולה להתרחב עד 1,500 סמ"ק בלא יצירת מתח על הדופן, כלומר בלא שינוי באורך הבסיסי של השרירים, ולכן שומרת על כושר התכווצות זהה בגדלים שונים - Receptive relaxation. במצב מנוחה כשהקיבה ריקה, יש התכווצויות, אחת ל-20-15 דקות. כשמזון נכנס לקיבה, קצב ההתכווצויות עולה בהדרגה.
פעילות הקיבה מתבטאת בגלי ניע (Peristalsis) מובהקים, המתחילים בפי הקיבה (קרדיה) ונעים לעבר השוער (פילורוס). כשהמזון מגיע לקיבה, הגלים מתחזקים בקרדיה ונחלשים בהגיעם לפילורוס. גלים אלה מתגברים בעוצמתם עם הזמן ונוטים להתחזק. קצב הגלים הוא 4 בדקה.
ההתכווצות הבסיסית של הקיבה נובעת מגירוי עצבי בתוך דופן הקיבה, המתחיל בגירוי של הרחבת הקיבה. סיבים אלה שולחים גם סיבים מביאים (אפרנטיים) לעצב התועה וגורמים לגירוי הואגוס.
האנטרום, שהוא בעל שריר מעגלי עבה יותר, שואב את המזון לתוכו בזמן התכווצות. בזמן מנוחה השוער פתוח והשריר במצב מנוחה (Relaxation). לכן, אין מפל לחצים בין הקיבה לתריסריון וזה מונע את יציאת הנוזל מהקיבה. כאשר האנטרום מתכווץ כיחידה אחת, השוער מורפה, ונוצר מפל לחצים בין האנטרום לתריסריון, ולכן המזון נדחף לתריסריון. כמויות המזון העוברות הן קטנות יחסית (כמה מ"ל). בסוף מעגל זה השוער מתכווץ, האנטרום מתרפה, וגל חדש של התכווצות מתחיל בקרדיה.
התכווצות הקיבה מבוקרת על-ידי ה-pH . pH חומצי מקטין את גלי ניע הקיבה. הדבר בולט במיוחד כשה-pH יורד לפחות מ-3.5. נוזלים חמים או מרוכזים מקטינים את קצב ניע הקיבה ואת התרוקנותה. ההשפעה במקרים אלה היא דרך ההורמונים המופרשים על-ידי המעי, כגון סקרטין, אנטרוגסטרין וכולציסטוקינין. שומנים מעכבים את התרוקנות הקיבה.
לאחר כריתת הואגוסים עולה טונוס השריר הסוגר את השוער ובד בבד תתרחש הרפיה של האנטרום. לאחר חיתוך השוער (פילורופלסטיקה) נותר הפילורוס פתוח והאנטרום רפה, ולפיכך תתקבל האטה במעבר מוצקים. לעומת זאת נוזלים יעברו מהר יותר.
ראו גם
- לנושא הקודם: אנטומיה של הקיבה והתריסריון - Gastric and duodenal anatomy
- לנושא הבא: כיב עיכולי (פפטי) - Peptic ulcer
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הצפק
- לפרק הבא: כירורגיה של המעי הדק
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק