הלם - Shock
הופניתם מהדף הלם - shock לדף הנוכחי.
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | הלם | |
הלם הוא מצב המתבטא במכלול של סימנים הנגרמים כתוצאה מאספקת דם לקויה לרקמות הגורמת להיפוקסיה תאית ולהפרעות בפעילות האיברים החיוניים ברמה התאית.
תת-פרפוזיה ברמה התאית יכולה להיגרם על-ידי כל אחד מהתהליכים הבאים:
- ירידה בנפח הדם - Hypovolemic shock
- ירידה בזרימת הדם עקב כישלון הלב - Cardiogenic shock
- ירידה בתנגודת פריפרית כמו בחבלות עמוד שדרה עם איבוד השליטה של המערכת האוטונומית על כלי הדם – Capacitance shock
- הלם זיהומי מטופל חלקית או לא מטופל - Septic shock
השוק ההיפוולמי יכול להיגרם כתוצאה מדימום, מהקאות, משלשולים, מחסימת מעי, מהצטברות הנוזל במעי ומאידוי מרובה כמו בכוויות וכדומה. כל דבר הגורם לאובדן של נוזלים בדרך לא פיזיולוגית יגרום לירידה בנפח הדם עד להיווצרות שוק. בשוק היפוולמי הגוף מגיב לירידה בנפח הדם על-ידי הפרשה של ואזופרסין ואנגיוטנסין הגורמים להתכווצות של הונולות והוורידים הקטנים בכל הגוף ולכיווץ של העורקים הקטנים בעור, ברקמת השומן, וברקמות חיבור עצמות שרירי השלד, המעי, הלבלב, הטחול והכבד, אבל לא של המוח והלב. התכווצות הונולות גורמת להזרמת דם לכלי הדם הגדולים וללב, מעלה את הנפח ה-End-diastolic ואת תפוקת הלב. התכווצות הארטריולות מסיטה את זרימת הדם מרקמות הסובלות איסכמיה לאלה הרגישות לאיסכמיה. בנוסף הפרשת אלדוסטרון ווזופרסין מעלה את הספיגה של מים ונתרן בכליות ובכך מקטינה את אובדן הנוזלים דרך השתן.
שוק קרדיוגני יכול להיגרם עקב הפרעות בקצב הלב, הפרעה בהתכווצות הלב עקב אוטמים, פגיעות במסתמים, קרדיומיופתיות וכו'. בכל האירועים הללו תפוקת הלב יורדת ולכן נגרם מחסור יחסי בדם מחומצן ברקמות, ושוק.
Capacitance shocks עקב אובדן השליטה של המערכת הסימפטטית מתרחבים כלי הדם הקטנים וכתוצאה מכך ישנה צבירה של דם במערכת הקפילרית. נפח הדם בכלי הדם הגדולים יורד וכתוצאה מכך מופיעים סימני ההלם.
הלם ספטי נגרם על-ידי מוקד מזוהם בגוף אשר אינו מטופל או אינו מטופל כראוי. חיידקים הנמצאים במוקד הזיהומי מייצרים טוקסינים המתפשטים וגורמים לירידה בטונוס כלי הדם, ולהיפוולמיה בגלל פגיעה במחסום האנדותלילי ובריחת נוזל לרקמות.
פתופיזיולוגיה
באופן נורמלי חלק גדול מנפח הדם נמצא במערכת הוורידית. החזרה של דם מהמערכת הוורידית ללב יוצרת את End diastolic pressured הקובע את תפוקת הלב. כאשר זרימת הדם דרך הארטריולות עולה, הלחץ במערכת הוורידית עולה, הוורידים מתרחבים באופן פסיבי, נפח הדם בתוכם עולה ונפח הדם היוצא מהם נשמר - כך שתפוקת הלב נשמרת. כאשר הזרימה בארטריולות יורדת, מתכווצות הארטריולות וגם הקפילרות הוורידיות, ועל-ידי כך גוברת זרימת הדם ללב ונשמרת תפוקת הלב. רוב השינויים בלב נורמלי מקורם בשינויים Preloads. המיטה הוורידית היא המווסתת את Preloads. מערכות ורידיות שונות מגיבות בצורה שונה לירידה בתפוקת הלב. ורידים במערכת השרירים מראים תגובה חלשה בלבד לגירוי סימפטטי, אולם שינויים ביחס שבין כוחות הגרביטציה למשאבת השרירים גורמים להתכווצות של מערכת ורידים זו. לעומת זאת הגירוי של המערכת הסימפטטית גורם להטיית הזרימה מהמערכת הספלנכנית לצירקולציה, וכך נוצרת זרימה של נפחי דם גדולים לצירקולציה. בזמן דימום הגירוי הסימפטטי גורם להטיית זרימת הדם מהמערכת הספלנכנית מחד ולהתכווצות המיטה הקפילרית בעור מאידך, ויוצר את השינויים האופייניים לשוק. באופן נורמלי איבוד נוזלים גורם לתגובה כלייתית. בתגובה להפרשה של אנגיוטנסין, רנין והורמון אנטידיאורטי - הכליה מגיבה בספיגת נוזלים ומלחים מוגברת וכתוצאה מכך קטן אובדן הנוזלים דרך השתן. תגובה זו היא איטית ולכן אינה מאפשרת מענה הולם לשינויים חדים בתפוקת הלב. בניסיון למלא את החסר הנגרם על-ידי Preloads הנמוך מגיב הלב לירידה בתפוקה על-ידי עלייה בדופק, כך שבכל דקה הלב מתכווץ יותר פעמים ובכך מזרים נפח דם גדול יותר לדקה.
ה-Afterload הוא הלחץ הקיים במערכת הדם, ועליו הלב צריך להתגבר בזמן התכווצותו. הלחץ העורקי הוא המרכיב העיקרי של ה-Afterload אשר משפיע על ה-Ejection fraction. המרכיבים הקובעים את הלחץ הזה הם הסוגרים הפרה-קפילריים וצמיגות הדם. כאשר ה-Afterload גובר - תפוקת הלב יכולה להישמר על-ידי עלייה Preloads. עלייה זו גורמת למתח גבוה יותר של שריר הלב, ולכן לפי אפקט סטרלינג הלב מתכווץ חזק יותר ומתגבר על Preloads.
בשוק - בגלל הירידה בנפח האפקטיבי של הדם בכלי הדם, אין די בפעולתו של מנגנון הפיצוי כדי לשמור כראוי על תפוקת הלב וכתוצאה מכך יחול גירוי סימפטטי מוגבר. הפרשת היתר של הקטכולאמינים בתגובה לגירוי הסימפטטי תגרום להתכווצות המיטה הקפילרית במטרה להעלות את Preloads. כאשר איבוד נפח הדם הוא קטן - מנגנון זה הוא יעיל; אולם עם המשך אובדן נפח הדם - אין די במנגנון זה, דבר שיתבטא בירידה בלחץ הדם ובטכיקרדיה ולבסוף בשינויים מנטליים עד תרדמת, דום לב ומוות.
במקביל לשינויים הללו כל מערכות הגוף מגיבות הן בניסיון לשמר את נפח הדם והן כתגובה משנית לניסיונות הללו. התגובה של כל המערכות מסוכמת בצורה מפורטת בפרק "חבלות" - התגובה לטראומה.
היפוולמיה היא פקטור חשוב ביותר בשלבים הסופיים של כל הגורמים להלם. השינויים הראשוניים הנגרמים על-ידי איבוד נפח חיצוני - דם או נוזלים - כמו בדמם, בכוויות, בהתייבשות, בחסימות מעי וכו' אינם דורשים דיון מיוחד. אולם השינויים המשניים הקשורים לשינויים התוך-תאיים, הנגרמים על-ידי תת-פרפוזיה רקמתית, אינם מובנים במלואם. השינויים הללו מתרחשים בעקבות השינויים בפרמאביליות של כלי הדם, הנובעת מחדירות גבוהה של תאי האנדותל, כתוצאה מפגיעה במחסום האנדותלילי.
איבוד משני של נוזלים, המתרחש בעקבות תת-פרפוזיה ממושכת של הרקמות, הוא הסיבה העיקרית לאובדן נפח הדם באלח-דם. הדלף דרך האנדותל יכול להיגרם על-ידי מספר רב של גורמים: שפעול של Hageman factor, אשר גורם לשחרור קינינים, במיוחד בראדיקינינים, יצירה של Procoagulant factors עם שפעול של מערכת הקרישה, הגורמת לפקקת מפושטת במיקרוצירקולציה. צבירה של נויטרופילים וטסיות במיקרוצירקולציה גורמת לפקקת בה, ולהרס משני של תאי האנדותל. מטבוליזם מוגבר של Arachidonic acid, המצויה במרבית התאים גורם ליצירת Vasoactive eicosanoids, הגורמים לשינויים בחדירות האנדותל. יצירת היפראוקסידים (,O2- ,H2O2, OH), הגורמים נזק לאנדותל ופקקת של המיקרוצירקולציה. מצב ההיפוולמיה הראשונית מוחמר בצורה ניכרת בעקבות פעולתם של הגורמים הללו, כך שמצב ההלם כולל הלם היפוולמי ראשוני ו-Capacitance shock. הירידה בתנגודת הפריפרית מגדילה את נפח הדם המצוי במערכת הוורידית, וכנראה גם גורמת לפתיחת דלפים ארטריו-ונוזיים המחמירים עוד יותר את מצב ההיפוולמיה.
התגובה הראשונית של מנגנון ההגנה של הגוף לירידה בנפח הדם, היא הוצאת נוזלים מהאינטרסטיציום לכלי הדם. כאשר ההלם מתמשך, כתוצאה ממנגנון זה, זרימת הדם במיקרוצירקולציה קטנה, וכתוצאה מכך נפגעות מספר פונקציות תאיות, במיוחד משאבת הנתרן-אשלגן שבדופן התא. פגיעה זו גורמת לתנועת נוזלים, יחד עם הנתרן, לתוך התאים ומקטינה את נפח הדם. השינויים הללו גורמים גם לשינוי פוטנציאל הממברנה של התאים, המשתנה מ-90- ל-60-. כתוצאה מהזרימה הלקויה במיקרוצירקולציה נוצרת חמצת מטבולית מקומית, המלווה בצבירת לקטט היכולה להתפתח מאוחר יותר לחמצת מטבולית מערכתית. הירידה בנפח הדם הנובעת מהאמור לעיל מחייבת טיפול על-ידי מתן נוזלים לווריד.
אבחנה
הסימנים הראשונים של שוק הם:
- Postural hypotension
- חיוורון של העור
- הזעה קרה
- שקיעה של ורידי הצוואר
- שתן מרוכז
- ירידה בכמות השתן
- דופק מהיר
- לחץ דם ירוד
- בלבול, שינויים בהכרה
- צמא
במצב שכיבה לחץ הדם של חולה השרוי בהלם תת-נפחי קל יהיה תקין אבל אם יושיבו את החולה ירד לחץ דמו ב-10 מילימטר כספית ויותר, ויישאר נמוך למספר דקות לפחות. לעיתים ניתן למצוא לחץ דם סיסטולי תקין ולחץ דם דיאסטולי גבוה כביטוי להתכווצות של כלי הדם הפריפריים בשוק. חולים המאבדים יותר מ-20% מנפח הדם יראו סימנים של עור חיוור, קר ורטוב. אם מופיעה גם ירידה במתן השתן - האיבוד הוא של 30% לפחות; כאשר החולה מבולבל, לא מתמצא בזמן ובמקום - האיבוד הוא גדול אף יותר. הסימנים העוריים מקורם בהפרשת הקטכולאמינים אשר גורמים להתכווצות כלי הדם הקטנים בעור וכתוצאה מכך מתקבל עור חיוור וקר. הקטכולאמינים גם משפעלים את מערכת ההזעה וגורמים להפרשת זיעה; מכיוון שהעור קר - גם הזיעה קרה. מילוי הדם בעור אצבעות הרגליים הוא מדד טוב לאובדן דם. לחץ על הבוהן גורם להלבנתה אולם הצבע חוזר לאחר פחות משתי שניות. אם הזמן הנדרש הוא רב יותר - לחולה יש היפוולמיה. יש לזכור שמצבים הגורמים להפרשת יתר של קטכולאמינים כמו מצבי פחד וחרדה יתנו סימנים דומים. תפוקת השתן חשובה מאוד - מיעוט שתן (oliguria) מוגדר במבוגר כתפוקת שתן הקטנה מ-0.5 סנטימטר קוב לקילודרם לשעה, ובילד כ-1 סמ"ק לק"ג לשעה.
בחולים הלוקים בתת-נפח (היפוולמיה) קל (אובדן נפח הדם > 20%) - חולים המתלוננים על קור, ניתן למצוא:
- שינויים בלחץ הדם ובדופק במעבר משכיבה לישיבה
- העור חיוור וקר
- השתן מרוכז והוורידים נפולים
בחולים הלוקים בתת-נפח בינוני (20%-40% אובדן נפח דם) - חולים המתלוננים על צמא ויובש בפה, ניתן למצוא בבדיקה:
- ירידה בלחץ דם
- דופק מהיר
- מיעוט שתן
בחולים בתת-נפח קשה (אובדן של יותר מ-40% מנפח הדם) —חולים באי-שקט פסיכומוטורי, ניתן למצוא:
- נשימה עמוקה ומהירה
- לחץ דם ירוד
- דופק מהיר וחלש
בחולים הלוקים בהלם קרדיוגני ניתן למצוא:
- ורידים גדושים
- בצקות פריפריות
- כבד מוגדל ורגיש
- ניתן לשמוע קול שלישי מעל הלב
- חרחורים מעל הריאות
- באק"ג ניתן לראות שינויים איסכמיים או הפרעות קצב קשות
- בצילום חזה ניתן לראות לב גדול וגודש ריאתי
בחולה הלוקה בהלם ממקור זיהומי ניתן למצוא: 1*היפרתרמיה ובחלק מהחולים אף היפותרמיה.
- צמרמורות מלוות בירידה בלחץ דם ובטכיקרדיה
- שינויים במצב הכרה עם אי-שקט פסיכומוטורי
- "רעב" לאוויר
- מיעוט שתן
- במעבדה ניתן למצוא חמצת מטבולית, לויקוציטוזיס עם סטייה שמאלה, הפרעות בקרישת הדם, תרביות דם חיוביות וכו'. כל אלה בנוסף לסימנים המתפתחים של היפוולמיה (תיאור מפורט ראה בהמשך בסעיף הלם זיהומי)
טיפול
ההתפתחויות בפעולות ההחייאה הן רבות. הגישה לחולים בהלם השתנתה, מגישה אמפירית לגישה פיזיולוגית, תוך התקדמות בהבנת הפתופיזיולוגיה של התהליכים המתרחשים. פעולות ההחייאה חייבות להתבצע באופן הגיוני, כאשר עדיפות ראשונה ניתנת למערכות החיוניות ביותר שפגיעה בהן תגרום לאיום על חיי החולה. לכן חוק הקדימויות לטיפול - ABC שריר וקיים, כאשר ה-A מייצג נתיב אוויר חופשי, ה-B מייצג נשימה אפקטיבית ועצירת דימום שגורם לאוקסנגבינציה, וה-C מייצג שמירה על צירקולציה ופרפוזיה טובה של הרקמות. לאחר פעולות אלה אפשר לגשת לאבחון מדויק ותיקון השינויים הפתופיזיולוגיים שלא טופלו עד שלב זה.
הירידה בנפח הדם מחייבת טיפול על-ידי מתן נוזלים במטרה להחזיר את נפח הדם שהלך לאיבוד ובכך לשפר את הפרפוזיה הרקמתית. בחולה נפגע בשוק יש להחדיר צנתר בעל קוטר רחב לווריד (עדיף שניים), ודרכו להזליף נוזלים. במקביל חשוב לעקוב אחר תפוקת השתן ולשם כך יש להחדיר צנתר לשלפוחית. בחלק מהחולים המבוגרים יותר, עם בעיות לבביות, כלייתיות, ריאתיות וכו', רצוי להחדיר צנתר לווריד מרכזי ולעקוב אחר השינוי ב-CVP כתגובה למתן הנוזלים.
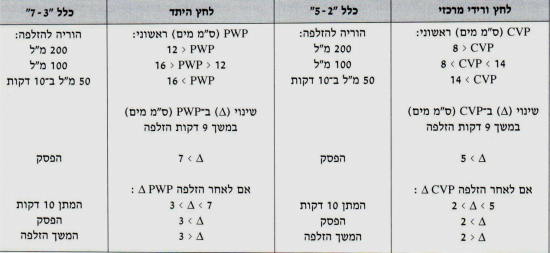
מתן מהיר ובטוח של נוזלים מחייב בקרה מתמדת של לחץ ורידי מרכזי או של לחץ היתד, כדי למנוע העמסת-יתר. הכמות הראשונה הניתנת בעירוי נקבעת בהתאם ללחץ המילוי הראשוני (לחץ ורידי מרכזי - CVP, או לחץ היתד - PWP), ואילו ההחלטה על מתן כמות נוספת נקבעת בהתאם לתגובת לחץ המילוי לכמות הנוזל שהוזלפה. לדוגמה, לחולה עם CVP ראשוני קטן מ-8 ס"מ מים, יש להזליף 200 מ"ל נוזל בווריד היקפי תוך 10 דקות. אם תוך זמן העירוי או לאחריו עולה ה-CVP ביותר מ-5 ס"מ מים, מופסק העירוי המהיר; אם לאחר העירוי עולה ה-CVP בפחות מ-5 ס"מ מים אך יותר מ-2 ס"מ מים - יש לחכות 10 דקות; אם גם אז ה-CVP נשאר גבוה מערכו הראשוני ביותר מ-2 ס"מ מים, יש להפסיק את העירוי המהיר. אם ה-CVP עולה בפחות מ-2 ס"מ יש להמשיך את הזלפת הנוזלים עד לתיקון מצב ההלם, או עד לחריגה מכלל ה-"5-2" שהוזכר לעיל. בכל מקרה, הלחץ הנמדד מיד לפני כל הזלפה, משמש כערך ההתייחסות למדידות הבאות. בצורה דומה יש לפעול, אם משתמשים בלחץ היתד כמדד לחץ המילוי, אלא שאז משתנה הכלל ל-"7-3" (טבלה 1.17).
יש מספר תמיסות שבהן משתמשים לצורך החייאה, ותיאור של כמה מהן, על יתרונותיהן וחסרונותיהן, יפורט בהמשך.
(Balance Salt Solutions (BSS
הבסיס לשימוש ב-BSS הוא:
- בזמן הלם ממושך, או חמור, קיים איבוד אובליגטורי של נוזלים איזוטוניים לא רק מכלי הדם אלא גם מהאינטרסטיציום. נוזלים אלה יש להחליף בנוזלים אשר יגיעו במהירות לשיווי משקל דינמי עם הנוזלים החוץ-תאיים
- לא הוכח שקיימת עלייה בשיעורי התחלואה והתמותה כתוצאה משימוש בנוזלים אלה
- אין עלייה בשכיחות של פגיעות במערכות אחרות של חולים שבהם ההחייאה בוצעה על-ידי BSS
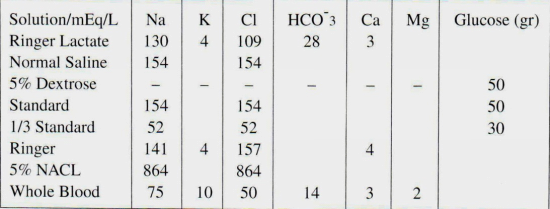
סוגי התמיסות השונות והרכבן מסוכמות בטבלה 2.17.
Shires וחבריו מדדו את נפח הדם ונפח הנוזל החוץ-תאי בחיות שנחשפו לאיבוד נוזלים בשיעורים שונים. הם מצאו, שבחיות שאיבדו כ-10% מנפח דמם, שיעור אובדן הנוזלים מכלי הדם ומהאינטרסטיציום היה שווה. לעומת זאת, כאשר החיות איבדו 25%-50% מנפח דמם, שיעור איבוד הנוזלים מהאינטרסטיציום היה גבוה בהרבה מזה של כלי הדם. ממצא זה מרמז על כך שקיימת חלוקה מחדש של נוזלי הגוף במצב זה.
כאשר ניסו לתקן את ההיפוולמיה על-ידי מתן דם נמצא שתיקון נפח הדם לא גרם לתיקון מקביל של הנפח האינטרסטיציאלי. מצב זה נמשך גם כאשר נפח הדם תוקן על-ידי דם ופלזמה. לעומת זאת, כאשר תיקון נפח הדם בוצע על-ידי דם ו-BSS - הנפח האינטרסטיציאלי חזר לתקנו במקביל לנפח הדם. בחיות בהלם קשה שטופלו על-ידי דם בלבד נמצאו שיעורי תמותה של 80%. כאשר הוסיפו לטיפול פלזמה - שיעורי התמותה ירדו ל-70%. לעומת זאת בחיות שטופלו על-ידי BSS בתוספת דם, שיעורי התמותה היו 30%.
בהלם קל, המטופל במהירות, איבוד הנוזלים האינטרסטיציאלי הוא מינימלי. אולם בהלם ממושך או חמור אובדן הנוזלים מהאינטרסטיציום הוא משמעותי. רק חלק קטן מהנוזלים הללו מחליף את הנוזלים בכלי הדם. בדרך זו ניתן להשלים רק כ-10%-20% מנפח הדם החסר בכלי הדם. רוב נפח הנוזלים החסרים במדור הבין-תאי, הם נוזלים שחדרו לתאים עצמם. לכן בתגובה למתן נוזלים ולשיפור בזרימת הדם, חלה עלייה באוסמולליות של הנוזל במדור הבין-תאי, וזו גורמת ליציאת הנוזלים מהתאים למדור הבין-תאי.
כניסת הנוזלים לתאים נובעת מהפרעה במשאבת הנתרן-אשלגן שבדופן התא, המוציאה את הנתרן מהתא ומכניסה אשלגן לתוכו, בניגוד למפל הריכוזים; ולכן זו משאבה אקטיבית, הדורשת אנרגיה ותלויה ATP-ASE. מפל הריכוזים הנוצר בין פנים התא לסביבתו החיצונית יוצר פוטנציאל חשמלי על פני ממברנת התא. בחיות הנתונות בהלם, נמצא שריכוז האשלגן החוץ-תאי, היה יותר מ-15 mEq/L אף על פי שריכוזו בנסיוב היה תקין. במקביל קיימת עלייה בריכוז הנתרן בתאים. פעולות ההחייאה המתחילות מוקדם מקטינות את השינויים הללו ושומרות על פוטנציאל הממברנה של התאים.
אחד החסרונות של ה-BSS הוא הצורך במתן כמות גדולה של נוזלים, כתוצאה משיווי המשקל המהיר המושג בין המדור הוסקולרי למדור הבין-תאי. כמות הנוזלים הגדולה, החודרת למדור הבין-תאי, יכולה לגרום מאוחר יותר לפגיעה בתפקוד איברים אחרים. נשאלת גם השאלה, האם בנוכחות דלף מהמיטה הקפילרית, עקב הרס האנדותל, כמות BSS שהיא גדולה פי 3 מכמות תמיסות האלבומין הנדרשת להחייאה, לא תגרום לבצקת ריאות? וזאת לאור הקביעה של Guyton וחבריו, שבנוכחות לחץ אונקוטי מופחת במדור הוסקולרי, החולים חשופים יותר לבצקת ריאות. המיקרוצירקולציה הריאתית שונה מזו של איברים אחרים בכך שקיים בה דלף מתמיד של נוזלים וחלבונים לממברנה האלואולוקפילרית, ואלה מפונים משם על-ידי מערכת הלימפה. מערכת זו, לאחר מתן BSS, מסוגלת להגביר את פינוי הנוזלים והחלבונים מהריאות ועל-ידי כך למנוע את הבצקת.
במעבדה ניתן היה להוכיח כי בחיות, במצב של הלם קשה, מתן BSS ודם, עד השגת תפקוד תקין של המערכת הצירקולטורית, הצריך אמנם פי 3 נוזלים מאשר בתמיסות אלבומין, אולם בשתי החלופות ההיענות הריאתית, שהייתה נמוכה בזמן ההלם, חזרה להיות תקינה לאחר ההחייאה בשיעורים דומים. מדידות ישירות של כמות הנוזלים בריאות, לאחר החייאה בשתי תמיסות אלה, הראו שכמות הנוזלים דומה. ניתן להראות שהקטנת הלחץ האונקוטי בנסיוב אינה גורמת לעלייה בכמות הנוזלים בריאות, מכיוון שבמקביל הלחץ האונקוטי בממברנה האלואולוקפילרית יורד אף הוא, כך שמפל הלחצים נשמר. על מנת לגרום לבצקת ריאות בחולים המקבלים BSS יש להעלות את הלחץ בעורק הפולמונרי ב-15 מ"מ כספית מעבר ללחץ התקין. לא ניתן להראות בניסויים in vivo שאפשר להקטין את כמות הנוזלים בריאות על-ידי עליית הלחץ האונקוטי של הפלזמה.
בחלק מהעבודות אשר השוו מתן כמות זהה של תמיסות אלבומין ו-BSS, הושגו תוצאות טובות יותר בחולים שטופלו על-ידי תמיסות אלבומין. ברור שמתן מנות זהות של התמיסות הללו יוצר שתי קבוצות, שאינן בנות השוואה, מכיוון שבטיפול ב-BSS נדרשת כמות נוזלים גדולה עד פי 3 יותר מזו של אלבומין. לכן המסקנה היחידה מעבודות אלו היא שמתן תמיסות BSS בכמות לא מספקת היא טיפול לא יעיל בהלם.
Lowe וחבריו הראו, שחולים העוברים פתיחת בטן עקב חבלה, ומטופלים על-ידי BSS ודם, או BSS ואלבומין, מגיבים בצורה דומה. ההשפעה של האלבומין היא לטווח קצר בלבד, מה עוד ששיקום הנפח התוך-וסקולרי נעשה על חשבון המדור החוץ-תאי, וזה יכול רק לעכב את החלמת הרקמות.
עבודות שונות הראו שמתן נוזלים ללא אלקטרוליטים גרמו לירידה בכמות השתן המופרש, ובמקביל גרמו להקטנת נפח הדם ולהפרעה בתפקוד הכלייתי. לעומת זאת, כאשר החולים קיבלו תמיסות מלחים נשמר התפקוד הכלייתי. חולים אשר טופלו בתמיסות אלבומין הראו ירידה בתפקוד הכלייתי ומשך זמן ההחייאה שלהם התארך. כמות הנוזלים שנדרשה לחולים אלה הייתה רבה יותר.
Postresuscitation hypertension יכול להופיע בחולים לאחר הצלחת פעולות ההחייאה. הם מפתחים יתר-לחץ-דם סיסטולי ודיאסטולי (150/100) למשך לפחות 6 שעות, מלווה באי-ספיקה נשימתית, בהמטוריה ובהפרעות מנטליות. הסיבה לתופעה זו היא בצקת של הרקמות, המתפתחת לאחר ההחייאה, עקב צבירת נוזלים במדור הבין-תאי. בעבר חשבו שניתן למנוע סיבוך זה על-ידי מתן של תמיסות אלבומין, אולם נמצא שאין התיאוריה חופפת את המציאות במקרה זה, מכיוון שנדרשת כמות גדולה של נוזלים גם במתן תמיסות אלבומין, ולכן שיעור הסיבוכים הללו שווה בשתי צורות הטיפול. הופעת סיבוך זה קשורה בעלייה בתחלואה ותמותה של החולים, שאותה ניתן למנוע על-ידי מתן מבוקר של משתנים בכמות קטנה. מתן כמות גדולה של משתנים עלולה לגרום לאיבוד מהיר של נוזלים מהמדור הוסקולרי וכתוצאה מכך לחידוש מנגנון ההלם.
השימוש בתמיסות האלבומין יכול לגרום להשפעות שליליות. מתן האלבומין שומר אמנם את רמת האלבומין בנסיוב, אולם גורם לירידה ברמת הסידן היוני שאינו קשור, וכתוצאה מכך גורם לדיכוי פעילות המיוקרד. חולים שטופלו על-ידי תמיסות אלבומין הראו רמה נמוכה של אימונוגלובולינים ביחס לחולים שטופלו על-ידי BSS. המכניזם קשור כנראה בקשירת האימונוגלובולינים לאלבומין, החודר למדור הבין-תאי. כמו-כן אפשר להדגים בחולים אלה תגובה מופחתת ל-Tetanus toxoid. יצירת האלבומין על-ידי ההפטוציטים מווסתת על- ידי רמת האלבומין במדור הבין-תאי של הכבד. כאשר הרמה עולה, כתוצאה ממתן של תמיסות עשירות באלבומין, קיים דיכוי של ייצור האלבומין האנדוגני. הירידה בייצור האלבומין, ובמקביל הסילוק המהיר של האלבומין האקסוגני, מעכבת את חזרת הלחץ האונקוטי לערך תקין.
מכל האמור לעיל, ובהתחשב במחיר הזול יחסית של תמיסות מלחים ביחס לתמיסות האלבומין, ברור שקיימת עדיפות לשימוש בתמיסות מלחים בזמן החייאה.
תמיסות מלחים (saline) היפרטוניות
השימוש בתמיסות הללו בפעולות ההחייאה בחולים הלוקים בהיפוולמיה, דורש מחקר נוסף. הוכח שתמיסות אלו יעילות בטיפול בחולים שהם יציבים מבחינה המודינמית, ובתנאי מעבדה - בחיות שנגרם להן הלם חריף עקב דימום, כאשר כמות הדם שהחיות איבדו הייתה ידועה. בשלב זה לא הוכח עדיין קלינית, שיש יתרון לתמיסות המלח ההיפרטוניות על פני ה-BSS ביחס לשמירה על תפקוד האיברים החיוניים או לתוצאות ההחייאה.
השימוש בתמיסות היפרטוניות דורש מעקב צמוד אחר החולה, מכיוון שמתן כמות גדולה מדי מהתמיסות יכולה לגרום להיפרנתרמיה מסוכנת ולעלייה באוסמולליות הדם. התמיסות ההיפרטוניות יכולות לגרום גם לדיכוי שריר הלב, עקב ירידה חדה ברמת האשלגן בנסיוב. מהסיבות הללו הפכו תמיסות אלו לבלתי שימושיות בחולים הלוקים בהיפוולמיה חריפה. החולים שבהם קיימת עדיפות תאורטית להחייאה עם תמיסות היפרטוניות הם חולי הכוויות, שלהם אפשר לתת בולוס קטן של תמיסות היפרטוניות ולהמשיך עם BSS. בחולים מדממים גורמות תמיסות היפרטוניות להחזרה מהירה של נפח הדם לתקנו וכתוצאה מכך מוגבר הדימום ונוצר הלם חוזר.
Artificial Plasma Expander
תמיסות אלו נועדו להחליף את האלבומין כתמיסות קולואידליות. תמיסת Hetastarch מורכבת מעמילופקטין בעל משקל מולקולרי של 450,000 ונמצאת בשימוש כתמיסה בעלת ריכוז של 6%. בתנאים המודינמיים בסיסיים יציבים, מתן התמיסה גורם לעלייה בנפח הדם במידה קלה בלבד ביחס לכמות הנוזל שניתנה. האפקט ההמודינמי של התמיסה נמשך כ-24 שעות, אף על פי שהמולקולות מסולקות על-ידי טיפול אנזימטי המאפשר זמן מחצית חיים של 17 יום. כל ההוראות לשימוש באלבומין קיימות גם בתמיסות הקולואידליות המלאכותיות. בחולים העוברים Cardiopulmonary bypass השימוש בתמיסות אלה הוא נרחב primeo של הממברנות באוקסיגנטור.
בהשוואת יעילות תמיסות Plasma expander שונות על ההחייאה נמצא שלכל התמיסות אפקט דומה. תמיסות אלו נותנות גם תוצאות השוות לטיפול ברינגר לקטט. בחולים הלוקים בהלם היפוולמי הטיפול העדיף הוא מתן תמיסות מלחים ולא תמיסות קולואידים.
הסיבוכים הקשורים בתמיסות הללו הם:
השכיחות המדווחת של תגובה אנפילקטית היא 0.003% בתמיסות אלבומין, 0.008% בתמיסות Hetastarch, 0.008% בתמיסות דקסטרוז ו-0.038% בתמיסות Genitale. הסיבה לפגיעה במערכת הקרישה על-ידי התמיסות הללו נעוצה בכך שהן גורמות לשקיעת פקטורים 1, 8, פיברין מונומר וייתכן גם של Von Willebrand factor, תוך יצירת תסמונת על-שם Von Willebrand מושרית, וקרישה בתוך כלי הדם עקב שקיעת פקטורי הקרישה. נצפתה גם עלייה ב-PTT וב-PT וירידה בתפקוד התרומבוציטים. בספרות דיווחו על שינויים במערכת החיסון בחולים שקיבלו תמיסות אלה, עקב הצפת המערכת הרטיקולואנדותליאלית על-ידי המולקולות הללו, שנבלעו על-ידי המקרופגים.
דקסטרן: קיימות שתי צורות של דקסטרן -
- דקסטרן 40
- דקסטרן 70
הנבדלות במשקל המולקולרי שלהן. הדקסטרן 40 הוא בעל משקל מולקולרי של 40,000 ואילו משקלו המולקולרי של הדקסטרן 70 הוא 70,000. הדקסטרן 70 נשאר בפלזמה 2–3 ימים ואילו הדקסטרן 40 כ-12–18 שעות. הדקסטרן יעיל כ- Plasma expander, כמו שאר התמיסות, ואינו עולה על BSS-rn בהחייאה של חולים במצב חד. המגבלה העיקרית של הדקסטרן הן תופעות הלוואי שהוא גורם, כמו: תגובה אנפילקטית והפרעות קרישה, שהן שכיחות יותר מאשר ה-Plasma expanders אחרים, ולכן מגבילים את השימוש בתמיסות אלו. בנוסף לכך, דקסטרן בעל משקל מולקולרי הפחות מ־60,000 עובר פילטרציה גלומרולרית ולכן פוגע בפונקציה הכלייתית, גורם לאי-ספיקה כלייתית חדה ולסתימת הטובולי. הדקסטרן גורם גם לדיכוי יצירת חלבוני הפלזמה כמו: haptoglobin,macroglobulin ,C3 ,C4 ,IGM, IGA ,IGG ופיברינוגן. כתוצאה מכך חלה ירידה בתגובה האימונית, למשל התגובה למתן טוקסואיד.
דם מלאכותי - Artificial Blood
התכונות הנדרשות מדם מלאכותי הן:
- שהתמיסה תהיה יציבה
- שהתמיסה תהיה ללא תופעות לוואי
- שהתמיסה לא תגרום להפרעות בתפקוד איברים חיוניים אחרים
- שהתמיסה לא תגרום להפרעות בביצוע ה-Cross match ולא תמנע מתן דם לחולה
אחת האפשרויות שהועלו היה מתן אקסטרקט של המוגלובין מדם ישן אשר יש ביכולתו לקשור חמצן. אקסטרקט זה נקרא Stroma Free Hemoglobin - SFH. היתרונות הצפויים היו:
- ניתן להפיקו מדם ישן
- הוא יכול לקשור ולהוביל חמצן
- הוא אינו אנטיגני ואינו מפריע בביצוע Cross
- הוא אינו גורם לאגירה של כדוריות במיקרוצירקולציה ולהפרעות במנגנון הקרישה
- הוא מוריד את צמיגות הדם
- הוא מתמוסס היטב בתמיסות פיזיולוגיות
- ניתן לשמר את התמיסה לטווח ארוך
ניסיונות להשתמש באקסטרקט זה העלו מספר בעיות:
- התמיסות היו פירוגניות וגרמו לתגובה אלרגית
- נצפה דיכוי של פעולת הכליות
- התמיסות גרמו ל- DIC
הסיבה לתופעות הללו הייתה נעוצה בכך שהתמיסות לא היו נקיות מ-debris תאי, והכילו כמויות משתנות של Stromal elements ושומנים, שהם אנטיגנים שגרמו נזק לכליות. כאשר ניקו את התמיסות הללו מה-debris שהיה בתוכן נעלמו למעשה הסיבוכים שהוזכרו. פינוי ההמוגלובין מתבצע על-ידי קשירתו להפטוגלובין ובליעת הקומפלקס על-ידי ההפטוציט. רק במקרים שבהם הייתה העמסה של התמיסות הללו והצפה של הכבד בהמוגלובין, פונה חלק מההמוגלובין דרך המערכת הרטיקולואנדותליאלית. לכן תמיסות אלו אינן משפיעות על מערכת החיסון כפי שאפשר היה לצפות מתמיסות מסוג זה.
בתמיסת ה-SFH הנקייה נשארו מספר בעיות: בהיעדר DPG2,3 בתמיסה, קשירת החמצן להמוגלובין היא חזקה יותר ושחרורו ברמה התאית הוא מינימלי. ה- PSO50 (שהינו לחץ החמצן שבו 50% מההמוגלובין קשור) של הדם הוא 27 מ"מ כספית ואילו של תמיסות ההמוגלובין הוא 14 מ"מ כספית. כלומר - לחץ החמצן ברקמות יאפשר שחרור מועט מאוד של חמצן מההמוגלובין. בעיה נוספת המתעוררת במתן התמיסות הללו, היא הפינוי המהיר של ההמוגלובין, כך שתוך שעתיים עד 5 שעות החומר נעלם מהדם. 35% ממנו מפונים דרך השתן ושאר החומר עובר מטבוליזם בכבד, בטחול, בכליות ובמח העצם.
ההמוגלובין מורכב משתי שרשראות נפרדות הנמצאות בשווי משקל. הצורה הדימרית היא הראשונה שעוברת פילטרציה בכליות ונקשרת להפטוגלובינים, והיא זו שהאפיניות שלה לחמצן ירודה. לכן נעשו ניסיונות לקשור את ההמוגלובין למקרומולקולות, על מנת למנוע את הפרשת ההמוגלובין בשתן ולהאריך את זמן מחצית החיים של התמיסות הללו בנסיוב. התוצאות שנתקבלו היו חלקיות בלבד, במיוחד לנוכח העובדה שהתמיסה שהתקבלה היא Plasma expander ולכן גורמת לדילול ההמוגלובין שבדם.
ההמוגלובין באריתרוציט מורכב משתי קונפיגורציות: האחת, שהיא בעלת אפיניות ירודה לחמצן ומיוצבת על-ידי DPG2-3, והשנייה בעלת אפיניות גבוהה. בתמיסת ההמוגלובין אין 2,3DPG ולכן כמות ההמוגלובין בעל האפיניות הירודה נמוכה, וכתוצאה מכך החמצן נקשר היטב להמוגלובין ולא משתחרר ברקמות. לאור מידע זה פותחה תמיסה שמכילה DPG2,3 ופולימרים של המוגלובין ועל-ידי כך נוצרו מקרו-מולקולות שאינן מופרשות. תמיסות אלו נקראות ה-Pyridoxalated polymerized hemoglobine או ה-HGB-PLP complex, שבהן היחס בין ה- PLP לבין ה- HGB הוא 4:1. תמיסה זו היא בעלת היתרונות הבאים: האפיניות לחמצן היא ירודה, זמן המחזור שלה הוא 25 שעות, ואין לה השפעה על מערכת הקרישה. כמות המטהמוגלובין שנוצרת היא קטנה (4.9% בתמיסה ועוד יצירה של 1% methemoglobin ליום).
מכיוון שמדובר בתמיסות נקיות מ-debris תאי - התמיסות הללו אינן גורמות לתגובה אנטיגנית. אולם כאשר מנסים להשתמש בתמיסות שמקור ההמוגלובין שבהן הוא בבעלי חיים - מוצאים שהן בעלות אנטיגניות ברורה. תמיסות שמקורן בדם חזיר הן בעלות האנטיגניות הירודה ביותר ולכן מהוות אלטרנטיבה לשימוש SFHs ממקור אדם. התמיסות הללו הן בעלות אפקט אונקוטי, ולכן גורמות לחדירת נוזלים מהרקמות לכלי הדם. לכן יכולות תמיסות אלה להחליף את Plasma expanders ולשמש בהחייאה של חולים במצב חריף יחד עם מתן תמיסות מלחים.
ה- SFH מתפקד כנושא חמצן לא פחות יעיל מהדם. בפציעות במסגרת צבאית או במקומות שלא ניתן לקבל אספקת דם אפשר להשתמש בתמיסות אלה כתחליף לדם בנוסף לפעולות ההחייאה הרגילות.
Perfluorochemical
אלה תחליפי דם מלאכותיים המיוצרים בתנאי מעבדה. נמצא שה-perfluoredecalin או perfluorotribulylamineS הם נושאי חמצן ו-CO2 טובים. חומרים אלה אינם מסיסים במים, ולכן על מנת להמיסם, יש ליצור תמיסה הדומה לכילומיקרונים על-ידי המסת החומר בתערובת של fluronic F-68, חלבון ביצה, פוספוליפידים וגליצרול כחומר מייצב. מכיוון שאוסמולריות התמיסה היא נמוכה מוסיפים לתמיסה קולואידים. באם התמיסות הללו אינן יציבות - הן מסוכנות, מכיוון שהן עלולות לגרום ליצירת טיפות שומן בפלזמה, הגורמות לפקקת במיקרוצירקולציה הקשורה בתמותה גבוהה.
חומרים אלה מעבירים חמצן לרקמות ומשחררים CO2 בריאות, בדומה להמוגלובין, אך מעט פחות טוב ממנו. בניסיונות קליניים שונים הוכחה יעילות התכשיר הזה. הסיבוכים המגבילים את השימוש בו הם: שפעול הקומפלמנט והטסיות הגורם להפעלת מערכת הקרישה, בנוסף לצורך בעלייה בלחץ החמצן הנדרש, על מנת להשיג פעולה פיזיולוגית של perfluorochemicals כנושא חמצן.
ATP-MgCl2-Chemicals
האדנוזין טריפוספט מגנזיום כלוריד הומלץ כבר בתחילת שנות ה-70 כטיפול בהלם היפוולמי. הבסיס התאורטי לשימוש בחומר זה נשען על תצפית בזמן הלם היפוולמי: עקב הירידה באספקת האנרגיה לתא, חל שיבוש בפעולת משאבת הנתרן-אשלגן שבממברנת התא, וכתוצאה מכך אשלגן יוצא מהתאים ונתרן חודר לתוכם. השינויים הללו קשורים בירידה במטבוליזם הכללי של התא ובמיוחד של המיטוכונדריה. השינויים הללו מחמירים ככל שמצב ההלם מתמשך עד למצב שבו הם אינם הפיכים יותר. במיטוכונדריה קיים עיכוב מטבולי של אלפא קטוגלוטמט והביתא הידרוקסיבוטירט כסובסטרטים, ולכן חל עיכוב בהפיכת ה-ADP ל-ATP.
באופן תאורטי מתן ATP יכול לשפר את המצב על-ידי אספקת אנרגיה לדופן התא וייצוב הממברנה.
מתן ATP-MgCl2 לפני הוצאת כליה המיועדת להשתלה מאריך את זמן האיסכמיה החמה (Warm ischemia) ומשפר את חיות הכליה. נמצא שריכוז ה-ATP בקורטקס בזמן האיסכמיה הקרה הוא גבוה יותר בכליות שטופלו ב- ATP-MgCl2. מולקולות ה-ATP הן מסוכנות בהזלפה ישירה לווריד, מכיוון שהן גורמות לחיזור ונקשרות לקטיונים ביוולנטיים, לכן יש לייצבם ולקושרם ל-MgCl2. המגנזיום מעכב את הדאמינציה והדפוספורילציה של ה-ATP על-ידי הרקמות והפלזמה.
הקומפלקס ATP-MgCl2 אינו מתמוסס בשומן ולכן לא ברור כיצד הוא חודר לתאים. יש הטוענים שה-ATP מתפרק לאדנוזין ופוספט החודרים לתאים ומשמשים סובסטרט ליצירת ה-ATP. התברר שלתמיסות אלה אפקט ווזודילטטורי אשר יכול לשפר את זרימת הדם במיקרוצירקולציה. אולם מכאן נובעת גם ההשפעה השלילית שלו. הוא גורם לירידה בלחץ הדם אפילו באנשים שהם נורמוולמיים, לא כל שכן בחולים היפוולמיים, שבהם הוא גורם גם לירידה בתפוקת הלב, לירידה בלחץ-הדם ובדופק.
אפקט נלווה של התמיסות הללו נובע ממתן המגנזיום. המגנזיום מתחרה עם הסידן על המעבר דרך אותם האתרים בממברנות התא. הסידן העובר במהירות דרך הממברנה גורם להפרעות בתפקוד המיטוכונדריה ולמוות של התאים. פעולת המגנזיום מקטינה את בריחת הסידן ומקטינה את הנזק התאי.
מתן של ATP-MgCl2 לאחר החייאה טובה בנוזלים משפר את ההיוותרות בחיים של חיות מעבדה (75% לעומת 20%).
מכיוון שקשה לצפות את התנהגות ה-ATP-MgCl2, הוא עדיין אינו בשימוש קליני במסגרת ההחייאה של חולים היפוולמיים. יעילות התמיסות הללו הודגמה במקרים הבאים:
- בחולים שעברו החייאה מלאה בנוזלים ויציבים מבחינה המודינמית
- בחולים נורמוולמיים שבהם יש צורך בשיפור תפקוד האיברים החיוניים כמו בחולים באי-ספיקה כלייתית חדה, או באי-ספיקה לבבית
- שימור איברים להשתלות
תמיסות מעושרות בחומצות אמינו מסועפות
חומצות האמינו המסועפות כמו: ואלין, לויצין ואיזולויצין הן בעלות חשיבות מיוחדת בטיפול בחולים הנמצאים בהלם ממושך ובעיקר בהלם זיהומי. חומצות האמינו המסועפות אינן עוברות מטבוליזם בכבד אלא ברקמות אחרות כמו רקמת השריר, המוח והלב. ברקמות אלה הם הופכים ל-ketoacid ולאחר מכן לגלוקוז, העובר מטבוליזם עד יצירת מולקולות עשירות אנרגיה המשמשות את התאים. חלק אחר מהם עובר מטבוליזם לחלבון. החומצות הללו משרות יצירה של חלבונים בכבד, אף על פי שאינן עוברות מטבוליזם בכבד. שאר חומצות האמינו עוברות פירוק בכבד. בזמן אי-ספיקת כבד הפירוק של חומצות האמינו פוחת, וכתוצאה מכך עולה ריכוזן בפלזמה ובנוזלים החוץ-תאיים. עלייה זו גורמת להצטברות של חומצות אמינו ארומטיות במוח, העוברות פירוק לטרנסמיטורים עצביים מדומים, אשר גורמים לחולים הללו להיכנס לתרדמת הפטית. בו-בזמן ריכוז החומצות האמיניות האחרות נשאר תקין, או עולה במצבי אי-ספיקת כבד קיצוניים. ריכוז החומצות האמיניות המסועפות יורד בצורה בולטת במצבים אלה עקב ניצול מוגבר של החומצות האמיניות המסועפות על-ידי הרקמות. במצב נורמלי רק 6%-7% מהתצרוכת האנרגתית מקורה בחומצות אמינו מסועפות. במצבי דחק אחוז זה עולה בצורה ניכרת. תכונה נוספת חשובה של חומצות האמינו המסועפות היא יכולתן להקטין את פירוק החלבונים.
בחולים הלוקים באלח-דם קיימים שינויים הורמונליים אשר אחראים לשינויים המטבוליים השונים. השינויים המטבוליים מתבטאים בניצול מוגבר של חלבונים כמקורות אנרגיה ובייצור של Acute reactive proteins החשובים ביותר במנגנון ההגנה של הגוף, במיוחד ה-C3 והטרנספרין. הפירוק המוגבר של החלבון נגרם על-ידי 1-interleukin או פרוסטגלנדינים המופרשים ביתר במצבים אלה. בנוסף, בכבד חל שיבוש בבקרה של האינסולין על מערכת הגלוקונאוגנזיס, ומתחיל ייצור בלתי מבוקר של גלוקוז שלא בהתאם לצרכים המטבוליים. המקור העיקרי לגלוקוז זה הוא פירוק של חלבונים ורק מקצתו גליצרול שמקורו בפירוק השומנים. בחולים אלה חלה גם הפרעה בהשפעת האינסולין על איבר המטרה, וכתוצאה מכך חלה הפרעה בניצול הסוכרים ברמה התאית.
כאשר בודקים את תבנית החומצות האמיניות בחולים זיהומיים נמצא שהם די דומים לאלה של החולים באי-ספיקה כבדית, אלא שכאן רמת החומצות האמיניות המסועפות היא נמוכה או בגבול התחתון של התקן. השינויים החלים ב-Blood brain barrier בחולים זיהומיים דומים לאלה של החולים באי-ספיקה כלייתית. מתברר מעבודות שונות, שניתן לנבא את הסיכון לאנצפלופתיה זיהומית וההיוותרות בחיים לפי תבנית החומצות האמיניות.
עבודות הוכיחו שניתן, על-ידי שימוש בתמיסות אלה, להקטין את שיעורי התמותה בחולים הלוקים בהלם זיהומי קשה. בחולים הלוקים בעקה (Stress) קלה יחסית לא הוכחה הטבה משמעותית. מתברר שתמיסות עשירות בלאויצין גורמות למאזן חנקן חיובי יותר מאשר תמיסות אחרות של חומצות אמינו מסועפות. היתרון של הלאויצין הוא גם בכך שהוא מקטין את הצורך באינסולין ממקור חיצוני היות שהוא מגרה הפרשה פנימית של אינסולין. (פירוט על התמיסות למתן TPN ניתן למצוא בחוברת על הזנת-על)
תרופות וזואקטיביות
אם למרות העמסת נוזלים בכמות מספקת החולה נותר היפוטנסיבי, יש להשתמש בתרופה מקבוצת האמינים הסימפאתטיים. שוב -הטיפול ייקבע בהתאם למצבו הקליני של החולה, כאשר מה שחשוב בסופו של דבר הוא הזילוח הרקמתי ולא הערך של לחץ הדם, שאינו משקף נאמנה את הנעשה ברמה התאית. מחקרים המודינמיים הוכיחו עדיפות לדופאמין ולדובוטמין על פני נוראדרנלין ואיזופרוטרנול, שכן לראשונים נודעים אפקט אינוטרופי חיובי ושיפור תפוקת הלב ללא עלייה משמעותית בתצרוכת החמצן או כיווץ מיותר של כלי דם היקפיים, במינון נכון. יתרון נוסף לדופאמין הוא שיפור הזילוח הכלייתי עד מינון של 10 מיקרוגרם לק"ג לדקה. בנוכחות אי-ספיקת לב, תרופת הבחירה היא דובוטמין המוריד את לחץ היתד לעומת הדופאמין. עם התקדמות מצב ההלם, ייתכן מצב של תת-לחץ דם, למרות תמיכה אינוטרופית ניכרת, עקב איבוד ניכר של טונוס כלי הדם, וירידה חדה בתנגודת ההיקפית. במקרה דנן, חובה להיעזר גם בתרופות מכווצות כלי דם בלבד, כגון מטראמינול (אראמין) או נוראדרנלין.
למרות הפיתוי להשתמש בתרופות וזואקטיביות כרפלקס בעת תת-לחץ דם, בראש ובראשונה יש להקפיד, שאכן הושלם הנפח של כלי הדם. מתן תרופות סימפאתטיות במצב היפוולמיה מסוכן יחסית, ואף מזיק עקב כיווץ כלי הדם ההיקפיים, המחמיר עוד יותר את הפגיעה המיקרוצירקולטורית - אלא אם מדובר בתת-לחץ דם חמור - ואז יש לשפוט כל מקרה לגופו.
איזון המודינמי מיטבי של החולה בהלם זיהומי יושג לעיתים ביתר קלות על-ידי שילוב תרופות, תוך ניצול יתרונות של כל תרופה בנפרד. לדוגמה, חולה בהלם זיהומי עם תת-לחץ דם הלוקה בנוסף באי-ספיקת לב, ייהנה משילוב מינון גבוה של דובוטמין לתמיכה אינוטרופית ולהורדת לחץ היתד, עם מינון נמוך של דופאמין לשמירת הזילוח הכלייתי.
Naloxone
נלוקסון נמצא יעיל בהפחתת השינויים ההמודינמיים במצבי הלם זיהומי, המורגי או ספינאלי. השפעתו הספציפית היא על בלימת ההשפעה המדכאת של האופיאטים, המשתחררים מההיפופיזה בתגובה למצבי לחץ על המערכת ההמודינמית. למרות ממצאים המצביעים על קיום השפעה ישירה של נלוקסון על כלי הדם הפריפריים ועל הלב - רוב ההשפעה מתבצעת דרך קולטנים במערכת העצבים המרכזית. בנוסף, ההשפעה תלויה בקיום של מערכת העצבים הסימפטטית והפאראסימפטטית וקיום המערכת האדרנלית- סימפטטית. ההשפעה המטיבה נובעת ברובה משחרור קטכולאמינים וסטרואידים, הגורמים לעלייה בתנגודת הפריפרית, ולהשגת יציבות של המערכת הקרדיווסקולרית בהשפעת הקורטיזול. ההשפעה הטובה ביותר של נלוקסון מושגת כאשר הוא ניתן לפני ההלם או בסמוך לו, וכאשר הוא ניתן במינון גבוה. ההשפעה של תרופה זו היא זמנית ואינה מתייחסת לסיבת ההלם, ולכן אם אין טיפול בגורם להלם - ההטבה תהיה זמנית בלבד. הנלוקסון מקנה למעשה פרק זמן ארוך יותר לטיפול הבסיסי בשוק.
ראו גם
- לנושא הבא: דם - היבטים כירורגיים - Blood - surgical aspects
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: חבלות
- לפרק הבא: ריפוי פצעים
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן - מומחה בכירורגיה, מנהל היחידה לבריאות השד מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק