הבדלים בין גרסאות בדף "הפרעות בשומני הדם בסוכרת מסוג 2 - Lipid disorders in Type 2 diabetes"
תגית: mobile edit |
תגית: mobile edit |
||
| שורה 17: | שורה 17: | ||
[[פעילות גופנית]], [[תזונה]] נבונה ו[[הפסקת עישון]], הם מרכיבים חשובים בטיפול בהפרעה בשומני הדם בסוכרת. | [[פעילות גופנית]], [[תזונה]] נבונה ו[[הפסקת עישון]], הם מרכיבים חשובים בטיפול בהפרעה בשומני הדם בסוכרת. | ||
| − | הטיפול התרופתי המקובל בהפרעות הללו הוא [[t:HMG CoA reductase inhibitors - C10AA|סטטינים]] להורדת ליפופרוטאין בעל צפיפות נמוכה ב-40-30 אחוזים לפחות. במקרים מסוימים ניתן לשלב סטטינים עם [[t:Ezetrol|Ezetrol]] {{כ}}(Ezetimibe) או [[Niacin]]{{כ}} (Vitamin B3). בנוכחות יתר טריגליצרידים בדם ורמות נמוכות של ליפופרוטאין בעל צפיפות גבוהה, ניתן להוסיף Niacin{{כ}}, [[t:Fibrates - C10AB|פיבראטים]] (Fibrates) ו-[[Omega-3]]. | + | הטיפול התרופתי המקובל בהפרעות הללו הוא [[t:HMG CoA reductase inhibitors - C10AA|סטטינים]] להורדת ליפופרוטאין בעל צפיפות נמוכה ב-40-30 אחוזים לפחות. במקרים מסוימים ניתן לשלב סטטינים עם [[t:Ezetrol|Ezetrol]] {{כ}}(Ezetimibe) או [[Niacin]]{{כ}} (Vitamin B3). בנוכחות יתר טריגליצרידים בדם ורמות נמוכות של ליפופרוטאין בעל צפיפות גבוהה, ניתן להוסיף Niacin{{כ}}, [[t:Fibrates - C10AB|פיבראטים]] (Fibrates) ו-[[t:Omega-3|Omega-3]]. |
מעניין לסקור את מנגנוני התפתחות ההפרעה בשומני הדם בסוכרת, מחקרים מבוקרים התערבותיים בחולי [[סוכרת מסוג 2]], והמלצות טיפוליות להפרעה בשומני הדם בסוכרת. | מעניין לסקור את מנגנוני התפתחות ההפרעה בשומני הדם בסוכרת, מחקרים מבוקרים התערבותיים בחולי [[סוכרת מסוג 2]], והמלצות טיפוליות להפרעה בשומני הדם בסוכרת. | ||
גרסה מ־00:58, 20 באוקטובר 2016
| הפרעות בשומני הדם בסוכרת מסוג 2 | ||
|---|---|---|
| Lipid disorders in Type 2 diabetes | ||
| יוצר הערך | ד"ר אלנה יצחקוב, פרופ' ארדון רובינשטיין
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – סוכרת, הפרעה בשומני הדם
הפרעה בשומני הדם בסוכרת היא גורם סיכון עיקרי בהתפתחות והתקדמות טרשת העורקים. הפרעות במשק שומני הדם בחולים סוכרתיים מתאפיינת בערכי טריגליצרידים מוגברים, ערכי ליפופרוטאין בעל צפיפות גבוהה (HDL, High Density Lipoprotein) נמוכים, חלקיקי ליפופרוטאין בעל צפיפות נמוכה (LDL, Low Density Lipoprotein) קטנים וצפופים, עלייה ביחס אפוליפופרוטאין B (Apo-B, Apolipoprotein-B)/אפוליפופרוטאין A (Apo-A, Apolipoprotein-A) והיפרליפידמיה ממושכת לאחר הארוחות.
פעילות גופנית, תזונה נבונה והפסקת עישון, הם מרכיבים חשובים בטיפול בהפרעה בשומני הדם בסוכרת.
הטיפול התרופתי המקובל בהפרעות הללו הוא סטטינים להורדת ליפופרוטאין בעל צפיפות נמוכה ב-40-30 אחוזים לפחות. במקרים מסוימים ניתן לשלב סטטינים עם Ezetrol (Ezetimibe) או Niacin (Vitamin B3). בנוכחות יתר טריגליצרידים בדם ורמות נמוכות של ליפופרוטאין בעל צפיפות גבוהה, ניתן להוסיף Niacin, פיבראטים (Fibrates) ו-Omega-3.
מעניין לסקור את מנגנוני התפתחות ההפרעה בשומני הדם בסוכרת, מחקרים מבוקרים התערבותיים בחולי סוכרת מסוג 2, והמלצות טיפוליות להפרעה בשומני הדם בסוכרת.
סוכרת וטרשת העורקים
חולי סוכרת מסוג 2 נמצאים בסיכון מוגבר פי 2-4 ביחס לכלל האוכלוסייה לתחלואה לבבית ושל כלי הדם בשל טרשת העורקים המוקדמת.[1] כ- 75%-80% מחולי סוכרת מסוג 2 מתים מטרשת העורקים וסיבוכיה.[2]
חשוב להדגיש כי הפרעה בשומני הדם בסוכרת מקדימה התפתחות סוכרת במספר שנים, ומהווה סיכון עיקרי בהתפתחות טרשת העורקים.[3]
הפרעה בשומני הדם בסוכרת
- איפיונים של הפרעה בשומני הדם בסוכרת
- ערכי טריגליצרידים וחלקיקי ליפופרוטאין בעל צפיפות נמוכה מאוד (VLDL, Very Low Density Lipoprotein) מוגברים;
- ערכים נמוכים של ליפופרוטאין בעל צפיפות גבוהה;
- ערכי ליפופרוטאין בעל צפיפות נמוכה תקינים או מוגברים מעט, אך חלקיקי ליפופרוטאין בעל צפיפות נמוכה קטנים וצפופים;
- היפרליפידמיה ממושכת לאחר ארוחה שומנית;
- פעילות נמוכה של ליפופרוטאין ליפאז (Lipoprotein lipase);
- פעילות מוגברת של ליפאזה כבדית;
- ערכי אפוליפופרוטאין B גבוהים, וערכי אפוליפופרוטאין A נמוכים.
מנגנוני התפתחות הפרעה בשומני הדם בסוכרת
בנוכחות תנגודת לאינסולין ו/או תת-הפרשת אינסולין (Hypoinsulinism) יחסית, חומצות שומן חופשיות משתחררות מרקמת שומן בקצב מואץ. התהליך הוא בסיס לייצור יתר של ליפופרוטאין בעל צפיפות נמוכה מאוד, בנוכחות עודף גליצרול, הנובע מעודף סוכר. השילוב של יצירת יתר של ליפופרוטאין בעל צפיפות נמוכה מאוד, מצד אחד, והשהיה של פירוקו בשל פעילות ירודה של ליפופרוטאין ליפאז, מצד שני, גורם לעלייה בערכי טריגליצרידים וליפופרוטאין בעל צפיפות נמוכה מאוד, כמו כן מאריך זמן נוכחותם בדם.
רמות ליפופרוטאין בעל צפיפות גבוהה בחולים סוכרתיים, נמוכות בשל מספר סיבות:
- בשל פעילות מופחתת של ליפופרוטאין ליפאז, נוצרים פחות חלקיקי ליפופרוטאין בעל צפיפות גבוהה מתפתחים (Nascent-HDL), המכילים מעט פוספוליפידים (Phospholipid) ואפוליפופרוטאינים, ומהווים גרעין להיווצרות חלקיק ליפופרוטאין בעל צפיפות גבוהה; [4]
- מאחר שהחלקיקים העשירים בטריגליצרידים, שוהים זמן רב יותר בזרם הדם, יש שהות ליותר שחלוף של טריגליצריד וכולסטרול אסטר (Ester), בעזרת החלבון המעביר כולסטרול אסטר (Cholesterol ester transfer protein), שתפקידו להעביר טריגליצרידים מחלקיקי ליפופרוטאין בעל צפיפות נמוכה מאוד, לחלקיקי ליפופרוטאין בעל צפיפות גבוהה. ליפופרוטאין בעל צפיפות גבוהה, מתעשר בטריגליצריד ועובר חילוף חומרים מהיר יותר. התהליך מפחית זמן נוכחות חלקיקי ליפופרוטאין בעל צפיפות גבוהה בנסיוב;
- פעילות ליפאזה כבדית מוגברת, גורמת להיווצרות ליפופרוטאין בעל צפיפות גבוהה, קטן וצפוף יותר, שחרור מהיר של אפוליפופרוטאין A1, ופינוי ליפופרוטאין בעל צפיפות גבוהה מהיר יותר מזרם הדם. [5]
ערכי ליפופרוטאין בעל צפיפות נמוכה בחולים סוכרתיים, בדרך כלל תקינים או מוגברים מעט, אך חלקיקי הליפופרוטאין בעל צפיפות נמוכה, קטנים וצפופים יותר (קרוי גם Pattern B), שמעודדים התפתחות והתקדמות טרשת העורקים. [6] המצב נוצר מפעילות יתר של ליפאזה כבדית, המסלקת טריגליצרידים מהחלקיקים הללו, והופכת אותם לקטנים וצפופים. חלקיקי ליפופרוטאין בעל צפיפות נמוכה בחולים סוכרתיים, מתאפיינים על ידי קישור מופחת לקולטן לליפופרוטאין בעל צפיפות נמוכה בכבד, נטייה לחמצון יתר וקישור יתר לקולטן מסוג Scavenger receptor במקרופאגים (Macrophage) ברובד הטרשתי. רמות גבוהות של אפוליפופרוטאין B, בשל תנגודת לאינסולין ופינוי מהיר של אפוליפופרוטאין A, הם גורם סיכון נוסף למחלה כלילית בחולים עם סוכרת מסוג 2. [7]
מחקרים מבוקרים בקרב חולי סוכרת
סטטינים
בין המחקרים הראשוניים הגדולים, שבדקו מניעה שניונית של טרשת עורקים, על ידי מתן Simvastatin במינון 20-40 מ"ג (מיליגרם), בקרב 4,444 חולים עם ערכים גבוהים של ליפופרוטאין בעל צפיפות נמוכה [210-309 מ"ג/ד"ל (דציליטר)], היה מחקר ה-4S (Scandinavian Simvastatin Survival Study). בתת-אנליזה (Analysis) של 202 חולים סוכרתיים, שנכללו במחקר לאחר 5.5 שנות מעקב, נמצאה הפחתה בתחלואה ותמותה לבבית ושל כלי הדם ב- 42%, לעומת חולי סוכרת שקיבלו אינבו. [8]
תוצאות דומות התקבלו במחקר ה-HPS (The Heart Protection Study), שעקב אחרי 20,000 חולים עם היסטוריה של מחלת לב וכלי דם , שטופלו ב-Simvastatin במינון 40 מ"ג או באינבו. [9] כ-6,000 חולים סוכרתיים נכללו במחקר, וכ- 56% מהם סבלו ממחלת לב וכלי דם. רמות ליפופרוטאין בעל צפיפות נמוכה ירדו בקבוצה הזו, בממוצע מ- 125 לכ- 89 מ"ג/ד"ל. עם ירידה בערכי הליפופרוטאין בעל צפיפות נמוכה, נצפתה ירידה משמעותית בשיעור האירועים הלבבים ושל כלי הדם, בכ- 25% בחולים סוכרתיים עם מחלת לב וכלי דם ידועה, ובכ- 33% בחולים סוכרתיים ללא מחלת לב וכלי דם ברקע, עם ערכי ליפופרוטאין בעל צפיפות נמוכה בסיסיים נמוכים מ- 116 מ"ג/ד"ל.
מחקר ה-CARDS בדק את השפעת Atorvastatin במינון של 10 מ"ג, לעומת אינבו, בכ-3,000 חולים סוכרתיים ללא עדות למחלת לב או כלי דם. ערכי ליפופרוטאין בעל צפיפות נמוכה ממוצעים בסיסיים היו כ-117 מ"ג/ד"ל, ובטיפול ירדו רמות הליפופרוטאין בעל צפיפות נמוכה עד כ-81 מ"ג/ד"ל (ירידה של כ- 39% לעומת רמות התחלתיות של ליפופרוטאין בעל צפיפות נמוכה). המחקר הופסק שנתיים טרם זמנו בשל ירידה משמעותית סטטיסטית של כ- 37% בתחלואה לבבית ושל כלי הדם בקבוצת המטופלים. [10]
מטה-אנליזה (Meta-analysis) שכללה כ-18,686 חולי סוכרת מ-14 מחקרים, אקראיים מבוקרים וכפולי-סמיות, הראתה ירידה בתמותה הכוללת של כ- 9% לאחר 4.3 שנות טיפול בממוצע בסטטינים שונים. הפחתה ברמת ליפופרוטאין בעל צפיפות נמוכה ב-40 מ"ג/ד"ל הביאה להפחתה בשיעור האירועים הלבבים ושל כלי הדם ב- 21%. [11] השפעה מיטבית של סטטינים, נמצאה גם בקבוצת חולים סוכרתים ללא עדות למחלת לב או כלי דם. חשוב לציין, כי תועלת מטיפול בסטטינים לא הייתה קשורה ברמות התחלתיות של ליפופרוטאין בעל צפיפות נמוכה, ליפופרוטאין בעל צפיפות גבוהה או גורמי סיכון נוספים.
מחקר STENO 2, חיזק חשיבות איזון גורמי סיכון בחולים סוכרתיים, בהפחתת תחלואה ותמותה לבבית ושל כלי הדם. טיפול מוגבר בגורמי סיכון הביא לירידה של כ- 50% בתחלואה ובתמותה לבבית ושל כלי הדם וכוללת. ראוי לציין, כי ניתוח התוצאות הראה חשיבות רבה לאיזון משק שומני הדם בחולים הללו.
כ- 70% מההפחתה בסיכון היו תלויים בטיפול בסטטינים. ממוצעי ליפופרוטאין בעל צפיפות נמוכה בקבוצה המוגברת ירדו עד 83 מ"ג/ד"ל, לעומת 126 מ"ג/ד"ל בקבוצת הטיפול השגרתי. [12]
פיבראטים
מחקר ה-Helsinki Heart Study בדק השפעת Gemfibrozil, על תחלואה לבבית ושל כלי הדם בקרב 4,081 גברים ללא מחלת לב ידועה. תת-אנליזה של קבוצת חולי סוכרת שכללה 135 נבדקים, הראתה שיעור אירועים כליליים של כ- 3.4% בקבוצת מטופלים ב-Gemfibrozil, לעומת כ- 10.5% בקבוצת האינבו, אך הנתונים לא הגיעו למשמעות סטטיסטית, ככל הנראה בשל מדגם קטן של נבדקים. [13] בתת-קבוצה שכללה נבדקים עם ערכי טריגליצרידים גבוהים יותר, וערכים נמוכים יותר של ליפופרוטאין בעל צפיפות גבוהה, ההשפעה המיטבית של התרופה הייתה בולטת יותר והגיעה ל- 71%.
מחקר ה-VA-HIT (Veterans Affairs High-density lipoprotein cholesterol Intervention Trial) בדק השפעת טיפול ב-Gemfibrozil על תחלואה ותמותה כלילית, בקרב גברים עם מחלה כלילית ידועה. גם בעבודה הזו, תת-אנליזה של קבוצת חולי סוכרת, הראתה ירידה משמעותית יותר בתחלואה כלילית ב- 32%, לעומת קבוצת חולים ללא סוכרת (22%). כמו כן, נצפתה ירידה בתמותה לבבית ושל כלי הדם ב- 41% בקבוצת סוכרתיים שטופלו תרופתית. [14][15]
במחקר ה-FIELD (Fenofibrate Intervention and Event Lowering in Diabetes), נבדקה השפעת טיפול ב-Tricor (Fenofibrate) בחולים סוכרתיים, עם עדות למחלת לב וכלי דם ובלי עדות כזאת, שלא קיבלו סטטינים. לאחר חמש שנות טיפול, נצפתה ירידה של כ- 11% בשילוב של אוטם שריר הלב או תמותה לבבית ושל כלי הדם, אך התוצאות לא הגיעו למשמעות סטטיסטית. עם זאת, נצפתה הפחתה בעלת משמעות סטטיסטית בשיעור הופעת אירועים כליליים, בעיקר על חשבון ירידה בשכיחות אוטם שריר הלב ללא תמותה. [16]
במחקר ה-BIP (Bezafibrate Infarction Prevention), לא נמצאה השפעה חיובית של Bezafibrate על תחלואה לבבית ושל כלי הדם. חשוב לציין, כי בתת-אנליזה של קבוצת חולים עם תסמונת מטבולית, נמצאה ירידה של כ- 25% בשכיחות אירועים כליליים, שהייתה בעלת משמעות סטטיסטית. [17]
לאחרונה פורסמה מטה-אנליזה של 6 מחקרים מבוקרים, שבדקו השפעת פיבראטים שונים מול אינבו, על תחלואה ותמותה לבבית ושל כלי הדם בקרב 11,590 חולים. שימוש בפיבראטים לא הביא להפחתה בתמותה כוללת וכלילית, כמו כן לא נצפתה ירידה בשיעורי שבץ מוחי, תעוקת חזה בלתי יציבה, או חידוש אספקת הדם (Revascularization) לעורקים הכליליים בצורה פולשנית. עם זאת, נמצאה ירידה של כ- 21%, בעלת משמעות סטטיסטית, בשיעור שכיחות אוטם שריר הלב, ללא תמותה בקבוצת מטופלי פיבראטים. [18]
הנושא של יעילות טיפול משולב בסטטין וב-Tricor על תחלואה ותמותה לבבית ושל כלי הדם נחקר במחקר ה-ACCORD-LIPID. מתן תוספת Tricor בקרב כ-5,500 חולים סוכרתיים שטופלו בסטטינים, לפני כניסתם למחקר, לא הביא לירידה בתחלואה לבבית ושל כלי הדם, למרות שיפור משמעותי בערכי טריגליצרידים. אנליזה של תת-קבוצת חולים, שסבלו מרמות גבוהות של טריגליצרידים, ורמות נמוכות של ליפופרוטאין בעל צפיפות גבוהה, הדגימה ירידה של 31%, בעלת משמעות סטטיסטית, בשיעור אירועים כליליים. [19]
תוצאות המחקר לא תומכות בשימוש גורף בפיבראטים כתוספת לטיפול בסטטינים, והנושא עדיין נתון בוויכוח.
ניאצין (Vitamin B3)
ניאצין היא תרופה ותיקה שלא נמצאת בשימוש רחב, בשל תופעות לוואי של גלי חום.
לתרופה זו השפעה ישירה על הפחתת ייצור ושחרור חומצות שומן חופשיות, נוסף על הגברת היפוך הובלת הכולסטרול (Reverse cholesterol transport). במינונים של 1-2 גרם ליום, ניתן לשפר את כל המרכיבים של שומני הדם:
- ירידה בערכי טריגליצרידים עד כ- 30%-35%;
- ליפופרוטאין בעל צפיפות נמוכה עד כ- 10%-25%;
- עלייה עד כ- 25%-30% בערכי ליפופרוטאין בעל צפיפות גבוהה.
במחקר ה-Oxford niaspan study נבדקו כ-70 חולים עם מחלת לב כלילית, או מטופלים בסיכון מוגבר למחלת לב כלילית שכבר טופלו בסטטינים, עם ערכי ליפופרוטאין בעל צפיפות נמוכה ממוצעים של 85 מ"ג/ד"ל. במהלך המחקר הוסף לטיפול בסטטין, בצורה אקראית, ניאצין או אינבו. לצורך הערכת טרשת העורקים בוצעה בדיקת תהודה מגנטית (MRI, Magnetic Resonance Imaging) של עורקי התרדמה. בקרב מטופלי ניאצין הודגמה הפחתה בטרשת העורקים, בעוד במטופלי אינבו נמצאה התקדמת הטרשת. [20]
לאחרונה פורסם מחקר ה-6 ARBITER, שבדק השפעת ניאצין על מדדי טרשת בבדיקת על-שמע (US, Ultrasound) של עורקי התרדמה (IMT, Intima-media Thickness). במחקר נכללו חולים עם מחלת לב כלילית או חולים בסיכון מוגבר למחלת לב כלילית, שטופלו בסטטינים טרם כניסתם למחקר. במהלך המחקר קיבלו המשתתפים בצורה אקראית ניאצין או Ezetrol. בקבוצת המטופלים בניאצין נמצאה נסיגה בטרשת העורקים, לעומת היעדר שינוי בקבוצת המטופלים ב-Ezetrol. [21]
עדיין אין עבודות פרוספקטיביות (Prospective) על השפעת ניאצין בשילוב סטטינים, על תמותה ותחלואה לבבית ושל כלי הדם.
ישנה ציפיה לפרסום תוצאות של שני מחקרים גדולים, שחוקרים השפעת טיפול משולב בסטטינים ובניאצין.
Ezetrol (Ezetimibe)
Ezetrol מעכב ספיגת כולסטרול במעי.
במינון 10 מ"ג כתוספת לסטטין, Ezetrol מוריד ערכי ליפופרוטאין בעל צפיפות נמוכה ב- 15%-20%, ערכי טריגליצרידים ב- 10%, ומעלה ליפופרוטאין בעל צפיפות גבוהה ב- 1%.
עדיין אין עבודות פרוספקטיביות על השפעת Ezetrol על תחלואה ותמותה לבבית ושל כלי הדם.
Omacor (Omega-3)
חומצות שומן Omega-3 מסוג אפ"א- (EPA, Eicosapentaenoic Acid) ודה"א- (DHA, Docosahexanoic Acid) במינונים גבוהים של כ- 3-4 גרם ליממה, מורידות ערכי טריגליצרידים (עד 34%) ומעלות בצורה מתונה ערכי ליפופרוטאין בעל צפיפות גבוהה (עד 9%). השפעות חיוביות נוספות הן מניעת הפרעות בקצב הלב, הפחתת דלקת, עיכוב צימות (Aggregation) טסיות וירידת לחץ דם.
להלכה (Theoretically), מינונים גבוהים של Omacor עלולים לגרום להארכת זמן דימום על ידי עיכוב מסלול החומצה הארכידונית (Arachidonic acid pathway). באופן קליני, ההשפעה היא מזערית ביותר. באנליזה של 19 עבודות שכללו חולים לאחר ניתוח מעקפים, הסרת רובד טרשתי מעורקי התרדמה (Carotid endarterectomy) או צנתור כלילי, לא נמצאה עדות לעלייה משמעותית בסיכון לדימום. [22]
עדיין לא בוצעו מחקרים פרוספקטיביים בקרב חולים סוכרתיים, בנושא של השפעה על תחלואה ותמותה לבבית ושל כלי הדם.
המלצות טיפוליות
- פעילות גופנית אירובית סדירה, מבוקרת ומובנית, לפחות במשך 150 דקות שבועיות. נוסף על כך, מומלץ לבצע פעילות גופנית לחיזוק קבוצות שרירים עיקריות (למשל, הרמת משקולות ותרגילים נגד התנגדות) לפחות פעמיים בשבוע; [23]
- דיאטה דלת פחמימות פשוטות, דלת שומן רווי (פחות מ- 7% מסך הקלוריות), דלת כולסטרול (פחות מ-300 מ"ג ליום), עשירה בסיבים תזונתיים וירקות, פחמימות מורכבות ושומן חד-בלתי רווי, צריכת אלכוהול מוגבלת ומבוקרת (עד 15 גרם ליום לאישה, או 30 גרם ליום לגבר);
- הפסקת עישון;
- טיפול תרופתי.
ערכי מטרה בטיפול בהפרעה בשומני הדם בסוכרת
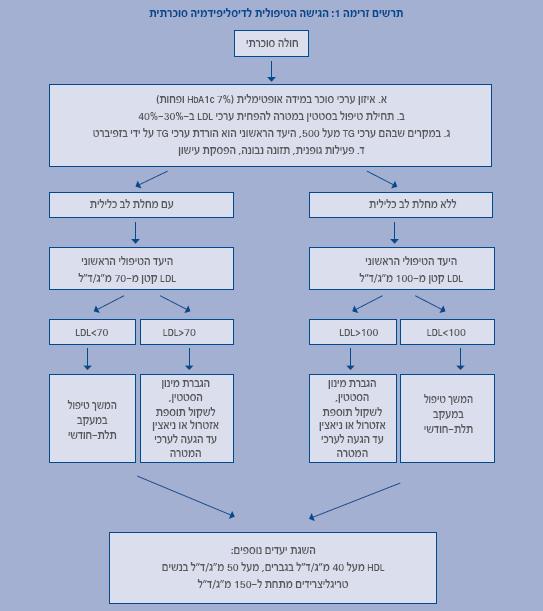
היעד הראשוני בטיפול בהפרעה בשומני הדם בסוכרת, הוא הורדת ליפופרוטאין בעל צפיפות נמוכה. סטטינים הם הקו הראשון לטיפול. עם זאת, אם ערכי טריגליצרידים הם גבוהים מ- 500, ההמלצה היא טיפול בפיבראטים, בשל סיכון מוגבר לדלקת לבלב חריפה.
היעדים הנוספים הם: הורדת טריגליצרידים, וכולסטרול שאיננו מסוג ליפופרוטאין בעל צפיפות גבוהה (Non-HDL cholesterol) (כולסטרול כללי פחות ליפופרוטאין בעל צפיפות גבוהה) והעלאת רמות הליפופרוטאין בעל צפיפות גבוהה.
בהנחיות של איגודים שונים, ובנייר עמדה מטעם החברה לחקר מניעה וטיפול בטרשת העורקים בישראל משנת 2005, מומלץ על טיפול בסטטינים בחולי סוכרת, לצורך מניעה ראשונית ושניונית של טרשת העורקים. מטרת הטיפול היא:
- להוריד ערכי ליפופרוטאין בעל צפיפות נמוכה ב- 30%-40% ועדיף אף ב- 50%, ולהגיע לערכים נמוכים מ- 100 מ"ג/ד"ל במניעה ראשונית, כלומר בחולי סוכרת ללא מחלת לב איסכמית;
- במניעה שניונית, כלומר בנוכחות מחלת לב איסכמית, היעד הוא להגיע לערכי ליפופרוטאין בעל צפיפות נמוכה נמוכים מ-70 מ"ג/ד"ל; [24][25][26]
- ערכי מטרה של טריגליצרידים הם ערכים נמוכים מ- 150 מ"ג/ד"ל;
- ערכי מטרה של ליפופרוטאין בעל צפיפות גבוהה הם בגברים: גבוהים מ- 40 מ"ג/ד"ל, בנשים: גבוהים מ- 50 מ"ג/ד"ל.
חשוב לציין, כי לאחר תחילת טיפול בסטטינים, כל הכפלת מינון תביא לתוספת של כ- 6% בהורדת ליפופרוטאין בעל צפיפות נמוכה. לכן, במקרים שבהם יש צורך להוריד ליפופרוטאין בעל צפיפות נמוכה בצורה משמעותית, יש לבחור בסטטין יעיל ו/או לשלב טיפול עם Ezetrol, ניאצין או מעכבי ספיגת חומצות מרה.
במקרים שבהם הגענו לערכי מטרה של ליפופרוטאין בעל צפיפות נמוכה, ועדיין ערכי טריגליצרידים גבוהים, או ערכי ליפופרוטאין בעל צפיפות גבוהה נמוכים, ניתן להוסיף לטיפול ניאצין, פיבראטים, ו- Omacor.
ביבליוגרפיה
- ↑ Kannel WB, McGee DL. Diabetes and glucose tolerance as risk factors for cardiovascular disease: The Framingham Study. Diabetes Care1979;2:120-126
- ↑ Pekkanen J, Linn S, Heiss G, et al. Ten-year mortality from cardiovascular disease in relation to cholesterol level among men with and without preexisting cardiovascular disease. NEJM 1990;322:1700-1701
- ↑ Turner RC, Millns H, Neil HAW, et al. UKPDS 23 risk factors for coronary heart artery disease in type 2 diabetes. BMG 1998;316:823-828
- ↑ Taskinen MR, et al. Lipoprotein lipase in diabetes. Diabetes Metab Rev 1987;3:551-570
- ↑ Taskinen MR, et al. New insights into lipid metabolism in non-insulin-dependent diabetes mellitus. Ann Med 1996;28:355-340
- ↑ Gardner CD, et al. Association of small low density lipoprotein particles with the incidence of coronary artery disease in men and women. JAMA 1996;276:875-881
- ↑ Lamarche B, et al. Fasting insulin and apolipoprotein B levels and low-density lipoprotein particle size as risk factors for ischemic heart disease. JAMA 1998;297:1955-1961
- ↑ Haffner SM, Alexander CM, Cook TJ, et al. Reduced coronary events in simvastatin-treated patients with coronary heart disease and diabetes or impaired fasting glucose levels: subgroup analyses in the 4S. Arch Intern Med 1999;159:2661-2667
- ↑ Collins R, Armitage J, Parish S, et al. MRC/BHF Heart Protection Study of cholesterol-lowering with Simvastatin in 5963 people with diabetes: a randomized placebo-controlled trial. Lancet 2003;361:2005-2016
- ↑ Colhoun H, Betteridge D, Durrington P, et al. Primary prevention of cardiovascular disease with Atorvastatin in type 2 diabetes in the CARDS: multicenter randomized placebo-controlled trial. Lancet 2004;364:685-696
- ↑ Kearney PM, Blackwell L, Collins R, et al. Efficacy of cholesterol-lowering therapy in 18,686 people with diabetes in 14 randomized trials of statins: a meta-analysis. Lancet 2008;371(9607):117-125
- ↑ Gaede P, Lund-Andersen H, Palving HH, at al. Effect of a multifactorial intervention on mortality in type 2 diabetes. NEJM 2008;358:580-591
- ↑ Koskinen P, Manttari M, Manninen V, et al. Coronary heart disease incidence in NIDDM patients in the Helsinki Heart Study. Diabetes Care 1992;15:820-825
- ↑ Rubins HB, Robins SJ, Collins D, et al. Gemfibrozil for the secondary prevention of coronary heart disease in men with low levels of high-density lipoprotein cholesterol. Veterans Affairs High-Density Lipoprotein Cholesterol Intervention Trial Study Group. NEJM 1999;341:410-418
- ↑ Rubins HB, Robins SJ, Collins D, et al. Diabetes, plasma insulin and cardiovascular disease: subgroup analysis from the Department of Veterans Affairs high density lipoprotein intervention trial (VA-HIT). Arch Intern Med 2002;162:2597-2604
- ↑ Keech A, Simes RJ, Barter P, et al. Effect of long-term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomized controlled trial. Lancet 2005;366:1849-1861
- ↑ Tenenbaum A, Motro M, Fisman EZ, et al. Bezafibrate for the secondary prevention of myocardial infarction in patients with metabolic syndrome. Arch Intern Med 2005;165:1154-1160
- ↑ Saha SA, Arora RR. Fibrate in the prevention of cardiovascular disease in patients with type 2 diabetes mellitus – a pooled meta-analysis of randomized placebo-controlled clinical trials. Int J Cardiol 2010;141(2):157-166
- ↑ ACCORD Study Group. Effect of combination lipid therapy in type 2 diabetes mellitus. NEJM 2010;362:1563-1574
- ↑ Oxford Niaspan Study. J Am Coll Cardiol 2009;54:1787-1794
- ↑ Arbiter 6. NEJM 2010;361:2113-2122
- ↑ Harris WS. Expert opinion: omega-3 fatty acids and bleeding – cause for concern? Am J Cardiol 2007;99:44-46
- ↑ Haskell WL, Lee IM, Pate RR, et al. Physical activity and public health: update recommendation for adults from the American College of Sports Medicine and the American Heart Association. Circulation 2007;116:1081-1093
- ↑ Snow W, Aronson MD, Hombake ER, et al. Lipid control in the management of type 2 diabetes mellitus: a clinical practice guideline from the American College of Physicians. Ann Intern Med 2004;140:644-649
- ↑ Standards of medical care in diabetes – 2009. Diabetes Care 2009;32(Suppl 1):13-61
- ↑ Ryden L, Standl E, Bartnic M, et al. Guidelines on diabetes' pre-diabetes, and cardiovascular disease: executive summary. The task Force on Diabetes and Cardiovascular Disease of the European Society of Cardiology (ESC) and of the European Association for the Study of Diabetes (EASD). Eur Heart J 2007;28:88-13
קישורים חיצוניים
- דיסליפידמיה בחולים הלוקים בסוכרת מסוג 2, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר אלנה יצחקוב ופרופ' ארדון רובינשטיין, המכון המטבולי, המרכז הרפואי ת"א ע"ש סוראסקי, תל אביב; הפקולטה לרפואה ע"ש סאקלר, תל אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק